Биотрансформирующая активность родококков в отношении насыщенных стеринов
Автор: Бажутин Г.А., Ноговицина Е.М., Гришко В.В., Ившин И.Б.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 3, 2015 года.
Бесплатный доступ
Исследована способность родококков, принадлежащих к видам Rhodococcus erythropolis и Rhodococcus ruber, к биотрансформации стеринов с насыщенным углеродным остовом на примере 5а-холестана и его 3р-гидроксипроизводного. Отобраны штаммы, трансформирующие в присутствии н-гексадекана или глюкозы 5а-холестан-3р-ол с образованием 90-100% 5а-холестан-3-она. Методом тонкослойной хроматографии проведен качественный анализ смесей продуктов биотрансформации 5а-холестана штаммами R. erythropolis и R. ruber. В ряде экстрактов обнаружены соединения, не совпадающие по значению Rf с 5а-холестаном.
Стерины, родококки, холестанол, холестан
Короткий адрес: https://sciup.org/147204727
IDR: 147204727 | УДК: 579.66+547.92
Biotransformation activity of Rhodococci towards saturated sterines
This study describes the possibility of Rhodococcus erythropolis and R. ruber members to biotran-formation sterines with a saturated carbon skeleton like ба-cholestane and its 3p-hydroxy derivative 5а-cholestan-3p-ol. We selected strains that can transform 5а-cholestan-3p-ol to ба-cholestan-3p-one with 90-100% effectiveness. Using a thin-layer chromatography, we performed the qualitative analysis of ба-cholestane biotranformation products by rhodococci. In some extracts a compounds that Rf value do not coincide with ба-cholestane have been found.
Текст научной статьи Биотрансформирующая активность родококков в отношении насыщенных стеринов
Природные сгерины (холестерол, Р-ситостерол, в частности), характеризующиеся наличием 3 伊 ГҢ2фОКСИЛЬНОЙ группы и двойной связи при С-5? эффективно трансформируются бактериями с образованием физиологически активных соединений стероидной структуры [Malaviya. Gomes, 2СЮ8; Bhatti, Khem, 2012]. Способность мшфоорганизмов к модификации стеринов с насыщенным углеродным остовом (производных 5а-холестана) практически не изучена. Опи- сан 5ИНИЧНЫЙ пример биотрансформации [Microbial
… , 1991] 2 ot,3 а-дигщфокси-5-холссган-бона Mycobacieriит vaccae Zimct 11094 с образованием андростановых соединении (рис. 1)+
Извсстно, что многие производные насыщенных стеринов обладают выраженной гормональной, ПрОТІІБООіПХОЛСБОЙ И антиангиогенной активностью [Factors … , 2008 ; Brassinostcroids +…2012] Стераны, в том числе 5а-холестан (рис. 2, 1), являются типичными компонентами сырой нефти [Seifert. Moldowan, 1979], что делает из^^ение процесса их биодеградации акпгальным. L.J. Mul-
电 Бажутин Г. А., Ноговицина Е. М, Гришко В. В., Ившина И. Б., 2015
heirn и J* Van Eyk [1981] с помощью метода pa- вители актинобактерий проявляют окислительною диоуглеродной метки предположили, что предста- активность в отношении 5а-[4-14С] холестана+
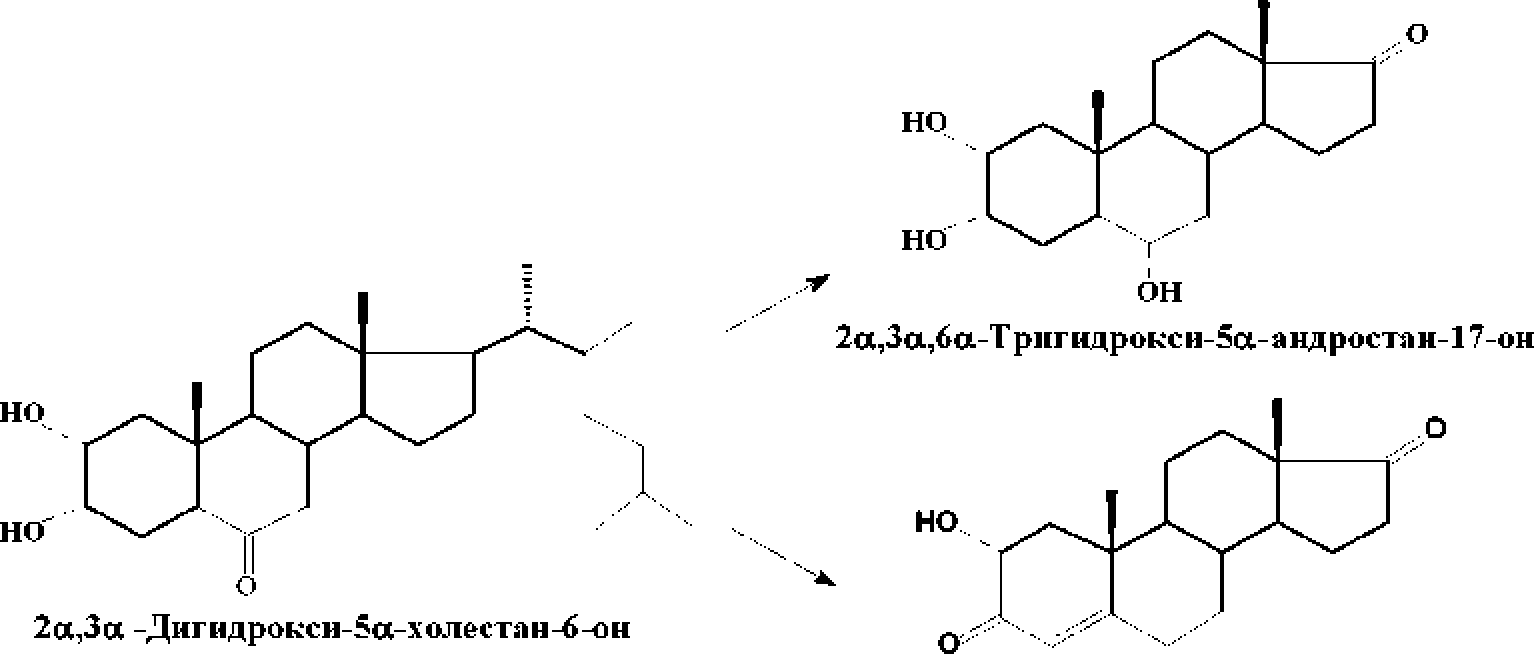
Рис. I* Биотрансформация 2аЗа-дигидрокси-5-холестан-6-она клетками М. vaccae Zimet 11()94
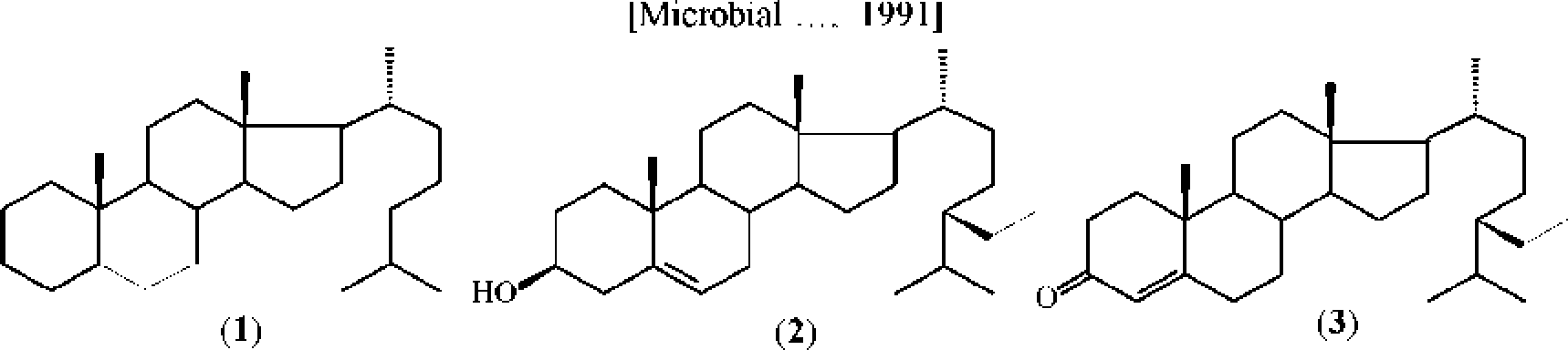
Рис. 2* Структуры 5а-холестана ⑴, p-ситостерола (2), стигмаст-4-ен-3 -она (3)
Ранее нами [Ноговицына, Гришко. ИвшинЯк 2011: Гришко, Ноговицина* Ившина. 2012] показана способность представителей Rhodococ-ctis erythropolis и A. ruber катализировать в при-с^тствии я-гсксадскана и глюкозы окисление 3 p-гидроксильной группы Р-сип ) ст«рола (рис. 2, 2) и изомеризацию его двойной связи при С-5 в положение 4 с образованием 25-98%-ного стигмаст-4-ен-З-она (рис. 2* 3)* обладающего гипогликемической и вазодепрессивной активностью, а также перспективного для лечения андроген-зависимых заболеваний [Alexander-Lindo, Morrison. Nairh 2004; Secondary +…2006 ; Streber. 199 3]t
Цель работы - оценка способности родококков к биотрансформации 5а-холестана и его 3 Р-ГИДрОКСИПрОИЛВОДНОГО в присутствии ростовых субстратов*
Материалы и методы
Б работе использовали штаммы родококков ш Региональной профилированной коллекции алка-нотрофных микроорганизйіов Института экологии и генетики микроорганизмов (официальный акроним коллекции ИЭГМ? номер во Всемирной федерации коллекций культур 768. www. iegm. ru/iegmcol). принадлежа шие к вша м Rhodococcus efyihropohs (И штаммов) и R. ruber (9 штаммов).
Родококки выращивали в условиях периодиче-ского культивирования на орбитальном шейкере (150 об/мин) при тсмпсрат ) -рс 28y Базовый состав минеральной среды включал следующие компоненты (г/л): KNO3 - L0 ; КНТО4 - 10: К2Hp0 日- 1.0 ; NaCl- IQ; MgSO4 - 。 2 CaCk 乂 2Hq - 0,02. В среду дополнительно вносили L0 г/л дрожжевого экстракта и 0+1 об+% микроэлементов по По-стгсйту [Романенко, Кузнецов, 1974]. В качестве посевного материала использовали родококки {5+0 父 10‘ кл/мл)? выращенные на скошенном мясо-ПСІГГОННОМ агаре и отобранные в экспоненциальной фазе роста. 5а-Холсстан или 5а-холсстан-30s добавляли б срс 屮 в концентрации 0+5 г/л Б виде 10%-ного раствора в изопропанолс через 2 с>т. роста бактериальных клеток в присутствии 0+1 об+% я-гсксадскана или 1.0%-ной глюкозы.
Продукты бактериального окисления субстратов экстрагировали этиловым эфиром уксусной кислоты* Объединенные этилацстатныс вытяжки промывали насыщенным водаым раствором NaCl и сушили с помощью обезвоженного №f, Качественный анализ полученных смесей проводили методом тонкослойной хроматографии (ТСХ) на силикагеле с использованием пластин с флуорсс-ценгной добавкой (Merck, Германия). Наличие продуктов биотрансформации определяли с помощью УФ облучателя LG/58 (Россия) и опрыскиванием пластин 5%-ной H2SO4 с послс/^ющим про- греванием при 95-100 С в течение 2-3 мин. Соотношение продуктов биотрансформации 5а-холестан-зр-ола подтверждали данными хромато-масс-спектромегрии с использованием системы Agilent 6890/ 5973N (кварцевая колонка HP-5MS SN US 15189741-1) Agilent technology, США. Ста-тистическхто обработку полученных результатов осуществляли с помощью компьютерной программы Excel 2003. рассчитывая среднее арифметическое и стандартную ошибку. Эксперименты проводили в 3-кратной повторности.
Результаты и их обсуждение
Установлено, что трансформирующие [З-сито-стерол коллекционные штаммы родококков способны аналогичным образом (по Зр-положению) окислять 5а-холестан-3 Р-ол с образованием 5а-холестан-3-она (рис. 3). уровень содержания которого в сумме продуктов реакции варьирует от 20 до 100% (рис. 4).
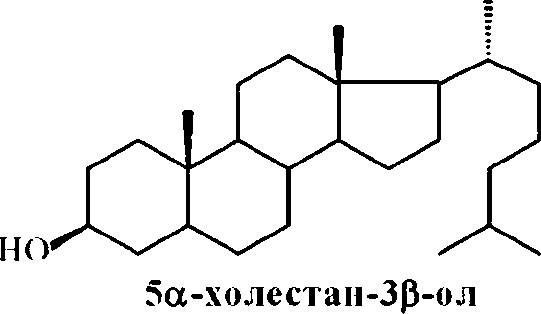
Рис. 3. Биотрансформация 5а-холестан-3 В-ола родококками
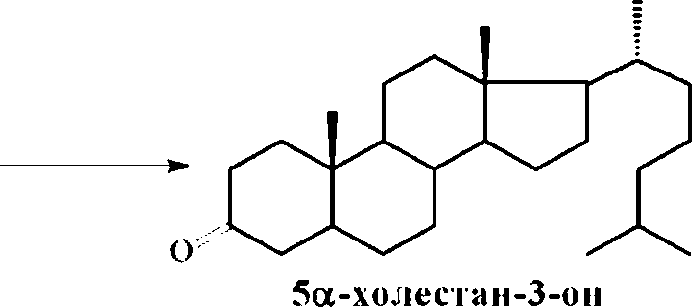
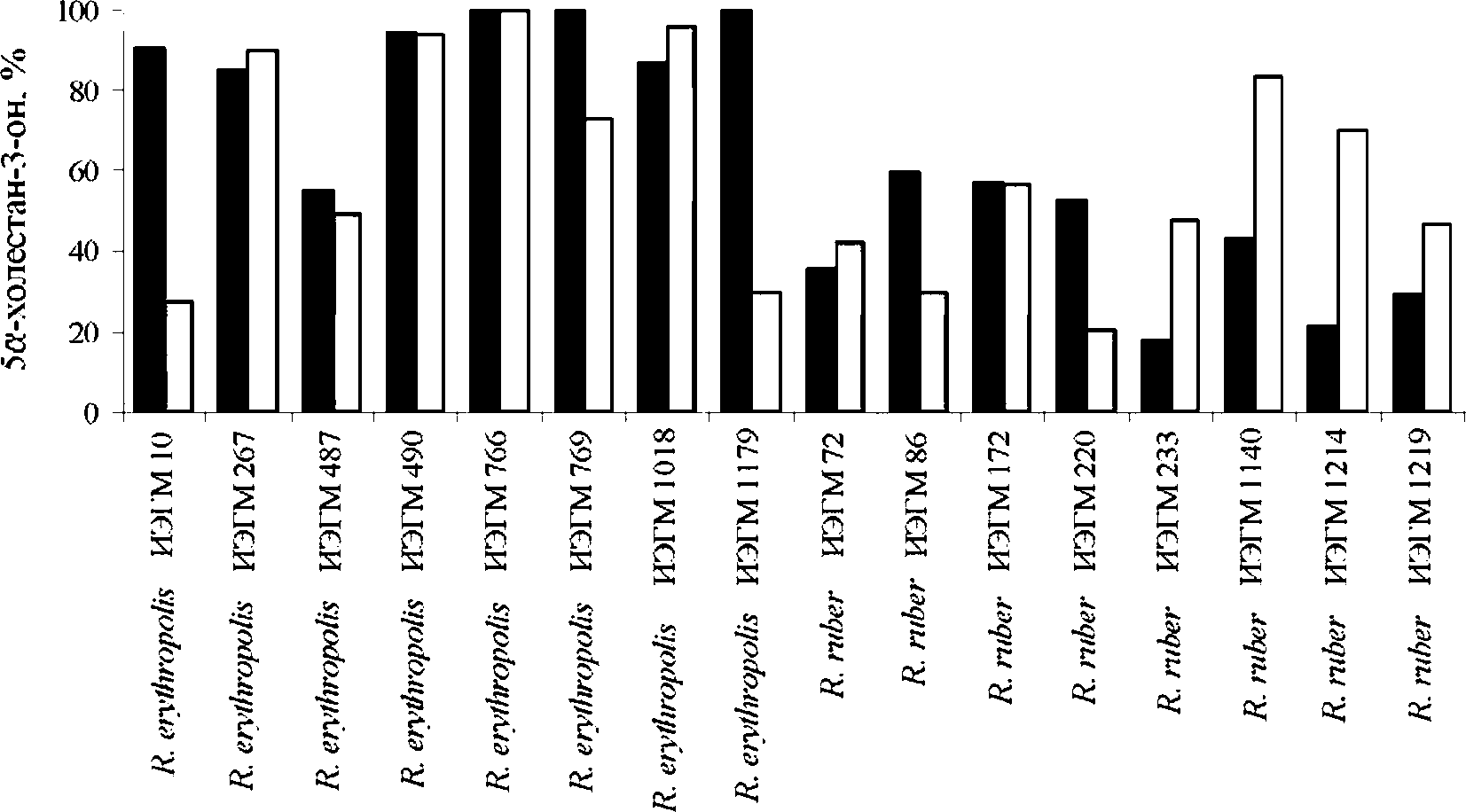
Рис. 4. Биотрансформация 5а-холестан-3|5-ола родококками в присутствии глюкозы ■ или //-гексадекана □.
Приведены данные после 5 сут. процесса биотрансформации
Отобраны культхры R. erythropolis ИЭГМ 490, ИЭГМ 766 и ИЭГМ 1018, обладающие высокой (87-100%) биотранссіюрмирутюіцей активносгью в отношении исходного соединения. Выявлено, что штаммы R. erythropolis ИЭГМ 10, ИЭГМ 769 и ИЭГМ 1179 эффективно трансформируют 5а-холестан-ЗР-ол только в присутствии глюкозы. При использовании н-гексадекана в качестве ростового субстрата их активность снижается в 1.3-3.3 раза.
С использованием метода ТСХ проведен качественный анализ продуктов биотрансформацин 5а-холестана штаммами R. erythropolis и R. ruber. В ряде экстрактов обнаружены соединения, не совпадающие по значению Rf с 5а-холестаном (рис. 5) ・
Отобраны штаммы R. erythropolis ИЭГМ 10, ИЭГМ 267, ИЭГМ 487, ИЭГМ 769. ИЭГМ 1140、 ИЭГМ 1167, ИЭГМ 1179 и R. ruber ИЭГМ 86、 ИЭГМ 172, ИЭГМ 220 для дальнейшего исследо- вания биотрансформир^ющей активности родо-кокков в отношении 5а-холестана.
ЗаЕСлючение
Проведена оценка способности родококковһ принадлежащих к ипаммам К, erythropolis и R. 也卜
О О О О О
.「 L0о
丨 Q О ber к биотрансформации 5а-холестана и его зр-гидроксипроизводного. В качестве основного про-дукта биотрансформации последнего идентифицирован 5а-холестан-3р чш* степень образования которого достигала 100%.
О О О О О О ^ О О。О О
О О
1 2 3
4 5 6 7
8 9 10 И 12
Рис. 5* Схема тонкослойной хроматографии экстрактов продуктов трансформации 5а-холсстана:
I - 5а-холестан, 2 - 5а-холестан-3р-ол, Штаммы /?. erythropolis. 3 - ИЭГМ 了 69, 6 - НЭГМ 1167, 8 - ИЭГМ 1140,9- ИЭГМ 487, И - ИЭГМ 267, 12 - ИЭПЛ 1179 : R. 厘加匕 4 - ИЭГМ 86, 3 - ИЭПЛ 220,7 - ИЭГМ 8 5, 10 - ИЭГМ 172. Эксперименты проводили в присутствии w-гсксадекана. В пробах 3 и 4 обнаружены соедшітіЕия, детектируемые в УФ, в остальных - после опрыскивания в 5%-ной H2SO^
Работа выполнена при поддержке грантов Российского научного фонда (14-14-00643), РФФИ к Министерства промышленности, инноваций и науки Пермского края (проект № 14-04-96005-р_>рала).
Библиографический сммсік
Гришко В.В., Ноговицына E.AZ* Пвишна И.Б. Оптимизация условий биокаталитического тюлу-нения стигмаст-4-ен-З-она // Химия природных соединений. 2012. № 3. С. 390-3 92.
Поговицина ЕА£ 、 Гришко В.В., Ивишна И.Б. Био-каталитичсскос получение фармакологически перспективного стигмаст-4 -ен-3 -она с использованием клеток родококков // Биоорганическа я химия. 2011. Т. 3 7. №5+ С 697-704/
Романенко ВЛ„ Кузнецов CJL Экология микроорганизмов пресных водоемов. Л. : Наука* 1974. 194 с.
A lexander-Lindo 兄上一 Xfowison Е. У. SI A. t Nair V< G. HvDOs>lvcaemic eiTecl of sli^iiiasl-4-en-3-one and its corresponding alcohol from the bark of Ana-cardium occidenta/e (Cashew) // PhvtOtherapv Research. 2 004. Vol. 18, № 5. P, 403-407. +
Bhatti 风乂. Khera RA. Biological transfbrmaticms of steroidal compounds: a review // Steroids. 2012. Vol. 7,№ 12. P. 1267-90.
Brassinosteroids inhibit in vitro angiogenesis in human endothelial cells / L. Rarova et al. // Steroids. 2012. Vol, 7 工 № 13. P. 1502-9.
Factors influencing the steroid profile in doping control analysis / U. Mareck et al. // Journal of Mass Speclroiiielnr+ 2008t Vol. 4 3* № 7. P, 877-91.
Malaviva 月.、 Gomes 7. Androstenedione production bv biotransforimtion of phviosterols // Bioresource Technology 2008. Vol. 99, № 15, P. 6725-6737.
Microbial degradation of 2a3a-dilivdro?tYT-5a
Mu!helm £J, 】行门 Evk J. Microbiological Oxidation of Steroid Hydrocarbons // Journal of General Mi-crobioloxv- 1981 Vol. 126. P 267-275.
Secondary metabolites from Euphorbia hehoscopia and their vasodepressor activity / A+ Baria et al+ // Turkey Journal of Chemistn . 2006. Vol. 30. P. 325-332. ‘
Seifert W.K., Mokhwan J.M. The eilect of biodegradation on steranes and tcrpancs in crude oils // Geochimica et cosmochimica Acta+ 1979. Vot 43. P 11-126
Streber A.S. Use stigmnsta-4-en-3 -on in the treatment of androgen dependent disease // US Patent. 1993. No. 5264428.
Список литературы Биотрансформирующая активность родококков в отношении насыщенных стеринов
- Гришко В.В., Ноговицина Е.М., Ившина И.Б. Оптимизация условий биокаталитического получения стигмаст-4-ен-3-она//Химия природных соединений. 2012. № 3. С. 390-392
- Ноговицина Е.М., Гришко В.В., Ившина И.Б. Биокаталитическое получение фармакологически перспективного стигмаст-4-ен-3-она с использованием клеток родококков//Биоорганическая химия. 2011. Т. 37, № 5. С. 697-704."
- Романенко В.И., Кузнецов С.И. Экология микроорганизмов пресных водоемов. Л.: Наука, 1974. 194 с
- Alexander-Lindo R.L., Morrison E.Y.S.A., Nair M.G. Hypoglycaemic effect of stigmast-4-en-3-one and its corresponding alcohol from the bark of Ana-cardium occidentale (Cashew)//Phytotherapy Research. 2004. Vol. 18, № 5. P. 403-407
- Bhatti H.N., Khera R.A. Biological transformations of steroidal compounds: a review//Steroids. 2012. Vol. 7, № 12. P. 1267-90
- BrassinoSteroids inhibit in vitro angiogenesis in human endothelial cells/L. Rarova et al.//Steroids. 2012. Vol. 77, № 13. P. 1502-9
- Factors influencing the steroid profile in doping control analysis/U. Mareck et al.//Journal of Mass Spectrometry. 2008. Vol. 43, № 7. P. 877-91
- Malaviya A., Gomes J. Androstenedione production by biotransformation of phytosterols//Bioresource Technology. 2008. Vol. 99, № 15. P. 6725-6737
- Microbial degradation of 2а,3а-dihydroxy-5а-cholestan-6-one by Mycobacterium vaccae/H. Vorbrodt et al.//Steroids. 1991. Vol. 56, № 12. P. 586-588
- Mulheirn L.J., Van Eyk J. Microbiological Oxidation of Steroid Hydrocarbons//Journal of General Microbiology. 198l. Vol. 126. P. 267-275
- Secondary metabolites from Euphorbia helioscopia and their vasodepressor activity/A. Barla et al.//Turkey Journal of Chemistry. 2006. Vol. 30. P. 325-332
- Seifert W.K., Moldowan J.M. The effect of biodegra-dation on steranes and terpanes in crude oils//Geochimica et cosmochimica Acta. 1979. Vol. 43. P. 11-126
- Streber A.S. Use stigmasta-4-en-3-on in the treatment of androgen dependent disease//US Patent. 1993. No. 5264428


