Ближний порядок в механоактивированных титанитах
Автор: Сидорова Ольга Владимировна, Алешина Людмила Александровна, Калинкин Александр Михайлович, Калинкина Елена Владимировна
Журнал: Ученые записки Петрозаводского государственного университета @uchzap-petrsu
Рубрика: Физико-математические науки
Статья в выпуске: 4 (125), 2012 года.
Бесплатный доступ
Показано, что скорость размола титанита в атмосфере СО 2 и на воздухе совпадает. Число кислородных соседей атома титана уменьшается в образцах, размолотых в обеих атмосферах. Число кислородных соседей атома кальция уменьшается только при размоле в воздухе.
Титанит, механоактивация, рентгенографический анализ, ближний порядок, аморфизация
Короткий адрес: https://sciup.org/14750143
IDR: 14750143 | УДК: 539.264;
Short-range order in mechanically activated titanites
It is shown, that the rate of titanite grinding is the same in the air and carbon dioxide. The number of oxygen neighbors of titanium atom decreases in milled samples in both atmospheres. The number of oxygen neighbors of calcium atom decreases only by grinding in the air.
Текст научной статьи Ближний порядок в механоактивированных титанитах
Синтез новых соединений является одной из основных задач химии и современной науки в целом. Для решения этой проблемы применяются и разрабатываются новые методы инициирования и ускорения химических реакций и физико-химических превращений. Одним из таких методов является метод механоактивации, заключающийся в тонком измельчении материалов при помощи различных измельчительных аппаратов. Было обнаружено, что Са- и Mg-со-держащие силикаты способны поглощать при определенных режимах измельчения углекислый газ из окружающей среды в количествах, сопоставимых с массой измельчаемого образца. Данный эффект был назван механохимическим [1], [2], [5], [6], и его открытие стимулировало интерес к исследованиям сопровождающих его структурных изменений.
Информацию о характере изменения структуры материалов при механоактивации в различных средах можно получить дифракционными методами.
Целью данной работы были рентгенографические исследования влияния размола в воздухе и атмосфере углекислого газа на структурное состояние титанита (сфена) CaTiSiO5.
ОБРАЗЦЫ И МЕТОДИКА ЭКСПЕРИМЕНТА
Объектами исследования были образцы мо-номинеральной фракции сфена Ковдорского месторождения (Кольский полуостров), предоставленные для исследований институтом химии и технологии редких элементов и минерального сырья (ИХТРЭМС, Апатиты), в исходном состоянии и после размола в течение 30 мин. в атмосфере углекислого газа и воздуха. Методика приготовления образцов изложена в [4].
Рентгенографирование проводилось на автоматизированных установках ДРОН-3 в Fe-и MoKα-излучениях. Монохроматором служил кристалл пиролитического графита. Методика рентгенографирования изложена в [7].
Анализ результатов эксперимента проводился методом Финбака – Уоррена с использованием пакета прикладных программ X-ray. Подробно методика обработки экспериментальных данных изложена в [2].
РЕЗУЛЬТАТЫ РЕНТГЕНОГРАФИЧЕСКОГО
ЭКСПЕРИМЕНТА
Из рентгенограмм, приведенных на рис. 1а, видно, что после 30 мин. размола в атмосферах углекислого газа и на воздухе на рентгенограммах сфена сохраняются слабые и размытые отражения от кристаллической фазы.
Размол сфена в атмосфере углекислого газа СО2 и на воздухе приводит к выходящему за пределы погрешности различию в рентгенограммах в области до 5 Å-1, что и обусловливает
различие в кривых D(r) (рис. 1б). Для расчета характеристик ближнего порядка (радиусов и размытий координационных сфер и координационных чисел) использовались кривые рассеяния, полученные на излучении МоK α .
Кривые распределения парных функций D(r) (рис. 1б) размыты, максимумы перекрываются, поэтому прежде чем проводить из них расчет характеристик ближнего упорядочения, была проанализирована кристаллическая структура сфена. Известно, что сфен кристаллизуется в моноклинной модификации. При комнатной температуре и нормальном давлении стабильна фаза с пространственной группой P21/a [8], [10], [11]. При температуре 270 °С происходит фазовый переход в высокотемпературную форму с сохранением сингонии, но с изменением пространственной группы на A2/a [8], [9], [11].
В табл. 1 приведены периоды (a, b, c), угол моноклинности β , число формульных единиц на элементарную ячейку (Z), объем элементарной ячейки V и плотность ρ обеих модификаций сфена.
Таблица 1
Кристаллографические характеристики полиморфных модификаций сфена, Z=4
|
Пр. гр. сим. |
a, Å |
b, Å |
c, Å |
β , º |
V, Å3 |
ρ, г/см3 |
|
P21/a [11] |
7,068 |
8,714 |
6,562 |
113,82 |
369,73 |
3,52 |
|
А2/а [11] |
7,060 |
8,737 |
6,565 |
113,70 |
370,80 |
3,51 |
Основу структуры сфена составляют зигзагообразные цепочки октаэдров TiO6 (рис. 2а), вытянутые вдоль оси а. Октаэдры связаны через анион О1 (рис. 2а). Тетраэдры SiO4 представляют собой изолированные друг от друга структурные единицы, то есть они не соединены между собой, а связывают цепочки октаэдров TiO6 (рис. 2б). Кальций находится в окружении 7 атомов кислорода и располагается между октаэдрическими цепочками координационных многогранников титана (рис. 2в). Анион кислорода, находящийся в позиции О1, связан с двумя ионами титана и одним ионом кальция; анионы О2 и О3 окружены тремя катионами: Ti, Si и Ca;
анионы О4 и О5 – четырьмя катионами: Ti, Si и двумя ионами кальция (рис. 2в).
Полиморфный переход от низко- к высокотемпературной модификации сфена (P21/a → А2/а) относится к классу деформационных и связан с повышением симметрии в расположении катионов в координационных многогранниках. В низкотемпературной форме (группа симметрии P21/a) ион титана смещен из геометрического центра октаэдра на 0,21 Å в направлении оси цепочек. В результате фазового перехода при 270 °С (группа симметрии новой фазы А2/a) ион титана размещается в геометрическом центре октаэдра: расстояния Ti-O попарно одинаковы (табл. 2). Атом кремния также смещается в центр симметрии тетраэдра (табл. 2).
Таблица 2
Расстояния между анионами и катионами в координационных многогранниках
|
Р21а |
А2а |
Р21а |
А2а |
||||||||
|
Ca |
O1 |
2,270 |
Ca |
O1 |
2,286 |
Ti |
O1 |
1,772 |
Ti |
O1 |
1,867 |
|
Ca |
O3 |
2,406 |
Ca |
O2 |
2,418 |
Ti |
O1 |
1,974 |
Ti |
O1 |
1,867 |
|
Ca |
O2 |
2,427 |
Ca |
O2 |
2,418 |
Ti |
O3 |
1,971 |
Ti |
O2 |
1,994 |
|
Ca |
O4 |
2,678 |
Ca |
O3 |
2,630 |
Ti |
O2 |
2,010 |
Ti |
O2 |
1,994 |
|
Ca |
O4 |
2,389 |
Ca |
O3 |
2,415 |
Ti |
O5 |
2,049 |
Ti |
O3 |
2,016 |
|
Ca |
O5 |
2,585 |
Ca |
O3 |
2,630 |
Ti |
O4 |
1,986 |
Ti |
O3 |
2,016 |
|
Ca |
O5 |
2,433 |
Ca |
O3 |
2,415 |
||||||
|
Si |
O5 |
1,634 |
Si |
O3 |
1,646 |
Si |
O3 |
1,654 |
Si |
O2 |
1,640 |
|
Si |
O4 |
1,659 |
Si |
O3 |
1,646 |
Si |
O2 |
1,624 |
Si |
O2 |
1,640 |
Атомы кислорода с одинаковыми номерами, но с различными расстояниями до одного и того же катиона связаны между собой симметричными преобразованиями соответствующей пространственной группы. В координационном многограннике Са в обеих фазах 4 расстояния Са-О близки: ∼ 2,4 Å. Расстояния Са-О3 и Са-О5 в высокотемпературной фазе одинаковы и составляют 2,63 Å. Один атом кислорода в координационном многограннике кальция имеет короткую связь Са-О1: 2,27 Å в низкотемпературной и 2,286 Å в высокотемпературной фазе.
Анализ рентгенограммы исходного образца сфена показал, что его структура соответствует моноклинной модификации, пространственная группа P21/a.
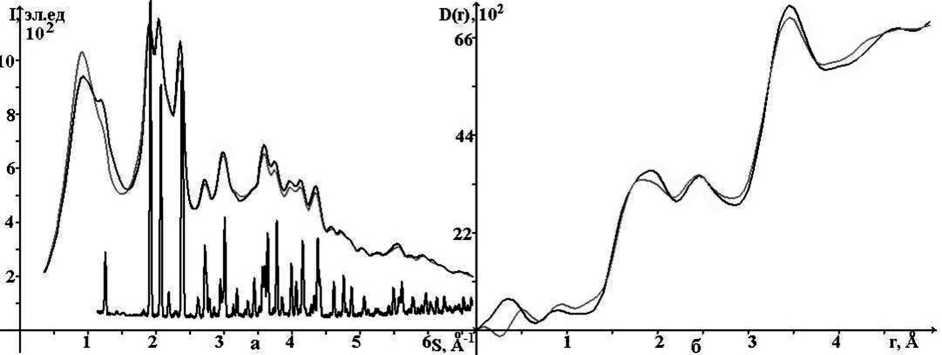
Рис. 1. Рентгенограммы кристаллического (в нижней части рисунка) и размолотых образцов сфена: а) ▬▬ 30 мин. в СО2; ▬▬ 30 мин. в воздухе; б) кривые распределения парных функций D(r)
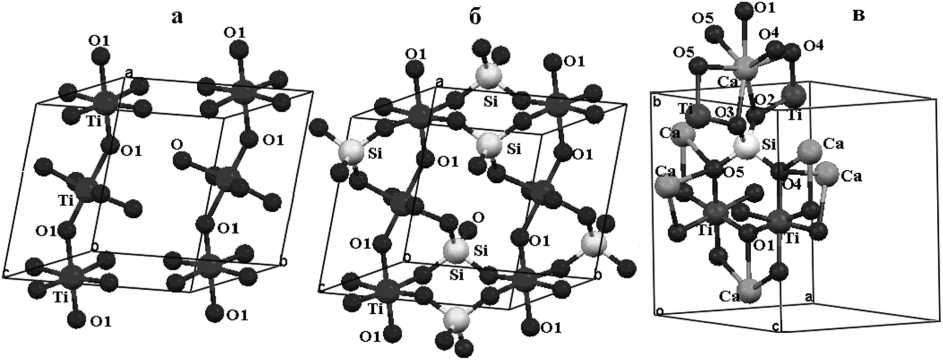
Рис. 2. Координационные многогранники в структуре сфена: а – цепочки октаэдров TiO6; б – тетраэдры SiO4, связывающие цепочки октаэдров TiO6; в – связь между координационными многогранниками Ti, Са и Si
Однако поскольку, температура фазового перехода P21/a →А2/а невысока и, кроме того, увеличение давления также приводит к указанному фазовому переходу [9], следует ожидать, что механическое воздействие при размоле может его активизировать. Поэтому c целью анализа кривых D(r) были рассчитаны радиусы координационных сфер и координационные числа для обеих кристаллических модификаций сфена. Результаты расчета представлены в табл. 3.
Значения радиусов и координационных чисел, рассчитанные из экспериментальных кривых D(r), соответствовали данным для объединенных координационных сфер (табл. 3). Поскольку объединялись сферы, состоящие из пар атомов разного сорта (i, j; i1, j1), координационные числа для кристаллов пересчитывались согласно соотношению
N ij = N i1,j1 ⋅ ZZi 1 ZZ j 1 , (1)
вытекающему из равенства площадей под максимумами [1].
В табл. 4 значения радиусов координационных сфер и координационных чисел размолотых образцов сфена, рассчитанные из экспериментальных кривых D(r), сравниваются с соответствующими данными для кристаллов.
Из табл. 4 следует, что при размоле сфена на воздухе расстояния rSi-О в тетраэдрах SiO4 совпадают с соответствующим средневесовым расстоянием для кристаллов. Для размолотого в атмосфере СО2 сфена значение радиуса координационный сферы rSi-О завышено примерно на 2 %. Координационное число NSi-О для размолотого на воздухе и в атмосфере СО2 сфена совпадает в пределах погрешности с координационным числом NSi-О для кристаллических модификаций сфена. Таким образом, координационные многогранники кремния SiO4 в структуре размолотых образцов сохраняются (табл. 4).
Число ближайших кислородных соседей (первое координационное число) около атомов титана уменьшается на 4 % при размоле в воздухе и на 8 % при размоле в атмосфере углекислого газа. Среднее значение межатомного расстояния rТi-О для образца, размолотого на воздухе, совпадает по величине с данными для высокотемпературной фазы сфена, тогда как для образца, размолотого в атмосфере СО2 оно практически равно соответствующему значению для низкотемпературной фазы (табл. 4).
При размоле на воздухе на 25 % уменьшается число кислородных соседей NСа-О около атома кальция, но при размоле в атмосфере СО2 оно близко к значениям, теоретически рассчитанным для кристаллов. Уменьшение числа ближайших кислородных соседей в координационном многограннике кальция при размоле в аналогичных условиях ранее было обнаружено для образцов псевдоволластонита [3], однако наиболее интенсивно этот процесс протекал при размоле в атмосфере CO2.
Вследствие уменьшения числа ближайших соседей Ca-O и Ti-O координационные числа NО-О(1) для размолотых на воздухе и в СО2 образцов сфена занижены, причем сильнее при размоле в атмосфере углекислого газа.
Координационные числа NCa-Si и NO-O(2) для размолотых на воздухе и в атмосфере CO2 образцов сфена совпадают в пределах погрешности с координационными числами NCa-Si и NO-O(2) для кристаллов.
Сферы Ti-Si, Ca-Ti, Ti-Ti, Ti-O(2), Ti-O(3), Ca-Ca не являются индивидуальными в кристалле (табл. 3, 4), поскольку в каждом случае одинаковые радиусы имеют сферы разного типа. Например, близкие по значениям радиусы имеют сферы Ti-Si, Ca-O и Si-O (табл. 3). При расчете координационных чисел из экспериментальной D(r) задавали тип сферы как Ti-Si, а координационные числаСф = О и S. i = O пересчитывались на Ti = Si по формуле (1).
Из приведенных в табл.4 данных для указанных выше сфер видно, что рассчитанные из эксперимента координационные числа для сфена, размолотого в атмосфере СО2, наиболее близки к суммарным координационным числам, рассчитанным для высокотемпературной модификации сфена (А2/а). В то же время рассчитанные из эксперимента координационные числа для сфена, размолотого на воздухе, не совпадают с соответствующими суммарными координа-
Таблица 3
Радиусы координационных сфер rij, разброс межатомных расстояний Δ rij, координационные числа Nij, средневесовые значения радиусов 〈 rij 〉 и суммарные координационные числа N'ij, рассчитанные для сфена
Таким образом, при размоле на воздухе нарушается характер распределения атомов по координационным сферам, тогда как при размоле атмосфере СО2 он соответствует таковому для высокотемпературной фазы сфена.
ОСНОВНЫЕ РЕЗУЛЬТАТЫ И ВЫВОДЫ
Установлено, что при 30-минутном размоле сфена на воздухе и в атмосфере CO2 полной аморфизации не происходит, содержание кристаллической фазы не зависит от атмосферы размола. Следует отметить, что в исследованном ранее в [2] псевдоволластоните после 30-минутного размола не было следов кристаллической фазы.
В размолотых образцах сфена координационные многогранники кремния сохраняются. Число ближайших кислородных соседей атома титана уменьшается при размоле, причем это изменение выражено наиболее ярко в образцах, размолотых в СО2. Число кислородных соседей
Таблица 4
Результаты расчетов радиусов координационных сфер rij, координационных чисел Nij и дисперсии радиусов для размолотых образцов титанита.
Ошибка в определении радиусов drij = ± 0,01Å, размытий dσij = ± 0,02 Å
Аналогичные исследования, проведенные в [2] для образцов псевдоволластонита СаSiO3, показали, что при размоле псевдоволластонита также происходит уменьшение числа кислородных соседей у атомов кальция [2], однако наибо- лее интенсивно этот процесс протекает при размоле в атмосфере CO2.
Работа выполнена при поддержке проекта № П801 в рамках Федеральной целевой программы «Научные и научно-педагогические кадры инновационной России» на 2009–2013 годы (мероприятие 1.2.1).
Список литературы Ближний порядок в механоактивированных титанитах
- Алешина Л. А., Никитина Е. А., Фофанов А. Д. Ренгенографические исследования ближнего порядка в аморфных анодных окисных пленках алюминия. Деп. в ВИНИТИ. 21.04.1995. № 1134-B95. 23 с.
- Алешина Л. А., Сидорова О. В., Осауленко Р. Н., Фофанов А. Д., Калинкин А. М. Рентгенонграфические исследования влияния размола на структурные характеристики образцов псевдоволластонита//Электронный журнал «Исследовано в России», 030, 297-306, 2009 [Электронный ресурс]. Режим доступа: http://zhurnal.ape.relam.ru/articles/2009/030.pdf
- Калинкин А. М. Механосорбция диоксида углерода перовскитом CaTiO3 и структурно-химические изменения//Журнал физической химии. 2008. Т. 82. № 2. С. 331-336.
- Калинкин А. М., Калинкина Е. В., Васильева Т. Н. Влияние механической активации сфена на его реакционную способность//Коллоидный журнал. 2004. Т. 66. № 2. С. 190-197.
- Калинкин А. М., Калинкина Е. В., Залкинд О. А. Механосорбция углекислого газа Са-и Mg-содержащими силикатами и алюмосиликатами. Поглощение СО2 и структурно-химические изменения//Коллоидный журнал. 2009. Т. 71. № 2. С. 194-201.
- Калинкин А. М., Неведомский В. Н., Калинкина Е. В. Наноструктура диопсида CaMgSi2O6 и перовскита CaTiO3, механоактивированных в углекислом газе//Неорганические материалы. 2008. Т. 44. № 6. С. 727-733.
- Лобов Д. В., Фофанов А. Д., Осауленко Р. Н., Калинкин А. М. Рентгенографическое исследование структурного состояния образцов диопсида после длительного помола.//Электронный журнал «Исследовано в России», 085, 889-907, 2005 [Электронный ресурс]. Режим доступа: http://zhurnal.ape.relam.ru/articles/2005/085.pdf
- Kunz M., Arlt T., Stolz J. In situ powder diffraction study of titanite (CaTiOSiO4) at high temperature//Am. Min. 2000. Vol. 85. P. 1465-1473.
- Kunz M., Xirouchakis D., Lindsley D. H., Hausermann D. High-pressure phase transition in titanite (CaTiOSiO5)//Am. Min. 1996. Vol. 8. P. 1527-1530.
- Speer J. A., Gibbs G. V. The crystal structure of synthetic titanite, CaTiOSiO4, and the domain texturesofnatural titanites//Am. Min. 1976. Vol. 61. P. 238-247.
- Teylor M., Brown G. E. High-temperature structural study of the P21/a ^A2/a phase transition in synthetic titanite CaTiSiO5//Am. Min. 1976. Vol. 61. P. 435-447.


