Брахитерапия с использованием источников I-125 у больных группы умеренного риска
Автор: Петровский Александр В., Амосова Виктория А., Черняев Виталий А., Автомонов Дмитрий Е., Бухаркин Борис В., Шолохов Владимир Н., Рощин Дмитрий А., Нечушкин Михаил И., Матвеев Всеволод Б.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Собственные исследования
Статья в выпуске: 3 (24), 2017 года.
Бесплатный доступ
Введение: Для лечения локализованного РПЖ группы умеренного риска возможно применение нескольких лечебных подходов, включая радикальную простатэктомию, дистанционную радиотерапию, брахитерапию, криотерапию, гормональную терапию, а также динамическое наблюдение. Цель: Провести оценку результатов выполнения низкодозной брахитерапии с использованием источников I-125 у пациентов РПЖ группы умеренного риска. Материалы и методы: В анализ включено 86 больных в возрасте от 48 до 76 лет (медиана возраста 66 лет). Всем пациентам проведена имплантация источников йод-125 в предстательную железу. Суммарная очаговая доза (СОД) на простату составила 145 Гр. Контроль ПСА после операции проводился каждые 3 мес. в течение первого года, затем каждые 6 мес. в течение 3 лет и далее ежегодно. Выживаемость оценивалась по методу Каплана-Майера с учетом влияния таких факторов, как возраст, D90 на предстательную железу, V100 предстательной железы, предоперационная антиандрогенная терапия. Оценка субъективных показателей качества жизни была проведена при помощи стандартизованных анкет IPSS. Результаты: При медиане наблюдения 60 мес. 5-летние показатели без ПСА-рецидивной, опухолево-специфической и общей выживаемости составили 90,5%, 100% и 95,2% соответственно. Изучаемый метод лечения обладает приемлемым спектром осложнений. Уретрит 1 степени по категории RTOG в течение 1 мес. после операции развился у 60 (69,3%) пациентов, при этом к 6-месячному сроку наблюдения симптомы дизурии оставались лишь у 11 (13,3%) больных, что было ассоциировано с хронической мочевой инфекцией, устойчивой к антибактериальной терапии. Лучевой рек-тит 1 степени в течение 1 мес. после операции развился у 2 (2,1 %) пациентов, при этом к 6-месячному сроку наблюдения симптомы ректита были купированы у всех больных. До проведенного лечения количество баллов по шкале IPSS составило 0-7 баллов - n=63 (74%), 8-19 баллов - n=23 (26%) (медиана IPSS 5,7). Через 1 мес. число пациентов с умеренной симптоматикой увеличилось до 69,3%, через 6 мес. после окончания лечения среднее значение IPSS составило 10 баллов. Через 12 мес. 0-7 баллов зарегистрировано у 94% пациентов. Заключение: При выполнении брахитерапии постоянными источниками I-125 у больных умеренной группы риска получены очень хорошие функциональные и онкологические результаты. Данный метод обеспечивает отличный контроль уровня ПСА при медиане наблюдения 65 мес. и при этом обеспечивает высокое качество мочеиспускания в отдаленные сроки после лечения.
Рак предстательной железы, качество жизни, брахитерапия i-125, умеренный риск, гормонотерапия
Короткий адрес: https://sciup.org/140223049
IDR: 140223049 | DOI: 10.18027
The results of I-125 brachytherapy in patients of moderate-risk prostate cancer
Background: The treatment for moderate-risk prostate cancer patients include several methods. There are radical prostatectomy, radiotherapy, brachytherapy, cryotherapy, hormone therapy, and dynamic observation. Purpose: The goal of our study was to analyze the results of brachytherapy using I-12.5 in patients with moderat.-risk prostate cancer. Materials and methods: Eighty six patients at the age of 48 to 76 (median 66 years) were included in the analysis. Implantation of iodine-125 sources was performed in all patients. The total dose to the prostate was 145 Gy. PSA monitoring after surgery was performed every 3 months during the first year, then every 6 months for the next 3 years, and then - annually. Survival was estimated using the Kaplan - Meier scale considering such factors as age, the D90 to the prostate, the V100 prostate, preoperative anti-androgen therapy. Quality of life analysis was made using standard IPSS questionnaire. Results: 5-year results with median follow-up of 60 months without PSA-recurrent, tumor-specific and overall survival were 90.5%, 100% and 95.2%, respectively. The treatment method has an acceptable spectrum of complications. 1st degree urethritis in the category of RTOG within 1 month after the operation developed in 60 (69.3%) patients while in the 6-month follow-up period the symptoms of dysuria had only 11 (13.3%) patients, which was associated with chronic urinary infection, resistant to antibiotic therapy. 1st degree radiation proctitis within 1 month after the operation developed in 2 (2.1%) patients, and after 6-month observation period the symptoms of proctitis ceased in all patients. Before the treatment, the number of points on the IPSS scale was 0-7 points -n = 63 (74%), 8-19 points - n = 23 (26%) (median IPSS 5.7). A month later, the number of patients with mild symptomatology increased to 69.3%, 6 months after the end of treatment, the mean IPSS was 10 points. After 12 months, 0-7 points were recorded in 94% of patients. Conclusion: The permanent brachytherapy with I-125 in patients with moderate-risk prognosis showed very good functional and oncological outcomes. This method provides excellent control of the PSA level with median follow-up of 65 months, and at the same time provides high quality of urination for 2-3 years after treatment.
Текст научной статьи Брахитерапия с использованием источников I-125 у больных группы умеренного риска
Введение: Для лечения локализованного РПЖ группы умеренного риска возможно применение нескольких лечебных подходов, включая радикальную простатэктомию, дистанционную радиотерапию, брахитерапию, криотерапию, гормональную терапию, а также динамическое наблюдение.
Цель: Провести оценку результатов выполнения низкодозной брахитерапии с использованием источников I-125 у пациентов РПЖ группы умеренного риска.
Материалы и методы: В анализ включено 86 больных в возрасте от 48 до 76 лет (медиана возраста 66 лет). Всем пациентам проведена имплантация источников йод-125 в предстательную железу. Суммарная очаговая доза (СОД) на простату составила 145 Гр. Контроль ПСА после операции проводился каждые 3 мес. в течение первого года, затем каждые 6 мес. в течение 3 лет и далее ежегодно. Выживаемость оценивалась по методу Каплана-Майера с учетом влияния таких факторов, как возраст, D90 на предстательную железу, V100 предстательной железы, предоперационная антиандрогенная терапия. Оценка субъективных показателей качества жизни была проведена при помощи стандартизованных анкет IPSS.
Результаты: При медиане наблюдения 60 мес. 5-летние показатели без ПСА-рецидивной, опухолево-специфической и общей выживаемости составили 90,5%, 100% и 95,2% соответственно. Изучаемый метод лечения обладает приемлемым спектром осложнений. Уретрит 1 степени по категории RTOG в течение 1 мес. после операции развился у 60 (69,3%) пациентов, при этом к 6-месячному сроку наблюдения симптомы дизурии оставались лишь у 11 (13,3%) больных, что было ассоциировано с хронической мочевой инфекцией, устойчивой к антибактериальной терапии. Лучевой рек-тит 1 степени в течение 1 мес. после операции развился у 2 (2,1 %) пациентов, при этом к 6-месячному сроку наблюдения симптомы ректита были купированы у всех больных. До проведенного лечения количество баллов по шкале IPSS составило 0–7 баллов – n=63 (74%), 8–19 баллов – n=23 (26%) (медиана IPSS 5,7). Через 1 мес. число пациентов с умеренной симптоматикой увеличилось до 69,3%, через 6 мес. после окончания лечения среднее значение IPSS составило 10 баллов. Через 12 мес. 0–7 баллов зарегистрировано у 94% пациентов.
Заключение: При выполнении брахитерапии постоянными источниками I-125 у больных умеренной группы риска получены очень хорошие функциональные и онкологические результаты. Данный метод обеспечивает отличный контроль уровня ПСА при медиане наблюдения 65 мес. и при этом обеспечивает высокое качество мочеиспускания в отдаленные сроки после лечения.
Для лечения локализованного РПЖ возможно применение нескольких лечебных подходов, включая радикальную простатэктомию, дистанционную радиотерапию, брахитерапию, криотерапию, гормональную терапию, а также динамическое наблюдение. При определении тактики лечения пациентов локализованного РПЖ решающее значение имеет оценка риска прогрессирования. На сегодняшний день в клинической практике применяется стратификация пациентов по группам риска [3], в основу которой положена шкала, предложенная в 1998 г. D’Amico. Согласно данной классификации к группе низкого риска относятся пациенты с клинической стадией Т1-2а, с уровнем простатспецифическо-го антигена ПСА ≤ 10 нг/мл, суммой баллов по шкале
Глисона ≤ 6; к группе умеренного риска – пациенты с ПСА от 10 до 20 нг/мл, индексом Глисона = 7 или клинической стадией T2b; к группе высокого риска были отнесены пациенты с ПСА > 20 нг/мл, индексом Глисона > 7 или клинической стадией ≥ T2c. Для каждой такой группы характерна определенная тактика и методы лечения.
Согласно практическим рекомендациям по диагностике и лечению рака предстательной железы Ассоциации онкологов России (АОР) [4], для пациентов РПЖ группы умеренного риска прогрессирования заболевания и ожидаемой продолжительностью жизни более 10 лет обычно проводятся ДЛТ в сочетании с коротким курсом гормонотерапии (4–6 мес.) или РПЭ с возможной лимфаденэктомией. Альтернативой может служить внутритканевая лучевая терапия – брахитерапия. Основные преимущества метода заключаются в малоинвазивности, удобстве проведения, возможности сохранения качества жизни, сравнимого с дооперационным уровнем, минимальные осложнения и сроки госпитализации.
Цель исследования
Оценка непосредственных и отдаленных онкологических результатов и качества жизни пациентов группы умеренного риска РПЖ после проведенной брахитерапии с использованием источников I-125.
Материалы и методы
В период с 01.01.2004 по 01.01.2014 в Российском онкологическом научном центре им. Н. Н. Блохина была выполнена брахитерапия 321 больному, из которых 86 соответствовали критериям РПЖ умеренного риска по D’Amico. Все они имели морфологически подтвержденный рак предстательной железы. Медиана возраста составила 66 лет (от 48 до 76). ПСА колебался в пределах от 10 до 20 нг/мл у 50 (58,1%) пациентов, у 36 (41,9%) больных составлял ≤ 10 нг/мл. Стадия Т1с зарегистрирована у 16 (18,6%) больных, Т2а (67,4%) – у 58, Т2b (14%) – у 12 пациентов. Распределение согласно градации по шкале Глисона было следующим: ≤ 6 баллов у 74 (86,0%) пациентов, 7 баллов – у 12 (14%).
Из 86 пациентов 24 (27,9%) проводилась неоадъювантная гормонотерапия с целью уменьшения объема простаты при исходном V > 50 мл. Основными методами гормонотерапии были агонисты ЛГРГ, антиандрогены либо их сочетание (МАБ); длительность применения препаратов до момента имплантации радиоактивных источников составила 2–6 мес.
Всем пациентам до оперативного вмешательства с целью исключения метастатического процесса выполнялось УЗИ органов брюшной полости, забрюшинного простран-
Таблица1.
Параметр Значение
|
Медиана возраста (годы) |
66 (48–76) |
|
Значение ПСА |
|
|
≤ 10 нг/мл |
36 (41,9%) |
|
10–20 нг/мл |
50 (58,1%) |
|
Т1с |
16 (18,6%) |
|
Т2а |
58 (67,4%) |
|
Т2b |
12 (14%) |
|
Сумма Глисона ≤ 6 |
74 (86%) |
|
Сумма Глисона = 7 |
12 (14%) |
Таблица 2.
На момент выполнения брахитерапии медиана ПСА составила 11,08 нг/мл, средний объем предстательной железы – 37,2 см3. Под УЗ-контролем всем больным была проведена имплантация источников I-125 на фиксирующей нити с активностью на день введения от 0,33 до 0,7 mCi. Дозиметрическое планирование осуществлялось с помощью программного обеспечения PSID и происходило в он-лайн режиме. В зависимости от объема предстательной железы и активности источников каждому пациенту было имплантировано от 35 до 130 зерен. Суммарная очаговая доза на предстательную железу у всех пациентов составила 145 Gy. Общая активность колебалась от 16,5 до 50,6 мКи. Доля предстательной железы, получившая 100% дозы, составила в среднем 98% (94,2–100%). Доза, полученная 90% объема предстательной железы (рD90), колебалась от 152,8 до 188,8 Гр (медиана 172,4 Гр). Медиана дозы на 1% поверхности уретры (uD1) составила 206,8 Гр, uD10 – 195,3 Гр; Медиана дозы на 1% поверхности прямой кишки (rD1) – 173,4 Гр, rD10 – 149,5 Гр. Среднее время операции составило 75 (40–180) минут. Проведенный дозиметрический контроль показал полное соответствие НРБ-99 и ОСПОРБ-99.
Послеоперационный контроль ПСА проводился каждые 3 мес. в течение первого года, затем каждые 6 мес. в течение 3 лет и далее ежегодно. Биохимическим рецидивом считали повышение уровня ПСА ≥ 2 нг/мл
Брахитерапия с использованием источников I-125 у больных группы умеренного риска от надира. Выживаемость оценивалась по методу Каплана-Майера. Оценка субъективных показателей качества жизни была проведена при помощи стандартизованных анкет IPSS.
Результаты
Полученные непосредственные и отдаленные результаты были оценены у 86 пациентов. Медиана наблюдения – 60 мес. (34–156 мес.). За время наблюдения прогрессирование основного заболевания в изучаемой группе наблюдалось у 7 больных, 3 пациента умерло в связи с прогрессированием онкологического заболевания другой локализации (рак легкого, рак толстой кишки, рак поджелудочной железы).
После проведенной брахитерапии пациенты выписывались из стационара на вторые сутки. Интраоперационных осложнений не было. Все пациенты получали поддерживающую терапию с использованием антибактериальных, противовоспалительных препаратов, альфа-адреноблокаторов в течение 3-х первых месяцев послеоперационного периода, что позволило практически избежать острой задержки мочи (в нашем исследовании частота ОЗМ составила 6%) и снизить до минимума дизурические явления в оцененной группе пациентов. Оценка осложнений выполненного лучевого лечения показала, что уретрит 1–2 степени по категории RTOG в течение 1 мес. после операции развился у 60 (69,3%) пациентов, при этом к 6-месячному сроку наблюдения симптомы дизурии оставались у 11 (13,3%) больных, что было ассоциировано с хронической мочевой инфекцией, устойчивой к антибактериальной терапии. Уретрит 3 степени был зафиксирован у 3 (3%) пациентов в течение первого месяца и сохранился у одного (1,1 %) из них через полгода наблюдения. Лучевой ректит 1 степени в течение 1 мес. после операции развился у 2 (2,1%) пациентов, при этом к 6-месячному сроку наблюдения симптомы ректита были купированы у всех больных. Выполненная через 1 мес. после имплантации компьютерная томография с последующей дозиметрией показала удовлетворительное (D90 > 145 Gy) дозное распределение у всех больных (рис. 1).
Результаты лечения оценивались: по уровню ПСА, клиническим и радиологическим проявлениям заболевания, оценке качества мочеиспускания по международной шкале IPSS.
К моменту начала лечения уровень общего ПСА колебался в пределах от 10 до 20 нг/мл у 50 (58,1%) больных, у 36 (41,9%) пациентов ≤ 10 нг/мл. Через 3 мес. после окончания лечения уровень общего ПСА в 97% не превышал 4 нг/мл (медиана 1,76 нг/мл); через 6 мес. зафиксирован уровень ПСА 1,5 нг/мл; 9 и 12 мес. у большинства пациентов ПСА был не выше 1 нг/мл (рис. 2).
70,00%
60,00%
50,00%
40,00%
30,00%
20,00%
10,00%
0,00%
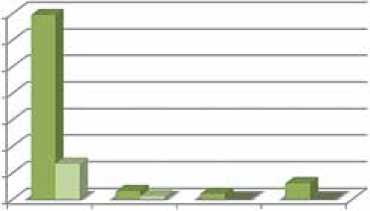
■ 1 мес
6 мес
Уретрит Уретрит Ректит ОЗМ 1–2 ст 3 ст 1ст
Рисунок 1. Лучевые осложнения RTOG
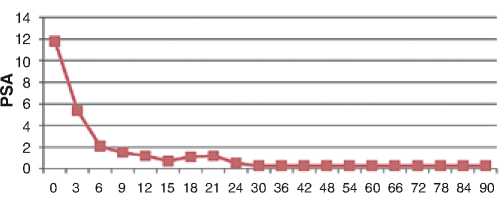
Рисунок 2. Изменение уровня ПСА после брахитерапии
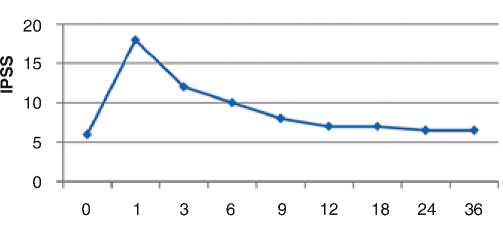
Рисунок 3. Изменение уровня IPSS после брахитерапии
Таблица 3. Анализ 5-летней выживаемости
5-ти летняя выживаемость
Общая 95,2%
Болезнь-специфическая 100%
Без клинического рецидива 92,9%
Без биохимического рецидива 90,5%
Вместе с тем у части пациентов наблюдался небольшой скачок ПСА через 15–24 мес. после проведения брахитерапии (так называемый PSA-bounce). Данный феномен не связан с прогрессированием заболевания и может возникать в течение первых трех лет после ЛТ. Вследствие этого биохимический рецидив диагностируется только при повышении уровня ПСА на 2 нг/мл по сравнению с минимальным достигнутым значением (надир) в соответствии с рекомендациями ASTRO [5].
До начала лечения объем предстательной железы у 24 больных был более 50 мл. С целью его уменьшения
84 месяцев 84,1% ± 6,0
Рисунок 4. Общая безрецидивная выживаемость в группе умеренного прогноза
36 месяцев 100%
60 месяцев 100%
84 месяцев 95,2%± 4,6
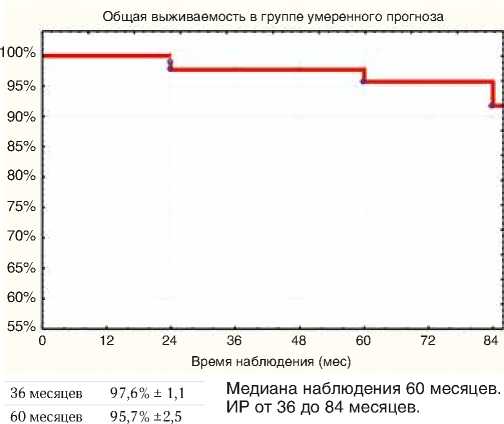
84 месяцев 91,7% ±4,5
Рисунок 5. Общая выживаемость в группе умеренного прогноза
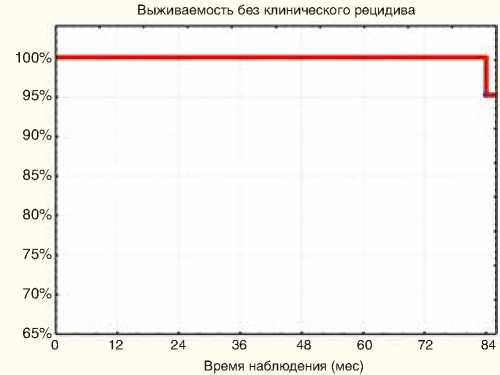
Рисунок 6. Выживаемость без клинического рецидива в группе умеренного прогноза
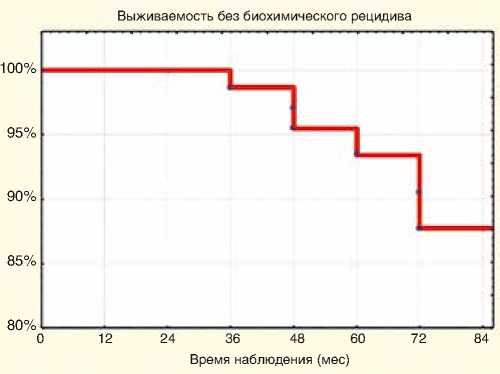
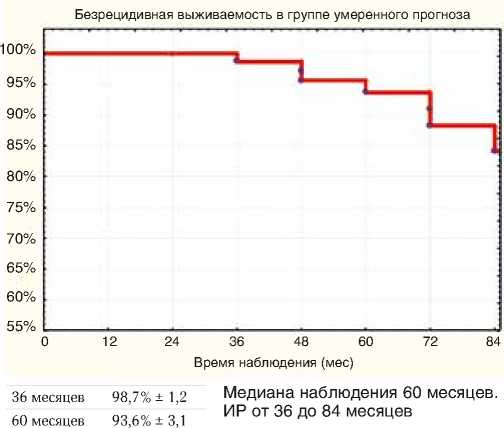
36 месяцев 98,6% ± 1,3
60 месяцев 93,4% ± 3,2
84 месяцев 87,7% ± 4,9
Рисунок 7. Выживаемость без биохимического рецидива в группе умеренного прогноза
этим пациентам (27,9%) проводилась неоадъювантная гормонотерапия агонистами ЛГРГ, антиантдрогенами или их комбинацией (МАБ) в течение 2–6 мес., что позволило снизить объем ПЖ в среднем на 36,1% и уровень ПСА – на 84,5%.
До проведенного лечения количество баллов по шкале IPSS составило 0–7 баллов – n=63 (74%), 8–19 баллов – n=23 (26%) (медиана IPSS 5,7). Через 1 мес. число пациентов с умеренной симптоматикой увеличилось до 69,3%, через 6 мес. после окончания лечения среднее значение IPSS составило 10 баллов. Через 12 мес. 0–7 баллов зарегистрировано у 94% пациентов (рис. 3).
Оценка отдаленных результатов лечения производилась путем расчета безрецидивной, болезнь-специ- фической, общей выживаемости. Анализ результатов показал, что при медиане послеоперационного наблюдения 60 мес. общая выживаемость составила 95,2%, без биохимического рецидива выявлено 90,5% пациентов, без клинического рецидива – 92,9 %, болезнь-спец-ифическая выживаемость – 100% (табл. 3, рис. 4–7).
Был проведен регресионный анализ для оценки влияния на выживаемость без ПСА-рецидива следующих факторов: D90 на предстательную железу, V100 предстательной железы, предоперационная ГТ, сумма Глисона (рис. 8–11). Согласно данному анализу ни один из перечисленных факторов не оказывал достоверного влияния на результаты лечения.
Брахитерапия с использованием источников I-125 у больных группы умеренного риска
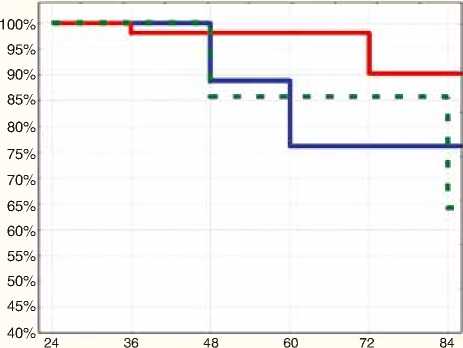
Время наблюдения (мес)
Глисон = 5 74,6%
Глисон = 6 98,01%
Глисон = 7 84,6% p = 0,233, различия статистически не значимы
D90 (Гр)
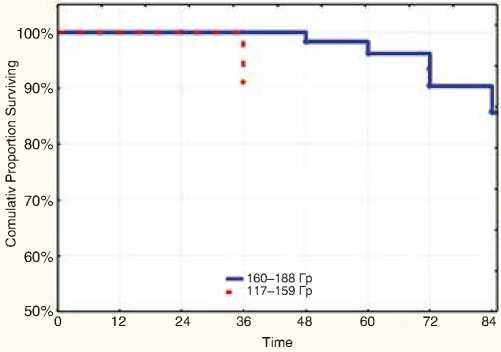
р=0,615, различия статистически незначимы
Рисунок 11. Безрецидивная выживаемость в зависимости от D90
Рисунок 8. Безрецидивная выживаемость в зависимости от суммы Глисона
Безрецидивная выживаемость в зависимости от гормонотерапии
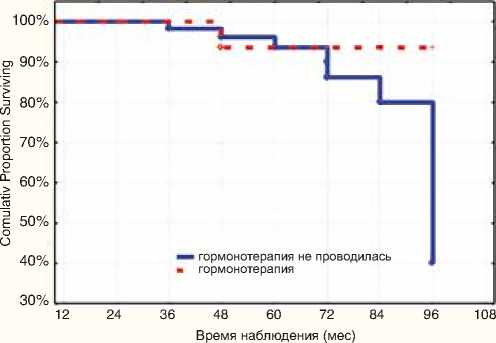
р=0,250, различия статистически незначимы. Медиана наблюдения 60 месяцев. ИР от 36 до 84 месяцев
Рисунок 9. Безрецидивная выживаемость в зависимости от проведения неоадъювантной гормонотерапии
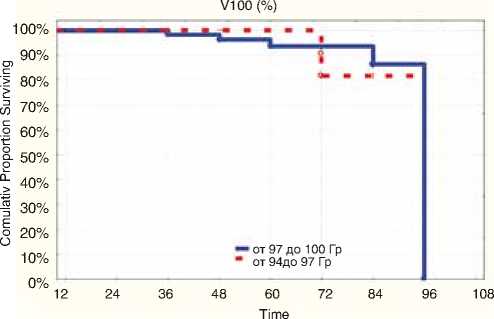
р=0,725, различия статистически незначимы
Рисунок 10. Безрецидивная выживаемость в зависимости от V100
Обсуждение
В последние годы выбор метода лечения больных группы умеренного риска РПЖ продолжает оставаться крайне актуальным вопросом. Хирургическое лечение не всегда возможно вследствие возраста пациента, наличия выраженных сопутствующих патологий, вероятности послеоперационных осложнений. Дистанционная лучевая терапия также имеет ограничения в применении: подведение высоких доз сопряжено с повышением риска осложнений со стороны мочевого пузыря, прямой кишки. В связи с этим требуется прицельный малоинвазивный метод с сохранением высокого качества жизни пациента. Таким методом является брахитерапия – эффективный способ лечения локализованного РПЖ, обеспечивающий отличные онкологические результаты.
Так, согласно данным мета-анализа, включающим результаты более 1400 опубликованных исследований [6], брахитерапия в качестве монотерапии обеспечивает сравнимый результат с РПЭ и ДЛТ при оценке выживаемости без биохимического рецидива. Многочисленные клинические исследования доказали безопасность и эффективность брахитерапии [7,8], в том числе радиационной онкологической группой (RTOG) [9,10].
Так, используя низкодозную брахитерапию в монорежиме в группе пациентов с промежуточным риском, J. C. Blasko с соавт. отметили 9-летнюю БРВ 82% [11]. В работе L. Potters и соавт. 12-летняя выживаемость без прогрессирования составила почти 80%. [12]. Эффективность брахитерапии в монорежиме подтвердила и группа во главе с N. N. Stone – 12-летняя БРВ 79,2% [13]. Таким образом, анализ ряда исследований низко-дозной брахитерапии у больных раком предстательной железы показывает, что 5-летний показатель безреци- дивной выживаемости находится в диапазоне от 71% до 93% и 10-летний – от 65% до 85% [14–19], что соответствует таковым показателям при применении как РПЭ, так и ДЛТ в сочетании с краткосрочной ГТ.
В результате проведенного нами исследования оценка отдаленных результатов показала, что безрецидивная выживаемость составляет 90,5%, что сопоставимо или даже несколько выше, чем в описанных исследованиях.
Специфическим осложнением, возникающим при данном виде оперативного вмешательства, является самостоятельная миграция источников после их установки, вследствие чего реальное распределение дозы может отличаться от запланированного. Поэтому через 1 мес. после имплантации была выполнена дозиметрия, которая показала удовлетворительное дозное распределение у всех больных.
Кроме того, ввиду анатомических особенностей расположения предстательной железы воздействие на нее механических и физических методов лечения может привести к значительным осложнениям со стороны мочеполовой системы. Задержка и недержание мочи, воспаления мочевых путей, эректильная дисфункция – наиболее частые осложнения, возникающие на фоне или после проведенного лечения.
Примерно у 2–4% пациентов наблюдается дизурия, требующая в дальнейшем катетеризации либо наложения эпи-цистостомы. В проведенном исследовании уретрит 1 степени в течение 1 мес. после операции развился у 60 (69,3%) пациентов, однако в течение короткого периода времени (уже к 6-месячному сроку наблюдения) симптомы дизурии остались только у 11 (13,3%). Установлено, что прогностическими факторами развития острой задержки мочеиспускания являются объем предстательной железы и индекс
IPSS, в то время как доза облучения не увеличивает частоту данного осложнения [20], что совпадает с результатами нашего исследования. При проведении оценки влияния на возникновение лучевых повреждений такого фактора, как D1 на уретру, в нашем исследовании статически значимых данных получено не было.
Согласно проведенному нами анализу такие показатели, как D90 на предстательную железу, V100 предстательной железы, предоперационная антиандрогенная терапия и сумма Глисона по отдельности не оказывают влияния на общие показатели выживаемости. Это можно объяснить небольшим количеством больных (всего 86 пациентов), а также полученными высокими показателями выживаемости. Дальнейшее накопление клинических и дозиметрических данных позволит выявить новые прогностические факторы, влияющие на лечение больных раком предстательной железы с использованием постоянных имплантатов.
Заключение
Таким образом, выполнение низкодозной брахитерапии постоянными источниками I-125 у больных умеренной группы риска обеспечивает очень хорошие функциональные и онкологические результаты. Данный метод обеспечивает отличный контроль уровня ПСА при медиане наблюдения 65 мес., характеризуется низким уровнем осложнений, при этом обеспечивая высокое качество мочеиспускания в отдаленные сроки после лечения, а также короткими сроками пребывания в стационаре и реабилитации больных после вмешательства.
Список литературы Брахитерапия с использованием источников I-125 у больных группы умеренного риска
- Ferlay J. et al. Cancer incidence and mortality worldwide: sources, methods and major patterns in GLOBOCAN 2012, Int. J. Cancer, 2015, Vol. 136, E359.
- Злокачественные новообразования в России в 2015 году (заболеваемость и смертность). Под ред. А. Д. Каприна, В. В. Старинского, Г. В. Петровой. М.: МНИОИ им. П.А. Герцена, филиал ФГБУ «НМИРЦ» Минздрава России. 2017. 250 с. ISBN 978-5-85502-227-8.
- Cooperberg M. R. et al. The University of California, San Francisco Cancer of the Prostate Risk Assessment score: a straightforward and reliable preoperative predictor of disease recurrence after radical prostatectomy, J. Urol., 2005, Vol. 173, p. 1938.
- http://oncology-association.ru/docs/recomend/may2015/39vz-rek.pdf.
- Heidenreich A. et al. Рак предстательной железы Перевод: О. В. Антонова. Научное редактирование: Б. Я. Алексеев, К. М. Нюшко//ЕАУ. 2010. -Modeofaccess: http://www.uroweb.org/gls/pdf/russian/3_Prostate_Cancer.pdf. Dateofaccess: 06.03.2013.
- Grimm P., Billiet I., Bostwick D. et al. Comparative analysis of prostate-specific antigen free survival outcomes for patients with low, intermediate and high risk prostate cancer treatment by radical therapy. Results from the Prostate Cancer Results Study Group, BJU Int., 2012 Feb, Vol. 109, Suppl. 1, pp. 22-29.
- Lee W. R., DeSilvio M., Lawton C., Gillin M., Morton G., Firat S., Baikadi M., Kuettel M., Greven K., Sandler H. A phase II study of external beam radiotherapy combined with permanent source brachytherapy for intermediate-risk, clinically localized adenocarcinoma of the prostate: Preliminary results of RTOG P-0019, Int. J. Radiat. Oncol. Biol. Phys., 2006, Vol. 64, No. 3, pp. 804-809.
- Feigenberg S. J., Lee W. R., Desilvio M. L., Winter K., Pisansky T. M., Bruner D. W., Lawton C., Morton G., Baikadi M., Sandler H. Health-related quality oflife in men receiving prostate brachytherapy on RTOG 98-05, Int. J. Radiat. Oncol. Biol. Phys., 2005, Vol. 62, No. 4. pp. 956-964
- Crook J. M., Gomez-Iturriaga A., Wallace K., Ma C., Fung S., Alibhai S., Jewett M., Fleshner N. Comparison of health-related quality of life 5 years aer SPIRIT: Surgical Prostatectomy Versus Interstitial Radiation Intervention, Trial. J. Clin. Oncol., 2011, Vol. 29, No. 4, pp. 362-368
- Hurwitz M. D., Halabi S., Ou S. S., McGinnis L. S., Keuttel M. R., Dibiase S. J., Small E. J. Combination external beam radiation and brachytherapy boost with androgen suppression for treatment of intermediate-risk prostate cancer: An initial report of CALGB 99809, Int. J. Radiat. Oncol. Biol. Phys., 2008, Vol. 72, No. 3, pp. 814-819.
- Blasko J. C., Grimm P. D., Sylsvester J. E., Cavanagh W. The role of external beam radiotherapy with I-125/Pd-103 brachytherapy for prostate carcinoma, Radiother. Oncol., 2000, Vol. 57 (3), pp. 273-278.
- Potters L., Morgenstern C., Calugaru E. et al. 12-year outcomes following permanent prostate brachytherapy in patients with clinically localized prostate cancer. J. Urol., 2005, Vol. 173 (5), pp. 1562-1566.
- Stone N.N., Stone M. M., Rosenstein B. S. et al. Influence of pretreatment and treatment factors on intermediate to long-term outcome after prostate brachytherapy, J. Urol., 2011, Vol. 185 (2), pp. 495-500.
- Grimm P. D., Blasko J. C., Sylvester J. E. et al. 10-year biochemical (prostate-specific antigen) control of prostate cancer with 125-I brachytherapy, Int. J. Radiat. Biol. Phys., 2001, Vol. 51 (1), pp. 31-40.
- Potters L., Klein E. A., Kattan M. W. et al. Monotherapy for stage T1-T2 prostate cancer: radical prostatectomy, external beam radiotherapy, or permanent seed implantation, Radiother. Oncol., 2004, Vol. 71 (1), pp. 29-33.
- Sylvester J. E., Blasko J. C., Grimm R. et al. Fifteen year follow-up of the first cohort of localized prostate cancer patients treated with brachytherapy, J. Clin. Oncol., 2004, Vol. 22 (14), pp. 45-67.
- Stone N.N., Stock R. G., Unger P. Intermediate term biochemical-free progression and local control following 125-iodine brachytherapy for prostate cancer, J. Urol., 2005, Vol. 173 (3), pp. 803-807.
- Lawton C. A., DeSilvio M., Lee W. R. et al. Results of a phase II trial of transrectal ultrasound-guided permanent radioactive implantation of the prostate for definitive management of localized adenocarcinoma of the prostate (RTOG 98-05), Int. J. Radiat. Oncol. Biol. Phys., 2007, Vol. 67 (1), pp. 39-47.
- Grimm P. D., Blasko J. C., Sylvester J. E. et al. 10-year biochemical (prostate-specific antigen) control of prostate cancer with 125-I brachytherapy, Int. J. Radiat. Biol. Phys., 2001, Vol. 51 (1), pp. 31-40.
- Roeloffzen E. M., Battermann J. J., van Deursen M. J. et al. Influence of dose on risk of acute urinary retention after iodine-125 prostate brachytherapy, Int. J. Radiation. Oncology. Biol. Phys., 2011, Vol. 80, pp. 1072-1079.


