Бронхопластические операции в лечении больных немелкоклеточным раком лёгкого
Автор: Аксарин А.А., Тер-ованесов М.Д., Копейка С.М.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Опыт работы онкологических учреждений
Статья в выпуске: 1 т.21, 2022 года.
Бесплатный доступ
Цель исследования - изучить отдалённые результаты органосохраняющих бронхопластических операций у больных немелкоклеточным раком лёгкого. Материал и методы. Проанализированы результаты хирургического лечения 740 больных с немелкоклеточным раком лёгкого i-iii стадии в Югре с 2002 по 2015 г. Лоб- и билобэктомия выполнены 477 больным, пневмонэктомия - 263, бронхопластическая лобэктомия - 32 пациентам. Всем больным проводилось срочное интраоперационное гистологическое исследование долевых лимфоузлов (12-я группа) остающейся доли лёгкого. При отсутствии метастатического поражения данной группы лимфоузлов выполняли бронхопластическую лобэктомию. При наличии метастазов в 12-й группе лимфоузлов остающейся доли выполняли пневмонэктомию. Все бронхопластические органосохраняющие операции выполнены больным мужского пола. Средний возраст - 55,3 ± 9,9 года. В 19 (59,4 %) случаях операции выполнялись справа, в 13 (40,6 %) - слева. Бронхопластических лобэктомий типа a выполнено 15, типа В - 9, типа С - 4 и типа d - 4 пациентам. У 4 больных выполнена циркулярная резекция лёгочной артерии. В 16 случаях (50,0 %) отсутствовали регионарные метастазы (pN0), pN1 отмечена в 19 (31,3 %), pN2 - в 6 (18,7 %) случаях. результаты. Послеоперационной летальности при бронхопластических лобэктомиях не было. В отдалённом периоде у 3 (9,4 %) пациентов развился умеренный стеноз бронхиального анастомоза. При органосохраняющих операциях с бронхопластическим компонентом отдалённые результаты были лучше, чем при пневмонэктомии. Медиана выживаемости после бронхопластических лобэктомий составила 66 мес, после пневмонэктомий - 34 мес (p=0,01). Общая выживаемость при бронхопластических лобэктомиях: 5-летняя - 52,9 %, 10-летняя - 36,2 %; при пневмонэктомиях - 38,0 и 31,9 % соответственно. заключение. Органосохраняющие бронхопластические операции при хирургическом лечении больных НМРЛ, при соблюдении онкологических принципов, по сравнению с пневмонэктомией не ухудшают отдалённые результаты.
Немелкоклеточный рак лёгкого, хирургическое лечение, бронхопластическая лобэктомия, отдалённые результаты
Короткий адрес: https://sciup.org/140290560
IDR: 140290560 | УДК: 616.24-006.6-089:616.23-089.87 | DOI: 10.21294/1814-4861-2022-21-1-85-90
Bronchoplatic surgery in the treatment of patients with non-small cell lung cancer
Aim. to study the effect of organ-preserving bronchoplastic surgery on long-term treatment outcomes of patients with non-small cell lung cancer (Nsclc). material and methods. the long-term results of surgical treatment of 740 patients with stage i-iii Nsclc, who were treated in ugra from 2002 to 2015, were analyzed. lobectomy and bilobectomy were performed in 477 patients, and pneumonectomy was performed in 263 patients. thirty-two patients underwent bronchoplastic lobectomy and bilobectomy. intraoperative pathological frozen sections of lymph nodes (# 12) of the remaining lobe of the lung were examined in all patients. if metastases in these lymph nodes were not detected, we performed bronchoplastic lobectomy. if metastases in lymph nodes of the remaining lobe were detected, we performed pneumonectomy. the median age of the patients (only male patients) was 55.3 ± 9.9 years. in 19 (59.4 %) patients, sleeve resections were performed on the right side and in 13 (40.6 %) patients, these resections were performed on the left side. there were 15 bronchoplastic lobectomies of type a, 9 of type B, 4 of type c, and 4 of type d. sleeve resection of the pulmonary artery was performed in 4 patients. in 16 cases (50.0 %), there were no regional metastases (pN0). in 10 (31.3 %) cases, there was pN1, in six - pN2 (18.7 %). Results. there were no cases of postoperative death. late complications (asymptomatic bronchial stenosis) occurred in 3 (9.4 %) patients. long-term treatment outcomes were better in patients who underwent organ-preserving bronchoplastic surgery than in patients who underwent pneumonectomy. median survival was 66 months after bronchoplastic lobectomies and 34 months after pneumonectomies (p=0.01). the 5- and 10-year survival rates in patients who underwent bronchoplastic lobectomies were 52.9 % and 36.2 %, respectively. the corresponding values in patients who underwent pneumonectomies were 38.0 % and 31.9 %, respectively. conclusion. organ-preserving bronchoplastic surgery compared to pneumonectomy does not worsen long-term outcomes in patients with Nsclc.
Текст научной статьи Бронхопластические операции в лечении больных немелкоклеточным раком лёгкого
Рак лёгкого (РЛ) – одна из главных медицинских и социальных проблем современной онкологии. Чрезвычайно высокий уровень заболеваемости (свыше 2 млн в год) и самый высокий уровень смертности среди онкологических больных (свыше 1,8 млн в год) требуют всестороннего подхода к решению этой медико-социальной проблемы. Несмотря на то, что в целом в Российской Федерации замедлился рост заболеваемости РЛ, в ряде экологически неблагополучных территорий наблюдается неуклонный рост рака лёгкого [1]. К таким территориям относится Югра. Стандартизованный показатель заболеваемости раком лёгкого в Югре в 2019 г. составил 30,5 на 100 тыс населения, в то время как в РФ – 22,7 на 100 тыс. [1].
Свыше 70 % вновь диагностированных случаев рака лёгкого приходится на распространённую и местнораспространённую стадии (III и IV стадии). Основными операциями при РЛ являются лобэктомия и пневмонэктомия с систематической лимфодис-секцией. Бронхопластическая лобэктомия является альтернативой пневмонэктомии при центральном
РЛ, особенно при немелкоклеточном раке лёгкого (НМРЛ). Во многих публикациях представлены благоприятные результаты бронхопластических лобэктомий, которые определялись отдалёнными результатами, сопоставимыми с пневмонэктомией, при низких показателях послеоперационной летальности. Бронхопластическая лобэктомия также связана с улучшением качества жизни за счёт сохранения паренхимы легких [2–11]. Однако проспективных рандомизированных исследований, сравнивающих бронхопластическую лобэктомию и пневмонэктомию, не проводилось [12–17]. Таким образом, идеальная хирургическая процедура для центрально расположенного НМРЛ оставалась спорной, а показания зависели от каждого случая и, в частности, от оперирующего хирурга.
Цель исследования – изучить отдалённые результаты бронхопластических операций у больных немелкоклеточным раком лёгкого.
Материал и методы
С 1999 по 2015 г. в Югре впервые зарегистрировано 6349 больных со злокачественными новообразованиями лёгких. Распространенность опухолей по стадиям TNM у всех больных была определена по классификации Международного противоракового союза (UICC). В исследование были включены 740 больных с немелкоклеточным раком лёгкого IА – IIIB стадий, которым выполнили радикальные хирургические вмешательства в объёме лобэктомии, билобэктомии и пневмонэктомии с различными вариантами медиастинальной лимфодиссекции. У 477 больных выполнены лоб- и билобэктомии, у 263 – пневмонэктомия. Наблюдение за отдалёнными результатами осуществлялось в сроки до 01.01.2021.
Кроме «типичных» вмешательств, у 101 (13,6 %) пациента с НМРЛ были выполнены комбинированные операции, которые были условно разделены на три типа: трахеобронхопищеводные, сосудистопредсердные и париетально-диафрагмальные. У 5 больных выполнены комбинированные операции с резекцией разных соседних органов. Таким образом, всего выполнено 106 комбинированных операций у 101 пациента. Больше всего было комбинированных операций сосудисто-предсердного типа – 52. Париетально-диафрагмальных операций – 14. Трахеобронхопищеводных операций –
-
40, у одного пациента при прорастании опухоли в пищевод потребовалась его резекция. Случаи с резекцией трахеи не включались в исследование, так как они сопровождались пневмонэктомией.
У 32 пациентов выполнены органосохраняющие бронхопластические операции (табл. 1). Показанием для циркулярной резекции главного бронха являлись опухоли устья долевого бронха или опухоли, распространяющиеся по главному бронху на устье долевого бронха с соседней доли. Окончательное решение о возможности выполнения циркулярной резекции бронха или артерии принималось интраоперационно. Всем больным, которым выполнялись бронхопластические операции, проводили срочное интраоперационное гистологическое исследование долевых лимфоузлов (12-я группа) остающейся доли лёгкого. При отсутствии метастатического поражения 12-й группы лимфоузлов выполняли лоб- либо билобэктомию с бронхопластикой. При наличии метастазов в 12-й группе лимфоузлов остающейся доли выполняли пневмонэктомию. После удаления доли проводили срочное гистологическое исследование краёв резекции бронха.
Бронхопластические органосохраняющие операции выполнены больным мужского пола. Сред- таблица 1/table 1
Общая характеристика пациентов с бронхопластическими лобэктомиями patient characteristics with bronchoplastic lobectomy
У подавляющего числа больных (78,2 %) морфологическая структура опухоли представлена плоскоклеточным раком. Аденокарцинома была у 4 (12,5 %) пациентов, крупноклеточный рак – у 2 (6,2 %), аденосквамозный рак – у 1 (3,1 %). У 2 пациентов после планового исследования гистологического материала выявлены опухолевые клетки по краю резекции (R1). Им проведена адъювантная лучевая терапия.
При формировании межбронхиального анастомоза на мембранозную часть бронхов накладывали непрерывный шов, на хрящевую часть – узловые швы. При большом различии в диаметре бронхов применяли методику телескопического анастомоза и гофрирующие швы на мембранозную часть главного бронха.
В работе использовали следующие типы бронхопластических операций: тип A, B, C, D в модифицированной классификации M. Okada (R. Waseda et al.) [15]. Бронхопластическая лобэктомия типа A осуществлена у 15 (46,9 %) больных, из них у 13 с локализацией опухоли в верхнедолевом бронхе справа и поражением главного бронха выполнена верхняя лобэктомия с резекцией правого главного бронха и наложением анастомоза между главным бронхом и промежуточным бронхом. Двоим больным с раком среднедолевого бронха и распространением опухоли по промежуточному бронху на верхнедолевой бронх справа выполнена верхняя билобэктомия с резекцией главного и промежуточного бронхов и наложением анастомоза между главным и нижнедолевым бронхом. У двух больных из этой группы также выполнена циркулярная резекция лёгочной артерии из-за прорастания метастатически поражённых лимфоузлов в артерию. У одного из них также выполнена циркулярная резекция лёгочной артерии из-за прорастания опухоли в артерию.
Бронхопластические лобэктомии типа B осуществлены у 9 (28,1 %) пациентов при центральном раке левого верхнедолевого бронха с переходом на левый главный бронх. После резекционного этапа наложен анастомоз между главным бронхом и нижнедолевым бронхом. У 2 больных выполнена циркулярная резекция лёгочной артерии.
У 4 (12,5 %) больных выполнены бронхопластические лобэктомии типа С. При раке нижней доли левого лёгкого с переходом на главный бронх произведена нижняя лобэктомия с циркулярной резекцией главного бронха и наложением анасто- моза между главным бронхом и верхнедолевым бронхом.
Бронхопластическая лобэктомия типа D выполнена у 4 (12,5 %) пациентов. При распространении опухоли нижнедолевого бронха справа по промежуточному на устье верхнедолевого бронха произведена нижняя билобэктомия с резекцией главного бронха и наложением анастомоза между главным бронхом и верхнедолевым бронхом.
Каждый тип бронхопластической операции имеет свои особенности. Операции типа А и В обычно требуют протяжённой резекции бронхов от уровня правого главного бронха до устья B6 или бронхов базальной пирамиды. Для профилактики осложнений со стороны анастомоза требуется уменьшение натяжения. Для этого мы выполняли освобождение перибронхиальных тканей и рассекали перикард вокруг нижней легочной вены. При операциях типа C и D всегда накладывали телескопический анастомоз и гофрирующие швы на мембранозную часть главного бронха. При наложении межбронхиальных анастомозов использовали васкуляризированные лоскуты для профилактики несостоятельности: лоскут медиастинальной плевры с клетчаткой, лоскут перикарда, межрёберный мышечный лоскут либо лоскут из диафрагмы.
У 25 (78,1 %) больных выполнена систематическая лимфодиссекция, у 4 (12,5 %) – селективная лимфодиссекция, у 3 (9,4 %) лимфодиссекция не производилась. Хирургический метод лечения применён у 12 (37,5 %) больных. Адъювантная химиотерапия назначалась 18 (56,3 %) пациентам, 5 из них также проведена лучевая терапия. 2 пациентам проведена адъювантная лучевая терапия.
Статистическая обработка данных и анализ результатов исследования выполнены в программе IBM SPSS Statistics 20. Показатель вариабельности ± m представляет среднеквадратическое отклонение. Отдалённые результаты оценены по лог-ранговому критерию (log rank, Mantel-Cox).
Результаты и обсуждение
В 3 (9,4 %) случаях послеоперационный период протекал с осложнениями. У 1 пациента развилась тромбоэмболия мелких ветвей лёгочной артерии. У 2 больных послеоперационный период осложнился пневмонией оставшейся доли лёгкого. Во всех случаях проведено успешное консервативное лечение. Послеоперационной летальности при бронхопластических операциях не было.
В отдалённом периоде у 3 (9,4 %) пациентов развился умеренный стеноз бронхиального анастомоза, из них в 2 случаях проводилась адъювантная лучевая терапия. Дополнительных лечебных мероприятий данные нежелательные явления не потребовали, так как клинических проявлений стеноза не было. У 3 (9,4 %) пациентов развились локорегионарные рецидивы: у 2 – в межбронхиальном анастомозе (R1), у 1 – в средостении.
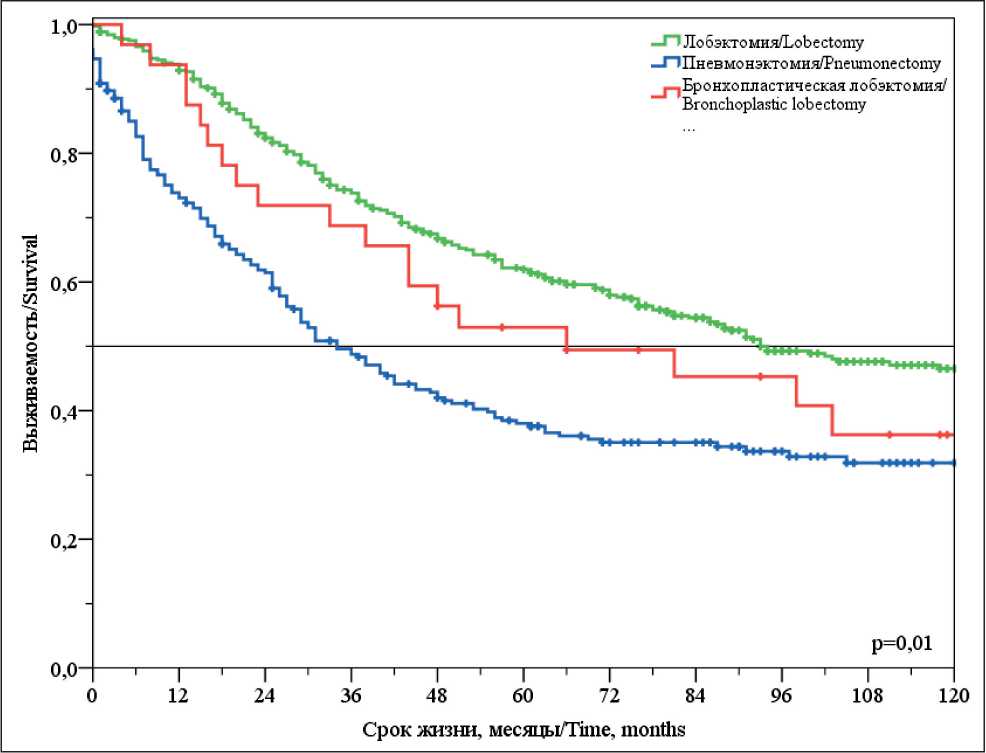
Рис. 1. Общая выживаемость больных НМРЛ с бронхопластическими лобэктомиями
Fig. 1. Overall survival of patients with NSCLC with bronchoplastic lobectomy
Общая десятилетняя выживаемость у пациентов с бронхопластическими лобэктомиями зависела от стадии заболевания: при IA стадии данный показатель составил 66,7 %, при IB стадии – 55,6 %, IIB стадии – 40,0 %, IIIA стадии – 28,6 %. Единственный пациент сo IIA стадией прожил 33 мес. При IIIB стадии максимальный срок жизни составил 15 мес. На общую выживаемость существенное влияние оказывало наличие регионарных лимфогенных метастазов. Общая 5- и 10-летняя выживаемость при pN0 составила 61,9 и 45,8 %, при pN1 – 50,0 и 26,7 % соответственно. При pN2 общая пятилетняя выживаемость составила 33,3 %.
При анализе отдалённых результатов отмечено, что при бронхопластических операциях эти показатели были значимо выше, чем при пневмонэктомии (log rank, p=0,01). Общая выживаемость при бронхопластических лобэктомиях составила: 5-летняя – 52,9 %, 10-летняя – 36,2 %, при пневмонэктомиях – 38,0 и 31,9 % соответственно (рис. 1).
Список литературы Бронхопластические операции в лечении больных немелкоклеточным раком лёгкого
- Мордовский А.А., Аксарин А.А., Парсаданян А.М., Тер-Ованесов М.Д., Троян П.П. Эпидемиологическая характеристика заболеваемости и смертности от рака легкого в Ханты-Мансийском автономном округе – Югре. Сибирский онкологический журнал. 2021; 20(4): 30–8. [Mordovsky A.A., Aksarin A.A., Parsadanyan A.M., Ter-Ovanesov M.D., Troyan P.P. Lung cancer incidence and mortality in the Khanty-Mansi autonomous okrug – Yugra. Siberian Journal of Oncology. 2021; 20(4): 30–8. (in Russian)]. doi: 10.21294/1814-4861-2021-20-4-30-38.
- Левченко Е.В., Левченко Н.Е., Юрин Р.И., Михнин А.Е., Ергнян С.М., Барчук А.С., Горохов Л.В., Слугин Е.Н., Гринкевич М.В. Отдалённые результаты бронхопластических оперативных вмешательств по сравнению с пневмонэктомиями при раке лёгкого. Вопросы онкологии. 2017; 63(2): 234–9. [Levchenko E.V., Levchenko N.E., Jurin R.I., Mihnin A.E., Ergnjan S.M., Barchuk A.S., Gorohov L.V., Slugin E.N., Grinkevich M.V. Long-term results of bronchoplastic surgical interventions in comparison with pneumonectomies in lung cancer. Problems in Oncology. 2017; 63(2): 234–9. (in Russian)].
- Решетов А.В., Елькин А.В., Николаев Г.В., Степанов С.С. Бронхо- и ангиопластическая лобэктомия как альтернатива пневмонэктомии в лечении немелкоклеточного рака легкого. Вестник хирургии им. И.И. Грекова. 2018; 177(3): 19–24. [Reshetov A.V., El’kin A.V., Nikolaev G.V., Stepanov S.S. Broncho- and angioplasty lobectomy as an alternative to pneumonectomy in treatment of non-small cell lung cancer. Grekov’s Bulletin of Surgery. 2018; 177(3): 19–24. (in Russian)]. doi: 10.24884/0042-4625-2018-177-3-19-24.
- Andersson S.E.M., Rauma V.H.S., Sihvo E.I., Rasanen J.V., Ilonen I.K., Salo J.A. Bronchial sleeve resection or pneumonectomy for non-small cell lung cancer: a propensity-matched analysis of long-term results, survival and quality of life. J Thorac Dis 2015; 7(10): 1742–8. doi: 10.3978/j.issn.2072-1439.2015.10.62.
- Berhet J.-P., Paradela M., Jimenez M.J., Molins L., Gomez-Caro A. Extended Sleeve Lobectomy: One More Step Toward Advoiding Pneumonectomy in Centrally Located Lung Cancer. Ann Thorac Surg. 2013; 96: 1988–97.
- D’Andrilli A., Maurizi G., Andreetti C., Ciccone A.M., Ibrahim M., Piraino A., Mariotta S., Venuta F., Rendina E.A. Sleeve Lobectomy Versus Standard Lobectomy for Lung Cancer: Functional and Oncologic Evaluation. Ann Thorac Surg. 2016; 101(5): 1936–42. doi: 10.1016/j.athoracsur.2015.11.057.
- Hishida T., Aokage K., Yoshida J., Miyoshi T., Tsuboi M. Extended bronchoplasty for locally advanced left lower lobe lung cancer: surgical technique and outcomes. Interact Cardiovasc Thorac Surg. 2018; 27(4): 602–5. doi: 10.1093/icvts/ivy081.
- Maurizi G., D’Andrilli A., Venuta F, Rendina E.A. Reconstruction of the bronchus and pulmonary artery. J Thorac Dis. 2016; 8: 168–80.
- Maurizi G., D’Andrilli A., Venuta F., Rendina E.A. Bronchial and arterial sleeve resection for centrally-located lung cancers. J Thorac Dis. 2016; 8: 872–81. doi: 10.21037/jtd.2016.06.48.
- Nagayasu T., Yamasaki N., Tsuchiya T., Matsumoto K., Miyazaki T., Hatachi G., Watanabe H., Tomoshige K. The evolution of bronchoplasty and broncho-angioplasty as treatments for lung cancer: evaluation of 30 years of data from a single institution. Eur J Cardiothorac Surg. 2016 Jan; 49(1): 300–6. doi: 10.1093/ejcts/ezv065.
- Okada M. [Bronchoplasty for lung cancer]. Nihon Geka Gakkai Zasshi. 2016; 117(4): 283–8.
- Rea F., Marulli G., Schiavon M., Zuin A, Hamad A-M., Rizzardi G., Perissinotto E., Sartori F. A quarter of a century experience with sleeve lobectomy for non-small cell lung cancer. Eur J Card Thorac Surg. 2008; 34: 488–92.
- Sarsam O.M., Dunning J., Pochulu B., Baste J.M. Robot-assisted bronchoplasty using continuous barbed sutures. J Vis Surg. 2018; 4(1): 3. doi: 10.21037/jovs.2017.12.14.
- Umeda Y., Marui T., Murakawa S., Matsumoto S. Our tips for bronchoplasty using suture holder and tourniquet. Gen Thorac Cardiovasc Surg. 2019; 67(4): 370–1. doi: 10.1007/s11748-018-01061-8.
- Waseda R., Iwasaki A. Extended sleeve lobectomy: its place in surgical therapy for centrally located non-small cell lung cancer and a review of technical aspects. J Thorac Dis. 2018; 10 (26): 103–8. doi: 10.21037/ jtd.2018.07.40.
- Yazgan S., Gursoy S., Ucvet A., Yagoi T., Unal M., Samancilar O., Erbaycu A.E. Long-term results of sleeve lobectomy with continuous suture technique in non-small cell lung cancer. Turk J Thorac Cardiovasc Surg. 2019; 27(1): 93–100. doi: 10.5606/tgkdc.dergisi.2019.16324.
- Yokota K., Okuda K., Fukai I., Nakanishi R. Extended Bronchoplasty Anastomosed between the Left Main and the Superior Segmental Bronchi for Locally Advanced Left Upper Lobe Lung Cancer with Invasion of the Basal Segment. Ann Thorac Cardiovasc Surg. 2020 Aug; 12(8): 4082–89. doi: 10.5761/atcs.cr.20-00215.


