Что определяет объем лимфодиссекции при раннем раке желудка?
Автор: Туркин И.Н., Давыдов М.И.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Клинические исследования
Статья в выпуске: 2 (56), 2013 года.
Бесплатный доступ
Стратегия хирургии больных ранним раком желудка остается предметом острой дискуссии. Основная причина разногласий – рациональный объем вмешательства на лимфатических коллекторах, а именно улучшает ли диссекция D2 результаты лечения раннего рака желудка? В представленной работе проведен анализ результатов лечения 394 больных, оперированных по поводу раннего рака желудка в период с 1990 по 2008 г. Установлено, что наличие основных факторов риска лимфогенного метастазирования у больных ранним раком желудка (лимфатическая инвазия, инвазия подслизистого слоя, размер опухоли более 4,0 см, венозная инвазия, переход опухоли на пищевод, макроскопические типы 0I и 0III, низкая степень дифференцировки) является показанием к выполнению лимфодиссекции D2. Ограничение объема до ЛД D1 обоснованно лишь при опухолях с ничтожным риском метастазирования – любом типе раннего рака независимо от степени дифференцировки размерами менее 1,0 см, внутрислизистом раке независимо от типа и степени дифференцировки менее 4,0 см, внутрислизистом раке высокой степени дифференцировки типа 0II независимо от размеров опухоли.
Ранний рак желудка, хирургическое лечение, объем перигастральной лимфодиссекции, отдаленные результаты
Короткий адрес: https://sciup.org/14056311
IDR: 14056311 | УДК: 616.33-006.6-089-035
What defines the extent of lymphodissection for early gastric cancer?
Surgery strategy for patients with early gastric cancer remains disputable. The main reason of controversy is the extent of surgical intervention, namely, whether D2 dissection improves treatment outcomes of early gastric cancer? The present study demonstrates treatment outcomes of 394 patients who underwent surgery for early gastric cancer between 1990–2008. The major risk factors for lymphogenic metastasis (lymphatic invasion, cancer invasion into submucous layer, tumor size > 4.0 cm, venous invasion, tumor spread to the esophagus, macroscopic types 0I and 0III and poorly-differentiated tumor) have been found to be an absolute indication for D2 lymphodissection. The restriction of surgery extent to D1-lymphodissection is possible only in patients with negligibly low risk of metastasis regardless of the type of early cancer.
Текст научной статьи Что определяет объем лимфодиссекции при раннем раке желудка?
Безусловным достоинством эндоскопических операций (резекция слизистой оболочки и резекция с диссекцией подслизистого слоя) является минимизация операционной травмы. Однако эти вмешательства требуют строгого отбора больных, у которых опухоль, как правило, не выходит за пределы слизистого слоя и характеризуется ничтожным риском лимфогенного метастазирования [8, 9, 23]. Но даже при соблюдении этих условий высокой остается частота местных рецидивов, по данным многоцентрового исследования, проведенного в Японии [13], частота нерадикальных эндоскопических вмешательств составила 19,5 %. В корейском исследовании эндоскопическая резекция слизистой
В последние годы все больше авторов придерживаются избирательного подхода к выбору объема диссекции: при наличии факторов риска лимфогенного метастазирования, главным из которых является инвазия в подслизистый слой, предпочтение отдается D2, при низком риске метастазирования (инвазия опухоли в пределах слизистой оболочки) – D1 [1, 2, 3, 6, 7, 12, 18]. Несмотря на многочисленность работ, посвященных хирургическому лечению больных РРЖ, абсолютное большинство из них базируется на изучении стандартно принятых в онкологии 5-летних результатов. Между тем этот срок не может рассматриваться при РРЖ как критерий эффективности лечения. Во-первых, более 50 % больных РРЖ переживают 5-летний срок и без всякого лечения [15, 20], во-вторых, от 30 до 60 % рецидивов РРЖ возникают в сроки более 5 лет после хирургического вмешательства [22].
Цель исследования. Выбор объема хирургического вмешательства при РРЖ.
Материал и методы
Макроскопические типы РРЖ (тип 0) оценивались согласно классификации Японского общества гастроинтестинальной эндоскопии 1962 г. Удельный вес РРЖ типа 0II в исследовании оказался наибольшим – 168 (42,6 %) наблюдений. Ранний рак 0I типа выявлен у 66 (16,8 %), 0III типа – у 118 (29,9 %) пациентов. У 42 (10,7 %) больных макроскопический тип опухоли не уточнен.
Морфологическая характеристика включала глубину инвазии (M, SM), размер, степень дифференцировки, тип Lauren, лимфатическую и венозную инвазию. Ранний рак с инвазией слизистого и подслизистого слоя встречался примерно с одинаковой частотой – в 196 (49,7 %) и 198 (50,3 %) случаях соответственно. Средний размер опухоли составил 2,7 ± 1,5 см. Аденокарцинома высокой степени дифференцировки выявлена у 100 (25,4 %) больных, умеренной – у 62 (15,7 %), низкой – у 232 (58,9 %). Распределение по классификации Lauren (1965) выявило преобладание опухолей кишечного типа – 192 (48,7 %) наблюдения. При этом диффузный тип по Lauren отмечен у 138 (35 %) пациентов, смешанный – у 43 (10,9 %). У 21 пациента (5,3 %) морфологический тип Lauren не уточнен.
Частота лимфатической и венозной инвазии (при анализе в группе из 314 наблюдений) составила 22,9 % и 10,8 % соответственно.
Достоверность различий определялась по критерию χ2, точному критерию Фишера и t-критерию Стьюдента. Критерий «выживаемость» оценивался по методу Kaplan–Meier (1958). Для сравнения кривых кумулятивной выживаемости использовался log-rank test. Многофакторный анализ проведен по методике кластерного регрессионного анализа.
Результаты и обсуждение
Частота лимфогенного метастазирования составила 12,2 % (48 из 394 пациентов). Преимуще- ственно поражение ограничивалось лимфоузлами I этапа метастазирования: у 44 из 48 больных – 91,7 %. У 4 (8,3 %) пациентов, помимо метастазов в узлах уровня N1, были поражены лимфоузлы уровня N2 – по ходу левой желудочной артерии и чревного ствола. Число пораженных лимфоузлов варьировало от 1 (23 пациента) до 8 (1 пациент) и в среднем составило 2,2 ± 1,6 на одного больного.
Было изучено влияние на частоту лимфогенного метастазирования следующих 9 морфологических факторов: глубины инвазии, локализации опухоли, мультицентричности, размеров, макроскопического типа, гистологического варианта опухоли и степени дифференцировки, типа Lauren, лимфатической инвазии, венозной инвазии. Из них значимое влияние оказали 7 факторов (табл. 1).
Риск метастазирования оказался ничтожным при размерах опухоли менее 1,0 см (0 из 65), а также при высокодифференцированном внутрис-лизистом раке (0 из 64). Низкая частота метастазирования отмечена также при внутрислизистом раке типа 0II – 1,1 % (1 из 88). Частота метастазирования при размере опухоли 1,1–4,0 см составила 11,1 % (6,1 % – при внутрислизистом и 15,7 % – при подслизистом раке), но при этом локализация метастазов ограничивалась только лимфоузлами уровня N1.
Факторы риска лимфогенного метастазирования ррж
Таблица 1
|
Фактор и его ранговое место |
Коэффициент информативности |
Частота лимфогенного метастазирования |
р |
|
1. Лимфатическая инвазия |
0,1726 |
47,2 % |
<0,001 |
|
2. Субмукозная инвазия |
0,0499 |
18,7 % |
<0,001 |
|
3. Размер опухоли >4,0 см |
0,0432 |
31 % |
=0,021 |
|
4. Венозная инвазия |
0,0429 |
44,1 % |
<0,001 |
|
5. Переход опухоли на пищевод |
0,0244 |
38,5 % |
=0,007 |
|
6. Макроскопический тип 0 I 0 III |
0,0241 |
21,2 % 16,9 % |
=0,041 |
|
7. Низкая степень дифференцировки |
0,0055 |
15,1 % |
=0,007 |
чин, не связанных с прогрессированием, – 11,7 %, от прогрессирования – 5,3 %, от метахронной злокачественной опухоли – 2,0 %.
Наличие лимфогенных метастазов оказалось наиболее сильным прогностическим фактором. Из 48 больных, у которых при исследовании удаленного препарата было выявлено метастатическое поражение регионарных лимфоузлов, прогрессирование в различные сроки зарегистрировано у 15 (31,3 %) пациентов. При отсутствии лимфогенных метастазов прогрессирование выявлено у 6 (1,9 %) пациентов. При метастатическом поражением трех и более лимфатических узлов прогноз ухудшался значительно. Безрецидивная 5-летняя выживаемость у больных с 3 и более лимфогенными метастазами (n=18) составила 46,6 %, 10-летняя – 0 %. При поражении 1 или 2 лимфоузлов 5- и 10-летняя безрецидивная выживаемость составила 65,3 (p<0,05) (рис. 1).
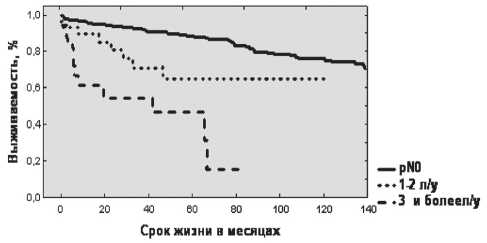
Рис. 1. Безрецидивная выживаемость в группах pN0, pN1–2, pN3 и более пораженных лимфатических узлов
Инвазия опухоли в подслизистый слой, являясь одним из факторов риска лимфогенного метастазирования, не вошла в число факторов, ухудшающих выживаемость больных РРЖ, что подтверждает целесообразность стадирования внутрислизистого и подслизистого рака в одной категории – Т1. Показатели 5- и 10-летней выживаемости составили для внутрислизистого и подслизистого рака – 88,9 %, 73,8 % и 80,4 %, 72,6 % соответственно. Анализ влияния на отдаленные результаты лечения степени дифференцировки опухоли, макроскопического типа, мультицен-тричного роста, типа Lauren также не выявил значимых различий.
Стратегия хирургии больных РРЖ до сих пор остается предметом острой дискуссии. Основная
Таблица 2
|
Фактор |
Число больных |
Выживаемость |
р |
|
|
5-летняя |
10-летняя |
|||
|
Лимфогенное метастазирование pN0 |
319 |
88,7 % |
76 % |
<0,001 |
|
pN+ |
48 |
55,4 % |
50,4 % |
|
|
Размер опухоли <4,0 см |
310 |
86,8 % |
74,4 % |
<0,01 |
|
>4,0 см |
57 |
73,8 % |
63,8 % |
|
|
Локализация опухоли н/треть |
175 |
88,9 % |
80,7 % |
|
|
с/треть |
143 |
83 % |
69,3 % |
<0,05 |
|
в/треть |
46 |
73,9 % |
48,3 % |
|
|
>1 отдела |
3 |
- |
- |
|
|
Радикальность операции R0 |
361 |
85,9 % |
73,6 % |
<0,01 |
|
R1 |
6 |
33,3 % |
0 |
|
причина разногласий – рациональный объем вмешательства на лимфатических коллекторах, а именно – улучшает ли D2 лимфодиссекция результаты лечения РРЖ?
Зависимости показателей общей выживаемости от объема лимфодиссекции в проведенном иссле- СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2013. № 2 (56)
довании не выявлено: 5- и 10-летняя выживаемость после ЛД D2 составила 86,5 % и 75,3 %, после ЛД D1 – 85,9 % и 73,5 % соответственно (p=0,93). Однако частота прогрессирования опухоли в группе больных, перенесших ЛД D2, была значимо меньше, чем при ЛД D1, – 1,3 % против 6,7 % (p<0,05). Ни в одном из двух случаев прогрессирования после ЛД D2 не было локорегионарных рецидивов. При ЛД D1 частота локорегионарно-го рецидива составила 4,3 %. Различия в частоте локорегионарных рецидивов в зависимости от объема лимфодиссекции оказались статистически значимыми (p<0,05).
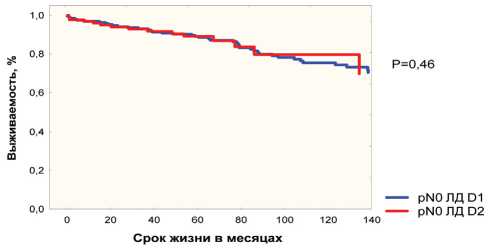
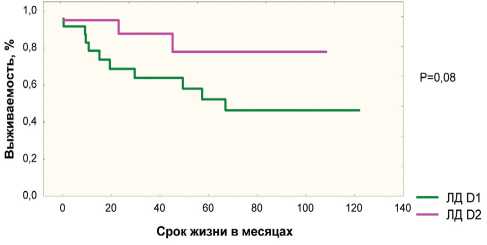
Эффективность лимфодиссекции D2 наиболее демонстративна в группе пациентов с метастатическим поражением регионарных лимфоузлов. Так, у больных без лимфогенных метастазов 5- и 10-летняя общая выживаемость в группе D1 составила 89,8 % и 76,7 %, в группе D2 – 87,5 % и 75,8 % соответственно (p=0,46). Частота прогрессирования и локорегионарных рецидивов при ЛД D1 – 2,7 % и 2,1 %, при D2 – 0 % (различия не значимы). Продолжительность жизни у больных с лимфогенными метастазами (pN+) после D2 лим-фодиссекции оказалась несколько выше, чем после D1: 5-летняя выживаемость составила 78,1 % и 51,6 %, 10-летняя – 78,1 % и 45,9 % соответственно (p=0,08). В то же время частота прогрессирования после ЛД D2 – 9,5 %, после ЛД D1 – 39,1 % (p<0,05), а частота локорегионарных рецидивов – 0 % и 26 % соответственно (p<0,05).
У больных с подслизистой инвазией опухоли и лимфогенными метастазами 5-летняя продолжительность жизни после лимфодиссекции D2 составила 73,6 %, после D1 – 35,9 % (p=0,03). Частота прогрессирования в этой же подгруппе больных после D2 лимфодиссекции составила 11,1%, после
D1 – 43,8% (p<0,05), а частота локорегионарных рецидивов – 0% и 25% соответственно (p<0,05).
Таким образом, выполнение лимфодиссекции D2 у больных РРЖ при наличии лимфогенных метастазов позволяет достоверно снизить частоту рецидивов и улучшить результаты хирургического лечения. В связи с этим наличие любого из перечисленных выше 7 факторов риска лимфогенного метастазирования при РРЖ следует считать показанием к выполнению лимфодиссекции D2. Ограничение объема ЛД до D1 обоснованно лишь при опухолях с ничтожным риском метастазирования – любом типе раннего рака независимо от степени дифференцировки размерами менее 1,0 см, вну-трислизистом раке независимо от типа и степени дифференцировки менее 4,0 см, внутрислизистом раке высокой степени дифференцировки типа 0II независимо от размеров опухоли.
Выводы
Факторами риска лимфогенного метастазирования РРЖ являются: наличие лимфатической инвазии, инвазия подслизистого слоя, размер опухоли более 4,0 см, наличие венозной инвазии, переход опухоли на пищевод, макроскопические типы 0I и 0III, низкая степень дифференцировки.
При наличии 3 и более пораженных регионарных лимфатических узлов прогноз ухудшается существенно (безрецидивная 5-летняя выживаемость составила 46,6 %, 10-летняя – 0 %).
Выполнение лимфодиссекции D2 у больных РРЖ при наличии факторов риска лимфогенного метастазирования позволяет значимо снизить частоту локорегионарных рецидивов и улучшить результаты хирургического лечения.


