Что считать структурно-функциональной единицей печени человека?
Автор: Аминова Гульшат Гареевна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Дискуссии
Статья в выпуске: 4 т.26, 2018 года.
Бесплатный доступ
В статье дискутируются вопросы структурно-функциональной организации печени человека. Проведен анализ классических представлений в этой проблеме и показаны их недостатки. Представлены данные ряда авторов в работах которых по реконструкции печеночных долек у человека и кошки показано, что паренхима печени состоит из комплексов печеночных долек. Каждый комплекс печеночных долек представляет собой совокупность 2-4 классических долек, объединенных одним общим основанием. Центральные вены в дольках комплекса начинаются со 2-й трети длины дольки. Сливаясь, они образуют собирательную вену, расположенную в общем основании долек. Комплекс печеночных долек объединен морфологически и функционально. Отдельная классическая печеночная долька в печени встречается редко. Автор доказывает, что портальные дольки и печеночные ацинусы как реальные морфологические структуры не существуют, так как их объемную реконструкцию создать невозможно.
Печень человека, строение печени, печеночная долька, структурно-функциональная единица печени
Короткий адрес: https://sciup.org/143177277
IDR: 143177277 | DOI: 10.20340/mv-mn.18(26).04.35-38
What need consider as a structural and functional unit of the human liver?
The article discusses the issues of structural and functional organization of the human liver. The analysis of classical ideas in this problem is carried out and their shortcomings are shown. The data of a number of authors are presented in whose works on the reconstruction of the hepatic lobules in humans and cats it was shown that the liver parenchyma consists of complexes of the hepatic lobules. Each complex of hepatic lobules is a combination of 2-4 classic lobules, united by one common base. The central veins in the lobules of the complex begin with the 2nd third of the length of the lobule. Merging, they form a collective vein located in the common base of the lobules. The hepatic lobule complex is morphologically and functionally combined. Separate classic hepatic lobule in the liver is rare. The author proves that portal lobules and hepatic acini do not exist as real morphological structures, since their volumetric reconstruction cannot be created.
Текст научной статьи Что считать структурно-функциональной единицей печени человека?
Аминова Г.Г. Что считать структурно-функциональной единицей печени человека?// Морфологические ведомости.- 2018.- Том 26.- № 4.- С. 35-38. (26).04.35-38
Aminova GG. What need consider as a structural and functional unit of the human liver? Morfologicheskie Vedomosti – Morphological Newsletter. 2018 Dec 30;26(4):35-38. (26).04.35-38
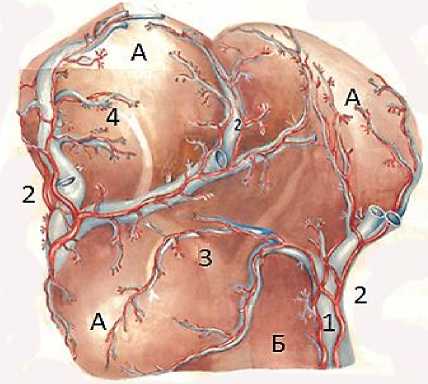
Рис. 1. Простой комплекс печеночных долек и его кровоснабжение (реконструкция с микропрепаратов): А – печеночные дольки; Б – основание печеночных долек. 1 – междольковые ветви портальной вены; 2 – междольковые ветви печеночной артерии; 3 – контуры центральной вены; 4 – септальные сосуды (рисунок Е.В.Капустиной).
Введение. С момента описания строения печени ее структурно-функциональной единицей принято было считать печеночную дольку, которая отчетливо выделяется при микроскопическом исследовании органа. В 50-е годы прошлого столетия многими исследователями [1-3] было поддержано новое представление о структуре печеночной дольки, предложенное Малле [4] и развитое Раппапортом [5-6]. За основу дольки предлагалось считать не центральную вену, вокруг которой концентрируется сложная система печеночных балок, а междольковые кровеносные сосуды вместе с окружающей их соединительной тканью и расположенными в ней структурами. Составными частями такой «дольки» являются сегменты нескольких классических долек, которые прилегают к соединительнотканным тяжам, расположенным между ними (портальная зона). Периферия таких «долек» ограничивается центральными венами. Это означает, что каждая центральная вена мысленно должна быть расчленена по количеству заканчивающихся на ней долек, точнее – выделенных их сегментов, Каждый такой сегмент классической дольки должен поочередно прикрепляться к ветвящемуся и постепенно все более истончающемуся соединительнотканному тяжу на всем его протяжении. Следуя концепции Раппопорта, невозможно выделить начало и окончание такой дольки, определить ее объемную конструкцию. Понятие о классической дольке опирается на существующую в печени богатую сеть венозной системы, обеспечивающей основную часть кровотока в органе. Оно отражает гармоничное сочетание паренхимы печени и ее сосудистой системы, но не отражает реальную структуру органа.
Цель дискуссии – на основе анализа данных ряда исследований показать, что паренхима печени человека состоит из множества морфологически и функционально объединенных комплексов классических печеночных долек. Материалом для дискуссии послужили данные имеющихся работ по реконструкции печеночных долек классического типа, в которых показана закономерность, заключающаяся в образовании дольками небольших комплексов (простых или более сложных), когда нижние отделы нескольких долек сливаются и образуют одно общее для всех долек основание (рис. 1). Комплексы печеночных долек объединены одним общим звеном оттока крови, образующимся в результате слияния нескольких центральных вен в одну собирательную [7-8]. Многообразное сочетание таких комплексов и составляет паренхиму всего органа.
Исследование соединительной ткани печени показало, что от крупных соединительнотканных тяжей в междольковые промежутки отходят тончайшие ее прослойки, которые полностью или частично отделяют дольки друг от друга. Эти прослойки, еще более истончаясь, проникают внутрь дольки и далее располагаются по ходу трабекул [9]. Соединительнотканный остов органа особенно четко представлен в печени свиньи, гистоархитектура которого свидетельствует в пользу классического понимания структуры дольки. В качестве правильности представлений о существовании классической дольки, как единственной реальной структуры служит процесс развития фиброза печени, при котором разрастание соединительной ткани начинается от портальных зон по направлению к междольковым границам, а позднее (при развитии цирроза) и внутрь дольки. Понятие об искусственно вычлененных дольках, которые получили название портальных и ацинарных, оказалось широко распространенным в научной и учебной литературе [2-3]. Увлечение концепцией Раппопорта привело к неправильной трактовке не только нормальной структуры печеночной дольки, но и макро-микроскопической конструкции паренхимы органа в целом. Основанная на фактическом материале, критика концепции Раппопорта осуществлялась и ранее, но не достаточно активно [8, 10-11]. Однако, четкость микроскопической картины структуры печени и не ясность очертаний вновь предложенного строения долек не позволяли авторам полностью отказаться от понятия классической дольки. Поэтому в настоящее время используется концепции существования трех форм печеночных долек: классической дольки [12], портальной дольки и печеночного ацинуса [1,13]. Если понятие «классическая долька» основано на опыте многолетних наблюдений, а строение самой дольки никогда не вызывало каких-либо сомнений, то для понимания структуры выделенных значительно позднее портальной дольки и ацинуса требуется умозрительное проведение не существующих в реальности границ между центральными венами. Следует отметить, что следы деструкции, напоминающей такие поля, можно наблюдать только в условиях патологии, связанных с изменениями сосудистого русла (портальная гипертензия, гематогенные токсические воздействия и др.). При этом в патологической практике принято использовать только понятие «классическая долька».
А
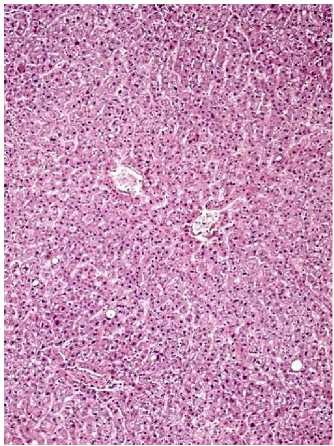
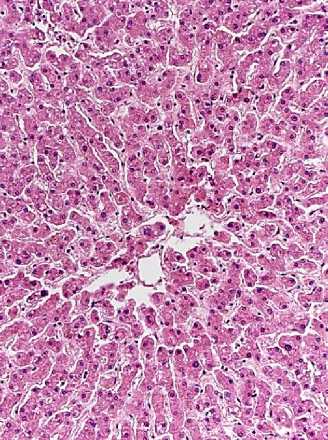
Рис. 2. Слияние центральных вен комплексов печеночных долек. А – близкое расположение 2-х центральных вен (печень мужчины 54 лет); Б – контакт стенок нескольких центральных вен (печень мужчины 61 года). Окр.: гематоксилином-эозином. Ув.: х100.
^BS
Б
Несмотря на то, что наличие классической дольки в печени, как функциональной единицы органа, является общепризнанным фактом [12], на самом деле структура печени оказывается намного сложнее, чем это принято считать. В научной печати в 60-е годы ХХ века незаметно прошли весьма интересные, тщательно исполненные, но, к сожалению, немногочисленные работы Е.В. Капустиной [7-8, 11]. В своих исследованиях автор обратилась к весьма трудоемкому методу реконструкции микроскопических объектов. Это позволило выявить истинную структуру печени и особенности ее кровоснабжения. Было показано, что отдельно расположенные печеночные дольки (классические дольки) в органе встречаются редко, а их центральные вены образуются из нескольких венул и впадают сразу в поддольковые вены. Основная же масса печеночных долек образует комплексы (рис. 1), в состав которых входят 2-4 дольки, расположенные на одном основании. Местами дольки комплекса соединяются друг с другом. В дольках, образующих комплексы, в отличие от одиночных, центральные вены формируются только на уровне второй трети дольки, т.е. на расстоянии 500-600 мкм от ее верхушки. Вся верхняя треть дольки центральной вены не имеет и состоит только из печеночных балок и синусоидов (рис. 3). Поэтому на гистологических препаратах нередко встречаются срезы долек, не имеющие центральной вены. Ближе к основанию центральные вены нескольких долек сближаются и сливаются, тогда на срезах печени можно наблюдать дольки с несколькими центральными венами (рис. 2А-Б). Здесь же происходит соединение синусоидов и печеночных балок соседних долек, в результате чего формируется одно общее основание для всех долек с более широкой в диаметре центрально расположенной веной (собирательная вена). Если слияние центральной вены какой-либо дольки с собирательной веной происходит значительно ниже остальных вен, то образовавшийся отрезок сосуда называется вставочной веной. По своей сути термин «центральная вена» не является правильным, т.к. этот сосуд не имеет оболочек, свойственных стенкам вен. По своему строению центральные вены скорее напоминают широкие венулы, стенка которых густо перфорирована устьями синусоидов. В собирательной вене вокруг увеличенного просвета наблюдается появление отдельных небольших пучков коллагеновых волокон. В комплексе печеночных долек этот сосуд является конечным звеном венозного русла. Вся кровь, протекающая через синусоиды и центральные вены долек, образующих комплексы, проходит через одну общую для них собирательную вену.
Для всего комплекса печеночных долек характерен ряд общих морфологических и функциональных закономерностей [7]. При сравнении структуры сети синусоидов на протяжении всего комплекса нетрудно заметить, что в центральных зонах печеночных долек (зона III) сеть более плотная, по сравнению с периферическими отделами (зона I). В связи с этим поверхность гепатоцитов, расположенных в центральной части долек, в большей степени контактирует со стенкой синусоидов (до 75% поверхности клетки), по сравнению с клетками периферических отделов [7]. Гепатоциты III зоны качественно отличаются от клеток, расположенных на периферии долек. Так, активность щелочной фосфатазы на всем протяжении комплекса печеночных долек выше в центральных частях, включая основание комплекса. Разное содержание ферментов в центральных и периферических зонах долек, а также особенности реакции этих зон на внешние воздействия отмечали и другие авторы [2, 14]. Установлено, что I-я и II-я зоны классических долек обладают более высоким пролиферативным потенциалом, по сравнению с центральными участками, что обеспечивает хорошую регенерацию печени даже при значительной ее резекции [15-17].
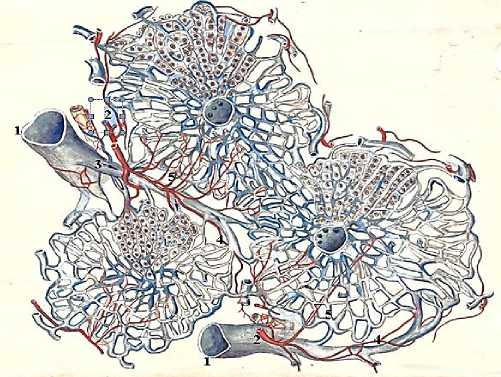
Рис. 3. Кровоснабжение печеночной дольки. 1 – междольковые ветви воротной вены; 2 – междольковые ветви печеночной артерии; 3 – септальная ветвь воротной вены (стрелками показано направление кровотока); 4 – септальная артерия; 5 – прекапилляры, проникающие в печеночную дольку на разную глубину (схема Е.В. Капустиной).
Исследование кровеносной системы печени с использованием инъекционных масс разных цветов для артериального и венозного русла показало, что внутрь дольки поступает не только смешанная кровь. В глубину дольки ступенчато проникают тончайшие прекапилляры, которые внутри дольки на разных ее уровнях сливаются с синусоидами (рис. 3). Такие сосуды достигают глубоких зон дольки и могут заканчиваться недалеко от центральной вены, где они также вливаются в синусоиды [1, 11]. Имеющиеся у сосудов сфинктеры регулируют поступление артериальной, а, возможно, и венозной крови в синусоиды долек [1].
Лимфатические капилляры, через которые осуществляется отток тканевой жидкости, располагаются в соединительной ткани портальной зоны [18]. Поэтому периферические части печеночных долек (I-я зона) оказываются в более благоприятных условиях и в ряде случаев позднее реагируют на некоторые патологические воздействия, по сравнению с их центральными участками, что отчетливо было показано в экспериментальных работах [7, 19]. Длительное изучение перестройки структуры печени и ее кровеносного русла при экспериментальной портальной гипертензии также продемонстрировало различия в сроках и особенностях реакций центральной и периферической зон долек после повышения давления в портальной вене. Так, на 3-и сутки эксперимента в центральных зонах печеночных долек наблюдалось расширение просвета синусоидов, тогда как по периферии – их сужение. Результаты исследования также показали, что на протяжении всего комплекса в первую очередь изменения наступают в центральных участках долек (гибель гепатоцитов, существенная перестройка синусоидов). Изменения периферической части долек комплекса наступают позднее, что объясняется усилением лимфоотока и разрастанием мелких желчных протоков. При более длительных сроках эксперимента разрастание соединительной ткани и развитие фиброза начинается уже с периферии долек, после того, как развивается динамическая недостаточность лимфатической системы [19]. Таким образом, были показаны не только различия в конструкции и функциональных особенностях центральных и периферических участков печеночных долек, но и отмечено, что эти закономерности распространяются на весь комплекс печеночных долек. Приведенные выше данные позволяют с объективных позиций документально продемонстрировать, что паренхима печени человека состоит из множества морфологически и функционально объединенных комплексов классических печеночных долек [8]. Поскольку такая же структура печени отмечается и у кошек [8], можно предположить, что эта закономерность является общебиологической, но для этого требуется продолжение исследований, в том числе и на макро-микроскопическом уровне.
Заключение. Таким образом, исходя из сказанного выше, можно сделать следующие выводы. Структура печени представляет собой совокупность простых или более сложных комплексов, образованных печеночными дольками классического типа, отдельно расположенные печеночные дольки встречаются редко. Портальные дольки и печеночные ацинусы как морфологические структуры не существуют, так как создание их объемной реконструкции невозможно. Введение искусственных понятий «портальная долька» и «печеночный ацинус» являются ошибочными и не отражают реальной картины о структуре печени человека.
Список литературы Что считать структурно-функциональной единицей печени человека?
- Bloger AF, Sinel'nikova MP. Prizhiznennoe morfologicheskoe izuchenie pecheni.-Riga: Izd-vo Akad.nauk Latv. SSR,1962.-89s.
- Mishnev OD, SHCHegolev AI. Strukturno-metabolicheskaya harakteristika acinusa pecheni. Arhiv anatomii, gistologii i embriologii. 1988;95(10):89-96.
- Hrushchov GK, Brodskij VYA. Organ i kletka (nekotorye problemy citologii i gistologii). Uspekhi sovremennoj biologii. 1951;52(2):181-207.
- Malle FP. A study of the structural unit of the liver. Amer J Anat. 1906;5:227-308.
- Rappaport AM, Borrowy Z, Lowgheed et al. Subdivision of hexagonal liver lobules into a structural and functional unit: role in hepatic physiology and pathology. Anat Reс. 1954;119:11-33.
- Rappaport AM. The structural and functional unit in the human liver. Anat Rec. 1958;130(4):673-690.
- Kapustina EV. O plotnosti kapillyarnoj seti, vzaimootnosheniipechenochnyh kletok s krovenosnymi kapillyarami v razlichnyh chastyah pechenochnyh dolek i raspredelenii shchelochnoj fosfatazy vnutri dolek pecheni. Arhiv anatomii, gistologii i embriologii. 1965;48(1):38-45.
- Kapustina EV. Konstrukciya kompleksov pechenochnyh dolek v pecheni cheloveka i koshki. Arhiv anatomii, gistologii i embriologii. 1973;65(12):37-41.
- Rasulev SHR. YAcheisto-plenochnye obrazovaniya -osnovnaya stroma dol'ki pecheni mlekopitayushchih. Arhiv anatomii, gistologii i embriologii. 1976;70(2):91-95.
- Aminova GG. Pis'mo v redakciyu. Arhiv anatomii, gistologii i embriologii. 1989;96(9):110-111.
- Kapustina EV. Ob arterial'nom krovosnabzhenii pechenochnyh dolek. Arhiv anatomii, gistologii i embriologii. 1962;43(10):19-35.
- Kartashova OYA. Maksimov LA. Funkcional'naya morfologiya pecheni.-S-Pb.: Trigon, 2000.-118s.
- Morfologicheskaya diagnostika zabolevanij pecheni. Pod red. V.V. Serova (SSSR), K. Lapisha (VNR).-M.: Medicina, 1989.-336s.
- Ivanov AV, Bobyncev II, SHepeleva OM,Kryukov AA. Morfologicheskie izmeneniya pecheni krys pri stresse i ih osobennosti pri vvedenii semiksa. Morfologiya. 2017;151(1):39-43.
- El'chaninov AV, Fathudinov TH, Makarov AV, Glinkina VV, Bol'shakova GB. Regeneraciya pecheni mlekopitayushchih. Klinicheskaya i ehksperimental'naya morfologiya. 2012;4:57-61.
- Romanov YUA, Savchenko TV. Topograficheskoe raspredelenie delyashchihsya gepatocitov v dol'ke regeneriruyushchej pecheni v period maksimal'noj mitoticheskoj aktivnosti. Byulleten' ehksperimental'noj biologii i mediciny. 1986;11:597-598.
- Michalopoulos GK. Liver regeneration. J Cell Physiol. 2007;213(2):286-300.
- Vyrenkov YUE, Kataev SI. Limfaticheskoe ruslo pecheni cheloveka i zhivotnyh i ego preobrazovaniya pri narushenii ottoka zhelchi. Arhiv anatomii, gistologii i embriologii. 1988;94(5):42-50.
- Kapustina EV. Izmenenie arhitektury krovenosnyh sosudov v dol'kah pecheni i perestrojka stenok vorotnoj veny, pechenochnoj arterii i pechenochnyh ven pri ehksperimental'noj portal'noj gipertenzii. Arhiv anatomii, gistologii i embriologii. 1968;55(8):91-100.