Цифровые носимые устройства как инструмент объективной оценки моторных нарушений при болезни Паркинсона: обзор современных исследований
Автор: Щеглов Б.О., Яковенко А.А., Артеменко А.Ф., Ледков Е.А., Биктимиров А.Р.
Журнал: Advanced Engineering Research (Rostov-on-Don) @vestnik-donstu
Рубрика: Информатика, вычислительная техника и управление
Статья в выпуске: 1 т.26, 2026 года.
Бесплатный доступ
Введение. Болезнь Паркинсона (БП) требует объективного и непрерывного мониторинга моторных симптомов. Носимые сенсоры — перспективный инструмент для повышения точности диагностики и контроля динамики заболевания. Его недостаточно задействуют в клинической практике из-за отсутствия единых стандартов и ограниченной воспроизводимости данных. Представленное исследование заполняет этот пробел. Цели научной работы: анализ современных подходов к использованию носимых систем для мониторинга моторных симптомов БП, выявление ограничений (в том числе по стандартам валидации), определение пути их преодоления для эффективного применения сенсоров в клинической практике. Материалы и методы. По методологии Prisma 2020 выполнен поиск литературы за 2020–2025 годы в базах данных PubMed, Scopus, Web of Science и Elibrary.ru. Изучались рецензируемые исследования по разработке, валидации и применению носимых устройств для оценки походки, тремора, брадикинезии и дискинезии. Для поиска использовались девять ключевых терминов цифровой медицины и нейродиагностики на русском и английском языках: «болезнь Паркинсона», «цифровые биомаркеры», «носимые устройства» и др. В финальной выборке из 48 исследований основное место заняли метааналитические (31 %) и клинические (29 %). В 19 % источников речь шла о разработках систем мониторинга, 15 % — лонгитюдные исследования, 6 % — систематические обзоры. Результаты исследования. Сопоставляются описания девяти носимых устройств для отслеживания особенностей моторики пациентов с БП. Учитываются типы метрик, клинических сценариев и задач. Обозначены две концепции исследуемых гаджетов: минимализм (один датчик, высокий уровень комфорта, фокус на интегральных индексах); детекция в реальном времени (акцент на эпизодах и моментальном распознавании). В двух этих случаях нужны разные эталоны разметки, окна анализа и критерии клинической значимости. Для повышения сопоставимости результатов необходим «минимальный набор валидации», специфический для класса задач. Условия преодоления противоречий: унификация протоколов сбора данных, набора метрик, индикации; внешняя и межцентровая валидация (разметка, критерии точности); устойчивость алгоритмов к смене устройства; критерии клинической полезности. Обсуждение. Массовому использованию носимых устройств для анализа моторных симптомов пациентов с БП препятствуют недостаток стандартов аналитической, клинической валидации и экономическая неоднозначность внедрения. В целом перспективны пять рассмотренных устройств. Однако клинические данные об их эффективности и влиянии на качество жизни недостаточны, т. к. исследуется главным образом потенциал концепций (точность алгоритмов), а не прикладная ценность и готовность к повседневному использованию реальных устройств. Редко изучается внешний (межцентровый) перенос, единые конечные точки и клиническая полезность. Заключение. Систематизированы современные данные о возможностях и ограничениях носимых сенсоров при болезни Паркинсона. Широкое распространение таких гаджетов невозможно без стандартизации, единых критериев эффективности, безопасности и экономической целесообразности. Решение выявленных проблем позволит изменить подход к диагностике и лечению, сделать носимые системы ключевым инструментом персонализированной медицины.
Болезнь Паркинсона, носимые сенсоры, инерциальные измерительные устройства, цифровые биомаркеры, мониторинг двигательных симптомов, клиническая валидация, персонализированная медицина
Короткий адрес: https://sciup.org/142247504
IDR: 142247504 | УДК: 616.858-073.75:004.925.8 | DOI: 10.23947/2687-1653-2026-26-1-2257
Wearable Digital Devices as a Tool for Objective Assessment of Motor Disorders in Parkinson’s Disease: A Review of Current Studies
Introduction. Parkinson's disease (PD) requires objective and continuous monitoring of motor symptoms. Wearable sensors are a promising tool for improving diagnostic accuracy and monitoring disease dynamics. However, they are underutilized in clinical practice due to the lack of uniform standards and limited data reproducibility. The presented study fills this gap. The objectives of the research are to analyze current approaches to the use of wearable systems for monitoring motor symptoms of PD, identify limitations (including those related to validation standards), and determine ways to overcome them for the efficient use of sensors in clinical practice. Materials and Methods. Using the Prisma 2020 methodology, a literature search was conducted for the years 2020–2025 in PubMed, Scopus, Web of Science, and Elibrary.ru. Peer-reviewed studies on the development, validation, and application of wearable devices for assessing gait, tremor, bradykinesia, and dyskinesia were examined. Nine key terms in digital medicine and neurodiagnostics in Russian and English were used for the search: “Parkinson's disease”, “digital biomarkers”, “wearable devices”, and others. The final sample of 48 studies was dominated by meta-analytics (31%) and clinical studies (29%). Nineteen percent of the sources discussed the development of monitoring systems, 15% were longitudinal studies, and 6% were systematic reviews. Results. Descriptions of nine wearable devices for monitoring motor performance in patients with PD were compared. The types of metrics, clinical scenarios, and tasks were considered. Two concepts of the devices under study were outlined: minimalism (one sensor, high comfort level, focus on integral indices); real-time detection (emphasis on episodes and instant recognition). These two cases required different labeling standards, analysis windows, and clinical significance criteria. To improve the comparability of results, a “minimum validation set” specific to the class of problems was needed. Conditions for overcoming these contradictions were: unification of data collection protocols, metric sets, and indicators; external and multicenter validation (labeling, accuracy criteria); algorithm stability to device changes; clinical utility criteria. Discussion. The widespread use of wearable devices for analyzing motor symptoms in patients with PD is hampered by a lack of analytical and clinical validation standards and economic ambiguity of implementation. In general, five of the devices reviewed show promise. However, clinical data on their efficiency and impact on quality of life are insufficient, as research is primarily focused on the potential of the concepts (accuracy of the algorithms) rather than the practical value and readiness for everyday use of real devices. There is little research on external (multicenter) transferability, unified endpoints, and clinical utility. Conclusion. Current data on the capabilities and limitations of wearable sensors for Parkinson's disease has been systematized. Widespread adoption of such devices is impossible without standardization and unified criteria for efficiency, safety, and economic viability. Addressing these identified challenges will transform approaches to diagnosis and treatment, making wearable systems a key tool in personalized medicine.
Текст научной статьи Цифровые носимые устройства как инструмент объективной оценки моторных нарушений при болезни Паркинсона: обзор современных исследований
Subject Field Overview
Wearable Digital Devices as a Tool for Objective Assessment of Motor Disorders in Parkinson’s Disease: A Review of Current Studies
Bogdan O. Shcheglov Ф и, Andrey A. Yakovenko, Andrey F. Artemenko, Evgeny A. Ledkov,
Artur R. Biktimirov
Federal Center of Brain Research and Neurotechnologies, Federal Medical-Biological Agency of the Russian Federation, Moscow, Russian Federation
Introduction . Parkinson's disease (PD) requires objective and continuous monitoring of motor symptoms. Wearable sensors are a promising tool for improving diagnostic accuracy and monitoring disease dynamics. However, they are underutilized in clinical practice due to the lack of uniform standards and limited data reproducibility. The presented study fills this gap. The objectives of the research are to analyze current approaches to the use of wearable systems for monitoring motor symptoms of PD, identify limitations (including those related to validation standards), and determine ways to overcome them for the efficient use of sensors in clinical practice.
Materials and Methods . Using the Prisma 2020 methodology, a literature search was conducted for the years 2020–2025 in PubMed, Scopus, Web of Science, and Elibrary.ru. Peer-reviewed studies on the development, validation, and application of wearable devices for assessing gait, tremor, bradykinesia, and dyskinesia were examined. Nine key terms in digital medicine and neurodiagnostics in Russian and English were used for the search: “Parkinson's disease”, “digital biomarkers”, “wearable devices”, and others. The final sample of 48 studies was dominated by meta-analytics (31%) and clinical studies (29%). Nineteen percent of the sources discussed the development of monitoring systems, 15% were longitudinal studies, and 6% were systematic reviews.
Results . Descriptions of nine wearable devices for monitoring motor performance in patients with PD were compared. The types of metrics, clinical scenarios, and tasks were considered. Two concepts of the devices under study were outlined: – minimalism (one sensor, high comfort level, focus on integral indices);
-
– real-time detection (emphasis on episodes and instant recognition).
These two cases required different labeling standards, analysis windows, and clinical significance criteria. To improve the comparability of results, a “minimum validation set” specific to the class of problems was needed. Conditions for overcoming these contradictions were:
-
- unification of data collection protocols, metric sets, and indicators;
-
- external and multicenter validation (labeling, accuracy criteria);
-
- algorithm stability to device changes;
-
- clinical utility criteria.
Discussion . The widespread use of wearable devices for analyzing motor symptoms in patients with PD is hampered by a lack of analytical and clinical validation standards and economic ambiguity of implementation. In general, five of the devices reviewed show promise. However, clinical data on their efficiency and impact on quality of life are insufficient, as research is primarily focused on the potential of the concepts (accuracy of the algorithms) rather than the practical value and readiness for everyday use of real devices. There is little research on external (multicenter) transferability, unified endpoints, and clinical utility.
Conclusion . Current data on the capabilities and limitations of wearable sensors for Parkinson's disease has been systematized. Widespread adoption of such devices is impossible without standardization and unified criteria for efficiency, safety, and economic viability. Addressing these identified challenges will transform approaches to diagnosis and treatment, making wearable systems a key tool in personalized medicine.
Acknowledgements. The authors would like to thank the Editorial board of the Journal and the reviewer for their professional analysis of the article and recommendations for its correction.
Funding Information . The research is done with the support from the Ministry of Science and Higher Education of the Russian Federation within the framework of the state program for the creation and development of the World-Class Research Center “Center for Cybernetic Medicine and Neuroprosthetics” (Agreement No. 075-15-2025-573).
Введение. Болезнь Паркинсона (БП) представляет собой нейродегенеративное заболевание с широким спектром моторных и немоторных проявлений. К числу основных двигательных симптомов относятся тремор покоя, брадикинезия и постуральная нестабильность. Немоторные проявления — это главным образом нарушения автономной регуляции, а также поведенческие и когнитивные дефициты [1] . Болезнь Паркинсона относится к числу наиболее распространенных нейродегенеративных патологий. Прогрессирующая утрата пациентом самостоятельности, необходимость длительного медицинского наблюдения и ухода снижают качество жизни больного и его семьи, создают дополнительные нагрузки для системы здравоохранения. На поздних стадиях заболевания лечение леводопой нередко сопровождается развитием моторных осложнений. Одно из них — так называемое «истощение окончания действия дозы», при котором продолжительность терапевтического действия препарата постепенно сокращается. В рамках данной работы будем называть это off-эффектом. Известны также отсроченные и случайные флуктуации on — off. Они характеризуются непредсказуемым изменением двигательной активности вне зависимости от времени приема препарата [2] .
Моторные флуктуации и дискинезии существенно ухудшают качество жизни, повышают риск падений и осложняют ведение пациента. Они требуют своевременной и часто индивидуализированной коррекции терапии, что усложняет ситуацию. Традиционные методы оценки симптомов БП базируются преимущественно на субъективных клинических наблюдениях, дневниках пациентов и опросниках. Известные слабые места таких подходов:
Информатика, вычислительная техника и управление
-
- возможность систематических ошибок;
-
- индивидуальная вариабельность;
-
- чрезмерная зависимость от квалификации наблюдателя [3] .
К тому же такие методы, как правило, отражают состояние пациента лишь при общении с медиками или во время коротких тестов. Этого недостаточно для стабильного выявления кратковременных эпизодов off (on). Следовательно, ограничивается возможность своевременной коррекции лечения и персонализированного ведения.
Развитие гибкой электроники и технологий искусственного интеллекта открывает новые перспективы для здравоохранения, включая создание носимых систем мониторинга, решений по типу «мозг — компьютер — интерфейс» и интеграцию с интернетом вещей [4] . Гибкие носимые медицинские электронные устройства способны регистрировать артериальное давление, частоту дыхания, температуру тела [5] , электрофизиологическую активность. Так поддерживается пролонгированная регистрация ключевых параметров [6] , обеспечивается непрерывный сбор данных о состоянии организма, открывается возможность повышения качества персонализированных медицинских решений [7] .
В контексте БП непрерывная регистрация моторных паттернов в естественных условиях позволяет сократить разрыв между реальной динамикой симптомов и их эпизодической клинической оценкой. Медики получают постоянный доступ к данным, в частности, могут отслеживать суточную вариабельность и эпизоды моторных флуктуаций.
Носимые устройства изменили подходы к мониторингу и лечению болезни Паркинсона [8] . Появилась возможность объективного, непрерывного дистанционного наблюдения за динамикой моторных симптомов [9] . Компактные и легкие носимые устройства закрепляются на теле пациента и фиксируют физиологические параметры: движения, тремор, походку, равновесие, а также когнитивные и поведенческие особенности, включая нарушения сна [10] . Для регистрации и передачи данных применяются сенсорные технологии: акселерометры, гироскопы [11] , магнитометры и электромиографические датчики [12] . Все это позволяет комплексно оценивать моторные и немоторные симптомы заболевания [13] .
Наибольшую клиническую ценность имеют решения, позволяющие сопоставлять цифровые показатели с клиническими шкалами (например, UPDRS 1 ) и выявлять изменения, значимые для коррекции терапии, прежде всего при моторных флуктуациях.
Современные подходы к сенсорному мониторингу предполагают использование:
-
– многоточечных систем с размещением сенсоров на разных участках тела [14] ;
-
– минималистичных решений — например, сенсоров, интегрированных в обувь, наручные устройства, смартфоны или браслеты [15] .
В последние годы получили широкое распространение методы анализа данных, которые задействуют пороговые алгоритмы, автоматическую классификацию и глубокие нейронные сети. На этой базе создаются недорогие и неинвазивные системы дистанционного наблюдения [16] . Поступающая от сенсоров информация может обрабатываться как в режиме реального времени [17] , так и ретроспективно [18] . Машинное обучение открыло новые возможности для фиксации прогрессирования болезни, оценки эффективности терапии и в целом для анализа качества жизни пациента [19] . Вместе с тем результаты ряда исследований остаются методологически неоднородными. Различия в протоколах, метриках, выборках и условиях тестирования затрудняют прямое сопоставление решений и перенос полученных показателей в рутинную клиническую практику.
Современные исследования демонстрируют значительный интерес к использованию в медицинских целях носимых сенсоров и алгоритмов машинного обучения [20] . Как следствие, расширяются возможности диагностики, развиваются интеллектуальные системы принятия врачебных решений [21] . Валидация алгоритмов и интерпретация данных [22] требуют участия специалистов различных профилей — неврологов, физиотерапевтов, биостатистиков, психологов и медицинских инженеров [23] . Совместная работа мультидисциплинарной команды обеспечивает повышение точности [24] и клиническую достоверность [25] алгоритмических моделей. Однако именно на этапе клинической и аналитической валидации наиболее заметен дефицит унифицированных подходов: отсутствуют общепринятые протоколы сбора данных, не согласованы критерии качества и воспроизводимости. Таким образом, цифровым платформам нужны единые требования к сопоставимости биомаркеров.
Ранее опубликованные обзоры фокусировались преимущественно на отдельных аспектах применения носимых технологий. В качестве примера можно привести использование мобильных приложений или инерциальных сенсоров для прогнозирования моторных и немоторных симптомов БП с помощью методов машинного обучения [26, 27] .
Для дальнейшего развития изучаемой сферы следует решить перечисленные ниже задачи:
-
– сопоставить разные классы носимых сенсорных систем в привязке к сценариям (медицинское учреждение — дом, краткосрочный тест — длительный мониторинг);
-
– выполнить сравнительный анализ алгоритмов и используемых метрик с указанием границ применимости и методологических ограничений;
-
– определить критерии «хорошей» клинической и аналитической валидации;
-
– назвать причины низкой сопоставимости результатов разных исследований.
В открытом доступе нет публикаций, в которых проработаны эти вопросы.
Таким образом, причины пробела в знаниях обусловлены в первую очередь слабыми местами предыдущих обзоров литературы, их недостаточно точной фокусировкой на проблеме. Кроме того, нет интегрированной картины, связывающей технологии, качество доказательств и требования к стандартизации (валидации). Все это необходимо для повышения качества персонализированного ведения пациентов с БП.
Цели представленного обзора — анализ современных носимых цифровых устройств для отслеживания моторных симптомов БП, выявление основных ограничений и недостатков валидации, а также определение методов их преодоления для эффективного использования в клинической практике.
Достижение заявленных целей требует решения перечисленных ниже задач:
-
1. Систематизация типов носимых сенсорных систем, применяемых при БП, а также их целевых клинических задач (определение походки, тремора, брадикинезии, дискинезии, флуктуации).
-
2. Классификация алгоритмов анализа данных и машинного обучения.
-
3. Сопоставление клинических и технических метрик эффективности разрабатываемых методик и устройств.
-
4. Анализ качества доступных исследований (выборки, условия тестирования, воспроизводимость, внешняя валидация).
-
5. Выявление нерешенных проблем стандартизации и валидации цифровых биомаркеров.
-
6. Сравнение платформ, представляющих интерес в контексте исследуемой проблемы.
-
7. Определение практически ориентированных направлений дальнейших исследований (протоколы, конечные точки, инфраструктура сбора и хранения данных).
Материалы и методы. Исследование базируется на систематическом поиске и анализе рецензируемых научных публикаций, посвященных разработке, архитектуре и логике функционирования цифровых систем, предназначенных для оценки неврологической дисфункции у пациентов с БП. Настоящая работа выполнена в соответствии с рекомендациями Prisma 2020.
Период поиска — с 2020 по 2025 годы. Изучались публикации в международных библиографических базах данных PubMed, Scopus, Web of Science (WoS), а также в российской научной электронной библиотеке Elibrary.ru. Дополнительно выполнялся ручной поиск по спискам литературы ключевых публикаций и отбор релевантных полнотекстовых материалов конференций. Цель отбора источников — выявление актуальных данных о принципах построения и функционирования цифровых платформ, применяемых для диагностики, мониторинга и реабилитации пациентов с БП (таблица 1).
Отбор источников для обзора по методологии Prisma 2020
Таблица 1
|
Идентификация |
Итог* |
|||
|
Записи из баз данных |
Количество источников |
Дополнительные источники |
Количество источников |
|
|
PubMed: n = 80 Scopus: n = 105 Web of Science: n = 88 Elibrary.ru: n = 15 |
288 |
Списки литературы: n = 6 Материалы конференций: n = 4 |
10 |
298 |
|
Скрининг по заголовкам и аннотациям |
||||
|
Дублирование |
210 |
Исключение по целевым показателям |
160 |
50 |
|
Исключение дубликатов: n = 88 |
Нерелевантная тема: n = 70 Не о болезни Паркинсона: n = 42 Не о носимых устройствах: n = 35 Публикации до 2020 года: n = 13 |
|||
|
Оценка соответствия по полным текстам |
||||
|
Исключение из-за недоступности полного текста: n = 2 |
48 |
– |
– |
48 |
|
Финальная выборка |
||||
|
Качественный синтез |
33 |
Метаанализ |
15 |
|
|
Клинические исследования: n = 14 Разработка систем: n = 9 Лонгитюдные исследования: n = 7 Систематические обзоры: n = 3 |
Консолидации данных нескольких исследований: n = 15 |
48 |
||
Примечание: * Итоговое количество источников по этапам и отбору в целом.
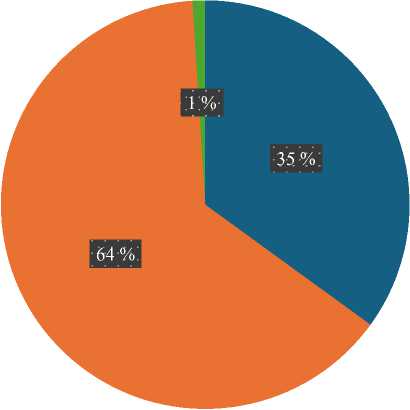
Некоторые данные таблицы 1 для большей наглядности визуализировали. Показатели представили в процентах, округлили до целых чисел. Как видим, чаще всего основанием для исключения из финальной выборки были итоги анализа названий и аннотаций. Нерелевантность выявили в 64 % случаев. Значимую долю (более трети) занимает дублирование (рис. 1).
Информатика, вычислительная техника и управление
-
■ Дублирование ■ Нерелеватные названия и аннотации ■ Отсутвие полного текста
Рис. 1. Причины исключения источников из обзора
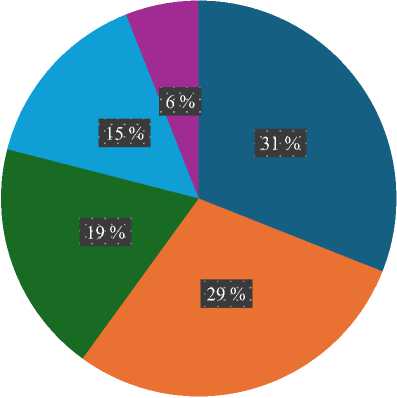
Проработка сведений, обобщенных в таблице 1, выявила крайне незначительное количество систематических обзоров (рис. 2). На такие источники пришлось всего 6 % в общем объеме материалов, попавших в финальную выборку. Изучение причин такого дисбаланса выходит за рамки данного исследования. Отметим, что наибольшую долю в выборке занимают работы с консолидацией данных нескольких исследований (метаанализ, 31 %). Почти столько же (29 %) — клинические исследования.
-
■ Метаанлиз ■ Клинические исследования ■ Разработка систем ■ Лонгитюдные исследования ■ Систематические обзоры
Рис. 2. Виды исследований в финальной выборке
Для поиска использовались ключевые термины цифровой медицины и нейродиагностики:
-
– болезнь Паркинсона — Parkinson’s disease;
-
– цифровые биомаркеры — digital biomarkers;
-
– носимые устройства — wearable devices;
-
– компьютерное зрение — computer vision;
-
– машинное обучение — machine learning;
-
– платформы телемедицины — telemedicine platforms;
-
– системы неврологической оценки — neurological assessment systems;
-
– мобильное здравоохранение — mobile health (mHealth);
-
– облачная диагностика — cloud diagnostics.
Поисковые запросы формировались на русском и английском языках. В анализ включались публикации, доступные на русском и (или) английском языках.
Статьи отбирались по критериям релевантности, научной значимости и новизны. В первую очередь рассматривались оригинальные исследования, комплексные аналитические обзоры, а также публикации с описанием архитектурных решений, алгоритмических подходов и клинической апробации цифровых систем.
В обзор включали материалы, соответствующие пяти критериям:
– выход в свет в 2020–2025 гг.;
-
– публикация в рецензируемых источниках;
-
– доступность полного текста;
-
– объект — пациенты с БП;
-
– предмет — носимые и (или) цифровые системы, применяемые для диагностики, мониторинга или количественной оценки неврологической дисфункции.
По поводу последнего критерия уточним, что речь идет преимущественно о моторных симптомах: тремор, брадикинезия, дискинезия, походка, постуральная устойчивость. Принимались во внимание публикации с описанием сенсорной платформы, алгоритмов обработки и (или) результатов клинической апробации.
Из обзора исключали источники, соответствующие семи критериям:
-
– выход в свет до 2020 г.;
-
– исследования не по БП;
-
– изыскания без анализа носимых цифровых устройств (например, исключительно молекулярные или фармакологические);
-
– работы о немоторных симптомах, без связи с наблюдением моторного состояния;
-
– публикации с объемом данных, недостаточным для извлечения ключевых параметров (метрики, протокол, характеристики системы);
-
– материалы с дублированием данных;
-
– недоступность полного текста.
Поясним по поводу последнего пункта. В обзор не включалась так называемая «серая литература»: диссертации и нерецензируемые препринты. Материалы конференций учитывались только при наличии полнотекстовой публикации и возможности извлечения данных.
Два независимых рецензента проводили отбор в два этапа. На первом выполнили скрининг заголовков и аннотаций, на втором — полнотекстовую оценку. Разногласия между экспертами разрешались путем обсуждения. При отсутствии консенсуса привлекали третьего участника. «Ослепленное» рецензирование не задействовали. В соответствии с Prisma (табл. 1) в базах данных идентифицировали 288 записей: PubMed — 80, Scopus — 105, Web of Science — 88, Elibrary.ru — 15. Дополнительно нашли 10 источников (по спискам литературы — 6, по материалам конференций — 4). После удаления 88 дубликатов осталось 210 записей.
На этапе скрининга исключили 160 публикаций:
-
– 70 оказались нерелевантными;
-
– 42 — не о болезни Паркинсона;
Информатика, вычислительная техника и управление
-
– 35 — не о носимых устройствах;
– 13 — опубликованы до 2020 года.
Соответственно, для оценки в перечне остались 50 статей. Из них исключили две из-за недоступности полнотекстовой версии. В итоге в качественный синтез включили 33 исследования, в метаанализ — 15. Всего 48.
Методология представляет собой критический анализ и систематизацию данных с целью определения ключевых направлений развития цифровых технологий для мониторинга паркинсонизма. Важно было выявить закономерности в архитектуре систем и логике их функционирования, а также сравнить преимущества и ограничения различных решений.
Для обеспечения воспроизводимости анализа выполнили стандартизированное извлечение данных по каждой включенной работе. Учитывались такие факторы, как:
-
– тип цифровой системы и сенсорной платформы;
-
– локализация сенсоров;
-
– режим и длительность измерений;
-
– клинический сценарий (в клинике и дома);
-
– целевые симптомы;
-
– алгоритмы обработки и машинного обучения;
-
– метрики качества и валидности;
-
– параметры исследования (размер выборки, наличие контрольной группы, длительность наблюдения);
-
– сведения о клинической и (или) внешней валидации.
Далее исследования группировались по четырем заданным аналитическим категориям.
Первая — функциональная задача системы. Принимаются во внимание диагностика, мониторинг флуктуаций, оценка симптомов и терапии, а также реабилитация и обратная связь.
Вторая — тип сенсорной платформы. Это могут быть одноточечные и многоточечные IMU 2 , смартфоны, смарт-часы, мультимодальные решения.
Третья — целевой моторный фенотип (походка, тремор, брадикинезия, дискинезия, равновесие).
Четвертая — уровень клинической или аналитической валидации (сопоставление с клиническими шкалами, наличие внешней валидации, испытания в реальных условиях, воспроизводимость протокола).
Для перехода от отдельных исследований к обобщенным выводам сопоставили результаты внутри каждой группы по единым критериям (метрики качества, дизайн, ограничения). Это позволило выявить повторяющиеся закономерности и системные барьеры для внедрения.
Результаты исследования. В ходе исследования изучили данные о возможностях применения различных классов сенсоров в диагностике и цифровизации БП (таблица 2).
Сравнительный анализ устройств для диагностики и цифровизации БП
Таблица 2
|
Устройство / сенсор |
Примеры |
Преимущества |
Недостатки / ограничения |
Ссылка |
|
Акселерометр |
Компонент IMU; используется в PKG 3 |
Замеры ускорения, анализ поз и характера движений. База для интегральных показателей моторики |
Неполная картина движения (для 3D-реконструкции часто требуется IMU). Есть вопросы по интерпретации сигналов |
[28] [29] |
|
Гироскоп |
Компонент IMU; DynaPort7 |
Фиксация вращательных перемещений и угловой скорости. Анализ походки, симметрии, постуры |
Неполные сведения об ориентации, линейных перемещениях. Нужны обработка и интерпретация |
|
|
Магнитометр |
Компонент IMU |
Отслеживание пространственной ориентации по изменениям магнитного поля |
Ограничения по клинической интерпретации. Требует интеграции с другими сенсорами, алгоритмами |
[31]
|
|
IMU: акселерометр + гироскоп + магнитометр |
IMU-модули (общий класс); PDMonitor |
3D-реконструкция линейных и угловых перемещений. Объективные, непрерывные, долговременные наблюдения вне клиники. Снижение эффекта Хоторна |
Слабая интеграция данных в практику. Снижение комплаентности у части пациентов. Нужны специальные инструменты аналитики и стандартизация платформ, алгоритмов, метрик |
|
|
Носимые сенсоры движения (общий класс) |
IMU, акселерометры и др. |
Легкость, компактность, энергоэффективность. Непрерывное, объективное наблюдение. Различие здоровой манеры движения и нарушений. Фиксация прогрессирования, активности, эффективности терапии. Учет выводов врача по тремору, брадикинезии, походке |
Проблемы с интерпретацией многомерных сигналов в клинике, соответствием нормативной базе, защитой персональных данных, этикой. Снижение комплаентности у части пациентов. Необходимость стандартизации. Ограниченность данных об эффективности и качестве жизни пользователей. Вопросы относительно экономической целесообразности |
[30] [33] [37]
|
2 От англ. inertial measurement unit — инерциальный измерительный блок.
3 От англ. personal kineti graph — график кинетического тремора.
|
Одобренные 4 клинические системы дистанционног о мониторинга |
PDMonitor, PKG, Stat-On, Kinesia360, KinesiaU |
Широкое применение в клинической практике |
Ограниченность клинических данных об эффективности и влиянии на качество жизни пациентов. Организационные и этические барьеры |
[41] [42] [43] |
|
Мультисенсор с облачной архитектурой |
Mobility Lab, PDMonitor 5 IMU + SmartBox |
Анализ суточной активности. Оценка походки, тремора, брадикинезии. Сбор, обработка и передача данных в облако |
Риски по защите данных. Вопросы по интеграции в клинический сценарий. Пациентам приходится носить несколько датчиков |
[44] [45] [46] |
|
Наручное устройство на акселерометре |
PKG |
Высокая чувствительность. Стандартные шкалы. Замеры тремора, дискинезии, брадикинезии. Интегральные показатели флуктуаций, дискинезий, неподвижности для коррекции терапии |
Недостаточность данных об экономической эффективности. Зависимость метрик от алгоритмов обработки |
[47] [48] [49] |
|
Поясничное устройство с ML 5 в реальном времени |
Stat-On |
Фиксация «застывания» походки, падения, дискинезии. Чувствительность более 93 % |
Сложности интерпретации данных. Ограничения практической интеграции. Вопросы по стандартизации и комплаентности |
[47] [48] |
Для снижения описательности и улучшения сопоставимости подходов результаты дополнительно структурировали по типам метрик, используемых при оценке эффективности и валидации, а также по типам клинических задач и клиническим сценариям применения:
– кабинет — дом;
– краткосрочные тесты — длительный мониторинг.
Выделили четыре типичные клинические задачи:
-
1) количественная оценка выраженности моторных симптомов (тремор, брадикинезия, дискинезии, постуральная нестабильность, параметры походки);
-
2) детекция событий и моторных осложнений (эпизоды off 6 , «застывания» походки, падения);
-
3) мониторинг динамики, прогрессирования и реакций на терапию (суточные профили активности, флуктуации);
-
4) поддержка клинических решений (отчеты для врача, дистанционное ведение).
При таком подходе можно обсуждать не только использование определенных сенсоров. Исследование позволяет судить о том, какую клиническую проблему решает система и насколько убедительно это подтверждено метриками и валидацией.
Информатика, вычислительная техника и управление
Результаты исследований дополнительно интерпретировались с учетом клинического сценария:
-
а) при контролируемых условиях (кабинет, лабораторный тест) достигается высокая повторяемость измерений и чаще фиксируется высокая точность;
-
б) при длительном мониторинге в домашних условиях выше экологическая валидность и возможность фиксации флуктуаций, при этом строже требования к комплаентности, устойчивости алгоритмов и интероперабельности данных.
Для унификации сопоставления эффективности условно выделим три группы метрик (таблица 3):
-
1) алгоритмические метрики распознавания и классификации (accuracy 7 , sensitivity 8 , specificity 9 , AUC 10 );
-
2) метрики согласования с клиническими шкалами (корреляция, согласие с UPDRS и др.);
-
3) метрики клинической полезности (влияние на коррекцию терапии, QoL 11 , частоту событий, клинико-экономические показатели).
Именно метрики из третьей группы, критичные для внедрения, встречаются существенно реже, что ограничивает доказательную базу практической эффективности ряда решений.
Аналитическая рамка сопоставления работ, включенных в обзор
Таблица 3
|
Измерение сопоставления |
Что сравнивается |
Примеры показателей |
Ограничения для широкого внедрения |
|
Тип задачи |
Мониторинг и оценка симптомов, событий, динамики, поддержка решений |
Тремор, брадикинезия, дискинезии, «замораживание», падения, off, суточные профили, отчет для врача |
Разнородные цели, несопоставимые наборы данных, некорректность разметки |
|
Клинический сценарий |
Кабинет (тест) и дом (длительное ношение) |
Результаты в контролируемых тестах, вариабельность |
Вопросы по комплаентности, проблемы контекста, дрейф сигналов, различия в протоколах |
|
Метрики |
Алгоритмическое и клиническое согласование, клиническая полезность |
Точность, чувствительность, специфичность, согласование с UPDRS, влияние на качество жизни |
Разнородность конечных точек, дефицит оценок клинической полезности |
|
Валидация |
Внутренняя, внешняя, межцентровая |
Внутренняя и внешняя валидация |
Отсутствие стандарта внешней валидации и протоколов воспроизводимости |
Инерциальные сенсоры, или сенсоры движения, — это компактные электронные устройства для измерения ускорения, угловой скорости и характеристик магнитного поля [28] . На основе указанных параметров определяются ориентация и движение объекта в трехмерном пространстве. Наиболее распространенные типы инерциальных сенсоров — акселерометры, гироскопы и магнитометры [29] . Благодаря малому весу, компактности и низкому энергопотреблению, носимые сенсоры движения широко используются для повседневного непрерывного и объективного мониторинга пациентов с БП вне клиники [30] . При этом клиническая ценность конкретного сенсорного решения определяется не только сенсорным составом, но и тем, какие клинические состояния можно воспроизводимо измерять (задача) и в каких условиях (сценарий).
Акселерометр регистрирует динамику ускорения, позволяя анализировать позу и характер движений, тогда как гироскоп фиксирует вращательные перемещения и угловую скорость. Магнитометр показывает изменения магнитного поля, чтобы отслеживать пространственную ориентацию. Сенсоры размещаются на запястье, голени, поясе, бедре, стопе. При объединении трех сенсоров (акселерометра, гироскопа и магнитометра) формируется инерциальный измерительный модуль (IMU), обеспечивающий трехмерную реконструкцию линейных и угловых перемещений [31] .
Объективная оценка ситуации требует минимизации хоторнского эффекта. В данном случае речь идет о том, что пациент знает о мониторинге, следит за своими движениями и по возможности их контролирует [32] . В итоге картина получается неестественная. Гаджеты позволяют добиться объективности, так как поддерживают долговременное наблюдение вне клинических условий.
С аналитической точки зрения IMU чаще оказывается конкурентным преимуществом в задачах отслеживания походки, постуры и комплексной моторики (где критична 3D-кинематика).
Одноосных или однотипных сенсоров (например, только акселерометра) достаточно для таких узких задач, как оценка тремора при определенных условиях. Однако их сложнее интегрировать с разными сценариями и протоколами.
Инерциальные сенсоры продемонстрировали высокую эффективность в дифференциации двигательных паттернов пациентов с БП и здоровых добровольцев. Это создает основу для применения алгоритмов машинного обучения при выделении диагностически значимых признаков [33] . Устройства также позволяют отслеживать прогрессирование заболевания [34] , выявлять изменения двигательной активности по времени [35] и оценивать эффективность терапии [36] .
Наблюдения на основе данных инерциальных сенсоров дают возможность врачам принимать обоснованные решения о коррекции лечения, в том числе по выраженности тремора, брадикинезии и нарушениям походки [37] .
В последние годы инерциальные сенсоры активно используются для разработки цифровых биомаркеров прогрессирования болезни Паркинсона [38] . Приведем названия некоторых комплексных исследований в этом направлении: Personalized Parkinson Project, Cincinnati Cohort Biomarker Program, Watch-PD, Oxford Parkinson Disease Centre Discovery Cohort и Alameda [39] . Устройства позволяют объективно оценивать эффективность новых терапевтических подходов с учетом медикаментозного лечения, физиотерапии и глубокой стимуляции головного мозга [40] . Непрерывная регистрация данных в естественных условиях обеспечивает более достоверную оценку влияния терапии на двигательную активность. Это повышает точность клинических испытаний и эффективность персонализированных схем лечения [41] . Однако даже в крупных проектах остается критическим вопрос унификации конечных точек, протоколов и валидации цифровых биомаркеров для воспроизводства и сопоставления результатов разных центров и платформ.
В клинической практике широко применяются такие устройства, как упомянутые выше PDMonitor, PKG, StatON, Kinesia360 и KinesiaU [42] . PDMonitor относится к классу медицинских изделий IIa. Решение объединяет пять IMU-сенсоров, размещаемых на запястьях, голенях и поясе, и систему SmartBox, обеспечивающую сбор, обработку и передачу данных в облако [43] . Это позволяет анализировать двигательную активность пациента на протяжении суток и судить о вероятности off по информации о походке, треморе и брадикинезии [44] .
В сравнении с односенсорными решениями мультисенсорные (как PDMonitor) выигрывают в плане охвата моторных фенотипов и устойчивости к шуму отдельных каналов. При этом ношение нескольких датчиков требует более высокой комплаентности и более сложной интеграции в клинические процессы.
Наручное устройство PKG с высокой чувствительностью измеряет тремор, дискинезии и брадикинезию [45] . На основе данных акселерометра формируются интегральные показатели двигательных флуктуаций, степени дискинезий и длительности неподвижных периодов, что позволяет врачу объективно оценить выраженность симптомов и корректировать терапию [46] . Stat-on использует алгоритмы машинного обучения в реальном времени для регистрации сигналов инерциальных сенсоров, расположенных в области поясницы [47] . Устройство с чувствительностью выше 93 % идентифицирует эпизоды «застывания» походки, падения и дискинезии туловища [48] .
В аналитическом сопоставлении можно говорить о двух разных концепциях:
-
– PKG — минимализм (один датчик, высокий уровень комфорта, фокус на интегральных индексах);
-
– Stat-on — событийная детекция в реальном времени (акцент на эпизодах и моментальном распознавании).
Отметим особое значение стандартизации протоколов разметки и анализа событий, а также критериев сравнения с клинической оценкой. От этого зависит возможность сопоставления метрик разных платформ.
Система KinesiaOne и ее расширенная версия Kinesia360 сочетают носимые сенсоры и программное обеспечение для планшета, что дает объективную оценку тремора, брадикинезии и других двигательных проявлений заболевания. Нейросети в облаке обрабатывают эти данные и рассчитывают тяжесть симптомов в баллах, соответствующих клиническим шкалам.
DynaPort7 — это комбинация гироскопов и акселерометров с частотой регистрации 100 Гц. Решение точно анализирует параметры походки, симметрию движений и поддерживает постуральный контроль.
Комплекс Mobility Lab из беспроводных сенсоров и специализированного программного обеспечения дает количественную оценку походки и равновесия. С его помощью можно выявлять слабо выраженные, или тонкие, признаки паркинсонической походки и эпизоды «замирания».
Информатика, вычислительная техника и управление
Анализ литературы позволяет обоснованно предложить практические шаги для преодоления обозначенных выше ограничений и конкретизации путей внедрения решений. Представим это как последовательность действий:
-
1) унификация протоколов сбора данных (минимальный набор тестов или режимов, размещение сенсоров, длительность мониторинга, требования к данным);
-
2) стандартизация набора метрик и отчетных показателей для конкретных задач (отдельно для оценки симптомов, детекции эпизодов и флуктуаций);
-
3) обязательная внешняя и по возможности межцентровая валидация с описанием разметки и критериев точности, корректности;
-
4) проверка устойчивости алгоритмов к смене устройства (версии программного обеспечения) и к работе в домашних условиях;
-
5) исследования клинической полезности (влияние на коррекцию терапии, качество жизни, безопасность и клинико-экономические результаты);
-
6) интеграция в клинические процессы (интерпретируемые отчеты, совместимость с медицинскими информационными системами) при обязательном соблюдении этики и обеспечении защиты данных.
Обсуждение. Итак, известны различия конкурирующих подходов к внедрению в клиническую практику гаджетов, фиксирующих состояние пациентов с БП. Они дифференцируются не только аппаратно, но и по логике клинической верификации. Производители ориентируют свои решения:
-
– на шкалы (привязка оценкам симптомов в баллах);
– на события (детекция эпизодов).
Очевидно, что двум этим подходам соответствуют разные стандарты валидации и разные конечные точки.
Многочисленные исследования и хороший выбор регуляторно одобренных систем не решают значимую проблему. Речь идет о незавершенном формировании единых и общепринятых стандартов валидации носимых решений при БП. В настоящем обзоре под «хорошей» валидацией цифровой системы понимается совокупность:
-
- аналитической валидности (стабильность и воспроизводимость измерений и обработки, устойчивость к шуму и дрейфу сенсоров);
-
- клинической валидности (согласование цифровых показателей с клиническими шкалами и (или) клинически значимыми состояниями, например, off);
-
- клинической полезности (доказательство влияния на решения врача, исходы, качество жизни и экономические показатели).
Отметим, что на практике во многих работах доминирует демонстрация алгоритмической точности в контролируемых условиях. Значительно реже рассматриваются внешняя валидация на независимых выборках, межцентровая воспроизводимость и оценка клинической полезности.
Есть и другие факторы, которые ограничивают сопоставимость результатов между платформами и препятствуют формированию универсальных клинических конечных точек. В их числе:
-
- вариабельность протоколов (расположение сенсоров, длительность записи, условия тестирования);
-
- различия в метриках и понимании целевых состояний (определение off, разметка эпизодов, точность, AUC, корреляция с UPDRS).
Информация, получаемая с помощью носимых сенсорных устройств, позволяет персонализировать терапевтические стратегии, оптимизировать дозирование лекарственных препаратов и оценивать эффективность лечения как в клинических, так и в домашних условиях. Сенсорные системы способны фиксировать даже незначительные изменения моторных функций, которые могут оставаться незамеченными при стандартных визитах к врачу, поэтому гаджеты незаменимы для раннего выявления прогрессирования заболевания или реакции на терапию. Интеграция физиологических данных, полученных с носимых устройств, открывает возможности для адаптивной глубокой стимуляции головного мозга. Например, скорость движения голени, регистрируемая инерциальными сенсорами, может использоваться в качестве управляющего параметра при динамической настройке стимуляции субталамического ядра с целью коррекции «замирания». К тому же данные технологии создают инфраструктуру для дистанционного наблюдения и телемедицинских консультаций. Пациенты получают помощь, не покидая дом, и это снижает нагрузку на лечебные учреждения.
Вместе с тем клиническая значимость таких решений наиболее убедительно подтверждается там, где исследования включают:
-
- сопоставление с клиническими шкалами (например, MDS UPDRS 12 );
-
- внешнюю валидацию;
-
- оценку результатов в естественных условиях.
При отсутствии перечисленных элементов разработки чаще остаются прототипами из-за сложностей интеграции с другими центрами и платформами.
Широкое внедрение носимых сенсоров сопряжено с методологическими и организационными ограничениями. Они обусловлены не только технологией, но и методологическим профилем доказательств. Назовем некоторые факторы снижения сопоставимости результатов исследований:
-
- небольшие выборки;
-
- особенности протоколов;
-
- различия в определениях целевых состояний (например, критерии off и правила разметки «заморозки»);
-
- ограниченная внешняя валидация.
Сложность интеграции сенсорных данных в рутинную клиническую практику объясняется в первую очередь тем, что врачам нужны специальные знания и инструменты аналитики для интерпретации многомерных сигналов, получаемых с гаджетов. Недавние исследования показали возможность упрощения протоколов оценки моторики с помощью единственного сенсора, расположенного в поясничной области, при выполнении типовых двигательных тестов, таких как «встань и иди» [46] . Выяснилось, что автоматическая сегментация и извлечение ограниченного числа параметров способны обеспечить точность диагностики [47] , сопоставимую с более сложными системами, и это открывает путь к внедрению сенсорных технологий в повседневную практику без избыточной вычислительной нагрузки [48] . Однако при таком подходе критично соблюдение требований стандартизированной валидации [49] :
-
- устойчивость метрик при смене условий (кабинет — дом);
-
- воспроизводимость при изменении версии алгоритма и устройства.
Следует отдельно оговорить вопросы этики и рисков утечки личной информации при операциях с данными сенсоров. Такие сведения необходимо полностью защитить от несанкционированного использования. В отсутствие гарантий показания не должны собираться и транслироваться.
Необходимо также организовать просветительскую работу, разъяснить пациентам и их семьям преимущества и риски цифрового мониторинга. Этические аспекты и проблемы операций с персональными данными следует предусмотреть на ранних этапах разработки. Это особенно важно в случаях:
-
- использования принципов открытого кода;
-
- расширения прав пациента на доступ к данным;
-
- внедрения моделей метасогласия.
Дополнительным ограничением остается тот факт, что не все пациенты с болезнью Паркинсона могут эффективно использовать носимые устройства. Когнитивные, двигательные нарушения, тремор снижают комплаент-ность. Результаты когнитивных тестов на смартфонах коррелируют с показателями традиционных нейропсихологических шкал, однако требуют адаптации для пациентов с выраженными моторными расстройствами.
Стандартизация аппаратных платформ, алгоритмов обработки сигналов и выходных клинических метрик остается необходимым условием для унификации подходов и включения сенсорных систем в регламенты диагностики. Пока же сложившаяся практика не соответствует этим задачам. Обзор литературы показал, что в исследованиях используются разные конечные точки и разные наборы метрик, по‑разному определяется успешность изысканий и готовых моделей. Так, например, не оценивается клиническая интерпретируемость по точности или AUC, что затрудняет формирование единых критериев качества цифровых биомаркеров.
Отметим также экономическую неоднозначность масштабного внедрения описанных решений. С этой точки зрения следует признать в целом перспективными такие устройства, как PKG, Stat-on, Kinesia360, KinesiaU и PDMonitor. Однако клинические данные об их эффективности и влиянии на качество жизни все еще недостаточны. Обзор литературы дал объяснение этому противоречию. Дело в том, что авторы публикаций работают главным образом с концепциями, доказывают их потенциал. Это довольно далеко от реальной прикладной ценности решений, то есть от их клинической полезности и рентабельности.
В настоящем обзоре недостаток стандартов валидации рассматривается как отдельный системный барьер внедрения. Для воспроизводимого и сопоставимого использования цифровых биомаркеров при БП следует достичь соблюдения приведенных ниже требований валидации и полезности:
-
- аналитическая валидация — стабильность измерений, контролируемость источников ошибок (частота дискретизации, дрейф сенсоров, предобработка), воспроизводимость вычисления признаков (индексов);
-
- клиническая валидация — доказанное соответствие цифровых показателей клинически значимым состояниям или шкалам (например, UPDRS), оценка в целевых сценариях применения (кабинет, дом), внешняя валидация на независимых данных;
-
- клиническая полезность — подтверждение того, что использование цифрового биомаркера улучшает принятие решений (коррекция терапии), исходы пациента или качество жизни при приемлемых затратах.
На практике в литературе чаще представлены элементы первого и частично второго уровня (особенно в контролируемых тестах). Реже встречаются внешний (межцентровый) перенос, единые конечные точки и оценки клинической полезности. Это формирует разрыв между демонстрацией точности алгоритма и готовностью технологии к рутинному применению.
Информатика, вычислительная техника и управление
Подчеркнем, что недостаточно отдельных рекомендаций и программ по цифровым конечным точкам в клинических исследованиях. Для повышения сопоставимости результатов необходим «минимальный набор валидации», причем собственный, специфический для каждого из двух классов задач:
-
- оценка выраженности симптомов (для шкало‑ориентированных систем),
-
- детекция off, «замораживаний» и падений (для событийно‑ориентированных систем).
Дифференциация объясняется тем, что в двух этих случаях нужны разные эталоны разметки, разные окна анализа и разные критерии клинической значимости.
Развитие носимых сенсоров в управлении болезнью Паркинсона связано с прогрессом в области искусственного интеллекта и машинного обучения. Важным направлением становится интеграция глубоких нейронных сетей с инерциальными сенсорами для анализа временных рядов. Существующие модели пока не дают стабильных результатов при обработке многомерных биомеханических данных в реальном времени. Перспективное решение в этом смысле — использование распределенных носимых сенсоров, обеспечивающих автономный сбор и анализ данных с возможностью быстрого принятия решений. При этом прогресс ИИ должен сопровождаться методологически прозрачной валидацией, что подразумевает:
-
- отчетность по протоколам;
-
- предотвращение переобучения;
-
- проверки на независимых выборках;
-
- анализ устойчивости к вариациям реальной жизни.
Интеграция сенсорных систем с мобильными приложениями и интеллектуальными устройствами усиливает вовлеченность пациентов в процесс самоконтроля, повышает приверженность терапии и способствует формированию персонализированных траекторий лечения. Экспериментальные исследования с использованием инерциальных сенсоров и сверточных нейронных сетей продемонстрировали возможность точного измерения эпизодов «замирания» походки в домашних условиях при высокой степени комплаентности пациентов. Однако уровень доказательности таких результатов зависит от качества разметки эпизодов и от наличия внешней валидации. При несоблюдении требований по качеству разметки и внешней валидации сохраняются ограничения для сравнения моделей и переноса их в клинический контур.
Заключение. Авторы представленного обзора на основе анализа рецензируемых публикаций 2020–2025 гг. реализовали две научные задачи:
-
- систематизировали современные подходы к применению носимых цифровых устройств для объективного мониторинга моторных симптомов болезни Паркинсона;
-
- сопоставили основные классы сенсорных систем (в первую очередь IMU‑платформы и клинически применяемые носимые гаджеты), их целевые клинические задачи (походка, тремор, брадикинезия, дискинезии, моторные флуктуации), а также типовые клинические сценарии использования (кабинет — дом, краткосрочные тесты — длительный мониторинг).
Классификация алгоритмов обработки и подходов машинного обучения показала, что наиболее убедительные результаты получаются в задачах количественной оценки моторики и распознавания отдельных фенотипов в контролируемых условиях. Вне клиники, в повседневной жизни пациента качество и воспроизводимость результатов могут снижаться из‑за различий протоколов, условий измерений и комплаентности.
Ключевой итог обзора — выявление системной проблемы стандартов валидации цифровых биомаркеров при болезни Паркинсона. В литературе нет унифицированных требований к протоколам сбора данных, набору метрик, доказательствам клинической полезности (влияние на коррекцию терапии, качество жизни и экономические показатели). Отсутствуют критерии воспроизводимости и сопоставимости результатов, генерируемых разными сенсорными платформами. В итоге можно утверждать, что широкому внедрению носимых сенсоров для пациентов с болезнью Паркинсона препятствуют не только технические ограничения, но и недостаточная стандартизация процедур аналитической и клинической валидации.
По результатам обзора авторы сформулировали первоочередные задачи теоретических и прикладных изысканий в данной области:
-
- унификация протоколов и конечных точек;
-
- проработка внешней (межцентровой) валидации;
-
- оценка устойчивости алгоритмов в реальных условиях;
-
- детальное изучение клинической полезности и клинико‑экономической эффективности.
В перспективе необходимо наладить взаимодействие между исследователями, клиницистами, инженерами, представителями индустрии и регулирующими органами. На этой базе можно будет создать стандартизированные, надежные и клинически валидированные решения для цифрового мониторинга болезни Паркинсона в контексте прецизионной медицины.


