Цитокиновые маркеры эффективности коррекции оксидативного стресса у больных ограниченной склеродермией
Автор: Тлиш М.М., Сорокина Н.В.
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Дерматовенерология
Статья в выпуске: 3 т.11, 2015 года.
Бесплатный доступ
Цель; улучшение результатов лечения больных ОСД за счет повышения эффективности и сокращения сроков их лечения. Материал и методы. Проведено обследование и лечение 52 пациентов с ограниченной склеродермией. Методом адаптивной рандомизации из этих пациентов было сформировано две группы. В контрольной группе проводилось комплексное лечение согласно стандартам при данной нозологии. В основной группе пациенты дополнительно получали антиоксидантную терапию. Курс лечения в обеих группах составил 21 день. Результаты лечения оценивали в соответствии с динамикой кожного патологического процесса и цито-кинового профиля. Результаты. В процессе лечения положительная клиническая динамика у больных основной группы проходила быстрее и сопровождалась более выраженным снижением воспалительной активности сыворотки крови. Заключение. Полученные результаты свидетельствуют о том, что антиоксидантная терапия повышает эффективность и сокращает сроки лечения больных ограниченной склеродермией.
Ограниченная склеродермия, оксидативный стресс, цитокины
Короткий адрес: https://sciup.org/14918162
IDR: 14918162
Cytokine markers of the efficiency of correction of oxidative stress in patients with limited sclerodermia
Objective: to improve treatment of patients with limited sclerodermia (LSD) by increasing efficiency and reducing the time of their treatment. Material and methods. The examination and treatment of 52 patients with circumscribed scleroderma were conducted. Two groups of these patients were formed with method of adaptive randomization. In the control group complex treatment was underwent according to the standards in this nosology. In the general group the patients additionally received antioxidant therapy. The course of treatment was 21 days in both groups. Results. Treatment results were evaluated in accordance with the dynamics of cutaneous pathological process and cytokine profile. In the course of treatment positive clinical dynamics in patients of the study group went faster and was accompanied by a more pronounced reduction in inflammatory activity in the blood serum. Conclusion. The results suggest that antioxidant therapy improves the efficiency and reduces the treatment time of patients with circumscribed sclerodermia.
Текст научной статьи Цитокиновые маркеры эффективности коррекции оксидативного стресса у больных ограниченной склеродермией
Существуют данные о важной роли нарушений клеточного иммунитета в развитии фиброза при ОСД. Так, у больных ОСД при биопсии здоровой на вид кожи вокруг очагов склероза обнаруживают ее периваскулярную и диффузную инфильтрацию преимущественно Т-лимфоцитами и макрофагами [10]. Еще одно подтверждение важной роли клеточного иммунитета в патогенезе данного заболевания — сходство кожных проявлений и хронической реакции «трансплантат против хозяина», которая, как известно, опосредована активированными Т-лимфоцитами. Иммунорегуляторный индекс (соотношение лимфоцитов CD4 и CD8) в крови больных ОСД обычно повышен за счет одновременного снижения числа лимфоцитов CD8 и повышения числа лимфоцитов CD4 [11].
В различных типах клеток стимуляция рецепторов для фактора некроза опухоли (ФНО) вызывает быстрое возрастание внутриклеточного уровня активных кислородных метаболитов (АКМ). Один из возможных механизмов образования АКМ при действии ФНО — нарушение функции митохондриальной цитохром-с-оксидазы. Энергетический дисбаланс в митохондриях приводит к снижению синтеза АТФ, усилению генерации АКМ и развитию оксида-тивного стресса [11, 12].
ФНО — основной, но далеко не единственный медиатор воспалительной реакции. По мере нарастания этой реакции в ней начинают участвовать интерлейкин (ИЛ) — 1, сходный с ФНО по своей био- логической активности, интерферон гамма (ИНФ-γ) и другие цитокины. Все они взаимодействуют между собой, усиливая действие друг друга и вызывая синтез и секрецию дополнительных медиаторов воспаления. Так, ИЛ-1 индуцирует синтез ИЛ-2 и ИЛ-4 — ростовых факторов, секретируемых T-хелперами. Кроме того, ИЛ-1 усиливает экспрессию рецепторов к ИЛ-2 и ИЛ-4, что создает условия для аутокринной регуляции пролиферации Т-хелперов. Повышенный уровень ИЛ-2 и свободных рецепторов ИЛ-2 на ранних стадиях склеродермии — признак прогрессирования заболевания. Выработка ИЛ-4 активированными Т-хелперами и тучными клетками стимулирует пролиферацию фибробластов и синтез коллагена, а также усиливает адгезию Т-лимфоцитов к эндотелию. Биологические эффекты ИЛ-6 сходны с таковыми ИЛ-1 и ФНОα. По многообразию клеточных источников продукции и мишеней биологического действия одним из наиболее активных цитокинов является ИЛ-6, который участвует в реализации воспалительной и иммунной реакций. Выраженным иммуносупрессорным эффектом обладает ИЛ-10, который снижает продукцию провоспалительных цитокинов, усиливает выработку антагониста рецептора ИЛ-1 и уменьшает адгезию лейкоцитов к эндотелиальным клеткам. Широко обсуждается роль ИЛ-17 в развитии аутоиммунных заболеваний за счет его способности запускать обширную тканевую реакцию, приводящую к миграции нейтрофилов в зону воспаления [11–14].
Тканевая ишемия и продукция некоторых провос-палительных цитокинов, в частности ФНО, способствуют формированию АКМ. Они, в свою очередь, индуцируют повреждение ДНК и эндотелиальных клеток, усиливают активацию тромбоцитов и приводят к повышенной секреции молекул адгезии или секреции воспалительных и профиброгенных цитокинов, стимулируют в низких концентрациях пролиферацию фибробластов кожи и повышенный синтез коллагена [15].
Изложенное свидетельствует о тесной взаимосвязи всех звеньев патогенеза ОСД и диктует необходимость коррекции оксидативных нарушений при данной нозологии. В этой связи представляет интерес «Цитофлавин» — препарат естественных метаболитов цикла Кребса, которые обуславливают метаболическую энергокоррекцию, антигипоксическую и антиоксидантную активность, оказывающую положительный эффект на процессы энергообразования в клетке, уменьшающую продукцию свободных радикалов и восстанавливающую активность ферментов антиоксидантной системы.
Цель: улучшение результатов лечения больных ОСД за счет повышения эффективности и сокращения сроков их лечения.
Материал и методы. Нами проведено обследование и лечение 52 пациентов (22 мужчин и 30 женщин) в возрасте 37±4,0 года с бляшечной формой ОСД. Длительность заболевания составляла 3,8±1,6 года. Прогрессирующая стадия дерматоза определена у подавляющего числа пациентов — 42 (80,8%) человек, стадия стабилизации — у 10 (19,2%). Методом адаптивной рандомизации из этих пациентов было сформировано две группы.
В первой группе (контрольная) 25 пациентам проводилось традиционное комплексное лечение согласно стандартам при данной нозологии: глюкокортикостероидные, противовоспалительные, анти-фиброзные, иммуномодулирующие, ферментные препараты, вазодилататоры, ангиопротекторы, анта- гонисты кальция и препараты, улучшающие метаболизм в тканях, витамины.
Во второй группе (основная) 27 больным, помимо традиционного лечения, дополнительно проводилась антиоксидантная терапия препаратом «Цитофла-вин» в режиме дозирования: по 760 мг двукратно — утром и вечером, с интервалом между приемами 8–10 часов, не позднее 17 часов, не менее чем за 30 мин до еды, не разжевывая и запивая водой.
Курс лечения в обеих группах составил 21 день.
Результаты лечения оценивали на 7-е, 14-е, 21-е сутки в соответствии с динамикой кожного патологического процесса:
значительное улучшение: исчезновение периферического венчика роста, уменьшение плотности и размеров очага, отсутствие субъективных ощущений (парестезии, чувства покалывания, жжения и дискомфорта в очаге);
улучшение: исчезновение периферического венчика роста, некоторое уменьшение плотности очага, прежние размеры поражения, отсутствие субъективных ощущений;
стабилизация: побледнение периферического венчика роста, отсутствие новых очагов поражения, прежние размеры и плотность очага, уменьшение субъективных ощущений;
без эффекта: отсутствие динамики;
ухудшение: прогрессирование патологического процесса, увеличение размеров очага или появление новых.
Выполняли иммунологические исследования пациентам обеих групп до и в конце лечения на 21-е сутки. Количественные показатели ФНО-а, ИЛ-1, ИЛ-2, ИЛ-4, ИЛ-6, ИЛ-10, ИЛ-17, ИНФ-у в сыворотке крови определяли методом иммуноферментного анализа с применением наборов реагентов, выпускаемых ЗАО «Вектор-Бест» (г. Новосибирск). Для получения сыворотки венозную кровь собирали в чистые пробирки с активатором свертывания в утреннее время с 9 до 11 часов (не ранее чем через 8 часов после приема пищи). Полученные результаты выражали в пикограмме вещества в 1 миллилитре плазмы (пг/мл).
Статистическую обработку результатов исследований проводили с использованием пакета статистических программ «Statistica 6.0» для персонального компьютера. Описательная статистика количественных признаков представлена средними и среднеквадратическими отклонениями. Для анализа нормально распределенных признаков применялись параметрические методы (t-критерий Стьюдента). Уровень достоверности соответствовал 95% (р<0,05).
Результаты. Динамика кожного патологического процесса у пациентов в обеих группах отличалась на каждом этапе обследования.
На 7-е сутки улучшение патологического процесса наблюдалось только в основной группе у 2 (7,4%) пациентов. Стабилизация кожного процесса в контрольной и основной группах констатирована соответственно у 4 (16,0%) и у 11 (40,8%) пациентов, отсутствие эффекта у 20 (80,0%) и у 14 (51,8%) (рис. 1а).
На 14-е сутки значительное улучшение отмечено только в основной группе у 2 (7,4%) пациентов. Улучшение в обеих группах (контрольной и основной) наблюдали у 5 (20,0%) и у 12 (44,5%), стабилизацию у 9 (36,0%) и у 10 (37,0%), отсутствие эффекта у 10 (40,0%) и у 3 (11,1 %) пациентов соответственно (рис. 1б).
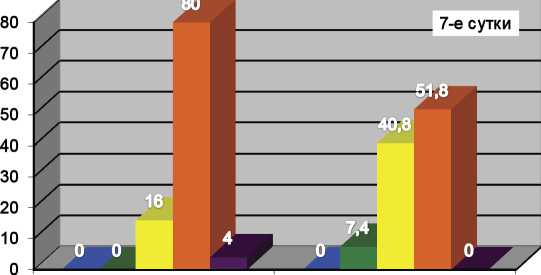
контрольная группа основная группа
а)
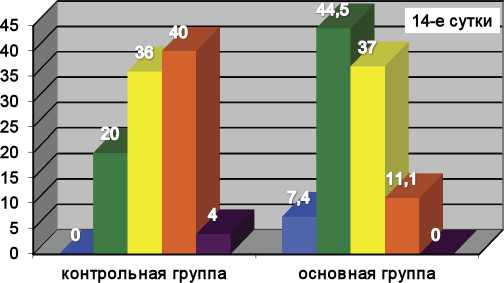
б)
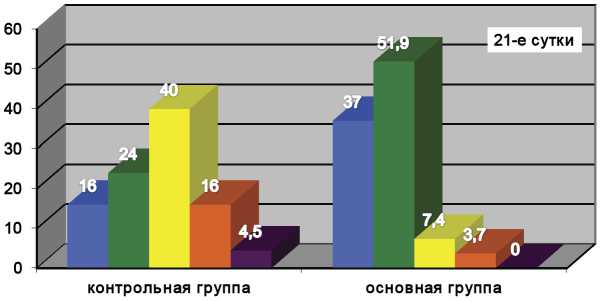
в)
-
■ значительное улучшение
-
■ улучшение
стабилизация без эффекта
-
■ ухудшение
■значительное улучшение
-
■ улучшение
стабилизация без эффекта
-
■ ухудшение
■значительное улучшение
-
■ улучшение
стабилизация без эффекта
-
■ ухудшение
Рис 1. Динамика кожного патологического процесса у больных ОСД:
-
а) динамика кожного патологического процесса у больных ОСД контрольной и основной групп на 7-е сутки; б) динамика кожного патологического процесса у больных ОСД контрольной и основной групп на 14-е сутки; в) динамика кожного патологического процесса у больных ОСД контрольной и основной групп на 21-е сутки.
На 21-е сутки значительное улучшение в контрольной и основной группах зарегистрировано у 4 (16,0%) и у 10 (37,0%), улучшение у 6 (24,0%) и у 14 (51,9%), стабилизация у 10 (40,0%) и у 2 (7,4%), отсутствие эффекта у 4 (16,0%) и у 1 (3,7%) пациентов соответственно (рис. 1в).
Ухудшение патологического процесса отмечалось только у одного больного (4,0%) контрольной группы на протяжении всего периода лечения.
Следует также отметить, что динамика кожного процесса сопровождалась улучшением показателей цитокинового профиля. Результаты иммунологического исследования представлены в таблице.
Анализируя содержание провоспалительных цитокинов на 21-й день после проведенного лечения, мы выявили следующие изменения.
Содержание ИЛ-1 в сыворотке крови у пациентов с ОСД было повышено в среднем до 6,8±2,4 пг/ мл. На фоне проводимой стандартной терапии у 14 (56,0%) пациентов контрольной группы отмечена тенденция к снижению концентрации данного интерлейкина в среднем до 4,8±1,4 пг/мл. В основной груп-
Показатели цитокинового профиля крови больных ОСД до и после лечения в контрольной и основной группах
|
Показатель |
До лечения |
Контрольная группа (n=25) после лечения |
Основная группа (n=25) после лечения |
норма |
|
ИЛ-1 |
6,8±2,4 |
4,8±1,4 |
3,2±1,1* |
1,8±0,7 |
|
ИЛ-2 |
9,3±3,3 |
7,1±2,3 |
6,7±1,8 |
5,0±2,3 |
|
ИЛ-4 |
0,7±0,1 |
1,8±0,1* |
2,1 ±0,9* |
2,2±1,0 |
|
ИЛ-6 |
7,7±2,5 |
5,9±2,7 |
4,1±1,2* |
2,0±1,3 |
|
ИЛ-10 |
1,3±0,4 |
1,8±0,4 |
2,0±0,8 |
3,2±1,5 |
|
ИЛ-17 |
6,4±3,0 |
5,2±1,5 |
4,3±1,4 |
1,2±0,5 |
|
ФНО |
5,6±2,4 |
4,3±1,2 |
2,5±1,2* |
1,5±0,3 |
|
ИНФ-y |
6,7±2,3 |
6,1±2,4 |
4,5±1,3 |
2,0±1,2 |
П р и м еч а н и е : * — статистически значимые различия с группой пациентов до начала лечения, при р<0,05.
пе пациентов снижение данного показателя было более выраженным (М= 3,2±1,1 пг/мл) и наблюдалось у 21 пациента (77,8%), р<0,05.
Концентрация ИЛ-2 до начала терапии у пациентов обеих групп была повышена до 9,3±3,3 пг/мл. Достоверных изменений содержания ИЛ-2 в периферической крови после проведенной терапии нами выявлено не было. Однако отмечалась общая тенденция к снижению данного показателя в обеих группах (без достоверных различий между группами). Концентрация ИЛ-2 в сыворотке крови больных контрольной группы у 12 (48,0%) снижалась в среднем до 7,1±2,3 пг/мл. У пациентов основной группы снижение уровня ИЛ-2 выявлено у 17 больных (62,9%), при этом концентрация цитокина составила в среднем 6,7±1,8 пг/мл.
У 23 пациентов (85,2%) основной группы концентрация ИЛ-6 статистически значимо снижалась (в среднем до 4,1±1,2 пг/мл (р<0,05). В 25% случаев имела место тенденция к снижению (в среднем до 5,5±1,6 пг/мл) без статистически значимых отклонений. После проведенного стандартного комплекса лечения (контрольная группа) у 14 пациентов (56,0%) также отмечалась тенденция к снижению уровня ИЛ-6 (М=5,9±2,7 пг/мл), однако достоверных изменений выявлено не было.
Повышенное содержание ФНО до начала лечения у пациентов с ОСД (М=5,6±2,4 пг/мл) статистически значимо снижалось у 24 (88,9%) пациентов основной группы исследуемых больных (М=2,5±1,2 пг/мл). При этом в контрольной группе данный показатель имел тенденцию к снижению у 17 пациентов (68,0%), составив в среднем 4,3±1,2 пг/мл.
Содержание ИНФ — y у исследуемых пациентов было повышено до 6,7±2,3 пг/мл в первый день госпитализации. После проведенной терапии концентрация данного показателя имела тенденцию к снижению у 10 человек (40,0%) контрольной группы до 6,1±2,4 пг/мл и более выраженную у 16 человек (59,3%) основной группы до 4,5±1,3 пг/мл. Достоверных различий по группам получено не было.
Исследование уровня ИЛ-17 выявило исходное его повышение у пациентов с ОСД (6,4±3,0 пг/мл). После курса лечения также отмечается подавление синтеза цитокина у 11 человек (44,0%) контрольной группы и у 15 человек (55,6%) основной, более выраженное у пациентов второй группы (4,3±1,4 пг/мл).
Противовоспалительные цитокины, сниженные у пациентов с ОСД до начала лечения, после окончания его курса имели тенденцию к повышению концентрации в сыворотке крови. Так, содержание ИЛ-4 статистически значимо повышалось у 18 пациентов
(72,0%) контрольной группы и у 21 пациента (77,8%) основной группы (1,8±0,1 пг/мл и 2,1±0,9 пг/мл соответственно; р<0,05).
Концентрация ИЛ-10 повышалась после проведенной терапии в обеих исследуемых группах и составила в среднем 2,0±0,8 пг/мл у пациентов основной группы и 1,8±0,4 пг/мл у пациентов контрольной группы. При этом повышение концентрации цитокина было отмечено у 10 пациентов контрольной группы (40,0%) и у 16 пациентов (59,3%) основной. Статистически значимых отличий при сравнении групп по данному показателю выявлено не было.
Обсуждение. Таким образом, у пациентов основной группы, получавших в составе комплексного лечения «Цитофлавин», регресс дерматоза начинался в более ранние сроки и проходил более активно. Нами также выявлено повышение концентрации провоспалительных и снижение уровня противовоспалительных цитокинов у больных ОСД до начала лечения [10–14]. После проведенного курса терапии отмечено в обеих группах снижение воспалительной активности сыворотки крови, причем достоверное повышение концентрации противовоспалительных цитокинов (ИЛ-4) и снижение содержания провоспа-лительных цитокинов (ИЛ-1, ИЛ-6, ФНО) зафиксировано у пациентов основной группы, прошедших курс традиционной терапии в сочетании с препаратом «Цитофлавин».
В ходе проведения лечения каких-либо побочных действий и осложнений ни в одном клиническом случае выявлено не было.
Заключение. «Цитофлавин», обладая антиги-поксическим и антиоксидантным действием, способствует снижению провоспалительных и повышению противовоспалительных цитокинов, сокращает сроки терапии и повышает эффективность лечения больных ОСД.
Список литературы Цитокиновые маркеры эффективности коррекции оксидативного стресса у больных ограниченной склеродермией
- Dacczak-Pazdrowska A, Kowalczyk M, Szramka-Pawlak B, Gornowicz-Porowska J, etal. Clinical research lnterleukin-17A and interleukin-23 in morphea/Arch Med Sci 2012; 8 (6): 1089-1095 DOI (digital object identifier): 10.5114/aoms.2012.32421
- Kreuter A, Krieg T, Worm M, et al. Diagnosis and therapy of localized scleroderma. J Deutsch Dermatol Ges 2009; 7 (suppl. 6): S1-14
- Xie Y, Zhang X, Wakasugi S, Makino T, Inoue Y, Ihn H. Im-munohistochemical characterization of the cellular infiltrate in localized scleroderma. Int J Dermatol 2008; 47: 438-42
- Dziankowska-Bartkowiak B, Gerlicz-Kowalczuk Z, Waszczykowska E. Angiogenin and SDF-1 alpha serum concentration in patients with systemie sclerosis: In relation to clinical status. Arch Med Sci 2011; 7: 92-96
- Carolyn A., Bangert, Kim A, Jacobe H. Localized Sclero-derma. In: MayesMD (ed.) A Visual Guide to scleroderma and approach to Treatment Springer. DOI 10.1007/978-1-4939-0980-3. Science+Business Media New York, 2014; p. 5-21
- Hatomochi A, Ono M, Arakawa M, et al. Analysis of collagen gene expression by cultured fibroblasts in morphea. Br J Dermatol 1992; 126:216-221
- Scharffetter Kochanek K, Goldermann R, Lehmann P, et al. PUVA therapy in disabling pansclerotic morphea of children. Br J Dermatol 1995; 132: 830-831
- El-Mofty M, Zaher H, Basseila M. Low dose broad-band UVA in morphea using a new method for evaluation. Photoder-matol Photoimmunol Photomed 2000; 16: 43-49. DOI: 10.1034/j.1600-0781.2000.d01 -1.x
- Mayes MD, Lacey JV Jr, Beebe-Dimmer J, et al. Prevalence, incidence, survival and disease characteristics of systemic sclerosis in a large US population. Arthritis Rheum 2003; 48: 2246-2255
- Ягода A.B., Гладких H.H. Аутоиммунные аспекты нарушения коллагенового гомеостаза при недифференцированной дисплазии соединительной ткани. Медицинская иммунология 2007; 9(1): 61-68
- Козлова B.A., Сенникова С.В. Система цитокинов. Новосибирск: Наука, 2004; 324 с.
- Калинина Е.П., Иванов E.M., Исаченко Е.Г. Нарушения межсистемных взаимодействий при хроническом воспалительном процессе. Медицинская иммунология 2007; 9 (6): 581)
- Abbas АК, Lichtman АН. Basic Immunology 2-ed. Else-vier, 2004; 322 p.
- Иванов A.A., Гладких О.П., Кузнецова A.B., Данилова Т.И. Межклеточные и клеточно-матриксные взаимодействия в патологии. Молекулярная медицина 2005; 2: 16-21
- Sambo Р, Baroni SS, Luchetti М, et al. Oxidative stress in scleroderma: Maintenance of scleroderma fibroblast phenotype by the constitutive upregulation of reactive oxygen species generation through the NADPH oxidase complex pathway. Arthritis Rheum 2001; 44: 2653-2664.


