Цитопротекторный эффект цитофлавина при лечении термической травмы различной степени тяжести
Автор: Божедомов Алексей Юрьевич, Моррисон Виталий Викторович, Шулаева Наталия Михайловна, Никитина Виктория Владимировна, Иваненко Ирина Львовна
Журнал: Саратовский научно-медицинский журнал @ssmj
Рубрика: Физиология и патофизиология
Статья в выпуске: 1 т.8, 2012 года.
Бесплатный доступ
Цель: изучение цитопротекторного эффекта препарата цитофлавин при термической травме различной степени тяжести. Материал и методы. В исследование включено 169 больных с термическими ожогами с благоприятным исходом и тяжестью термической травмы от 30 до 170 баллов по Франку; 28 больных в составе комплексной терапии получали цитофлавин в стандартной дозировке. Результаты. Убольных с тяжестью термической травмы более 60 баллов по Франку при использовании цитофлавина отмечалось снижение выраженности синдрома системного воспалительного ответа (ССВО), уменьшение доли палочкоядерных нейтрофилов, более медленное снижение числа эритроцитов, меньшая активация тромбоцитопоэза, снижение концентрации фактора роста эндотелия сосудов. В группе больных с термической травмой менее 60 баллов, которые получали цитофлавин, выраженного положительного эффекта не выявлено. Заключение. Использование препарата цитофлавин наиболее эффективно при тяжести термической травмы более 60 баллов по Франку
Ожоги, цитофлавин, эндотелий
Короткий адрес: https://sciup.org/14917465
IDR: 14917465
Текст научной статьи Цитопротекторный эффект цитофлавина при лечении термической травмы различной степени тяжести
Адрес: 410012, г. Саратов, ул. Б. Казачья, 112.
Тел.: 89173114148.
у пострадавших с активаций перекисного окисления липидов, выбросом цитокинов и развитием синдрома системного воспалительного ответа [1–4].
Медицина в настоящее время не располагает эффективными средствами, способными предотвратить развитие системного воспалительного ответа и полиорганной недостаточности у пациентов с критическими ожогами, и многочисленные исследования направлены на поиск путей защиты органов.
Перспективным направлением представляется использование препаратов, улучшающих энергетический обмен, обладающих свойствами антиоксиданта, антигипоксанта и мембранопротектора. Одним из представителей этой группы является препарат цитофлавин.
Цель: изучить возможность цитопротекторного эффекта препарата цитофлавин у больных с термической травмой различной степени тяжести в динамике развития ожоговой болезни.
Методы. В исследование были включены 169 больных, находившихся на стационарном лечении в Саратовском центре термических поражений. Критериями включения в группу комплексного обследования пациентов являлось отсутствие тяжелой сопутствующей патологии, в частности заболеваний сердечно-сосудистой и дыхательной систем, периферической крови, а также инфекционных заболеваний. Обследуемый контингент пациентов включал преимущественно лиц мужского пола (78,1% от общего количества больных) (табл. 1). Все больные были в возрасте от 16 до 70 лет. В основу рандомизации групп наблюдения легли общеизвестные принципы оценки тяжести термической травмы [5], включающие определение площади ожоговой поверхности, глубины ожога, индекса Франка. В исследование вошли больные с тяжестью термического поражения от 30 до 170 баллов по Франку, причем только с благоприятным исходом термической травмы.
141 больной получал стандартную комплексную терапию, направленную на купирование болевого синдрома, восполнение объема циркулирующей крови, восстановление микроциркуляции, коррекцию метаболических расстройств и гемостаза, восполнение дефицита белка, устранение нарастающей интоксикации с использованием общепринятых медикаментозных средств. В указанный комплекс терапевтических мероприятий 28 больным включали цитофлавин, который вводили внутривенно курсом 10–14 дней 1–2 раза в сутки в стандартных дозировках, начиная с момента поступления в стационар.
В группу контроля вошли 19 здоровых доноров.
Для изучения цитопротекторного эффекта препарата цитофлавин при разной тяжести термического поражения были сформированы 4 группы: группа I A — больные с тяжестью поражения менее 60 баллов, получавшие стандартную терапию, I Б — больные с тяжестью поражения менее 60 баллов, получавшие лечение с использованием препарата цитофлавин, II А — больные с тяжестью поражения более 60 баллов, получавшие стандартную терапию, II Б — больные с тяжестью поражения более 60 баллов, получавшие лечение с использованием препарата цитофлавин.
У больных определяли количество эритроцитов, лейкоцитов, тромбоцитов периферической крови. Выраженность синдрома системного воспалительного ответа (ССВО) определяли по наличию двух и более критериев Чикагской согласительной конференции [6]. В качестве интегративного показателя стабильности биомембран изучали активность сывороточных трансаминаз (наборы реактивов фирмы
ДДС Виакон, Москва). Для оценки гипоксического поражения эндотелия применяли определение фактора роста эндотелия сосудов (ФРЭС) (наборы для иммуноферментного анализа фирмы «Bender Med-Systems», Австрия). С целью выявления некробиоти-ческих процессов в эндотелии сосудов определяли количество циркулирующих в крови эндотелиоци-тов (ЦЭК) по методике J. Hladovec в модификации Н. Н. Петрищева с применением фазово-контрастной микроскопии [7].
Данные исследования проводились на 1, 3, 7, 15, 30-е сутки с момента получения термической травмы.
Статистическую обработку осуществляли с использованием пакета прикладных статистических программ Statistica 8.0 (StatSoft, USA). Данные выражали в виде M±m, где М — среднее, m — ошибка среднего. Достоверность различий определяли с помощью t-критерия Стьюдента. Критерием достоверности разности средних величин считали величину p<0,05.
Результаты. Выраженность ССВО у больных с тяжелой и крайне тяжелой термической травмой (индекс Франка > 60 баллов) при проведении традиционной комплексной терапии была значительно выше, чем у пациентов с ожогом средней тяжести во все сроки наблюдения. ССВО при термической травме, оцененной менее 60 баллов по Франку, или совсем не возникает, или возникает на короткое время в период очищения и инфицирования ран (рисунок).
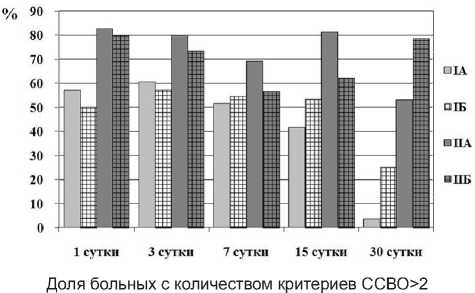
Применение препарата цитофлавин у больных с термической травмой средней тяжести несколько усиливает выраженность ССВО, что наблюдалось также и при других видах патологии [8] Использование этого препарата при тяжелой и крайне тяжелой термической травме снижает выраженность ССВО.
Использование препарата цитофлавин способствует развитию более выраженного лейкоцитоза как при термической травме среднетяжелой, так и при тяжелой термической травме по сравнению с больными, не получавшими цитофлавин. Однако
Таблица 1
Характеристики групп ожоговых больных, получавших традиционную терапию и терапию с использованием цитофлавина
|
Группа |
Индекс Франка, баллы |
Пол (муж./жен.) |
Возраст, лет |
Продолжительность лечения, сутки |
|
I A (n=66) |
47,5±1,2 |
48/18 |
40,8±1,2 |
37,6±2,2 |
|
I Б (n=11) |
49,3±3,1 |
9/2 |
34,9±4,4 |
33,7±3,1 |
|
II А (n=75) |
93,7±2,5 |
61/14 |
35,9±1,2 |
59,9±2,3 |
|
II Б (n=17) |
102,3±7,2 |
14/3 |
31,5±2,5 |
56,8±5,3 |
Таблица 2
Количество форменных элементов крови в динамике развития ожоговой болезни на фоне традиционной терапии и использования цитофлавина
|
Показатель |
Группа |
Этап исследования |
||||
|
1-е сутки |
3-и сутки |
7-е сутки |
15-е сутки |
30-е сутки |
||
|
I A (n=66) |
9,5±0,6 |
7,9±0,7 |
7,8±0,4 |
7,6±0,4 |
6,4±0,3 |
|
|
Лейкоциты, |
I Б (n=11) |
13,7±1,4* |
9,5±1,6 |
11,4±1,5* |
13,1±1,2* |
9,7±1,1* |
|
х10 9 /л |
II А (n=75) |
13,9±1,0 |
7,8±0,5 |
9,0±0,4 |
8,0±0,3 |
7,7±0,4 |
|
II Б (n=17) |
15,3±1,5 |
9,4±1,2 |
10,1±0,6 |
11,6±1,0* |
11,5±1,3* |
|
|
Контроль |
6,3±0,2 |
|||||
|
I A (n=66) |
6,6±1,4 |
12,4±1,9 |
12,9±1,5 |
9,7±1,0 |
3,7±0,5 |
|
|
Молодые |
I Б (n=11) |
9,9±2,2 |
16,1±5,6 |
15,7±3,9 |
13,0±2,0 |
6,5±2,1 |
|
гранулоциты, % |
II А (n=75) |
14,3±1,8 |
19,2±1,9 |
18,6±1,2 |
22,6±1,1 |
18,6±1,9 |
|
II Б (n=17) |
7,0±1,5* |
16,5±4,3 |
10,5±1,3* |
11,7±1,7* |
16,7±3,3 |
|
|
Контроль |
1,7±0,4 |
|||||
|
I A (n=66) |
4,8±0,1 |
4,0±0,1* |
3,9±0,1 |
3,6±0,0 |
4,2±0,6 |
|
|
Эритроци- |
I Б (n=11) |
4,9±0,4 |
4,5±0,2 |
3,8±0,2 |
3,6±0,1 |
3,4±0,3 |
|
ты, x1Q 12 /n |
II А (n=75) |
4,8±0,1 |
4,0±0,1 |
3,5±0,1 |
3,2±0,1 |
3,0±0,1 |
|
II Б (n=17) |
5,4±0,2* |
4,4±0,2* |
3,8±0,1* |
3,6±0,2* |
3,0±0,1 |
|
|
Контроль |
4,4±0,1 |
|||||
|
I A (n=66) |
374,4±61,1 |
244,8±39,1 |
406,6±80,2 |
483,4±43,4 |
413,5±63,3 |
|
|
Тромбоци- |
I Б (n=11) |
277,6±82,9 |
189,7±34,6 |
260,7±24,4 |
534,8±48,8 |
400,8±50,9 |
|
ты, х10 9 /л |
II А (n=75) |
365,6±53,1 |
231,4±36,1 |
379,1±47,3 |
674,5±55,7 |
634,0±37,3 |
|
II Б (n=17) |
243,8±19,8 |
159,9±23,1 |
204,8±18,1* |
389,3±42,6* |
594,4±52,2 |
|
|
Контроль |
231,4±45,7 |
|||||
П р и м еч а н и е : * — в этой и последующих таблицах р<0,05 по сравнению с соответствующим показателем I А или II А группы.
при этом у больных с индексом Франка более 60 баллов имеется снижение процента молодых форм нейтрофильных гранулоцитов по сравнению с группой пациентов, получавших традиционную терапию (табл. 2), что косвенным образом свидетельствует о более длительном функционировании лейкоцитов и меньшей активации лейкоцитарного пула у больных, получавших цитофлавин.
Включение препарата цитофлавин в лечение показало положительный цитопротекторный эффект в отношении эритроцитов периферической крови. При этом у больных с тяжелой термической травмой отмечался более выраженный эффект применения препарата (см. табл. 2).
Общее количество тромбоцитов косвенным образом отражает активацию системы свертывания крови. Проведение этапных некрэктомий, которое выполнялось через 7–13 суток после получения термической травмы и сопровождалось кровопотерей, активировало тромбоцитопоэз (см. табл. 2) во всех группах больных.
У больных, получавших в комплексе лечения ци-тофлавин, отмечались более низкие уровни тромбоцитов периферической крови, чем у пациентов, получавших стандартную терапию. При этом клинических и лабораторных показателей нарушения свертываемости крови у них отмечено не было. Число тромбоцитов в группе пациентов, получавших цитофлавин, не выходило за пределы нормальных значений, что может указывать на меньшую напряженность тром-боцитопоэза у этой категории больных и большей стабильности тромбоцитов при действии как токси- ческих факторов, так активаторов свертывания крови, попадавших в кровоток их ожоговых ран. К 30-м суткам этот показатель выравнивался у больных в группах с одинаковой тяжестью ожога (см. табл. 2).
Активность сывороточных трансаминаз, являющихся одним из показателей стабильности биологических мембран гепатоцитов и миоцитов, при термической травме различной тяжести держится на высоком уровне в течение всего времени наблюдения при проведении как традиционной комплексной терапии, так и терапии с использованием цитофла-вина (табл. 3).
В дальнейшем было изучено содержание в сыворотке крови десквамированных эндотелиальных клеток. Данный тест является объективным показателем, свидетельствующим о повреждении эндотелия сосудов [7]. Как видно из табл. 4, при проведении традиционной терапии количество циркулирующих эндотелиальных клеток возрастает спустя трое суток после нанесения травмы и держится повышенным в течение всего периода наблюдения. Эти нарушения более выражены при получении тяжелой термической травмы. Следует отметить, что включение в комплексную терапию препарата цитофлавин не оказывало существенного влияния на содержание в крови десквамированных эндотелиоцитов.
ФРЭС отражает как регенераторную активность эндотелия, так и проявления гипоксии тканей [9]. Этот показатель был подвержен большой вариабельности у больных всех групп. При ожоговой травме при проведении традиционной терапии наблюдается значительное возрастание уровня ФРЭС (см. табл. 4). При
Таблица 3
Активность АСТ и АЛТ в сыворотке крови в динамике развития ожоговой болезни на фоне традиционной терапии и использования цитофлавина
|
Показатель |
Группа |
Этап исследования |
||||
|
1-е сутки |
3-и сутки |
7-е сутки |
15-е сутки |
30-е сутки |
||
|
I A n=66 |
38,6±4,1 |
58,3±10,5 |
27,6±3,5 |
60,8±13,8 |
36,5±8,5 |
|
|
АСТ, Е/л |
I Б n=11 |
80,6±20,0* |
54,0±16,2 |
35,5±5,0 |
32,6±6,5 |
18,5±2,2 |
|
II А n=75 |
75,1±16,6 |
43,2±7,1 |
40,6±5,0 |
34,3±3,5 |
39,8±6,7 |
|
|
II Б n=17 |
45,4±9,5 |
65,3±21,2 |
49,2±10,1 |
39,5±4,8 |
29,1±2,0 |
|
|
Контроль |
17,6±2,0 |
|||||
|
I A n=66 |
34,8±4,6 |
40,5±6,5 |
34,4±3,7 |
61,8±9,6 |
34,2±7,9 |
|
|
АЛТ Е/л |
I Б n=11 |
60,1±15,1* |
34,1±7,0 |
40,9±10,4 |
37,4±9,9 |
18,9±3,1 |
|
II А n=75 |
44,183±6,1 |
31,0±3,6 |
41,3±8,5 |
41,7±5,0 |
42,1±7,0 |
|
|
II Б n=17 |
30,27±6,3,8 |
37,0±2,4 |
65,8±14,1 |
74,3±14,2* |
52,7±10,3 |
|
|
Контроль |
17,1±1,8 |
|||||
Таблица 4
Концентрация ФРЭС и число ЦЭК в плазме крови в динамике развития ожоговой болезни на фоне традиционной терапии и использования цитофлавина
Обсуждение. Цитофлавин находит свое применение во многих областях медицины, является испытанным средством в борьбе с интоксикацией и гипоксией, препаратом со свойствами антигипоксанта, антиоксиданта, мембранопротектора. Основой действия ци-тофлавина является активация утилизации глюкозы в цикле трикарбоновых кислот и, как следствие, усиление энергообеспечения клеток [10–12].
При термической травме отмечается тяжелое токсическое поражение клеток организма, которое обусловлено развитием тяжелой гипоксии, расстройствами регионарного кровотока и микроциркуляции, развитием метаболического оксидантного стресса, приводящего к усилению генерации активных форм кислорода, прогрессирующей активации процессов липопероксидации и ослаблению механизмов антиоксидантной защиты. Использование препарата ци- тофлавин в комплексной терапии ожогового шока обеспечивает положительную динамику метаболических сдвигов, препятствуя чрезмерной интенсификации процессов липопероксидации [3, 12].
Проведенное исследование показало, что комплексная интенсивная терапия с использованием метаболического корректора — препарата цитоф-лавин — способна замедлить развитие анемии, увеличить количество лейкоцитов при одновременном снижении доли незрелых форм нейтрофилов, ограничить возрастание количества тромбоцитов. Более низкие значения ФРЭС свидетельствуют о снижении гипоксического поражения эндотелия. Активация системного воспалительного ответа на поздних сроках наблюдения (15, 30-е сутки после получения травмы), вероятно, можно объяснить повышенной активацией клеток гранулоцитарного ростка, которые способны более длительное время эффективно выполнять свою функцию, а продуцируемые ими биологически активные вещества являются стимуляторами системной воспалительной реакции. Возможно, использование цитофлавина способствует развитию так называемого «второго удара», т.е. активированные вследствие травмы полиморфно-ядерные лей- коциты отвечают на последующие воздействия намного сильнее [13].
Заключение. Резюмируя приведенные данные, можно сделать заключение, что использование ци-тофлавина в комплексной терапии является эффективным при тяжелой и крайне тяжелой термической травме, оцененной по индексу Франка в 60 и более баллов. Эффективность данного препарата при среднетяжелой термической травме является сомнительной.
Список литературы Цитопротекторный эффект цитофлавина при лечении термической травмы различной степени тяжести
- Abdel-Hafez N.M., Saleh Hassan Y, El-Metwally Т.Н. A study on biomarkers, cytokines, and growth factors in children with burn injuries//Ann. Burns Fire Disasters. 2007. Vol. 20, № 2. P. 89-100.
- Обоснование применения антиоксидантной терапии при лечении синдрома эндогенной интоксикации у больных с тяжелой термической травмой/Н. М. Шулаева, Е. В. Куспиц, B. В. Щуковский, A.M. Фисун//Скорая медицинская помощь. 2010. №3. С. 76-81.
- Патогенез ожогового шока и термических поражений различной степени тяжести/Н. П. Чеснокова, Н.В. Полутова, Н. В. Островский, Т. А. Невважай//Шок как проявление дезадаптации при стрессе. М.: Академия естествознания, 2009. C. 237-279.
- Самойленко Г. Е. Синдром полиорганной недостаточности в хирургии ожогов у детей//Травма. 2000. Т. 1, № 1. С. 46-52.
- Парамонов Б.А., Порембский Я. О., Яблонский В. Г. Ожоги: рук-во для врачей. СПБ.: СпецПит, 2000. 488 с.
- Definitions for sepsis and organ failure and guidelines for the use of innovative therapies in sepsis/R.C. Bone, R.A. Balk, F. B. Cerra [et al.]. American College of Chest Physicians. Society of Critical Care Medicine Consensus Conference//Crit. Care Med. 1992. Vol. 20. № 6. P. 864-874.
- Петрищев H.H., Беркович О. А. Диагностическая ценность определения десквамированных эндотелиоцитов в крови//Клиническая лабораторная диагностика. 2001. № 1. С. 50-52.
- Показатели запрограммированной гибели лимфоцитов и нейтрофилов у лиц с алкогольной интокскацией в динамике терапии препаратов с антиоксидантными свойства-ми/Е. В. Жернова, Н. М. Вялова, А. Н. Бохан, С. А. Иванова//Вестник ТГПУ. 2009. № 3. С. 59-62.
- Ferrata N., Gerber Н.Р, Le Couter J. The biology VEGF and its receptors//Nat. Med. 2003, № 9. P. 669-676.
- Афанасьев В. В. Цитофлавин в интенсивной терапии. СПб., 2005. 35 с.
- Точки приложения цитофлавина на внутриклеточные биохимические процессы (обзор литературы)/П.С. Маркевич, С. Ю. Даниленко, А. В. Янкин, А. Н. Плеханов//Бюллетень ВСНЦ СО РАМН. 2011. № 1 (77). С. 232-246.
- Положительное влияние цитофлавина на сдвиги метаболического статуса при ожоговом шоке/Н.В. Полутова, Н. В. Островский, М. Г. Романцов, Н. П. Чеснокова//Экспериментальная и клиническая фармакология. 2011. Т. 74, № 7. С. 33-37.
- Михальчик Е.В. Показатели окислительного стресса при ожоговой травме: автореф. дис... д-ра биол. наук. М., 2006.


