Cовременные принципы лечения hallux rigidus
Автор: Мурсалов А.К., Иванов К.С., Дзюба А.М., Рогова М.С., Федотов Е.А., Шипилов А.С.
Журнал: Кафедра травматологии и ортопедии @jkto
Рубрика: Обзор литературы
Статья в выпуске: 3 (61), 2025 года.
Бесплатный доступ
Обоснование. Боль в области первого пальца стопы, вызванная артрозом первого плюснефалангового сустава (ПФС1), является одной из самых распространенных патологий стопы человека. При данной патологии болезненность обуславливается артрозным изменением сустава, движения в суставе становятся болезненные, подвижность сустава снижается [1]. Вышеуказанное является клиническим проявлением заболевания hallux rigidus. При диагностике данной патологии рентгенологическое исследование выявляет сужение суставной щели первого плюснефалангового сустава и наличие дорсальных остеофитов ПФС1 [3]. В клинической практике врача довольно часто встречаются пациенты с hallux rigidus. Этиология hallux rigidus охватывает целый ряд факторов, и существует множество подходов к лечению данного заболевания. На сегодняшний день, выбор метода лечения основан на комбинированной оценке клинических и рентгенологических данных. Цель этой статьи — обзор актуальных знаний о методах лечения hallux rigidus. Цель. Определение современных принципов консервативного и хирургического лечения заболевания первого плюснефалангового сустава hallux rigidus. Материалы и методы. Был проведен систематический поиск литературы в соответствующих базах данных с поисковыми терминами «hallux rigidus». Глубина поиска составила 24 года. Количество статей, использованных для написания данной работы – 42. Систематический обзор научных работ, посвященных лечению hallux rigidus, был проведен в соответствии с предпочтительными элементами отчетности для систематических обзоров и метаанализов (PRISMA). Результаты. В современной литературе представлено множество вариантов лечения hallux rigidus. Лечение hallux rigidus можно разделить на консервативное и хирургическое. Хирургическое лечение обычно разделяют на операции, сохраняющие первый плюснефаланговый сустав, и не сохраняющие первый плюснефаланговый сустав. Тактика лечения зависит от степени выраженности hallux rigidus, от клинической картины и жалоб пациента. При I–II степени поражения ПФС1 следует использовать такие методы как хейлоэктомия в сочетании c операцией Moberg, либо без неё, укорачивающая шевронная остеотомия. При hallux rigidus III степени существует опыт лечения методом эндопротезирования ПФС1, однако данный метод лечения имеет недостаточно положительную результативность и приводит к затруднениям последующих оперативных вмешательств. Данная методика требует дальнейших наблюдений и более глубоких клинических исследований. Таким образом, «золотым стандартом» лечения пациентов с hallux rigidus в поздних стадиях до настоящего времени остается артродезирование ПФС1. Также появились методики, с сопоставимыми клиническими результатами, но позволяющие сохранить подвижность в суставе, однако достаточного количества достоверных результатов долгосрочных исследований на данный момент нет.
Ригидный первый палец, hallux rigidus, остеоартроз первого плюснефалангового сустава
Короткий адрес: https://sciup.org/142246167
IDR: 142246167 | УДК: 617-089.844 | DOI: 10/17238/issn2226-2016.2025.3.70-82
Modern principles of hallux rigidus treatment
Introduction: pain in the area of the first toe caused by osteoarthritis of the first metatarsophalangeal joint (I MTP) is one of the most common pathologies of the human foot. In this pathology, painfulness is caused by arthritic changes in the joint, movements in the joint become painful, and joint mobility decreases [1]. The above is a clinical manifestation of hallux rigidus disease. When diagnosing this pathology, radiologic examination reveals narrowing of the articular gap of the first metatarsophalangeal joint and the presence of dorsal osteophytes of I MTP [3]. Patients with hallux rigidus are quite often encountered in the clinical practice of a physician. The etiology of hallux rigidus encompasses a variety of factors, and there are many approaches to the treatment of this disease. To date, the choice of treatment is based on a combined assessment of clinical and radiologic findings. The aim of this article is to review the current knowledge on the treatment of hallux rigidus. Research objective: to determine the modern principles of conservative and surgical treatment of the first metatarsophalangeal joint disease hallux rigidus. Materials and methods: A systematic literature search was conducted in relevant databases with the search terms “hallux rigidus”. The depth of the search was 24 years. The number of articles used for this paper was 42. A systematic review of research papers on the treatment of hallux rigidus was conducted according to the preferred reporting elements for systematic reviews and meta-analyses (PRISMA). Results: There are many treatment options for hallux rigidus in the current literature. Treatment of hallux rigidus can be divided into conservative and surgical treatment. Surgical treatment is usually divided into surgery that preserves the I MTP and surgery that does not preserve the I MTP. Treatment tactics depend on the severity of hallux rigidus, the clinical picture and the patient's complaints. For I-II degrees of first metatarsophalangeal joint damage, methods such as cheillectomy combined with or without Moberg surgery, shortening chevron osteotomy should be used. In the case of III degree hallux rigidus, there is experience with treatment by endoprosthesis of the I MTP, but this method of treatment has insufficient positive results and leads to difficulties in subsequent surgical interventions. This technique requires further observation and more in-depth clinical studies. Therefore, arthrodesis of the first metatarsophalangeal joint remains the "gold standard" for the treatment of patients with advanced hallux rigidus. However, other methods have emerged with comparable clinical results that allow preservation of joint motion, but there are not enough reliable results from long-term studies.
Текст научной статьи Cовременные принципы лечения hallux rigidus
Hallux rigidus (ригидный, или тугоподвижный, первый палец стопы) – это заболевание, характеризующееся дегенеративными изменениями гиалинового хряща первого плюс-нефалангового сустава [11].
Hallux rigidus встречается у 1 из 40 взрослых людей старше 50 лет и в два раза чаще встречается у женщин. Этиология данного заболевания не изучена в достаточной степени, но одной из наиболее частой причин развития hallux rigidus считают травму суставной поверхности первого плюснефа-лангового сустава [2].
Остеоартроз I плюснефалангового сустава по своей этиологии встречается как идиопатического, так и травматического генеза. Тыльное сгибание преимущественно ограничено из-за образования дорсальных околосуставных остеофитов. Кроме ограничения подвижности в суставе пациентов беспокоит болевой синдром, усиливающийся по мере прогрессирования дегенерации хрящевого покрова и образования остеофитов. В совокупности данные проявления hallux rigidus приводят к изменению биомеханики походки и снижают качество жизни пациентов [8, 12].
Комментарий
В данном систематическом обзоре рассматриваются методы, подтверждающие эффективность консервативных и хирургических методов лечения распространенного заболевания – остеоартроза первого плюснефалангового сустава.
Авторы исследований, использованных при подготовке в написании данной работы, предоставляют сбалансированную и объективную оценку методов лечения и делятся своим предпочтительным алгоритмом лечения hallux rigidus.
Материалы и методы
Был проведен систематический поиск литературы в соответствующих базах данных с поисковыми терминами «hallux rigidus». Глубина поиска составила 24 года.
Критерии включения в исследование:
– работы, имеющие высокий уровень достоверности
– работы с давностью выполнения не позднее 24 лет
– работы на английском и русском языках
Критерии невключения в исследование:
– работы, имеющие низкий уровень достоверности
– работы с давностью выполнения более 24 лет
– работы не на английском и русском языках
Был проведен систематический поиск литературы в соответствующих базах данных с поисковыми терминами «hallux rigidus»; «hallux limitus»; «stiff first toe»; «osteoarthritis of the first metatarsophalangeal joint».
Глубина поиска составила 24 года. Количество статей, использованных для написания данной работы – 42. Систематический обзор клинических руководств, посвященных лечению hallux rigidus, был проведен в соответствии с предпочтительными элементами отчетности для систематических обзоров и метаанализов (PRISMA).
Стратегия поиска и выбора исследований
Для сбора и селекции доказательств был проведен поиск в электронных базах данных, с предпочтением работ, имеющих высокий уровень достоверности.
Ссылки на источники информации указаны в тексте. Доказательная база для рекомендаций основана на публикациях из PubMed, Medline, Embase, Web of Science, eLibrary, Cyberlenika.
Использованные поисковые термины: «hallux rigidus», «hallux limitus», «first MTP arthritis».
Стратегия поиска в базе данных Pubmed была: ((hallux rigidus) ИЛИ (osteoarthritis of the first metatarsophalangeal joint)) И ((систематический обзор) ИЛИ (руководство) ИЛИ (метаанализ)).
Поиск работ происходил на английском и русском языках. Поисковые запросы отбирались по названию, аннотации и чтению полной статьи.
Результаты и обсуждение:
Этиология
Вопрос этиологии hallux rigidus остается открытым до настоящего времени. Согласно данным литературы, этиология HR сводится к нескольким факторам. J.T. Deland, B.R. Williams описывали, что травма является одной из основных причин появления ригидности первого пальца стопы [33]. Coughlin MJ, Shurnas PS в выборке пациентов, которым с 1981 по 1999 проводилась хейлэктомия и артродез I плюс-нефалангового сустава при ригидном первом пальце стопы отмечали, что ригидность связана с вальгусной деформацией первого пальца стопы, а двустороннее поражение связано с наследственностью и женским полом [12]. A. Migues, G. Slullitel описывали развитие дегенеративных изменений вызванными повторяющимися нагрузками, воспалительными или метаболическими заболеваниями, такими как подагра, ревматоидный артрит и серонегативные артропатии [9]. Также было высказано предположение, что повреждение суставной поверхности плюснефалангового сустава может быть вызвано расслаивающим остеохондритом. Биомеханические и структурные факторы, такие как длинная первая плюсневая кость, высокое положение плюсневой кости и приведение плюсневой кости, также могут повышать риск развития hallux rigidus [34].
Классификация
Система классификаций должна помогать в принятии решения о выборе тактики лечения и их возможного сравнения. Кроме того, классификация нужна для того, чтобы сравнить результаты различных исследований. Beeson et al. (2008) выполняли систематический обзор литературы и оценивали различные классификации hallux rigidus. Авторы отметили, что нет классификации, которая отвечала бы надежностью и валидностью. Принимая во внимание эти недостатки, они посчитали, что классификация M.J. Coughlin с соавторами наиболее приближена к «золотому стандарту» [35].
Один из вариантов классификации hallux rigidus – это рентгенологическая классификация Hattrup и Johnson, 1988 год:
-
• I стадия – незначительное сужение суставной щели, отсутствие остеофитов.
-
• II стадия – значительные изменения суставной поверхности, сужение суставной щели, остеофиты на головке первой плюсневой кости и основной фаланге, субхондральные кисты и зоны склероза.
-
• III стадия – фиброзный анкилоз сустава, выраженные остеофиты, отсутствие суставной щели.
Каждой рентгенологической стадии соответствует определенная клиническая картина. С учетом клинической картины можно выделить 5 стадий hallux rigidus по классификации Coughlin и Shurnas, таблица 1 (ОД – объем движений, ТС – тыльное сгибание, ПС – подошвенное сгибание):
Таблица 1
Стадии HR по Coughlin и Shurnas
|
Стадия |
Клинические параметры |
Рентгенологические параметры |
|
0 |
ТС = 40–60°(менее 20 % от нормального ОД), боли нет |
Норма |
|
1 |
ТС = 30–40° (менее 20-50 % от нормального ОД), небольшой болевой синдром |
Небольшие тыльные остеофиты, нормальная суставная щель |
|
2 |
ТС = 10–30° (менее 50-70 % от нормального ОД), умеренный болевой синдром, связанный с движением |
Умеренные тыльные (лате-ральные/медиальные) остеофиты, сужение суставной щели < 50 %, остеосклероз |
|
3 |
ТС < 10° (часто ПС < 10°), боль в крайних положениях ПФС1, отсутствие боли в середине движения |
Выраженные тыльные остеофиты, сужение суставной щели > 50 %, субхондральные кисты или эрозии, сесамовидные кости увеличены, кистозно/дегенеративно изменены |
|
4 |
Выраженная туго-подвижность, боль в крайних положениях ПФС1, боль в середине движения |
Выраженный тыльный остеофит, сужение полости сустава > 50 %, свободные тела или остеохон-дральные дефекты, сесамовидные кости увеличены, кистозно/ дегенеративно изменены |
Клиническая картина
Клиническая картина пациентов с hallux rigidus проявляется болью и ограничением движения в ПФС1. Кроме того, развивающиеся нарушения стереотипа походки, связанные с попыткой пациента перенести опору на латеральную колонну стопы, могут вызвать боли в латеральном отделе стопы. Пациенты также могут предъявлять жалобы на проблемы с подбором обуви из-за образования остеофитов на дорсальной поверхности головки 1 плюсневой кости и на проксимальной фаланге 1 пальца стопы. Также, в литературе существуют данные, что образовавшиеся остеофиты могут приводить к компрессии тыльного медиального кожного нерва стопы [2].
Физикальный осмотр
Осмотр стопы следует проводить в положении пациента стоя и сидя. В положении стоя следует оценивать динамическую функцию первого пальца стопы. В положении сидя, при расслабленных мягких тканях также оценивается активная и пассивная амплитуда движений.
При пальпации в области ПФС1 часто отмечается болезненность, больше по дорсальной поверхности. Пальпаторно оценивается наличие остеофитов. Как указывалось выше, образовавшиеся остеофиты могут приводить к компрессии тыльного медиального кожного нерва стопы, поэтому следует оценить чувствительность 1 пальца.
Оценка амплитуды движений в ПФС1 имеет решающее значение. Непосредственно подвижность указывает на степень тяжести остеоартроза. Наиболее распространённым признаком считается ограничение пассивных движений, особенно при тыльном сгибании. При наиболее легкой степени тяжести боль может возникать только в крайних положениях при пассивном тыльном или подошвенном сгибании. Если пациента беспокоит боль даже при движении в средней амплитуде, это указывается на более обширные артозные изменения сустава.
Также при физикальном осмотре следует обратить внимание на межфаланговый сустав 1 пальца стопы. Если межфаланговый сустав также имеет артрозные изменения, то это стоит учитывать при выборе хирургической тактики лечения. В подобных случаях следует избежать операции артродезирования ПФС1. При артродезировании ПФС1, с компенсаторной целью развивается гипермобильность межфаланогового сустава 1 пальца стопы. В случае артроза межфалангового сустава гипермобильность может не возникнуть, или возникнуть, вызвав болевой синдром у пациента, что в обоих случаях привет к нарушению походки и возможным повторным оперативным вмешательствам [2].
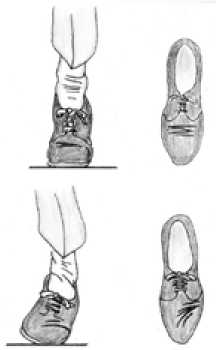
Рисунок 1 . Изменение походки пациентов с болевым синдромом при HR
Как указывалось выше, у пациентов с hallux rigidus могут возникать изменения походки. В попытках снизить болевой синдром, пациенты переносят опору на внешний край стопы, уменьшая нагрузку на первый плюснефаланговый сустав [36] (рис. 1).
Рентгенографическое исследование
Необходимо сделать передне-заднюю, боковую и косые проекции поражённой стопы. При оценке выполненной рентгенографии, следует учитывать некоторые особенности. Степень сужения суставной щели лучше всего видна на косой проекции. На более поздних стадиях ригидности первого пальца стопы в околосуставной области головки плюсневой кости и проксимальной фаланги можно наблюдать образование остеофитов. Также, по мнению авторов Deland и Williams, отмечалось, что наличие остеофитов может вводить в заблуждение относительно степени сужения суставной щели, поскольку остеофиты визуально могут ложно свидетельствовать о более тяжёлой форме остеоартроза. Другие рентгенологические признаки включают такие изменения как костный склероз и субхондральные кисты. Для диагностики заболевания или планирования операции, как правило, не требуется магнитно-резонансная томография (МРТ) и компьютерная томография (КТ). Рентгенологического исследования вполне достаточно для диагностики hallux rigidus.
Дифференциальная диагностика
Говоря о дифференциальной диагностике, необходимо провести важное различие между hallux rigidus и hallux limitus. В клинической практике hallux rigidus определяется как боль, вызванная артрозными изменениями сустава, в то время как hallux limitus определяется как функциональная боль, вызванная напряжением мягких тканей, как пример, мышечными контрактурами, длинной или приподнятой первой плюсневой костью (metatarsus primus elevatus). У пациентов с hallux limitus, при осмотре стопы в положении подошвенного сгибания, как правило, наблюдается повышенное тыльное сгибание I пальца стопы, так как в положении подошвенного сгибания стопы, снимается напряжение длинного сгибателя первого пальца и устраняется ограничивающий фактор. Однако следует отметить, что hallux limitus может прогрессировать до hallux rigidus, поэтому могут наблюдаться признаки обоих состояний.
Также дифференциальный диагноз следует проводить с деформацией и болевым синдромом при вальгусной деформации 1 пальца, подагрой, псевдоподагрой. Данные заболевания имеют сходные клинические проявления и приводят к деформирующему остеоартрозу плюснефалангового сустава, но этиология, патогенез и лечение имеет свои характерные особенности.
Консервативная терапия
Консервативная терапия hallux rigidus направлена исключительно на поддержание заболевания на текущей степени деформации и не исправляет её, соответственно, не восстанавливает объём движений. Основная задача консервативного лечения – это снизить воспалительный процесс, купировать болевой синдром и замедлить прогрессирование остеоартроза в первом плюснефаланговом суставе.
В ретроспективном обзоре 772 пациентов от 2002 года, страдающих hallux rigidus, сообщалось о 55 % успешных случаев консервативного лечения, и эти меры остаются первой линией лечения в большинстве случаев [4].
В своей работе, Ali S. Alshehri с соавторами указывает, что наиболее распространенным методом лечения было консервативное (66,7 %). Осложнения были минимальными (2,4 % инфекций, 1,2 % метатарзалгии), и 67,9 % пациентов сообщили об отсутствии беспокоящих симптомов после лечения [37].
Gabriele Colò с соавторами указывал, что блокады и внутрисуставные инъекции кортикостероидов приносят облегчение некоторым пациентам с HR, но только на ранних стадиях и длительность облегчения болевого синдрома сохраняется в течение 3–6 месяцев. Инъекции, обогащённой тромбоцитами плазмы, или аспирата костного мозга уменьшают боль и скованность в суставе, улучшая качество жизни, однако имеющиеся научные данные недостаточны для окончательных выводов. Также в этой работе приводились данные о применении ортопедической обуви и стелек для уменьшения боли, так как основное действие направлено на изменения биомеханики I плюснефалангового сустава. Также может быть полезна физиотерапия, включающая манипуляции с суставом, мобилизацию и улучшение подвижности. Тренировка походки, обеспечение покоя и прикладывание льда уменьшают болевой синдром и воспаление. Применение методов, таких как экстракорпоральная ударно-волновая терапия, ионофорез и ультразвуковая терапия также применяются при лечении HR. Однако доказательства, подтверждающие эффективность этих методов лечения, по-прежнему недостаточны [36].
Противовоспалительная терапия
Пероральные нестероидные противовоспалительные препараты (НПВП) являются основой консервативного лечения, они используются при болях и воспалительных процессах в суставах. Однако одних НПВП недостаточно, их следует сочетать с другими методами консервативного лечения. Кроме того, внутрисуставные инъекции оказались эффективными у некоторых пациентов с hallux rigidus. Нестероидные противовоспалительные препараты могут облегчить острую боль и снять отек, однако при длительном применении следует учитывать их потенциальные побочные эффекты со стороны сердца, почек и желудочно-кишечного тракта.
Ортропедический режим
Следует соблюдать определенный ортопедический режим, а именно избегать действий, приводящих сустав в положение тыльного сгибания. Это включает в себя бег и прыжки. Подъем по лестнице, по возможности, следует ограничить, что позволит уменьшить нагрузку на ПФС1 во время лечения.
Обувь
Выбор обуви очень важен, так как обувь с высоким каблуком приводит к избыточной нагрузке на ПФС1 при тыльном сгибании первого пальца, что, вероятно, со временем усугубляет симптомы. Некоторые виды обуви могут усиливать симптоматику, например, обувь с жёстким верхом и швами или вставками на тыльной части в области ПФС1, это обусловлено контактом обуви с образовавшимися при hallux rigidus остеофитами. Также ношение спортивной обуви, например, для футбола и гольфа, или рабочей обуви, способствует развитию заболевания. В отличие от вышеуказанного, обувь с мягким верхом и просторным носком минимизирует раздражение от контакта с остеофитами. Обувь с высоким носком может быть полезна для предотвращения прямого контакта между обувью и дорсальными остеофитами, тем самым снимая нагрузку с сустава. Также, для снижения нагрузки на I плюснефаланговый сустав, снижение в нём подвижности, рекомендуется носить обувь на жесткой подошве [36].
Внутрисуставные инъекции и блокады
По результатам рандомизированного исследования, Solan MC с соавторами пришли к выводу, что инъекции в I плюснефаланговый сустав могут обеспечить временное облегчение болевого синдрома. Рекомендуются как стероидные препараты, так и гиалуроновая кислота. Инъекции кортикостероидов наиболее полезны пациентам с менее тяжелой степенью артрита, их эффективность при тяжелом артрите снижена [13].
Pons M, Alvarez F, Solana J, Viladot R, Varela L. в 2015 году опубликовали собственное исследование. По результатам, при сравнении терапии гиалуроновой кислотой и терапии кортикостероидами в проспективном исследовании с участием 37 пациентов в обеих группах через 3 месяца было отмечено улучшение как функциональных возможностей, так и уменьшение болевого синдрома. Было показано, что гиалуроновая кислота превосходит инъекции кортикостероидов по результатам оценки с помощью визуальной аналоговой шкалы (ВАШ) при ходьбе через 28 и 56 дней. При клиническом обследовании не было выявлено различий между группами [14].
В исследование от 2001 года указывается, что эффект от внутрисуставных инъекций может сохраняться до шести месяцев у пациентов с ранними стадиями заболевания, а по мере прогрессирования заболевания эффект уменьшается, и пациентам в конечном итоге может потребоваться хирургическое вмешательство [37].
Также, в работе от 2021 года, посвящённой комплексному подходу к консервативному лечению пациентов с остеоартрозом первого плюснефалангового сустава, Д.В. Ильченко с соавторами указывает на краткосрочный положительный эффект после применения внутрисуставных инъекций. Однако, основываясь на современных литературных данных, авторы приходят к выводу, что на сегодняшний день не существует консервативного метода, позволяющего достичь стойкого положительного результата на различных стадиях остеоартроза ПФС1, что во многом связано с отсутствием комплексного подхода к диагностике и лечению заболевания. По результату своего исследования авторы приходят к выводу, что использование комплексного и структурированного подхода к лечению hallux rigidus с применением физических методов восстановительного лечения показало его высокую эффективность на ранних стадиях заболевания с наличием 96% положительных результатов по оценке пациентов. Медиана AOFAS для переднего отдела стопы по окончании курса составила 87 баллов, медиана итогового показателя повседневной функциональной активности по FAAM – 98 %, показатель спортивной активности – 97 % [42].
Хирургические методы лечения hallux rigidus
При низкой эффективности консервативной терапии hallux rigidus стоит применять хирургические методы лечения. Выбор метода хирургического лечения зависит от стадии заболевания.
Ранние стадии (I–II по Coughlin)
При hallux rigidus I–II стадии рекомендуется выполнять хирургическое лечение, направленное на сохранение плюснефалангового сустава. К таким методикам можно отнести хейлоэктомию, операцию Moberg, укорачивающую шевронную остеотомию.
Хейлоэктомия
Общие показания к хейлэктомии — это ригидность первого плюснефалангового сустава I–II стадии с наличием остеофитов, вызывающих раздражение и болевые синдромы при ношении обуви у пациентов, которым не помогло длительное консервативное лечение [6]. На стадии I (с легким ограничением тыльного сгибания и легкими степенями остеоартоза) хейлэктомия является предпочтительным методом лечения [5]. Данный метод хирургического лечения является примером классического щадящего подхода к лечению hallux rigidus, который на ранних стадиях заболевания демонстрирует хорошие результаты [11]. Хейлэктомия считается относительно простым методом хирургического лечения, который сохраняет подвижность 1 плюснефалангового сустава, что позволяет пациенту быстрее вернуться к повседневной деятельности. Сообщается о низком уровне осложнений после хейлэктомии (от 0% до 3%) [8].
Техника хейлэктомии I плюснефалангового сустава включает в себя удаление дорсальных остеофитов с головки плюсневой кости и проксимальной фаланги, а также удаление одной трети дорсальной суставной поверхности I плюсневой кости. Не рекомендуется удалять более 30 % дорсальной части головки I плюсневой кости, так как может развиваться нестабильной в 1ПФС, а проксимальная фаланга может вывихиваться. Результаты лечения после данного метода хирургического лечения – восстановление функции ходьбы, поскольку увеличивается объем тыльного сгибания в первом плюснефаланговом суставе, в результате чего увеличивается и максимальная сила отталкивания стопы в сагиттальной плоскости. Также стоит отметить, что риск развития тромбоза глубоких вен после хейлоэктомии составляет менее 1 % и снижается значительнее, если пациентам сразу после операции рекомендуется полностью опираться на ногу в специальной послеоперационной обуви [7].
Также одним из вариантов выполнения хейлоэктомии является артроскопическая методика выполнения операции. Преимуществом является малоинвазивная техника исполнения, что еще более благоприятно влияет на процесс восстановления пациентов после проведенной операции. Несмотря на преимущество артроскопической методики над стандартной открытой методикой хейлоэктомии, для исполнения необходимо дополнительное оборудование и навык владения артроскопической техникой. На сегодняшний день нет объективных данных по сравнению методик артроскопической и открытой хейлоэктомии.
Несмотря на все преимущества хейлоэктомии, стоит учитывать, что хейлэктомия не предотвращает прогрессирование заболевания и редко является окончательным решением проблемы. Образование дорсальных остеофитов наблюдается в 31 % случаев у пациентов с продолжающимся остеоартрозом 1ПФС [8].
Операция Moberg
Операция Moberg заключается в проведении дорсальной клиновидной остеотомии основной фаланги 1-го пальца, что увеличивает тыльное сгибание 1-го пальца, однако достигается это ценой уменьшения объема подошвенного сгибания 1-го пальца (рис. 2).
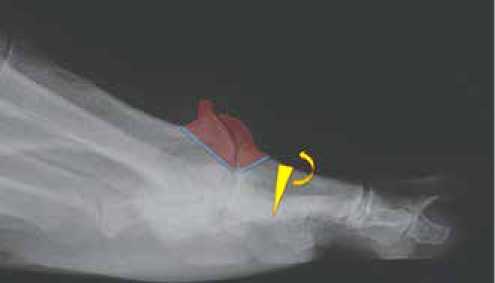
Рисунок 2 . Операция Moberg
Операция Moberg редко может выполняться как отдельная процедура, чаще её выполняют в сочетании с хейлоэктомией, либо в качестве следующего этапа после хейлоэктомии. Данный метод хирургического лечения является оптимальным выбором для пациентов с hallux rigidus I–II стадии при сохранённой суставной щели. В сочетании с хейлектомией операция Moberg обеспечивает хорошие функциональные результаты с низким риском осложнений. Итог операции – смена точки контакта суставных поверхностей. В норме при тыльном сгибании контакт происходит в дорсальной части сустава. При HR эта зона разрушена, а нагрузка после операции Moberg переносится на подошвенную часть сустава, где хрящ ещё сохранён.
В своей работе от 2015 года Paul Hyon-Uk Kim с соавторами указывает, что потенциальная краевая нагрузка на дорсальную часть хряща после хейлэктомии может быть предотвращена при остеотомии Moberg благодаря смещению центра давления в подошвенную сторону [37]. Однако данные о необходимости применения операции Moberg разнятся. Существует точка зрения, что добавление остеотомии Moberg существенно не изменяет краткосрочные и среднесрочные результаты хейлэктомии для лечения hallux rigidus, о чем свидетельствует существующий метаанализ Jaeyoung Kim с соавторами от 2023 года [38, 39].
Укорачивающая шевронная остеотомия
В качестве альтернативы хейлоэктомии и операции Moberg можно рассматривать укорачивающую шевронную остеотомию I плюсневой кости. Некоторые авторы описывают лечение hallux rigidus методом модифицированной шевронной остеотомии, укорачивающей 1 плюсневую кость. Предложена новая модификация шевронной остеотомии, при которой дорсальная часть распила остеотомии выполняется перпендикулярно горизонтальной плоскости первой плюсневой кости. Основное преимущество заключается в том, что это позволяет гораздо легче и точнее произвести дорсальный трапециевидный клин, особенно для коррекции угла наклона суставной поверхности головки первой плюсневой кости по отношению к её оси (PASA). К другим преимуществам относится возможность выполнения дорсального закрытоугольного клина, особенно для декомпрессии плюснефалангового сустава при умеренной степени ригидности первого пальца стопы, а также фиксация окончательной остеотомии одним винтом [10]. Основные этапы выполнения трапециевидного клина представлены на рисунках 3, 4, 5.
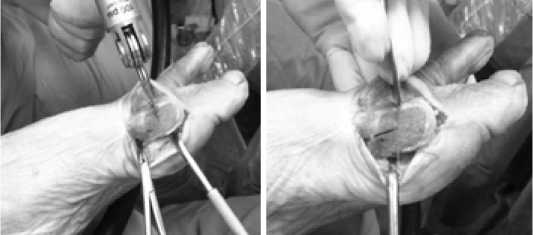
Рисунок 3 . Этап остеотомии Рисунок 4. Этап остеотомии
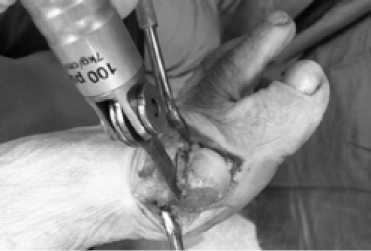
Рисунок 5. Этап остеотомии
Послеоперационное наблюдение за пациентами с выполненной модифицированной шевронной остеотомией показывает хороший результат лечения.
В исследовании от 2015 года Michele Vasso с соавторами указывается, что средний балл AOFAS улучшился с 56,6 (диапазон 49–64) балла до операции – до 90,6 (диапазон 81–94) балла после операции, а средний показатель боли по ВАШ снизился с 5,7 (диапазон 4–8) до операции – до 1,6 (диапазон 0–3) после операции [10].
Поздние стадии (III–IV)
При hallux rigidus III–IV стадии деформация и ограничение подвижности в ПФС1 значительно прогрессируют. На поздних стадиях можно попытаться сохранить движение в суставе используя методики интерпозиционной артропластики или эндопротезирования, либо произвести артродезирование ПФС1. В современно литературе описываются преимущества и недостатки каждого из данных методов.
Интерпозиционная артропластика I плюснефалангового сустава
Интерпозиционная артропластика I плюснефалангового сустава выполняется как суставосохраняющий метод лечения III стадии заболевания, и может выполняться несколькими методами:
-
1. Интерпозиция капсулы. Из апоневроза и капсулы сустава выкраивают лоскут, который служит интерпозиционным материалом.
-
2. Интерпозиция сухожилия (интерпозиция алло- или аутотрансплантата). Во время операции из сухожильного лоскута формируется спейсер который помещается в сустав.
-
3. Интерпозиция синтетических материалов. Например, интерпозиция Polyvinyl Alcohol Hydrogel (PVA) используется для замещения хрящевых дефектов головки первой плюсневой кости.
P.K. Givissis, P.D. Symeonidis, D..M Kitridis в своей работе указывают интерпозиционную артропластику ПФС1 с использованием аллографта широкой фасции бедра после предварительной хейлотомии. Анализ даннной методики проведен среди 18 пациентов. Авторы пришли к выводу, что методика позволяет добиться хороших среднесрочных результатов, особенно у пожилых пациентов. К преимуществам метода можно отнести сохранение функциональности I ПФС, простоту технического исполнения и получение пластического материала [15]. Однако следует учитывать недостатки методики, такие как дополнительный хирургический доступ к фасции бедра.
Модифицированна косая капсульная интерпозиционная артропластика Келлера (MOKCIA)
В своей работе от 2014 года J.E. Johnson с соавторами публикуют результаты анализа проведенной модифицированной косой капсульной интерпозиционной артропластики Келлера. По мнению авторов, альтернативой радикальным операциям для молодых пациентов, которые хотят сохранить подвижность первого пальца стопы может стать артропластика с использованием собственного биологического импланта. При этом не исключаются радикальные операции в случае неудачи. Авторы отмечают, что послеоперационный режим и период восстановления аналогичны таковым при дорсальной хейлэктомии и относительно коротки по сравнению с артродезом [29].
Среди методов артропластики метод MOKCIA показал более низкий уровень осложнений по сравнению с другими методами артропластики. Также данный метод является дешевле и не требует установки сторонних имплантов, что снижает риск аллергических реакций у пациентов. Некоторые авторы указывают, что MOKCIA обеспечивает лучшее распределение нагрузки на стопу, чем артродез [31, 32] и позволяет избежать недостатков артропластики с использованием имплантов.
Данный метод хирургического лечения hallux rigidus заключается в том, что в сустав вводится дорсальная часть капсулы плюснефалангового сустава первого пальца стопы, что снижает боль без ущерба для объема движений [29]. Важно сохранить крепление плантарной пластинки на проксимальной фаланге для поддержания стабильности в суставе. Метод MOKCIA не требует полной резекции I плюснефалангового сустава стопы, сохраняет его стабильность и не изменяет длину первого пальца (рис. 6, 7, 8). В то время как в оригинальном описании артропластики с резекцией по Келлеру выполнялась резекция всего основания проксимальной фаланги, процедура MOKCIA, использует дорсальную хейлэктомию и частичную резекцию фаланги с сохранением плантарной пластинки и коротких сгибателей ПФС1, что приводит к сохранению более правильной биомеханике сустава.
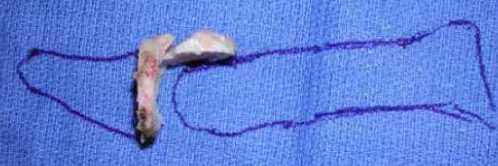
Рисунок 6. Удаленные костные фрагменты
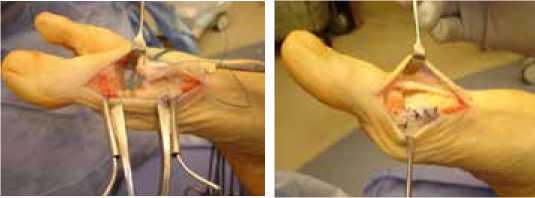
Рисунок 7. Этап подшивания капсулы
Рисунок 8. Ушивание капсулы с медиальной стороны
При выполнении стандартной артропластики по методу Келлера у пациентов были отмечены метатарзалгия или когтеобразная деформация первого пальца, когда плантарная пластинка отделялась при более агрессивной резекции проксимальной фаланги. Как отмечают авторы исследования, пациент должен быть проинформирован о таких возможных осложнениях, однако методика MOKCIA, которая сохраняет прикрепление подошвенной пластинки, должна свести к минимуму вышеуказанные осложнения [30].
Стоит отметить, что для операции MOKCIA не проводились долгосрочные рандомизированные контролируемые исследования, но по мнению авторов, полученные результаты сопоставимы с другими альтернативами лечения hallux rigidus на поздней стадии. По мнению авторов данные результаты свидетельствуют о том, что MOKCIA может быть подходящей альтернативой для лечения hallux rigidus у молодых активных пациентов [29].
Эндопротезирование I плюснефалангового сустава
Эндопротезирование I плюснефалангового сустава выполняется при поздних стадиях hallux rigidus и является альтернативой выполнения операции артродезирования (рис. 9).
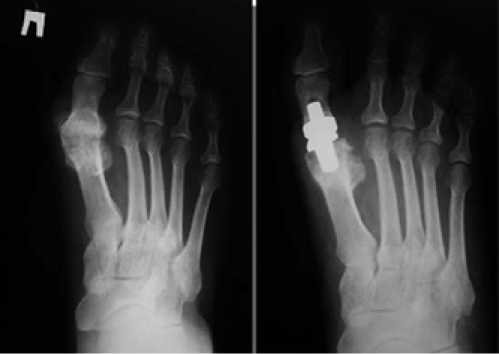
Рисунок 9. Тотальное эндопротезирование ПФС1
По типу конструкции эндопротезирование может быть как однополюсным, так и двухполюсным (тотальным). Тотальное эндопротезирование также можно разделить по виду фиксации импланта. Фиксация протеза существует цементная и бесцементная. По материалу изготовления эндопротезы делятся на силиконовые, металлические и керамические. При выборе тактики лечения, стоит учитывать, что эндопротезирование ПФС1 требует большей предоперационной подготовки, это технически более сложный метод лечения, имеющий противопоказания, такие как остеопороз, выраженная деформация или неблагоприятный инфекционный анамнез пациента.
Несмотря на то, что несколько авторов сообщали об удовлетворительных результатах после эндопротезирования [16], высокие показатели остеолиза, нестабильности имплантата ограничивают его использование [17, 18].
При первоначальных попытках замены I плюснефалангового сустава использовались силиконовые имплантаты «Silastic». Результаты лечения hallux rigidus данным методом отмечали некоторые отрицательные результаты. Силиконовые имплантаты не только приводили к остеолизу и нестабильности импланта, но и вызывали иммунную реакцию, которая приводила к дополнительным осложнениям. В результате потеря костной ткани становилась клинической проблемой при последующей попытке артродезирования, поэтому сегодня эти имплантаты используются крайне редко [8, 19].
Эффективность использования металлических имплантов также показала неоднозначные результаты. По данным некоторых авторов частота повторных операций в течение 5 лет после операции в нескольких хорошо проведённых исследованиях по эндопротезированию первого межфалангового сустава составляет от 5,5 % до 24,1 %. Кроме того, у трети пациентов при среднем сроке наблюдения было обнаружено проседание имплантата [8, 18, 20].
Керамические имплантаты показали аналогичные плохие результаты: частота повторных операций составляет от 26 % до 32 %. Осложнения включали 1 поверхностную инфекцию раны, а в 5 случаях (16 %) была проведена повторная операция из-за нестабильности импланта или появления боли. Выживаемость имплантатов составила 92 % через 5 лет, 85 % через 7 лет и 68 % через 9 лет [21, 22].
Ретроспективный анализ 21 случая эндопротезирования головки первой плюсневой кости показал, что по сравнению с группой из 27 пациентов с артродезом, уровень удовлетворённости после эндопротезирования был ниже, показатели боли по шкале ВАШ были выше, а показатели AOFAS были хуже, чем у группы пациентов с артродезом [18].
В исследовании от 2014 года Г.М. Кавалерский с соавторами предоставили результаты лечения 12 пациентов с hallux rigidus, из них 7 мужчин (55 %) и 5 (45 %) женщин, лечение проводилось в период с 2010 по 2012 гг. Средний возраст пациентов составил 59,5 лет (минимальный возраст в группе пациентов 42 года, максимальный – 73). По данным работы, несмотря на небольшое количество операций, в выборе хирургической тактики лечения проводимых при hallux rigidus сохраняются разногласия относительно показаний к операции.
В исследовании от 2005 года J.N. Gibson, C.E. Thomson опубликовали работу, сравнив тотальное эндопротезирование и артродезирование ПФС1. По мнению авторов результаты после артродеза были лучше, чем после эндопротезирования. Результаты были частично обусловлены неприемлемо высокой частотой расшатывания компонентов фаланг, что приводило к удалению имплантатов. Однако даже с учетом данных о неудачах большинство пациентов явно предпочитали артродез [17].
Эндопротезирование первого плюснефалангового сустава, в сравнении с артродезом, технически более требовательная операция, и требует тщательного планирования и подготовки. Тем не менее, по мнению авторов, эндопротезирование является одним из методов, достоверно позволяющим устранить болевой синдром и восстановить амплитуду движений в полном объеме. Таким образом, Г.М. Кавалерский с соавторами пришли к выводу, что тотальное эндопротезирование является перспективой развития в хирургическом лечении остеоартроза первого плюснефалангового сустава, но требует тщательного анализа отдаленных результатов [41].
Гемиартропластика гидрогелем из поливинилового спирта
В 2016 году FDA 1 предварительно одобрили использование Polyvinyl Alcohol Hydrogel (PVA) – гидрогелевого имплантата из поливинилового спирта (ПВС) в Соединенных Штатах. Материал имплантата по свойствам аналогичен суставному хрящу человека с точки зрения процентного содержания воды, прочности при растяжении и модуля упругости при сжатии [23, 24]. Имплант удерживается на месте с помощью запрессовки и должен фиксироваться ровно на 1,5 мм, что позволяет ему выполнять функцию как однополюсного эндопротеза (гемиартропластика), так и межпозиционной вставки между пораженными артрозом поверхностями (рис. 10, 11) [25].
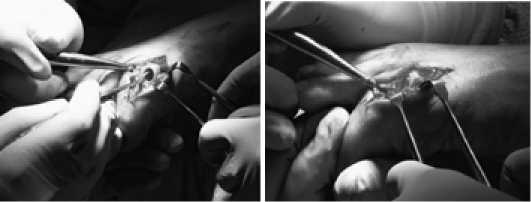
Рисунок 10. Имплант из ПВС
Рисунок 11. Имплант из ПВС
Проспективное рандомизированное исследование от 2016 года, в котором сравнивали гидрогелевый имплантат ПВС с артродезом, показало, что послеоперационная боль, функциональность и частота повторных операций были схожими в обеих группах через 12 и 24 месяца, однако подвижность улучшилась на 27 % в группе с гидрогелевым имплантатом ПВС [26].
В исследовании от 2017 года аналогичные результаты в группе с гидрогелевым имплантатом ПВС и в группе с артродезом были подтверждены у пациентов с деформацией до 20 градусов и выраженной тугоподвижностью до операции [27]. Подгруппа из 29 пациентов была доступна для проспективного наблюдения в течение 5 лет, и было показано, что показатели боли по шкале ВАШ, опросника SF-36, опросника для оценки состояния стопы и голеностопного сустава (FAAM) в повседневной жизни и спортивных подшкалах FAAM улучшились и были близки к показателям, полученным в ходе первоначального исследования. Только 1 пациенту (4 %) потребовалась повторная операция по артродезу [28]. Ни в одном из исследований не было выявлено случаев износа имплантата, нестабильности или остеолизиса [26, 28]. Кроме того, было показано, что замена гидрогелевого
1Food and Drug Administration (FDA) — агентство Министерства здравоохранения и социальных служб США, один из федеральных исполнительных департаментов.
имплантата из поливинилового спирта на артродез дает результаты, эквивалентные первичному артродезу, что является существенным улучшением по сравнению с предыдущими попытками первичного эндопротезирования сустава [26]. Ранние и промежуточные результаты применения гидрогеля из поливинилового спирта показывают хорошие результаты, однако долгосрочных исследований еще не проводилось.
Артродезирование 1 плюснефалангового сустава
Говоря о III и IV стадии hallux rigidus, при ограничении движения в первом плюснефаланговом суставе, а также наличии угловой деформации, остеофитов, нервно-мышечной этиологии развития болезни и слабости костной ткани многие авторы считают преимущественным методом лечения операцию артродезирования [8].
На сегодняшний день операция артродезирования 1 плюснефалангового сустава признана «золотым стандартом» оперативного лечения hallux rigidus. Суставные поверхности 1ПФС и образовавшиеся остеофиты резецируются, сустав фиксируется пластиной или винтами (рис. 12, 13). Данный метод хирургического лечения долгое время являлся предметом дискуссий. Некоторые авторы подчеркивают суставоразрушающий характер данного вида лечения и относительно длительный период восстановления пациентов в сравнении с суставосберегающими методами лечения hallux rigidus [9].
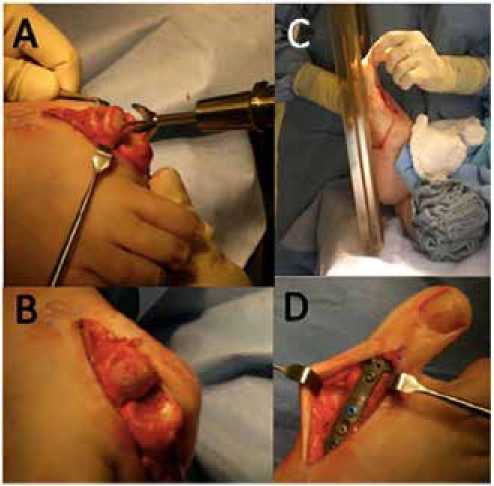
Рисунок 12. Этапы артродезирования ПФС1
В 2020 году Д.В. Ильченко, А.В. Королев, А.А. Карданов, в своей работе провели анализ отдаленных функциональных результатов после артродеза первого плюснефалангового сустава при деформирующем остеоартрозе. По мнению авторов стабильность первого луча и отсутствие боли в ПФС1 являются залогом положительного исхода лечения, а функция стопы после артродеза ПФС1 отличается незначительно от других оперативных пособий. Результат выполненной работы указывает на высокую эффективность данного вида оперативного лечения у пациентов с выраженным осеоартрозом ПФС1. Положительные результаты были получены в 92 % случаев хирургических вмешательств. Высокие показатели, полученные при изучении отдаленных функциональных результатов, позволяют рекомендовать артродез как основной метод лечения hallux rigidus 3–4 стадии по классификации Coughlin и Shurnas [40].
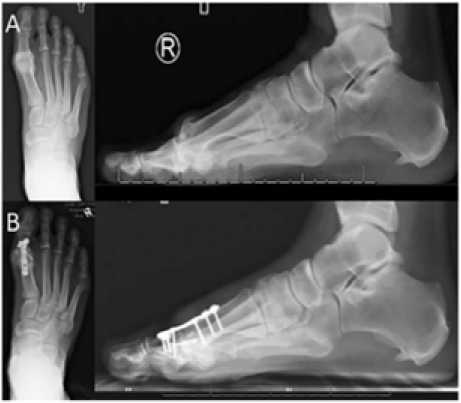
Рисунок 13. Рентгенограмма до и после артродезирования ПФС1
Выводы
Hallux rigidus является одним из самых распространённых заболеваний переднего отдела стопы человека. В современной литературе описано множество вариантов лечения пациентов с данной патологией. Имея достаточно доказанных данных из литературы, можно утверждать, что лечение пациентов с hallux rigidus следует начинать с консервативной терапии. При недостаточном положительном эффекте стоит применять хирургические методы лечения, которые в свою очередь можно разделить на сохраняющие и не сохраняющие первый плюснефаланговый сустав. В зависимости от степени поражения сустава и клинических проявлений тактика хирургического лечение будет варьироваться.
При I-II степени поражения I плюснефалангового сустава хорошие результаты показывают такие методы как хейлоэктомия в сочетании c операцией Moberg, либо без неё, укорачивающая шевронная остеотомия.
При hallux rigidus III и IV степени появились методики лечения, с сопоставимыми артродезированию клиническими результатами, но позволяющие сохранить подвижность в суставе. Такие методы хирургического лечение, как модифицированна косая капсульная интерпозиционная артропластика Келлера (MOKCIA) и гемиартропластика гидрогелем из поливинилового спирта. Данные методики показывают хорошие результаты лечения, однако достаточного количества достоверных результатов долгосрочных исследований на данный момент нет.
Также при поздних стадиях hallux rigidus существует опыт лечения в виде эндопротезирования I плюснефалангового сустава, однако данный метод имеет недостаточно положительную результативность и приводит к затруднениям выполнения последующих оперативных вмешательств. Данная методика требует дальнейших наблюдений и более глубоких клинических исследований. «Золотым стандартом» лечения пациентов с hallux rigidus на поздних стадиях до настоящего времени остается артродезирование I плюснефалангового сустава.


