Деструкция биопленок коагулазонегативных стафилококков под действием бактериальных катионных пептидов
Автор: Коробов В.П., Лемкина Л.М., Полюдова Т.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 3, 2015 года.
Бесплатный доступ
В результате проведенных исследований установлено, что бактерии разных штаммов коагулазоне-гативных стафилококков обладают выраженной способностью к образованию биопленок. Динамика роста биопленок бактерий разных штаммов существенно различается. Биопленки, образованные антибиотикочувствительными бактериями, достигают своего максимума через сутки. Пленкофор-мирующий процесс бактерий полирезистентного штамма развивается более медленно, характеризуется перманентным ростом и достигает максимума лишь на 4 сутки. Предупреждение развития биопленок стафилококков возможно при внесении в среду роста низкомолекулярных антибактериальных катионных пептидов - варнерина и хоминина. Как показали эксперименты, данные пептиды способны не только предупреждать развитие биопленок, но и активно разрушать уже сформированные зрелые биопленки коагулазонегативных стафилококков.
Антибиотикорезистентность, биопленки, катионные антибактериальные пептиды, коагулазо-негативные стафилококки
Короткий адрес: https://sciup.org/147204728
IDR: 147204728 | УДК: 579.22
Destruction biofilms of coagulase-negative staphylococci by bacterial cationic peptides
Pronounced ability of different strains of coagulase-negative staphylococci to form biofilm was found. Dynamics of biofilm growth considerably different among the bacteria of varies strains. Biofilm, formed by antibiotic susceptibility bacteria, reaches its peak after a day. Biofilm formation of multidrug-resistant strains was more slowly process, which is characterized by permanent growth and reaches a maximum only 4 day. Introduction into the growth medium low molecular weight cationic antimicrobial peptides warnerin and hominin can prevent the development of staphylococcal biofilms. These peptides are not only able to prevent the development of biofilm, but also to actively destroy the already formed mature biofilms of coagulase-negative staphylococci.
Текст научной статьи Деструкция биопленок коагулазонегативных стафилококков под действием бактериальных катионных пептидов
Уникальные биологические особенности бактерий, такие как наличие разнообразных механизмов адаптации к постоянно меняющимся параметрам сре-ды: позволяют их подавляющем}7 большинству' сохранять жизнеспособность и поддерживать опреде-пенную численность тюпуляции даже в самых экстремальных и агрессивных условиях. Одними из самых значимых адаптивных свойств бактерий является их способность формировать биопленки на грани цах раздела фаз, а также быстрое формирование устойчивости к токсичным соединениям и, в частности, к антибиотикам. В настоящее время считается, что эти два чрезвычайно важных проищи взаимосвязаны, поскольку развитие а нгибиотикорезистентности бактерий в составе биопленки происходит значительно быстрее [Лямин и др. 2012].
Широкое применение б медицинской практике биоматхриалов и искусственных устройств (дре-
电 Коробов В. П., Лемкина Л. М., Полюдова Т. В., 2015
нажи* катетеры, сетки, протезы) способстБует формированию на их поверхностях бактериальных биопленок и повышает риск распространения инфекции в организме [Псрспанова, 2013]. Заболевания, обусловленные биоматсриал-ассоциированны-ми инфекциями, требуют более тщательного подбора доз антибактериальных препаратов, поскольку минимальные ингибирующие концентрации антибиотиков для бактерий в составе биопленок значительно превышают таковые для планктонных клеток [Frank et al.. 2007]. Учитывая высокую приспособляемость бактерий к антибиотическим соединениям, наиболее остро стоит вопрос о поиске средств, эффективно препятствующих образованию биопленок и способствлтощих разрушению зрелых бактериальных пленок. К группе таких соединений, по-видимом>; мопгт быть отнесены антибактериальные катионные пептиды, выделяемые всеми живыми организмами, в том числе, и самими бактериями [Коробов, 2011; Jorge et al, 2012]. Для катионных пептидов варнерина и хоминина, выделенных из коагуглазонегэтивных стафилококков, показана высокая эффективность предотвращения адгезии к полистирол бактерий Staphylococcus epidermidis [Eroshenko. Korobow 2015] и Propion / b acien if tn acnes [Полюдова и др. 2015]t
Целью настоящей работы явилось изучение динамики формирования биопленок на поверхности полистирола чувствительными и антибиотикорезистентными бактериями разных штаммов коаг ) ла- 而 негативных стафилококков (КНС)* а также экспериментальное обоснование возможности применения а нтиба ктериа льных пептидов варнерина и хомнннна для предупреждения пленкообразования и разрушения зрелых биопленок КНС.
Материалы и методы исследования
В качестве объекта исследования использовали ба ктерии коа г^лазонегативных стафилококков (КНС): Staphylococcus epidermidis ГИСК 33 (「 осу-дарственная коллекции патогенных микроорганизмов Государственного на^но-исследователь-ского ннстнтута стандартизации и контроля медицинских и биологических препаратов, Москва), полученный селекционным путем штамм, устойчивый к ципрофлоксацину' 5 : epidemidis ЗЗ-Cf1 [Коробов и др., 2015]. Кроме того, при скрининге более 1000 клинических штаммов КНС, обладающих резистентностью к антибиотикам, был выделен штамм стафилококков, обладающий устойчивостью к 10 антибиотикам. Штамм получил лабораторный порядковый номер 831. Проведенная процедура идентификации с использованием диагностического набора StaphVest 24 (Lachema, Чехия), позволила отнести эти бактерии к вш^у У xyhsus.
Культивирование микроорганизмов проводили на модифицирова иной жидкой богатой питательной среде Luria-Bertani (LB), содержащей (г/л):
триптон (Sigma) - 10.0, дрожжевой экстракт (Sigma)-5 Д КС1-64
Планктонные культуры стафилококков выращивали при 37℃ на ротационном шейкере CERTOMAT IS (Sanorius, Германия) при 150 об/мин. Интенсивность роста в жидких к>гльтуграх оценивали по оптической плотности при длине волны проходящего света 600 нм (口 D^J на спек-тро 巾 отометре PD-3O3 (Япония).
Культуры бактерий, выращенные на среде LB до середины лог-фазы, разводили свежей питательной средой до оптической плотности OD^oo 0.015 (107^КОЕ/мл) и вносили по 100 мкл в лунки плоскодонных полистироловых планшетов (Мед-полимер* Россия). Культивирование проводили в течение 15 сут при 37℃ в термостате. Далее планктонные клетки аккуратно удаляли, лунки дважды промывали 200 мкл 10 мМ фосфатного буфера (pH 7.2).
Для оценки влияния антибактериальных пептидов на формирование биопленок; в лунки планшетов одновременно вносили по 90 мкл среды LB с растворенными в ней препаратами варнерина или хоминина в количестве 8-128 мг/мл. После чего добавляли 10 мкл индикаторных бактериальных культур, содержащих 106> : КОЕ/мл.
Для изучения влияния пептидов на уже образовавшиеся биопленки растворы варнерина и хоми-нтна в LB вносили в ^гнки с Отмыты\ги ^иопден-ками и культивировали в течение 24 ч. В контрольном варианте биопленки инкубировали с0.14 М раствором NaCl. Затем из jij hok планшетов удаляли жидкую часть, лунки промывали фосфатным буфером и подсушивали. Далее для определения биомассы пленок б каждую лунқу планшета вносили по 100 мкл 0.1%-ного раствора генцианвио-лета в 0.14 М растворе NaCl? выдерживали 20 мин.. 箍 тем краситель удаляли, лунки дважды промывали фосфатным буфером, высушивали, и производили экстракцию связавшегося с биопленками красителя 96%-ным этанолом (100 мкл на лунку) в течение 20 мин. Количественную оценк5г этанольных экстрактов осуществляли на микропла ншетнойі спектрофотометре Benchma rk Plus , (Bio-Rad, США) при длине волны 570 нм.
Для определения жизнеспособности клеточных элементов окрашивание биопленок проводили тег-разолием с использовиниейі системы Cell Proliferation Assay в соответствии с инструкцией фирмы (Prainega, США). В каждую лунку на отмытые от срепы биопленки бактерий вносили по 100 мкл во ды, добавляли 20 мкл реакционной смеси и инкубировали 4 ч. при 37℃. Интенсивность окраски измеряли на м икропланшетном спектрофотометре Benchmark Plus (Bio-Rad? США) при длине волны 490 нм.
Поста новк5г антибактериального теста проводи- ли методом серийных разведении в стерильных иммунологических планшетах (Медполимер. Россия). В лунки планшетов вносили по 100 мкл среды LB, не содержащей КС1. В первою лунку ряда вносили 100 мкл исследуемого раствора антибактериальных пептидов и готовили серию двукратных разведений. Затем в каждою лунку вносили по 10 мкл суспенмнм бактерий, содержащей 10б>^КОЕ/мл (в качестве инокулятов использовали клетки лог-фа^ы роста).
При подсчете минимальных подавляющих концентраций (МПК) пептидов для разных бактерийһ учитывали их известное значение МПК для бактерий S. epidermidis ГИСК 33* составляющее 0.25 мкг/мл (как для варнерина. так и для хоминина). При расчете количеств пептидов необходимых для подавления роста антибиотикорезистентных бак-т€рий, учитывали максимальное разведение, при котором наблюдалось отсутствие роста через 16-18 4. инкубации и сраЕннЕалп с разведеним, ингибирующим рост S. epidenftidis ГИСК 33.
Определение антибиотикорезистентности проводили ДИСКОДиффу зионным методом согласно Методическим указаниям [МУК, 2004]. Для постановки тестов использовали бактерии лог-фазы роста и диски, пропитанные стандартными растворами антибиотиков (НИЦФ, Россия). Чувствительность к антибиотикам определяли по диаметру зон подавления роста колоний исслед>гемых бактерий.
Повторность всех экспериментов трехкратная. Статистическою обработку экспериментальных данных проводили с помощью компьютерной программы Microsoft Excel 2000 (Microsoft Inc+, 1999). рассчитывая среднее арифметическое значение и стандартное отклонение.
Результаты и обсуждения
Диско-диффузионный метод определения анти-биотикочувствительности исследуедіых штаммов показал, что бактерии штамма S epideruudis ГИСК 33 обладают ВЫСОКОЙ чувствительностью ко всем щученным антибиотикам, кроме клиндамицина (табл, 1).
Бактерии S epidmnidis 33 Cf проявляли устой-чивось к ципрофлоксацин), и новобиоцину, а бактерии полирезистентного клинического штамма S xylosus S31 были устойчивы к 10 антибиотикам, но обладали низкой чувствительностью к амикацину, оксациллину и ципрофлоксацину (табл, 1).
Таблица 1
Антибиотикочувствите<чьность бактерий исследуемых штаммов КНС (диаметр $ин подавления роста, мм)
Изучение чу ветвите льности планктонных культур исследуемых стафилококков к катионным пептидам варнерину и хоминину [Коробов и др+ 2010“ 2014] показало, что минимальная подавляющая концентрация (МПК) пептидов значительно различается для разных штаммов. Из представленных данных ВИДНО. ЧТО наибольшей Ч) БСТБИТеЛЬНОСТЬЮ к катионным антибактериальным пептидам обладали бактерии вида S. epiden?iidis, а с приобретением устойчивости к ципрофлоксацину незначительно снижалась чувствительность ЛИШЬ К катионному пептиду хоминину. При действии на поли- резистентный штамм S xytcsus 831 варнерин и сниженной ч^ъствительности этих бактерий к дан-хоминин проявляли активность при значительно ным соединениям (табл. 2).
больших конце игра циях^ св идете льств >ю щих о
Таблица 2
Минимальная подавляющая концентрация анпгбактернальны\ катионные пептидов лл 篇 исслелонанных штаммов КНС (мкг/мл)
|
Пептид |
S.epidefmidis ГИСК 33 |
S.epidermidis ГИСК 33 Cf |
S. xy^osus 831 |
|
Варнерин |
0.25 |
0.25 |
1000 |
|
Ходіинин |
0.25 |
S5 |
1000 |
При изучении способности бактерий формировать биопленки на поверхности полистирола было показано, что динамика роста биомассы пленок и количества живых клеток в них различаются у разных штаммов.
Биомасса пленок бактерий S. epidevmidis ГИСК 33 г и численность живых клеток в них достигали максимума уже 'іерез 24 ч+ При дальнейшем к ) тль-тиБировании наблюдалось снижение обоих показателей. Важно отметить, что на фоне постепенного падения биомассы пленок происходило резкое снижение содержания в них жизнеспособных кле-
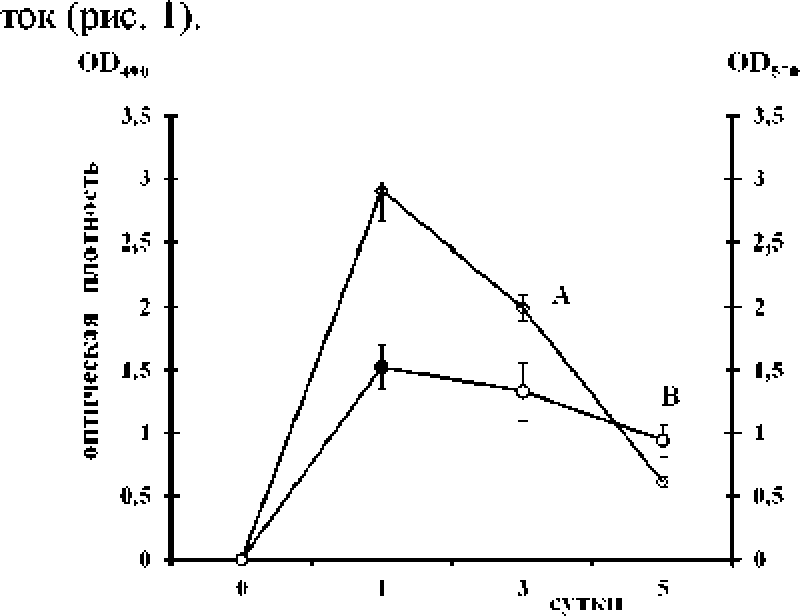
Рис. 1. Динамика роста биопленок
5 : epidemidis ГИСК 33:
А - число живых клеток в биоплснке; В -биомасса плеіпси
Несколько иная картина динамики развития биопленок была характерна для бактерий £ epidermidis ГИСК 33 С 产, устойчивых к ципрофлоксацину, В это^< случае максимумы биомассы пленок и количества живых клеток в них также достигались уже через сутки. При дальнейшем ку л ьтив ирова нии наблюдалось резкое снижение биомассы пленок? однако, количество живых клеток в них продолжало возрастать (рис. 2).
Снижение биомассы пленок бактерий S epi-dermidis ГИСК 33. вшможно. было связано с истощением питательных веществ в среде и разрушением по лисахар идного матрикса собственными литическими ферментами, которые присутствуют в клеточных стенках данного штамма стафилококков [Коробов и др., 2010].
Формирование биопленок бактериями полире-зистентного штамма S xylosus 831 происходило более длительное время (рис. 3)+ Максимальны* значений биомасса пленок достигала лишь на ЗТ-е сут+ культивирования* Следует отметить* что перманентный рост биопленок S xy^osus 831* ха-рактери^овалея двумя фазами увеличения их биомассы и содержания жизнеспособных клеток - фазой быстрого роста (1 сут) и фазой стабилизации этих показателей (2-4 сут.)+
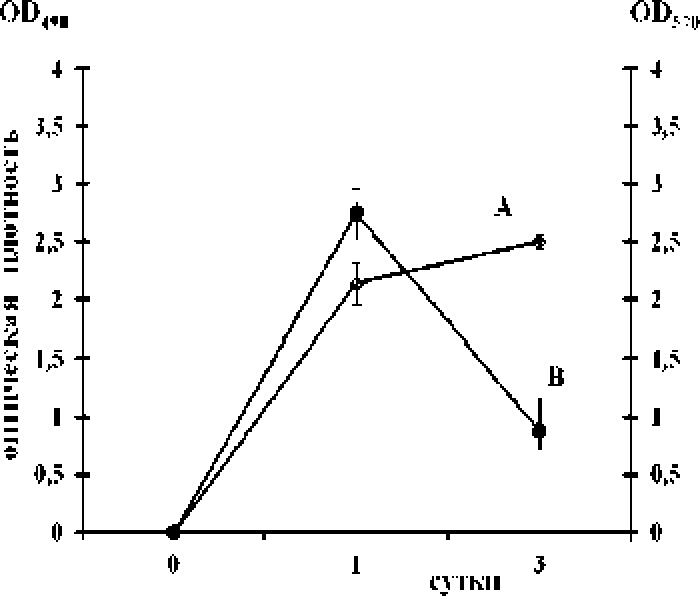
Рис. 2* Динамика роста биопленки S epidermidis ГИСК 33 Cf:
А - число живых клеток в биоплеіЕке. В -биомасса пленки
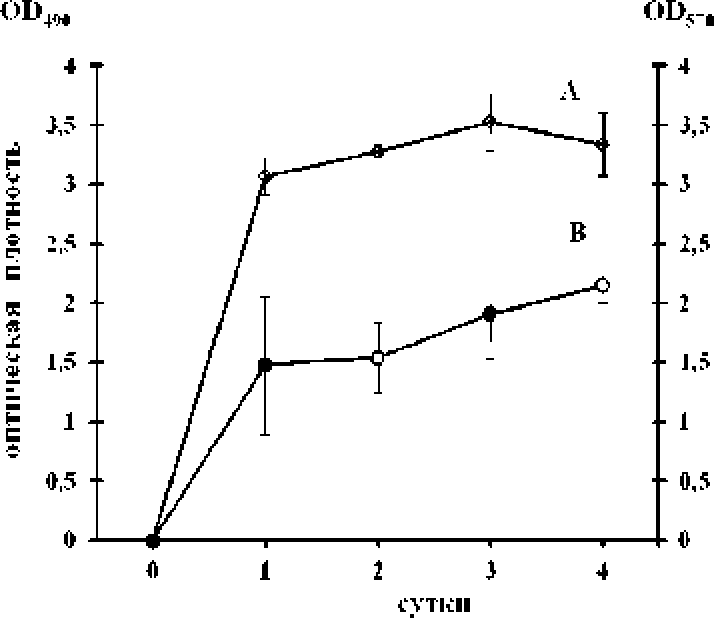
Рис. 3* Динамика роста биопленки Sxylostis 831:
А - число живых клеток в биоппенке, В -биомасса пленки
Для определения влияния варнерина и хомини-на на способность бактерий к образованию биопленок. одновременно с инок\тлумом в питательную среду добавляли эти антибактериальные пептиды. Согласно полученным данным, наличие в среде роста стафилококков варнерина или хоми-нина. приводило к значительному уменьшению биомассы пленок (рис. 4) и количества жизнеспособных бактериальных клеток в сформированных в течение 1 сут. биопленках (рис. 5).
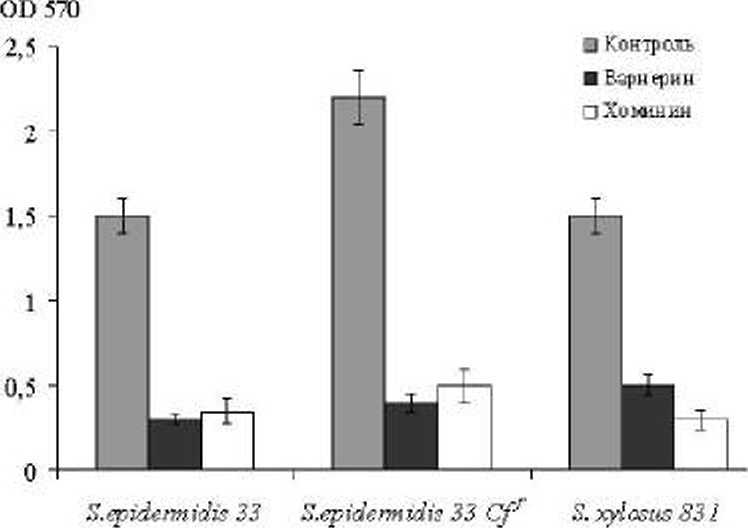
Рис. 4. Формирование биомассы пленок стафилококков в течение суток в
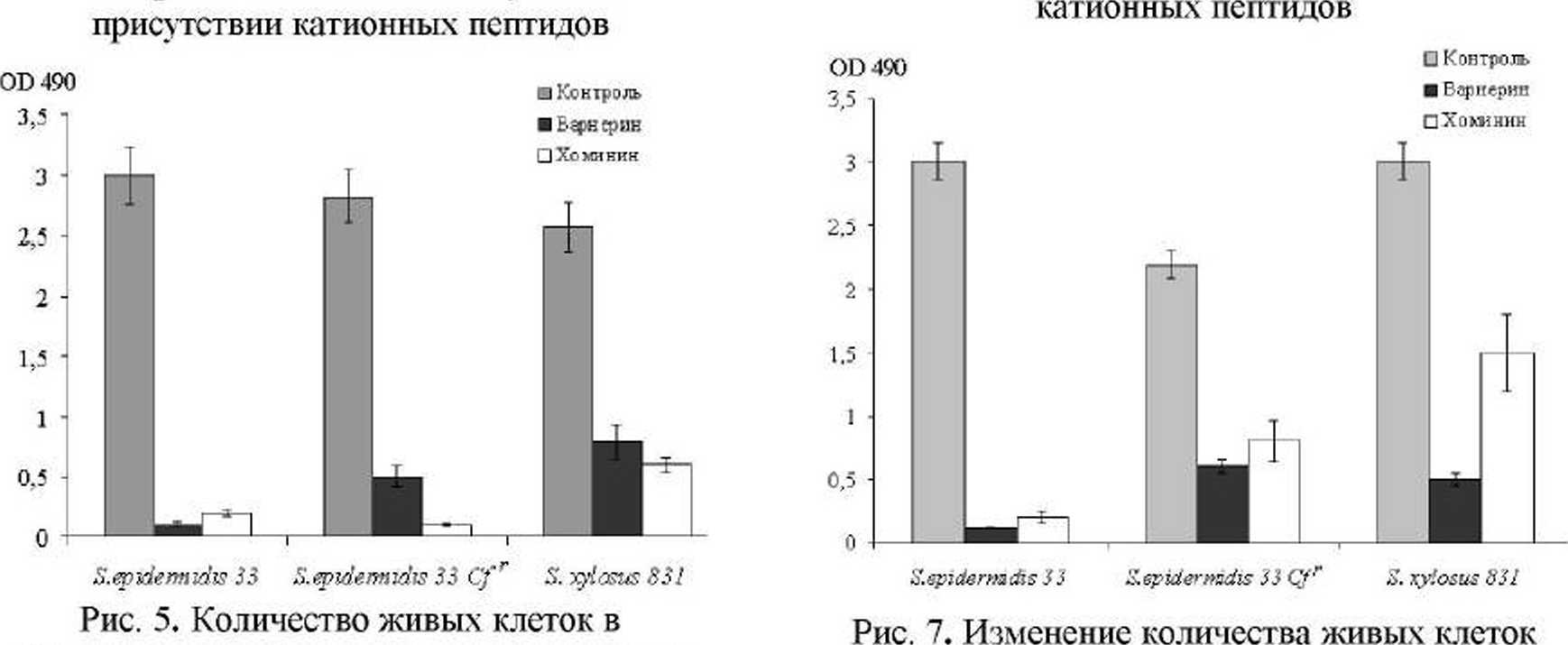
биопленках стафилококков, выращенных в течение суток в присутствии катионных
пептидов
Важным практическим аспектом поллненных результатов является факт ингибирокшия процесса пленкообразования полирезистентных бактерий клинического изолята S xylosus 831.
Однако известно, что бактерии в составе биопленок имеют повышенную выживаемость в при-сутствми антибактериальных веществ, позтому важно было исследовать влияние низкомолекулярных катионных пептидов на сформировавшиеся в течение суток биопленки использованных в работе штаммов стафилококков. Влияние низкомолекулярных катионных пептидов на зрелые биопленки было обнаружено после их инкубации с пептидами в течение суток.
Из представленных на рис. 6 и 7 данных видно, что при наличии в среде пептидов как биомасса суточных пленок исследованных штаммов КНС. так и жизнеспособность их клеточных элементов значительно снижаются.
Таким образом, результаты экспериментов свидетельствуют о том. что использованные в работе катионные пептиды проявляют свое действие и на с ( {юрмированных бактериальных пленках, снижая их
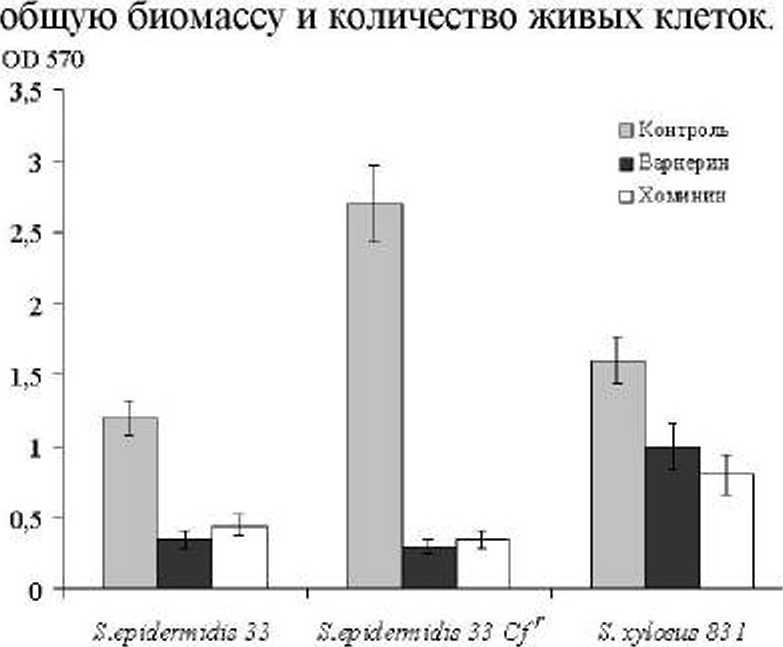
Рис. 6. Разрушение биомассы суточных биопленок стафилококков при действии
при действии катионных пептидов на сутохіные биопленки стафилококков
Результаты проведенного исследования позволяют сделать следующие выводы:
-
1. Изученные штаммы коагулазонегативных стафилококков S. epidermidis ГИСК 33, S. epider-midis ГИСК 33 Cf и 5. xylosus 831 обладают выраженной способностью к образованию биопленок. Динамика формирования клеточных и неклеточных компонентов биопленок бактерий исследуе-
- ммх штаммов существенно различается.
-
2. Присутствие в среде роста низкомолекулярных катионных пептидов варнерина и хоминина подавляет развитие биопленок бактерий всех исследованных штаммов стафилококков.
-
3. Бактериальные катионные пептидоы вызывают деструкцию зрелых биопленок КНС. в том числе и полирезистентного клинического штамма S. xylosus 831.
Работа выполнена при поддержке грантов: РФФИ № 14-04-0068 7. Программ фундаментальных исследований УрО РАН и Министерства образования и науки Пермского края -«Межлугнародные исследовательские группы», № С-26/632.
Список литературы Деструкция биопленок коагулазонегативных стафилококков под действием бактериальных катионных пептидов
- Коробов В.П., Лемкина Л.М., Полюдова Т.В., Акименко В.К. Выделение и характеристика нового низкомолекулярного антибактериального пептида семейства лантибиотиков//Микробиология. 2010. T. 79, № 2. С. 228-238
- Коробов В.П., Лемкина Л.М., Полюдова Т.В., Филатова Л.Б., Панькова Н.В. Активация аутолитической активности Staphylococcus epidermidis 33 низкомолекулярным катионным пептидом варнерином//Микробиология. 2010. T. 79, № 1. С. 133-135
- Коробов В.П. Лантибиотики -природные антибиотики широкого спектра действия//Вестник уральской медицинской академической науки. 2011. № 4/1. С. 10-11
- Коробов В.П., Полюдова Т.В., Лемкина Л.М. Изучение биологических свойств антибиотикорезистентных бактерий Staphylococcus epidermidis 33 и их чувствительности к варнерину//Вестник Пермского университета. Серия Биология. 2015. № 1. С. 5-14
- Коробов В.П., Полюдова Т.В., Лемкина Л.М. Антибактериальный пептид хоминин KLP-1 широкого спектра действия//Патент РФ № 2528055. 2014
- Лямин А.В., Боткин Е.А., Жестков А.В. Проблемы в медицине, связанные с бактериальными пленками//Клин. микробиол. антимикроб. химиотер. 2012. Т. 14, № 4. С. 268-275
- Методические указания. МУК. 4.2.1890-04. Определение чувствительности микроорганизмов к антибактериальным препаратам (утв. Главным государственным санитарным врачом РФ 04.03.2004)
- Перепанова Т.С. Значение инфекций, обусловленных образованием биопленок, в урологической практике//Эффективн. Фармакотер. 2013, № 4. С. 18-27
- Полюдова Т.В., Коробов В.П., Зидина Н.М. Сравнительный анализ формирования биопленок бактериями Propionibacterium acnes Ac-1450 на нативных и обработанных катионными пептидами поверхностях полистирола//Рос. имму-нол. журнал. 2015. Т. 9, № 2. С. 661-663
- Eroshenko D.V., Korobov V.P. New AMPs from Staphylococcus spp., warnerin and hominin, reduce Staphylocococcus epidermidis adhesion and biofilm formation//Multidisciplinary approach for studying and combating microbial pathogens/by ed. A. Mendez-Vilas. -BrownWalker Press. 2015. P. 98-101.
- Frank K.L., Reichert E.J., Piper K.E., Patel R. In vitro effects of antimicrobial agents on planktonic and biofilm forms of Staphylococcus lugdunensis clinical isolates//Antimicrob Agents Chemother 2007. № 51. P. 888-895
- Jorge P., Lourengo A., Pereira M.O. New trends in peptide-based anti-biofilm strategies: a review of recent achievements and bioinformatic approaches//Biofouling. 2012. Vol. 28, № 10. P. 1033-1061


