Деструкция фталевых кислот штаммом Paenarthrobacter sp. SA101, выделенным из сточных вод химического предприятия
Автор: Ястребова О.В., Прохорова А.П., Плотникова Е.Г.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 2, 2023 года.
Бесплатный доступ
Фталевая и терефталевая кислоты (ОФК и ТФК) имеют широкое применение в химической промышленности в качестве пластификаторов для получения полимерных материалов, в связи с чем являются распространенными экополлютантами. Изучена способность штамма Paenarthrobacter sp. SA101, выделенного из образца сточных вод химического предприятия (г. Пермь), к росту в присутствии ОФК и ТФК в высоких концентрациях. Показано, что штамм SA101 способен расти на данных субстратах в концентрациях до 20 г/л, что для представителей рода Paenarthrobacter показано впервые. В средах с ОФК зафиксированы более высокие параметры роста штамма, чем в средах с ТФК: максимальное значение ОП600 (1.64), наиболее высокая удельная скорость роста (0.073±0.003 ч-1) и наименьшая продолжительность лаг-фазы наблюдались в среде с 10 г/л ОФК. При использовании 20 г/л ТФК зафиксирована более высокая удельная скорость роста (0.04±0.002 ч-1) и максимальное значение ОП600 (1.6), однако подготовительная фаза роста была более продолжительной, чем в среде с 10 г/л ТФК. Штамм SA101 способен к утилизации 76% ОФК за 39 ч. и 74.2% ТФК за 71 ч. культивирования при использовании данных субстратов в концентрации 10 г/л. Клетки штамма SA101 содержат плазмиду молекулярной массой ~100 т.п.н. Штамм SA101 является перспективным для разработки биотехнологических методов очистки загрязненных фталатами почв и промышленных стоков.
Орто-фталевая кислота, терефталевая кислота, рост, утилизация
Короткий адрес: https://sciup.org/147241919
IDR: 147241919 | УДК: 579:873:579.222.2 | DOI: 10.17072/1994-9952-2023-2-172-178
Destruction of phthalic acids by Paenarthrobacter sp. SA101 isolated from the wastewater of a chemical plant
Phthalic and terephthalic acids (PA and TPA) are widely used in the chemical industry as plasticizers, for the production of polymer materials, and therefore are common eco-pollutants. The ability of the strain Paenarthrobacter sp. SA101, isolated from a sample of a chemical plant wastewater (Perm), to growth on high concentrations of PA and TPA was studied. It was shown that strain SA101 is capable of efficient growth on these substrates at concentrations up to 20 g/l, which is shown for the representatives of the genus Paenarthrobacter for the first time. Higher strain growth parameters were recorded in media with PA, than in media with TPA: the maximum value of OD600 (1.64), the highest specific growth rate (0.073±0.003 h-1) and the shortest lag phase were observed in a medium with 10 g/l of PA. The highest specific growth rate (0.04±0.002 h-1) and the maximum value of OD600 (1.6) were observed with 20 g/l of TPA, however, the lag phase of growth was longer than in the medium with 10 g/l of TPA. The strain SA101 was able to utilize 76% of PA in 39 hours and 74.2% of TPA in 71 hours of cultivation, when using these substrates at a concentration of 10 g/l. The cells of the strain SA101 contain a plasmid with a molecular weight of ~ 100 bp. The strain SA101 is promising for the development of biotechnological methods for cleaning phthalate-contaminated soils and industrial effluents.
Текст научной статьи Деструкция фталевых кислот штаммом Paenarthrobacter sp. SA101, выделенным из сточных вод химического предприятия
Фталевые кислоты – двухосновные ароматические карбоновые кислоты, существующие, в зависимости от положения карбоновых групп, в трех изомерных формах: фталевой ( орто -фталевой, ОФК), изофталевой и терефталевой (ТФК) кислот. Фталаты и сложные эфиры фталевых кислот имеют повсеместное применение в промышленности, используются в качестве пластификаторов для получения полимерных материалов. Эфиры фталевой кислоты (дибутилфталат, диметилфталат, диэтилфталат) используются для пластификации поливинилхлорида (ПВХ), при синтезе полиэфирных волокон, полиэтилена, а также в производстве строительных и смазочных материалов, лаков, косметики [Liang et al., 2008; Gao et al., 2018]. Терефталевая кислота (с пара- расположением карбоксильных групп) применяется в производстве насыщенных полиэфиров, химических волокон, пластмасс, красителей. ТФК является основным исходным соединением для получения полиэтилентерефталата (ПЭТФ), который составляет 90% от общего производимого количества насыщенных полиэфиров [Zhang et al., 2005; Karthik et al., 2008]. Фталаты и их эфиры не связаны ковалентно с пластиковым полимером и выщелачиваются в окружающую среду, представляя угрозу для здоровья человека и животных. Хотя фталаты подвергаются абиотическому фотолизу с периодом полураспада от месяцев до нескольких лет, микробная деградация является основным и экологически безопасным методом утилизации фталатов [Benjamin et al., 2015; Wang et al., 2023].
К настоящему времени биодеградация ОФК, ТФК и их сложных эфиров описана для ряда бактерий различных филогенетических групп, в том числе для штаммов рода Arthrobacter и для принадлежащих ранее к данному роду бактерий, реклассифицированных как представители родов Pseudoarthrobacter, Glutamicibacter, Paenarthrobacter [Eaton 2001; Stanislauskienė et al., 2011; Chen et al., 2021; Shariati et al., 2022; Ren et al., 2023]. Однако среди бактерий рода Paenarthrobacter способность к утилизации фталатов описана лишь для штамма Paenarthrobacter sp. Shss., растущего на ОФК, а также дибутилфталате (1 г/л) и других эфирах фталевой кислоты [Shariati et al., 2022]. Утилизация ОФК и ТФК аэробными бактериями проходит с образованием протокатеховой кислоты как ключевого промежуточного метаболита. При этом разложение ОФК до протокатехата проходит в три этапа: диоксигенирование, дегидрирование и декарбоксилирование; а деградация ТФК до протокатехата включает только две стадии, поскольку декарбоксилирование осуществляется цис -дигидродиолдегидрогеназой. Протокатехат в дальнейшем расщепляется диоксигеназами по орто- , либо мета- пути [Dagley et al., 1971; Liang et al., 2008; Boll et al., 2020].
Материалы и методы исследований
Объект исследования и условия культивирования. Из рабочей коллекции Лаборатории микробиологии техногенных экосистем «Института экологии и генетики микроорганизмов УрО РАН» ПФИЦ УрО РАН для исследований отобран штамм SA101, способный к росту на фталатах.
Культивирование бактерий проводили в минеральной среде К1 [Зайцев, Карасевич, 1981] с добавлением ОФК или ТФК в концентрациях 1, 10, 20, 30, 40 г/л. В качестве инокулята использовали бактериальные клетки в экспоненциальной фазе роста, выращенные в среде К1 с ОФК или ТФК (1 г/л) в качестве субстрата. Бактериальные культуры выращивали в колбах Эрленмейера объемом 250 мл (объем среды – 100 мл) при 28°С, на термокачалке при 100 об/мин.
Определение оптической плотности (ОП) культуральной жидкости проводили на спектрофотометре UV-Visible BioSpec-mini (“Shimadzu”, Япония) при длине волны 600 нм в кювете с длиной оптического пути 1 см. Расчет удельной скорости роста (μ, ч-1) проводили по стандартной формуле
μ = (ln B 2 – ln B 1 )/( t 2 - t 1 ), где В 1 и В 2 – оптические плотности культуры в моменты времени t 1 и t 2 , соответственно [Нетрусов, 2005].
Убыль ОФК и ТФК из среды культивирования определяли методом высокоэффективной жидкостной хроматографии (ВЭЖХ) с использованием хроматографа LC-20AD Prominance (“Shimadzu”, Япония) с колонкой (С-18 150 × 4.6 мм; “Shima-Aldrich”, США) и УФ-детектором SPD-20A (при 205 нм) в системе ацетонитрил – 0.1%-ная H 3 PO 4 (70 : 30). В качестве подвижной фазы использовали 80%-ный раствор ацетонитрила при скорости потока 1.0 мл/мин и температуре 40ºС. Идентификацию соединений проводили при сравнении времени выхода пиков экстрактов со стандартными растворами ОФК и ТФК в концентрациях 50 и 100 мг/л. Количественное содержание рассчитывали с помощью пакета программ “LCsolution” (“Shimadzu”, Япония). Расчет удельной скорости ( μ , ч-1) утилизации ОФК и ТФК проводили по стандартной формуле
μ = (ln С 1 – ln C 2 )/( t 2 - t 1 ), где С 1 , С 2 – концентрация субстрата в начальный и конечный момент времени t 1 и t 2 соответственно [Не-трусов, 2005].
Наличие плазмидной ДНК выявляли модифицированным методом щелочного лизиса [Marko et al., 1982].
Результаты и их обсуждение
Штамм SA101 выделен ранее из образца сточных вод химического предприятия (г. Пермь) и идентифицирован как представитель рода Paenarthrobacter, близкородственный виду Paenarthrobacter ureafa-ciens NCТ (NR 029281) (уровень сходства по гену 16S рРНК составил 99.3%) [Малышева, Ястребова, Плотникова, 2021].
Установлено, что штамм Paenarthrobacter sp. SA101 способен к деструкции ряда ароматических углеводородов и фталатов, в том числе ОФК, ТФК, дибутилфталата, бензоата [Малышева и др., 2021]. На основании способности штамма SA101 к росту на протокатеховой кислоте можно предположить, что штамм осуществляет утилизацию ОФК и ТФК через образование протокатехата – ключевого метаболита фталатов, с расщеплением последнего до основных клеточных метаболитов [Liang et al., 2008; Boll, 2020].
Исследована способность штамма использовать в качестве единственного источника углерода и энергии ОФК и ТФК (в концентрациях 1, 10, 20, 30 г/л) при росте в минеральной среде К1. Установлено, что штамм SA101 растет на данных субстратах в концентрациях до 20 г/л. Увеличение концентрации обоих субстратов приводило к накоплению биомассы, при этом в средах с ОФК были зафиксированы более высокие параметры роста штамма, чем в средах с ТФК (рис. 1). Максимальное значение ОП 600 (1.64), наиболее высокая удельная скорость роста (0.073±0.003 ч-1) и наименьшая продолжительность лаг-фазы роста штамма наблюдались в среде с 10 г/л ОФК. При выращивании штамма в среде с 20 г/л ТФК фиксировали наиболее высокую удельную скорость роста (0.04±0.002 ч-1) и максимальное значение ОП 600 штамма (1.6), однако подготовительная фаза роста была более продолжительней, чем в среде с 10 г/л ТФК (рис. 1, таблица).
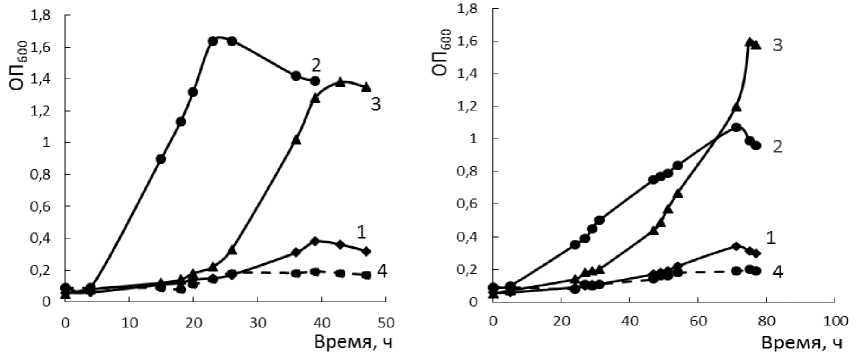
А B
Рис. 1. Рост клеток штамма SA101 в среде с ОФК ( А ) и ТФК ( B ) (г/л): 1 – 1; 2 – 10; 3 – 20; 4 – 30 [Growth of strain SA101 on PA ( A ) and TPA ( B ) (g/l): 1 - 1; 2 - 10; 3 - 20; 4 – 30]
Наиболее высокий уровень утилизации фталатов был зарегистрирован при выращивании в среде с 10 г/л ОФК и ТФК (76% за 39 ч. и 74.2% за 71 ч. соответственно). Максимальная удельная скорость потреб- ления данных субстратов также наблюдалась при их концентрации 10 г/л: 0.052±0.006 ч-1 при культивировании на ОФК и 0.034±0.004 – на ТФК (рис. 2, таблица).
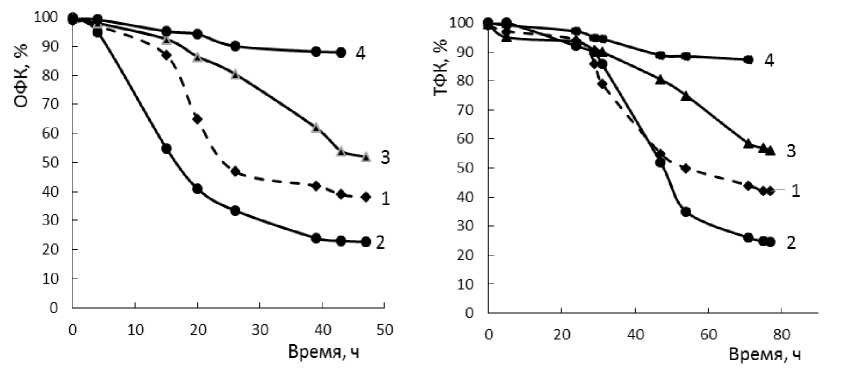
А
B
Рис. 2. Утилизация с использованием клеток штамма SA101 ОФК ( А ) и ТФК ( B ) в концентрации (г/л): 1 – 1; 2 – 10; 3 – 20; 4 – 30
[Utilization of PA ( A ) and TPA ( B ) by strain SA101 (g/L): 1 – 1; 2 – 10; 3 – 20; 4 – 30]
Параметры роста штамма SA101 и утилизация ОФК и ТФК [SA101 strain growth parameters and PA utilization and TPA]
|
Параметры |
Ростовой субстрат, г/л |
|||||
|
ОФК |
ТФК |
|||||
|
1 |
10 |
20 |
1 |
10 |
20 |
|
|
Удельная скорость роста, ч-1 |
0.038 ±0.003 |
0.073 ±0.003 |
0.070 ±0.004 |
0.028 ±0.001 |
0.03 ±0.002 |
0.04 ±0.002 |
|
Максимальное значение ОП 600 |
0.37 |
1.64 |
1.38 |
0.32 |
1.07 |
1.6 |
|
Лаг-фаза роста, ч |
25 |
3 |
18 |
51 |
24 |
31 |
|
Утилизация, % |
60.6 ± 0.4 |
76.0 ± 0.3 |
46.2 ± 0.4 |
55.5 ± 0.4 |
74.2 ± 0.4 |
57.2 ± 0.4 |
|
Удельная скорость утилизации, ч-1 |
0.040 ±0.003 |
0.052 ±0.006 |
.,020 ±0.001 |
0.027 ±0.003 |
0.034 ±0.004 |
0.010 ±0.002 |
Подавление роста бактерий высокими концентрациями фталевых кислот ранее показано для ряда штаммов разных родов, в том числе для Arthrobacter sp. 0574, способность которого к разложению ТФК подавлялась уже при концентрации 10 г/л и выше [Zhang et al., 2013]. Описан штамм Rhodococcus sp. N2, утилизирующий 10 г/л ТФК за 5 сут., а также штамм R. wratislaviensis КТ112-7, растущий в среде с ОФК в концентрации 8 г/л [Егорова и др. 2013; Suwanawat et al., 2019]. Ранее нами описаны бактерии рода Glutamicibacter , способные к росту и утилизации ТФК в концентрации до 30 г/л [Ястребова, Малышева, Плотникова, 2022]. Исследуемый штамм Paenarthrobacter sp. SA101 способен к эффективному разложению ОФК и ТФК за 23 и 71 ч. соответственно в концентрации до 20 г/л, что для представителей рода Paenar-throbacter показано впервые.

Исследование на наличие экстрахромосомной
ДНК модифицированным методом щелочного лизиса [Marko et al., 1982] показало присутствие в клетках Paenarthrobacter sp. SA101 плазмиды молекулярной массой ~100 т.п.н. (рис. 3). Плазмидная локализация генов деградации ОФК описана для штаммов Arthrobacter keyseri 12B и Arthrobacter phenanthrenivorans Sphe3 [Eaton, 2001; Kallimanis et al., 2011]. Для ряда штаммов рода Paenarthrobacter показано наличие плазмид биодеградации аромати-
М 1 2
Рис. 3. Электрофореграмма плазмидной ДНК штамма Paenarthrobacter sp. SA101 (1). M – маркер O'GeneRuler™ 100 bp Plus DNA Ladder (“Fermentas”, Литва); 2 – штамм-деструктор ТФК Rhodococcus sp.
S6 (плазмида ~100 т.п.н.)
[Electropherogram of plasmid DNA of Paenarthrobac-ter sp. SA101 (1). M - O'GeneRuler™ 100 bp Plus DNA Ladder marker (“Fermentas”, Lithuania); 2 – TPA destructor strain Rhodococcus sp. S6 (plasmid ~100 kb)]
ческих соединений. Так, у штаммов Paenarthrobacter nicotinovorans pAO1 и Paenarthrobacter sp. YJN-5 обнаружены плазмиды, включающие гены катаболизма никотина и ипродиона соответственно [Mihăşan et al., 2021; Zhang et al., 2021]. Можно предположить, что гены, контролирующие деструкцию ОФК и ТФК, у штамма SА101 также расположены на плазмиде.
Заключение
Таким образом, исследованный нами штамм Paenarthrobacter sp. SA101 способен к эффективному росту и утилизации до 20 г/л ОФК и ТФК, при этом в средах с ОФК зафиксированы более высокие параметры роста бактериальных клеток, чем в средах с ТФК: при использовании 20 г/л ТФК наблюдались наиболее высокие ростовые характеристики штамма, чем в среде с 10 г/л ТФК, однако подготовительная фаза роста была более продолжительней. Штамм SA101 способен к утилизации 76% ОФК в течение 39 ч. и 74.2% ТФК за 71 ч. культивирования при использовании данных фталевых кислот в концентрации 10 г/л. Штамм Paenarthrobacter sp. SA101 является перспективным для разработки биотехнологических методов очистки загрязненных фталатами почв и промышленных стоков.
Список литературы Деструкция фталевых кислот штаммом Paenarthrobacter sp. SA101, выделенным из сточных вод химического предприятия
- Зайцев Г.М., Карасевич Ю.Н. Утилизация 4-хлорбензойной кислоты штаммом Arthrobacter globi-formis // Микробиология. 1981. Т. 50. С. 35-40.
- Егорова Д.О. и др. Деструкция ароматических углеводородов штаммом Rhodococcus wratislaviensis КТ112-7, выделенным из отходов соледобывающего предприятия // Прикладная биохимия и микробиология. 2013. Т. 49, № 3. С. 267-278.
- Малышева А.А., Ястребова О.В., Плотникова Е.Г. Выделение и характеристика штамма-деструктора сложных эфиров фталевой кислоты Paenarthrobacter sp. SA101 // Фундаментальные и прикладные аспекты биоинформатики, биотехнологии и недропользования: сб. статей всерос. науч. конф. с междунар. участием. Пермь, 2021. С. 69-71.
- Нетрусов А.И. Практикум по микробиологии. М.: Академия, 2005. 608 с.
- Ястребова О.В., Малышева А.А., Плотникова Е.Г. Галотолерантные бактерии рода Glutamicibacter - деструкторы терефталевой кислоты // Прикладная биохимия и микробиология. 2022. Т. 58, № 5. С. 476483.
- Benjamin S. et al. A monograph on the remediation of hazardous phthalates // J. Hazard. Mater. 2015. Vol. 298. P. 58-72.
- Boll M. et al. Minireview. Microbial degradation of phthalates: biochemistry and environmental implications // Environ. Microbiol. Reports. 2020. Vol. 12(1). P. 3-15.
- Chen F. et al. High-efficiency degradation of phthalic acid esters (PAEs) by Pseudarthrobacter defluvii E5: Performance, degradative pathway, and key genes // Sci. Total Environ. 2021. Vol. 794 : 10. doi: 10.1016/j.scitotenv.2021.148719. 48719.
- Dagley S. Catabolism of aromatic compounds by microorganisms // Adv. Microb. Physiol. 1971. Vol. 6. P. 1 -46.
- Eaton R.W. Plasmid-encoded phthalate catabolic pathway in Arthrobacter keyseri 12B // J. Bacteriol. 2001. Vol. 183. P. 3689-3703.
- Gao D. et al. An overview of phthalate acid ester pollution in China over the last decade: Environmental occurrence and human exposure // Sci. Total Environ. 2018. Vol. 645. P. 1400-1409.
- Kallimanis A. et al. Complete genome sequence of Arthrobacter phenanthrenivorans type strain (Sphe3) // Stand. Genomic Sci. 2011. Vol. 4. P. 123-30.
- Karthik M. et al. Biodegradability enhancement of purified terephthalic acid wastewater by coagulation-flocculation process as pretreatment // J. Hazard. Mater. 2008. Vol. 154. P. 721-730.
- Liang D.W., Zhang T., Fang H. Phthalates biodegradation in the environment // Appl. Microbiol. Bio-technol. 2008. Vol. 80. P. 183-198.
- Marko M.A., Chipperfield R., Birnboim H.C. A procedure for the large-scale isolation of highly purified plasmid DNA using alkaline extraction and binding to glass powder // Analit. Biochem. 1982. Vol. 121. P. 382-387.
- Mihä§an M. et al. Time-dependent analysis of Paenarthrobacter nicotinovorans pAO1 nicotine-related proteome // ACS Omega. 2021. Vol. 6. P. 14242-14251.
- Ren C. et al. Complete degradation of di-n-butyl phthalate by Glutamicibacter sp. strain 0426 with a novel pathway // Research Square. 2023. doi.org/10.21203/rs.3.rs-2696404/v1.
- Shariati S. et al. Degradation of dibutyl phthalate by Paenarthrobacter sp. Shss isolated from Saravan landfill, Hyrcanian Forests, Iran // Biodegradation. 2022. Vol. 33. P. 59-70.
- Stanislauskiene R., Rudenkov M., Karvelis L. Analysis of phthalate degradation operon from Arthrobacter sp. 68b // Biologija. 2011. Vol. 57. P. 45-54.
- Suwanawat N. et al. Biodegradation of terephthalic acid by Rhodococcus biphenylivorans isolated from soil // Int. J. Environ. Sci. Dev. 2019. Vol. 10. P. 30-33.
- Wang Z. et al. Environmental health risks induced by interaction between Phthalic Acid Esters (PAEs) and biological macromolecule: A review // Chemosphere. 2023. Vol. 4. 138578. doi: 10.1016/j..138578.
- Zhang M. et al. Comparative genomic analysis of iprodione-degrading Paenarthrobacter strains reveals the iprodione catabolic molecular mechanism in Paenarthrobacter sp. strain YJN-5 // Environ. Microbiol. 2021. Vol. 23. P. 1079-1095.
- Zhang X. et al. Purified terephthalic acid wastewater biodegradation and toxicity // J. Environ. Sci. (China). 2005. Vol. 17(5). P. 876-880.
- Zhang Y.M. et al. Degradation of terephthalic acid by a newly isolated strain of Arthrobacter sp. 0574 // South African J. of Science. 2013. Vol. 109. doi.org/10.1590/ sajs.2013/20120019.


