Деструктивно-некротические процессы костно-хрящевого комплекса грудины при инфекционно-воспалительных осложнениях после хирургических операций на открытом сердце
Автор: Касатов Анатолий Владимирович, Четвертных Виктор Алексеевич, Щеткина Ирина Николаевна, Трефилова Юлия Викторовна
Журнал: Морфологические ведомости @morpholetter
Рубрика: Оригинальные исследования
Статья в выпуске: 3 т.26, 2018 года.
Бесплатный доступ
Изучены особенности и степень выраженности декструктивно-некротических процессов костно-хрящевого комплекса грудины при различных клинических формах инфекционно-воспалительных осложнений, возникших после операций на открытом сердце. Установлено, что у пациентов с диагнозом нестабильность грудины патоморфологические изменения костной ткани грудины развиваются в области продольного разреза. Они характеризуются поражением костного мозга, нарушением кровоснабжения, формированием очагов нагноения и некроза костной ткани. У пациентов с диагнозами «остеомиелит и стерномедиастинит» деструктивно-некротические процессы распространяются на различные участки костно- хрящевого аппарата грудины, сопровождаются развитием очагов полной деструкции кости, образованием секвестров и свищевых ходов. В ряде случаев гнойный процесс распространяется на плевру и средостение. Этиопатогенами наиболее выраженных патоморфологических процессов являлись Staphylococcus aureus и Pseudomonas aeruginosa.
Деструктивно-некротические процессы, патологическая морфология, кардиохирургия, открытое сердце
Короткий адрес: https://sciup.org/143177261
IDR: 143177261
Destructive necrotic processes of the sternum's bone-cartilaginous complex at infectious and inflammatory complications after surgical operations on open heart
The features and severity of destructive-necrotic processes of the bone-cartilage complex of the sternum in various clinical forms of infectious and inflammatory complications arising after open-heart surgery have been studied. It has been established that in patients with a diagnosis of instability of the sternum, pathological changes in the bone tissue of the sternum develop in the area of the longitudinal incision. They are characterized by lesions of the bone marrow, impaired blood supply, the formation of foci of suppuration and necrosis of bone tissue. In patients with diagnoses of “osteomyelitis and sternomediastinitis,” destructive-necrotic processes spread to various parts of the bone and cartilage apparatus of the sternum, accompanied by the development of centers of complete bone destruction, the formation of sequestrum and fistulous passages. In some cases, the purulent process extends to the pleura and mediastinum. The etiopathogens of the most pronounced pathological processes were Staphylococcus aureus and Pseudomonas aeruginosa.
Текст научной статьи Деструктивно-некротические процессы костно-хрящевого комплекса грудины при инфекционно-воспалительных осложнениях после хирургических операций на открытом сердце
Касатов А.В., Четвертных В.А., Щеткина И.Н., Трефилова Ю.В. Деструктивно-некротические процессы костно-хрящевого комплекса грудины при инфекционно-воспалительных осложнениях после хирургических операций на открытом сердце// Морфологические ведомости.- 2018.- Том 26.- № 3.- С. 18-22. (26).03.18-22
Введение . Изучение патоморфологических изменений в тканях при инфекционно-воспалительных процессах в месте хирургического вмешательства важно для определения тактики и объемов хирургического лечения, оценки репаративных возможностей поврежденных тканей. Особенно значимы такие исследования при осложнениях после кардиохирургических вмешательств с учетом области расположения жизненно важных органов и системы крово- и лимфообращения в зоне средостения. По данным различных авторов причиной возникновения осложнений могут быть как экзо-, так и эндогенные источники инфицирования, которые могут индуцировать различную степень поражения органов и систем с первичным вовлечением в процесс различных тканей [1 -3]. Чрезвычайно существенным является определение степени деструктивных изменений тканей в месте послеоперационного вмешательства при инфекционно-воспалительных состояниях после операций на открытом сердце с транс-стернальным доступом, осложняющихся расхождением операционного шва грудины, остеомиелитом костно-хрящевого комплекса грудины и ребер, стерномедиастинитом. В предыдущей статье мы сообщали о патоморфологических изменениях только костной ткани грудины при хроническом остеомиелите, развившемся у пациентов после кардиохирургических операций со стернальным доступом [4]. В настоящем исследовании анализируются данные по степени выраженности, особенностям деструктивно-некротических процессов костно-хрящевого аппарата грудины при различных клинических формах инфекционно-воспалительных осложнений после операций на открытом сердце.
Цель исследования – анализ степени тяжести развития деструктивно-некротических процессов костно-хрящевой части грудины и ребер при различных клинических формах пост-стернотомических инфекционно-воспалительных осложнений.
Материалы и методы исследования. Для исследований использовали образцы костной и хрящевой тканей, резецированных во время хирургического вмешательства, от 11 пациентов (7 мужчин и 4 женщин). Возраст пациентов колебался составлял от 45 до 70 лет. Основными диагнозами были «нестабильность грудины» (3 пациента), «гнойный деструктивный остеомиелит грудины» (6 пациентов) и «стерномедиастинит с поражением грудины и ребер» (2 пациента).
Материал фиксировали в 10%-ном нейтральном формалине от 3-4 дней до недели, затем промывали в проточной воде в течение 24 часов. После промывки проводили обезвоживание в спиртах возрастающей крепости (от 700 до 960), меняя спирты каждые сутки. Затем материал декальцинировали, помещая его в трилон Б, в течение последующих 3–4 месяцев. Декальцинатор (трилон Б) меняли ежедневно. После декальцинации материал вновь промывали водопроводной водой в течение 24 часов, затем помещали в 960 спирт, меняя его трижды через сутки, после чего обрабатывали абсолютным спиртом (1000) в течение 12 часов. Впоследствии по общепринятой методике материал заливали в парафин с воском и целлоидин с касторовым маслом в соотношении 1:1. Срезы толщиной 5-6 мкм готовили на микротоме марки МС-2 производства фирмы Точмедприбор (Харьков) и окрашивали гематоксилином-эозином. Всего приготовлено и изучено 220 препаратов, по 20 от каждого пациента из различных отделов костно-хрящевого ткани грудной клетки, которые исследовали с помощью микроскопа марки МС-50 (фирмы Micros, Австрия), при увеличении 70 и 400 Фотосъемку препаратов осуществляли в программе Scope Photo при помощи фотокамеры для микроскопа САМ V-200 фирмы Vision (Австрия).
Результаты исследования и их обсуждение . У всех пациентов с диагнозом «нестабильность грудины» инфекционный процесс, как правило, локализуется в центральных отделах кости в области продольного разреза грудины, где прежде всего происходит нарушение микроциркуляции крови, приводящее к значительному нарушению трофики костной ткани. В концевых отделах, особенно мелких сосудов, замедляется кровоток с образованием тромбов. Патологический процесс поражает костный мозг, который приобретает сначала темновато-красный цвет, сменяющийся затем желтоватым оттенком. Инфекционные очаги сливаются, образуя гнойные полости различной величины. Колонии микроорганизмов располагаются в межтрабекулярных зонах миелопоэза, способствуя гнойному воспалению. Распространению инфекции вдоль кости благоприятствуют не только нагноившиеся участки кости, но и значительное число отверстий во взаимосвязанных костных перегородках. Воспалительный процесс обусловливает изменение рН среды, которое наряду с локальным отеком, активностью лейкоцитов и нарушением гемоциркуляции, в совокупности приводят к омертвению тканей. Нагноение распространяется также через питательные каналы, обусловливая одновременно в очаге тромбоз артерий и вен. В подобной ситуации гной скапливается под надкостницей, в которой находятся остеобласты и кровеносные сосуды (рис. 1).
Соединительная ткань надкостницы, как известно, подразделяется на два слоя – внутренний (камбиальный), в котором находятся последовательно стволовые клетки, преостеобласты и фибробласты; между остеобластами располагаются капиллярные сети, которые при остеомиелите поражаются прежде всего. Происходит их тромбоз, разрыв стенок и кровоизлияния. Над внутренним слоем располагается наружный, состоящий из плотной волокнистой соединительной ткани, представленной в большей степени коллагеновыми волокнами, а также небольшим количеством эластических волокон и фибробластов; между ними располагается сеть кровеносных и лимфатических сосудов. Важно, что коллагеновые волокна одновременно крепят надкостницу к кости за счет их проникновения в кость (прободающие волокна Шарпея). За счет их при остеомиелите гнойные массы определенное время находятся в поднадкостничном пространстве, не прорываясь наружу. Все указанные процессы в той или иной степени распространяются вдоль грудины по линии ее разреза.
В итоге частичный послеоперационный некроз смежных участков грудины с одновременным развитием нагноительного процесса и некрозом ее костных балок приводит к нарушению прочности соединения и возникновению подвижности кости в зоне операции. Краевой характер некроза костной ткани по всей линии разреза грудины протекает неравномерно, что обусловливает образование зазубренного стыка оперированной кости. У пациентов с более тяжелыми клиническими формами осложнений гнойный процесс во всех случаях захватывает не только зону разреза грудины, но и начинает распространяться на соседние участки. Особенно ускоренно это происходит в области швов, где кость прокалывается, и создаются условия для дополнительного инфицирования тканей. Как и в области разреза кости, здесь повреждаются сосуды надкостницы, костные перекладины и костный мозг. В результате развиваются те же патологические изменения кости, что и в области разреза. В итоге вокруг шовного материала возникает расширяющаяся круговая зона некроза костной ткани. Более того, в последующем она сливается с подобными участками, распространяющимися от линии разреза грудины в поперечном направлении.
Как правило, на границе некротизированной и живой ткани в результате реактивного воспаления образуется грануляционный вал. При этом гистологическая картина некробиотических процессов также неравнозначна. Имеются участки как незрелой грануляционной ткани с большим количеством распадающихся нейтрофилов, вакуолизированных макрофагов и плазматических клеток, так и более зрелые зоны – с образованием фиброзной ткани. В ряде случаев по краю грануляционной ткани встречаются очаги грубоволокнистой кости. Подобного рода кость не подвергается оссификации и нередко разрушается остеокластами. Последние определяются и в живой кости на границе с некротизированной тканью. В некоторых препаратах фиброзирующаяся грануляционная ткань иногда формирует так называемую «пиогенную мембрану», инфильтрированную первоначально лейкоцитами, которые мигрировали в формирующиеся секвестральные полости. Такая полость, как правило, окружается секвестральной капсулой, состоящей из грубоволокнистой и пластинчатой кости. Под капсулой выявляются мелкие и несколько укрупненные пространства, заполненные грануляциями, гноем и секвестрирующимися участками костной ткани. Однако, капсула не является полноценным изолирующим материалом, содержит щели и отверстия, через которые выделяется гноеродная масса, распространяющаяся на прилегающие участки.
После расплавления гноем фиброзной части надкостницы у этой группы пациентов в различных участках грудины образуются секвестры, при этом их величина, локализация и скорость распространения различны (рис. 2). Более того, гнойный процесс распространяется и на мышечную ткань. Этот процесс сопровождается не только тромбозом артерий и вен, расплавлением мышечных волокон и соединительной ткани, но и массивными кровоизлияниями. В зонах, где наблюдается относительно медленное развитие секвестров, активность остеобластов на предсуществующих перегородках кости приводит к их утолщению. В этом случае развиваются аномально уплотненные секвестры, которые разрушаются медленнее, чем другие. Возможно, это обусловлено различной степенью предшествующей обсемененности бактериями тех или иных частей грудины. С другой стороны, подобное явление может быть обусловлено чередованием процесса усиления и частичного затухания воспалительной реакции (в ходе общего и местного лечения), при котором активизируются остеобластические элементы. Одной из причин может являться также реактивное усиление деятельности остеобластов надкостницы и ячеек кости, соседствующих изначально с секвестральной полостью. В случае рассасывания мелких секвестров наблюдаются выраженные репаративные процессы на их периферии с временным образованием новых костных балок, постепенно заполняющих образовавшийся дефект.
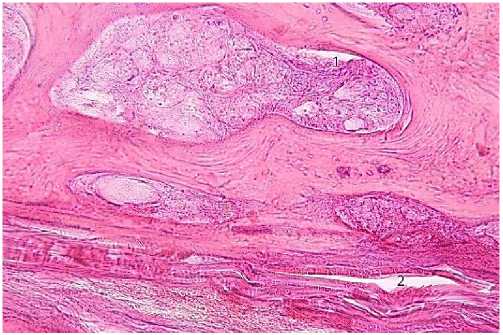
Рис. 1. Образование гнойных очагов в кости и в поднадкостничном пространстве (1), расслоение надкостницы (2). Окр.: гематоксилином-эозином. Ув.: х100.
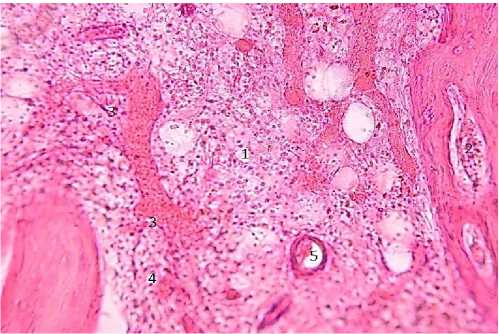
Рис. 2. Секвестрация костных балок, обширный гнойный очаг (1) и формирование более мелких очагов в в костных останках (2), разрушение тонкостенных сосудов (3), кровоизлияния (4), тромбоз сосудов (5). Окр.: гематоксилином-эозином. Ув.: х200.
Развитие хронического остеомиелита так или иначе на всем протяжении грудины характеризуется не только различным течением, но и различным исходом. Мозаичность поражения костной ткани - от начальных стадий воспалительного процесса до образования секвестров, частичной регенерации костной ткани и формирования зон склерозирования кости, а также возникновения свищевых ходов в мышечной ткани и кровоизлияний, обусловлена в первую очередь неравномерностью распространения гнойного процесса вдоль грудины.
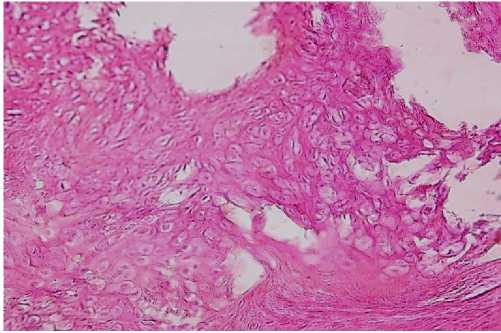
Рис. 3. Деструктивные изменения гиалинового хряща. Окраска: гематоксилин-эозином. Ув.: х600.
В далеко зашедших случаях зоны разрушения кости полностью доминируют над явлениями регенерации костной ткани и начинают распространяться также и на костно-хрящевые сочленения и ребра. Этот процесс сопровождается прорывом гноя в мягкие ткани одновременно в нескольких местах, являясь причиной образования обширной параоссальной и околохрящевой флегмоны. Соседствующей с грудиной глиалиновый хрящ является бессосудистым образованием (за исключением надхрящницы), поэтому процесс в нем протекает несколько иначе, несмотря на то, что первые этапы, связанные с поражением сосудов надхрящницы, являются сходными. Тромбоз артерий и вен надхрящницы, как и в кости, нарушает питание хряща. В результате происходит быстрая гибель всей надхрящницы с расплавлением ее волокнистых структур и камбиальных элементов, полная отслойка от хряща. И если при остеомиелите процесс первоначально развивается эндостально, то при поражении хряща развивается хондролиз, в результате которого хрящ либо разделяется на островки, либо наблюдается его краевое расплавление (рис. 3). На месте разрушающегося хряща развивается грануляционная ткань, которая в дальнейшем частично рубцуется, особенно при затухании процесса остеомиелита, или сохраняется более длительное время, захватывая все большие пространства. В этом случае по ее краю иногда можно заметить формирование новых хрящевых островков, быстро теряющих, однако, структурность, напоминая больше тени с неясными очертаниями хрящевых клеток. Складывается четкое представление, что разрушение хрящей происходит быстрее чем ткани кости. Распространение гнойного процесса с костной ткани на хрящевую возможно двумя путями. Одним из них является прямой переход в области сочленения кости и хряща, другой - через формирование флегмон, образующихся в мягких тканях над хрящами и ребрами.
В связи с двойственным характером воздействия на ребра, как со стороны хряща, так и со стороны развивающейся параоссальной флегмоны, эндостальное костеобразование в ребрах нарушается. Вблизи эндоста быстро развивается и формируется грануляционная ткань, в которой видны массивные очаги некроза костного мозга, резко расширенные сосуды, густо инфильтрированные миелоидными элементами, различными по степени зрелости. Гнойные массы, находящиеся снаружи от реберных костей, быстро нарушают их кровоснабжение с дальнейшим некрозом наружной костной пластинки. Гной через входные ворота (места входа сосудов в кость) проникает и внутрь костей, в результате чего происходит слияние гнойных процессов, идущих эндо- и периостально. В результате происходит полное разъединение костно-хрящевого сочленения с опасностью распространения инфекции на органы грудной полости.
Таким образом, остеомиелит по характеру своего течения в зоне разреза грудины не является однотипным. Более того, в одних зонах он протекает как острый процесс, а в других имеет хроническое течение, что зависит от скорости распространения инфекции. При этом в разных участках может происходить частичная регенерация костной ткани, даже с утолщением перегородок, но без типичного восстановления структуры кости. Доминирующим процессом является полная деструкция кости с формированием грануляционной ткани, приобретающей в последующем рубцовый характер строения. Помимо того, в различных участках грудины развиваются свищи, имеющие тенденцию захватывать и мягкие ткани с образованием свищевых ходов как результат флегмонозного процесса. Переход гнойных очагов на хрящевую ткань приводит к разъединению ее с грудиной, а в последующем с ребрами, которые, в свою очередь подвергаются разрушению. Следует иметь в виду, что остеомиелит имеет тенденцию к полному захвату всех тканей грудной клетки, что является естественной причиной перехода гнойного процесса на плевру и внутренние органы. В этих случаях развивается стерномедиастинит. Возбудителями подобного рода инфекционно-воспалительных осложнений чаще всего является грамположительная микрофлора, как правило, бактерии рода Staphylococcus [5-6]. В последние годы возрастает роль и грамотрицательных бактерий, в частности, Pseudomonas aeruginosa [7-9]. У пациентов, которые находились под нашим наблюдением, в случаях нестабильности грудины из отделяемого раны выделяли коагулазоотрицательные стафолококки fS. epidermidis, S. saprophiticus) , у остальных - этиопатогенами служили S. aureus и Pseudomonas aeruginosa (5 и 3 пациента, соответственно). Именно эти микроорганизмы обусловливали наиболее тяжелые клинические формы осложнений.
Заключение. Итак, следует отметить, что основные исследования, касающиеся механизмов развития и патоморфологических проявлений остеомиелитов различной природы относятся к 70-80-м годам прошлого столетия [10-11]. В настоящее время в доступной литературе мы не встретили таких работ и, прежде всего, исследований, связанных с изучением особенностей и степени выраженности деструктивно-некротических процессов костно-хрящевого комплекса грудины при различных клинических формах инфекционно-воспалительных осложнений, развивающихся после кардиохирургических вмешательств. В то же время, учитывая изменение фено- и генотипических характеристик этиопатогенов, в частности, широкой циркуляции антибиотико-резистентных штаммов, такие исследования представляются целесообразными.
Упациентов с диагнозом нестабильность грудины патоморфологические процессы костной ткани грудины развиваются в области продольного разреза. Они характеризуются поражением костного мозга, нарушением кровоснабжения, формированием очагов нагноения и некроза костной ткани. У пациентов с более тяжелыми клиническими формами осложнений деструктивно-некротический процесс распространяется на различные участки костно-хрящевого комплекса грудины, сопровождается развитием очагов полной деструкции кости, образованием секвестров и свищевых ходов. В ряде случаев остеомиелитические поражения охватывают все ткани грудины, и гнойный процесс распространяется на органы средостения. Возбудителями инфекционно-воспалительных осложнений после операций на открытом сердце, наряду с бактериями рода Staphylococcus , в ряде случаев является Pseudomonas aeruginosa . Именно эти микроорганизмы вызывают наиболее выраженные патоморфологические изменения костно-хрящевого комплекса грудины.
Список литературы Деструктивно-некротические процессы костно-хрящевого комплекса грудины при инфекционно-воспалительных осложнениях после хирургических операций на открытом сердце
- Bokeriia L.A., Beloborodova N.V. Infektsiia v kardiokhirurgii.- M.: Izd-vo NTSSSKH im. A.N. Bakuleva RAMN, 2007.- 582s.
- Меshаlkin Е.N., Litasova Е.Е., Iasnova L.N. i dr. Мikroekologiia bolnykh kardiokhirurgicheskoi kliniki//Sistemnyi podkhod k otsenke faktorov riska u bolnykh s serdechno-sosudistoi patolodiei/ Pod red. Е.Е. Litasovoi.- Novosibirsk, 2002.- S.13-83.
- Вrachton JH, Marrin CA, McGrath PD., Morton JR, Norotsky M, Charlesworth DC, Lahey SJ, Clough R, Ross CS, Olmstead EM, O’Connor GT. 10-year follow-up of patients with and without mediastinitis. Semin Thorac Cardiovasc Surgery. 2004 Spring;16(1):70-76.
- Kasatov А.V. Chetvertnykh V.А., Shchetkina I.N. Patomorfologiia khronicheskogo poststernotomicheskogo osteomielita grudiny, razvivshegosia posle kardiokhirurgicheskikh vmeshatelstv// Моrfologicheskie vedomosti.- 2017.- № 3.-S.43-45.
- Upton A, Roberts SA, Milsom P, Morris AJ. Staphylococcal post-sternotomy mediastinitis: five year audit. ANZ J Surgery 2005 Apr;75(4):198-203
- Naidu SI, Donepudi SK, Stocks RM, Buckingham SC, Thompson JW. Methicillin-resistant Staphylococcus aureus as a pathogen in deep neck abscesses: a pediatric case series. IZnt J Pediatr Otorhinolaryngol. 2005;Oct 69(10):1367-1371.
- Rudnov VА. Sovremennoe klinicheskoe znachenie sinegnoinoi infektsii i vozmozhnosti ee terapii u patsientov otdelenii reanimatsii. Инф антимикроб тер. 2002;5:170-177.
- Okonta KE, Anbarasu M, Jamesraj J et al. Sternal wound infection following open heart surgery: appraisal of incidence, risk factors, changing bacteriologic pattern and treatment outcome. Ind J Thorac Cardiovase Surg. 2011;27:28-32.
- Kasatov А.V., Gorovits E.S., Kuznetsova М.V., Timasheva О.А., Sukhanov S.G. Osobennosti biologicheskikh svoistv shtammov Pseudomonas aeruginosa, izolirovannykh ot bolnykh osteomielitom grudiny i reber// Zhurnal mikrobiologii, epidemiologii i immunobiologii.- 2015.- № 2.- S. 69-74.
- Akzhigitov G.N., Galeev М.А., Sakhautdinov V.G., Iudin Ia.B. Osteomielit.- М.: Меditsina, 1986.- 205s.
- Grinev М.V. Оsteomielit.- L: Меditsina, 1977.- 159s.


