Диагностика и факторы риска нозокомиальной пневмонии у больных тяжелым инсультом
Автор: Гусаров В.Г., Замятин М.Н., Теплых Б.А., Бардаков В.Г., Пихута Д.А., Бронов О.Ю.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.7, 2012 года.
Бесплатный доступ
Для оценки качества диагностики нозокомиальной пневмонии (НП) у больных острым инсультом выполнен ретроспективный анализ данных историй болезни, результатов аутопсий, архива рентгенограмм 80 больных. Чувствительность рентгенографии составила 21,2% во время лечения пациентов и 12,1% - при анализе архива, чувствительность шкалы CPIS - 97%, специфичность - 97,9%. Стремление подтвердить диагноз рентгенологически привело к увеличению продолжительности неадекватной антибактериальной терапии, повышению лучевой нагрузки на пациента и стоимости лечения. Выявлены факторы риска развития НП у больных тяжелым инсультом: время до интубации трахеи > 1 час (АР +56; ОР 6,22 ± 0,56 ДИ 2,05-18,8), количество фибробронхоскопий (ФБС) > 2 (АР +44; ОР 3,53 ± 0,44 ДИ 1,49-8,36), время до начала энтерального питания > 3 сут (АР +61; ОР 4,23 ± 0,36 ДИ 2,07-8,63), наличие бульбарных нарушений (АР +42; ОР 4,23 ± 0,56 ДИ 1,4-12,77).
Инсульт, нозокомиальная пневмония, диагностика, рентгенография, шкала cpis, факторы риска
Короткий адрес: https://sciup.org/140188072
IDR: 140188072 | УДК: 616.24-002:616.831-005.1
Текст научной статьи Диагностика и факторы риска нозокомиальной пневмонии у больных тяжелым инсультом
Ранняя постановка правильного диагноза является фундаментальной основой ведения пациентов с НП [7]. Поздняя диагностика и последующее запоздалое начало адекватного лечения могут приводить к неблагоприятному течению и исходу НП [12, 15].
В соответствии с существующими методическими рекомендациями ключевым признаком НП является появление на рентгенограмме «свежих» очагово-инфильтративных изменений в легких, что в комплексе с клинической картиной позволяет поставить диагноз и изменить программу лечения [2, 6].
Клинические, микробиологические и рентгенологические симптомы пневмонии имеют различный (часто низкий) уровень чувствительности и специфичности [5, 8], вследствие чего, ни один из отдельно взятых критериев не может являться золотым стандартом диагностики НП.
К сожалению, при рентгенографии грудной клетки в палатах реанимации, где выполнение снимков в двух проекциях технически трудноосуществимо, вероятность ложноотрицательных результатов остается очень высокой, а выявленные на рентгенограмме изменения врачи нередко трактуют по-разному [1, 5]. Несоответствие клинической картины и данных рентгенологического заключения затрудняет процесс лечения пациента, препят- ствует своевременной коррекции проводимой терапии, правильной экспертной оценке причин и последствий развившихся осложнений. Одним из подходов к решению этой проблемы является использование в реаниматологической практике комплексных бальных методов верификации НП с применением шкал, основанных на одновременной оценке нескольких наиболее достоверных клинико-лабораторных и рентгенологических симптомов пневмонии. Примером такой шкалы является «Клиническая шкала легочной инфекции» (Clinical Pulmonary Infection Score, CPIS), однако и ее значение до настоящего времени оценивается неоднозначно. Шкалу нередко предлагают использовать для первичной оценки вероятности наличия НП и динамики процесса в легком, подчеркивая, что для постановки диагноза, его необходимо подтвердить рентгенологически или бактериологически, что удается сделать далеко не всегда [16, 18]. В конечном итоге, процесс принятия решения о наличии у больного пневмонии вновь затягивается, что может ухудшить результаты лечения этой категории пациентов.
Некоторую помощь в диагностике инфильтративных изменений в базальных отделах легких может оказать компьютерная томография (КТ). Однако сама КТ имеет ряд ограничений, и при выявлении уплотнения (консолидации) легочной паренхимы приходится проводить дифференциальную диагностику с более чем 20

различными заболеваниями легких. Среди них пневмонии, ателектазы, бронхо-альвеолярный рак, отек легких, респираторный дистресс-синдром взрослых (РДСВ), кровоизлияния, саркоидоз и многие другие заболевания и состояния [3]. Наибольшие трудности представляет дифференциальная КТ-диагностика нозокомиальной ИВЛ-ассоциированной пневмонии (НПивл) и ателектазов легочной ткани вследствие плеврального выпота, высокого стояния диафрагмы, респираторного дистресс-синдрома взрослых (РДСВ). Помощь в проведении дифференциальной КТ-диагностики этих состояний может оказать применение маневра открытия легких, впервые предложенного Бурхардом Лахманом в 1992 году [14]. При выполнении данного метода отмечается расправление ателектазированных участков легочной паренхимы при РДСВ и компрессионных ателектазах, однако уплотнение легочной ткани, вызванное пневмонией, сохраняется. Это положение можно подтвердить, выполняя КТ легких до и после проведения маневра открытия. При проведении данного исследования авторам не удалось найти работ, в которых проведение КТ до и после проведения маневра открытия легких использовалось бы в качестве метода дифференциальной диагностики НПивл.
Таким образом, на сегодняшний день существует острая необходимость использования в клинической практике комплексных методов верификации воспалительного процесса в легких с применением нескольких наиболее достоверных клинико-лабораторных и рентгенологических симптомов пневмонии.
Риск развития пневмонии при инсульте значительно выше, чем при многих других тяжелых заболеваниях, травмах, критических состояниях. Среди факторов риска развития пневмонии у пациентов с инсультом известны следующие: возраст старше 65 лет, тяжелый неврологический дефицит, обширный инфаркт в бассейне средней мозговой артерии, нарушения сознания и глотания, дизартрия, афазия, ХОБЛ, гипергликемия, несбалансированное питание, уремия. [4, 9, 11, 17, 19, 20]. У пациентов с инсультом в возрасте старше 65 лет наличие даже одного из этих факторов позволяет с высокой чувствительностью и специфичностью предсказать развитие пневмонии [19].
Цель исследования
Оценить качество диагностики и определить наиболее значимые факторы риска развития НП у больных острым инсультом.
Материалы и методы
Данное исследование выполнено в процессе ретроспективного анализа результатов лечения 80 больных острым инсультом, госпитализированных в отделение реанимации «НМХЦ им. Н.И. Пирогова». 55 больным потребовалась респираторная поддержка, средней продолжительностью 13,6 ± 11,2 суток. Проведен анализ летальности, данных аутопсии и качества диагностики НП среди пациентов с острым инсультом.
Во время лечения всем пациентам с острым инсультом проводили систематическое физикальное и лабораторное обследование 2 раза в сутки. При появлении признаков системной воспалительной реакции: повышении температуры тела выше 38° С, нарастании лейкоцитоза > 11,0 X 10 9 /л, либо появлении лейкопении < 4,0 X 10 9 /л, тахикардии > 90 в мин., а также присоединении симптомов острой дыхательной недостаточности диагностическую программу изменяли в направлении поиска очага инфекции в легких. Выполняли: рентгенографию грудной клетки в прямой проекции в палате ОРИТ портативным рентгеновским аппаратом, забор материала из нижних дыхательных путей для бактериологического исследования методом эндотрахеальной аспирации или брохоаль-веолярного лаважа. Параллельно занимались поиском источников интоксикации другой локализации.
В случае отсутствия рентгенологических критериев НП рентгенографию повторяли каждые 1–3 суток до выявления признаков воспалительных изменений в легких либо до установки диагноза НП другими методами. При ретроспективном анализе историй болезни выполнена дополнительная, повторная оценка архива рентгенограмм этих пациентов пятью сотрудниками отделения лучевой диагностики. Однако в последнем случае рентгенологи при изучении снимков не знали клинических и лабораторных данных пациентов.
В ходе ретроспективного анализа данные обследования были подвергнуты повторному изучению, но уже с применением шкалы CPIS. В случае, если оценка по CPIS составляла 6 и более баллов, устанавливали диагноз НП. День установки диагноза НП при использовании CPIS принят за день 0 (начало НП).
В качестве методов, позволяющих подтвердить диагноз НП (с учетом клинических данных), использованы: рентгенография грудной клетки (в случае выявления инфильтративных изменений), КТ грудной клетки, аутопсия.
Для повышения диагностической ценности КТ при НП использован маневр «открытия легких», который выполняли непосредственно в кабинете КТ.
Определены следующие критерии: чувствительность и специфичность рентгенографии грудной клетки в прямой проекции, выполненной в палате ОРИТ портативным рентгеновским аппаратом, чувствительность и специфичность шкалы CPIS, сроки принятия решения о назначении или смене антибактериальных средств, количество выполненных в процессе диагностики рентгеновских снимков органов грудной клетки, лучевая нагрузка на пациента, прямые расходы на выполнение рентгенографии.
Были изучены факторы риска развития НП (пол, возраст > 65 лет, сахарный диабет, ХОБЛ, первичная тяжесть инсульта, локализация инсульта, бульбарные нарушения, время до выполнения интубации трахеи, сроки выполнения трахеостомии, частота выполнения ФБС, время начала энтерального питания) у пациентов
в острой стадии инсульта. Рассчитан относительный и абсолютный риск развития НП при наличии каждого из указанных признаков.
Результаты
При проведении ретроспективного анализа историй болезни было выявлено 27 случаев НП у 25 пациентов из 80 (33,7%), вошедших в исследование. Данная патология была диагностирована либо в ходе госпитализации на основании клинических и рентгенологических признаков, либо во время аутопсии. В таблице 1 представлены данные об уровне летальности и сроках диагностики НП.
Из таблицы 1 видно, что летальность в группе больных с НП значимо отличается от контрольной группы. При этом диагноз НП в период госпитализации был установлен только 23 из 25 больных. Два случая НП были выявлены лишь посмертно при проведении патологоанатомического исследования.
Проводя дальнейший анализ, выявлено следующее, в контрольной группе из 9 умерших аутопсия не проводилась в 2 случаях, однако в качестве причины смерти у этих двух пациентов отмечен синдром полиорганной недостаточности, связанный с интоксикацией и у них нельзя было полностью исключить НП в качестве возможного источника эндотоксикоза.
Таким образом, при проведении анализа летальных исходов выявлена группа пациентов, которым диагноз НП не был установлен в ходе госпитализации, и этот факт с высокой вероятностью мог повлиять на исход заболевания. В качестве инструмента, позволяющего повысить качество диагностики НП, нами использована шкала CPIS, которая объединяет в себе ряд клинических, лабораторных и инструментальных данных и позволяет количественно оценить вероятность наличия у пациента НП.
Проведен повторный ретроспективный анализ всех 80 историй болезни пациентов, вошедших в исследование. Использование шкалы CPIS оказалось более информативным. При ретроспективном анализе с применением этой шкалы было выявлено 33 случая НП у 30 пациентов с острым инсультом. Средняя оценка по шкале CPIS составила 8,3 ± 1,55 балла. Лишь в 1 наблюдении, при подтвержденной на аутопсии НП значение оценки по шкале CPIS оказалось менее 6 баллов. В результате чувствительность шкалы CPIS, как способа диагностики НП у больных острым инсультом составила 97%. Высокой оказалась и специфичность этой шкалы. Лишь в 1 случае получен ложноположительный результат, когда оценка по CPIS составила 6 баллов, а проведенная впоследствии КТ грудной клетки не выявила инфильтративных изменений в легких. В конечном итоге специфичность оказалась равной 97,9%. Данные о чувствительности и специфичности шкалы CPIS представлены в таблице 2.
Таким образом, применение бальных методов верификации НП позволило выявить дополнительно 7 случаев НП у пациентов с острым инсультом. Во всех
Табл. 1. Уровень летальности и сроки диагностики НП
|
Признак |
Контрольная группа (n=55) |
Основная группа (n=25) |
Уровень значимости отличий (р) |
|
Летальность, абс. число (%) |
9 (16,3) |
10 (40,0) |
< 0,05 |
|
Прижизненная диагностика НП, абс. число (%) |
0 |
23 (92,0) |
– |
|
Посмертная диагностика НП*, абс. число (%) |
0 |
2 (8,0) |
– |
Примечание : * – по данным аутопсии.
Табл. 2. Чувствительность и специфичность шкалы CPIS*
|
НП, абс. число |
Всего |
|||
|
Присутствует |
Отсутствует |
|||
|
CPIS |
≥ 6 баллов |
33 |
1 |
34 |
|
< 6 баллов |
1 |
48 |
49 |
|
|
Всего |
34 |
49 |
||
|
Чувствительность, % |
97% |
– |
||
|
Специфичность, % |
– |
97,9% |
||
Примечание : * – в таблице указана частота случаев НП среди 80 пациентов, вошедших в исследование.
этих случаях у пациентов присутствовали клинические и микробиологические признаки НП, однако в связи с отсутствием рентгенологического подтверждения, диагноз НП так и не был установлен в период госпитализации. Из 7 случаев, когда только оценка по шкале CPIS помогла поставить диагноз НП, в трех – лечение закончилось летальным исходом, еще у двух больных антибактериальная терапия, назначенная, несмотря на отсутствие явного очага инфекции, привела к выздоровлению, а два пациента были переведены в другие стационары.
По современным представлениям ключевым признаком НП рассматривается появление на рентгенограмме «свежих» или прогрессирование имеющихся очагово-инфильтративных изменений в легких [1, 2, 6, 10, 13]. Этот постулат заставляет практикующих врачей искать обязательное рентгенологическое подтверждение НП. Кроме того, некоторые авторы указывают на высокую чувствительность отдельных рентгенологических признаков НП [21]. В нашем исследовании при проведении анализа данных историй болезни в 33 случаях НП (оценка по CPIS ≥ 6 баллов) присутствовали клинические, лабораторные и микробиологические признаки воспалительного процесса в легких, но лишь в семи из них диагноз НП был подтвержден при выполнении рентгенографии органов грудной клетки в прямой проекции. Таким образом, чувствительность рентгенографии в прямой проекции составила 21,2% и была достоверно (р<0,001) ниже, чем чувствительность диагностики с использованием шкалы CPIS. Интересно, что при контрольном анализе архива рентгенограмм («слепым методом») чувствительность рентгенографии

оказалась еще ниже (12,1%), поскольку признаки НП на рентгенограммах были выявлены только у 4 больных. Сравнительные данные о чувствительности методов диагностики НП представлены на рисунке 1.
Важно подчеркнуть, что главным достоинством применения шкалы CPIS для оценки вероятности НП стало значительное опережение динамики балльной оценки в сравнении с появлением рентгенологических изменений. Данная зависимость отражена на рисунке 2.
На диаграмме за точку отсчета принят условный день 0, когда оценка по CPIS впервые за время лечения больного достигла 6 и более баллов. Как видно из графика в день диагностики НП по шкале CPIS рентгенография легких была выполнена 17 пациентам, и ни в одном случае на снимках не было выявлено признаков НП. Такую разницу в диагностической ценности клинических и рентгенологических данных в этот день можно понять, она закономерна, т. к. рентгенологические изменения всегда несколько отстают от клиники. Но наиболее показательны дальнейшие события: к 6 дню общее количество рентгеновских снимков составило 48 (у большинства больных продолжался интенсивный, целенаправленный поиск возможных очагов инфекции), а изменения, характерные для НП выявлены только на 7.
Одним из самых серьезных последствий упорного поиска рентгенологического подтверждения НП явилась длительность неадекватной антибактериальной терапии, которая составила в среднем 6,1 ± 5,5 суток. Как только диагноз НП подтверждали рентгенологически или с помощью КТ антибактериальную терапию назначали (или меняли) немедленно. В семи случаях терапию назначили, поставив диагноз НП без рентгенологического подтверждения, поскольку признаки интоксикации увеличивались и стали приобретать угрожающий характер, повысилась концентрация прокальцитонина в плазме. Ретроспективный анализ показал, что использование шкалы CPIS могло бы помочь и в этой ситуации. Так, из семи случаев, когда диагноз НП был установлен только ретроспективно с помощью шкалы CPIS, в одном наблюдении антибиотики так и не были назначены, а в остальных задержка с назначением антибактериальных средств составила от 2 до 16 дней. В течение этого срока, из-за отсутствия явного очага инфекции, полагали, что лихорадка, как и другие признаки воспалительного ответа, имеют «центральное происхождение» и являются следствием морфологических изменений в головном мозге. Но, поскольку такое объяснение, не позволяло исключить наличие источников интоксикации, диагностические мероприятия продолжались. При этом количество рентгенограмм, выполненных одному больному, составило в среднем 5,35 ± 4,5 снимков, а в одном наблюдении достигло 19. Лучевая нагрузка на одного пациента в результате выполнения многочисленных рентгенографий оказалась равной в среднем 1,46 ± 1,17 мЗв (максимально до 4,94 мЗв). Только прямые затраты на выполнение рентгенографии превысили в некоторых
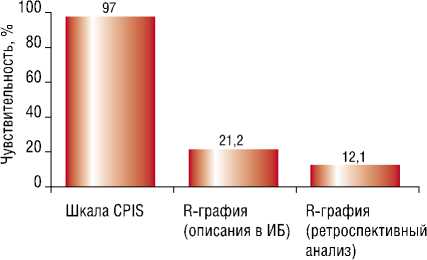
Рис. 1. Чувствительность методов диагностики НП
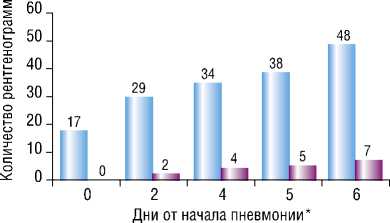
Общее количество рентгенограмм
I ■ Число рентгенограмм с картиной пневмонии
Рис. 2. Отставание рентгенологических данных от оценки по CPIS.
* – за 0 принят условный день, когда оценка по CPIS впервые достигла 6 и более баллов случаях 20000 руб (в среднем 6187 ± 4959 руб на одного пациента).
С целью улучшения качества рентгенологической диагностики НПивл, может быть использована КТ легких. В нашем исследовании данный метод помог установить диагноз в 11 случаях. Однако, выявленный на КТ синдром консолидации легочной ткани совсем не обязательно может быть связан с инфильтрацией паренхимы легких на фоне НП. Достаточно часто данные изменения обусловлены развитием, так называемых, компрессионных ателектазов базальных отделов легких вследствие длительного положения на спине, высокого стояния диафрагмы, применения миорелаксантов и других причин. Для дифференциальной диагностики между ателектазированием и инфильтрацией легочной ткани, а также для определения истинного объема НП нами с успехом использован маневр «открытия легких», который выполняется непосредственно в кабинете КТ. На рисунках 3, 4, 5 вы можете видеть различные варианты изменений в легочной паренхиме до и после проведения рекруитмента легких.
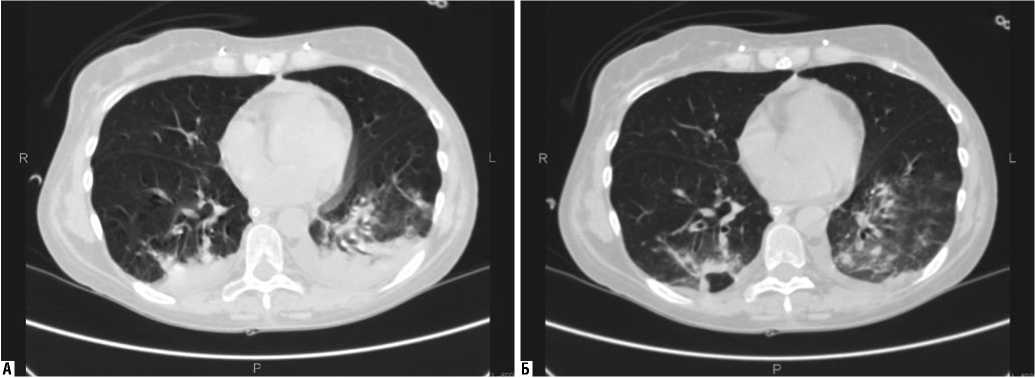
Рис. 3. Пациент Ш., 74 лет. Компрессионные ателектазы базальных сегментов легких. А – скан до маневра рекруитмента легких. Б – скан после маневра
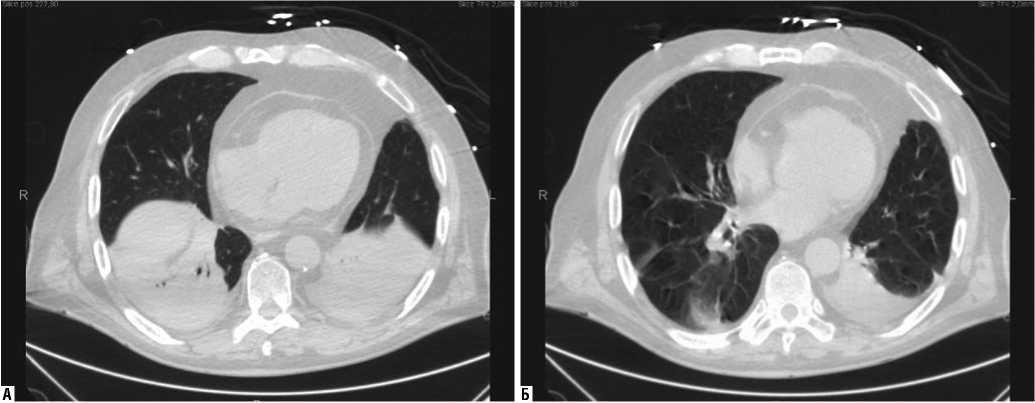
Рис. 4. Пациент Г., 46 лет. Компрессионные ателектазы базальных сегментов обоих легких и пневмония в 10 сегменте левого легкого. А – скан до маневра рекруитмента легких. Б – скан после маневра
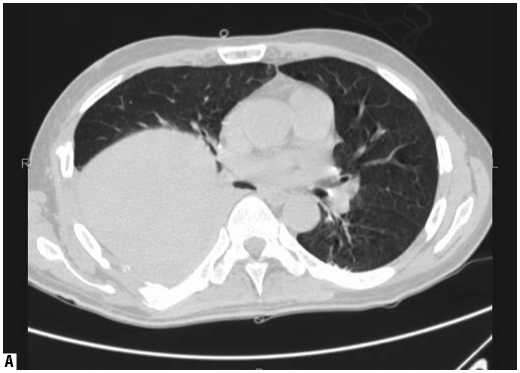
Рис. 5. Пациентка М., 51 года. Компрессионные ателектазы базальных сегментов правого легкого и пневмония в 6, 9, 10 сегментах правого легкого. А – скан до маневра рекруитмента легких.Б – скан после маневра
Факторы риска развития НП у больных с острым инсультом
Таким образом, при обработке данных историй болезни с использованием шкалы CPIS, установлено, что НП развилась у 30 из 80 пациентов с острым инсультом. Анализируя известные факторы риска развития НП у больных инсультом [19, 20], выявлено, что все 80 пациента имеют 2 и более следующих фактора риска: возраст > 65 лет, дизартрия или афазия, балл по модифицированной шкале Ранкина ≥ 4, нарушения глотания. Следовательно, НП должна была развиться практически у всех пациентов с чувствительностью 90,9% и специфичностью 75,6%, однако этого не произошло.
Нами были проанализированы дополнительные признаки, наличие которых с высокой вероятностью могло повлиять на развитие НП в остром периоде инсульта. Данные факторы представлены в таблице 3.
Табл. 3. Факторы риска пневмонии (n=30)
|
Признак |
АР, % |
ОР (95% ДИ) |
р |
|
Мужской пол |
+ 15 |
1,51±0,36 (0,74–3,09) |
> 0,05 |
|
Женский пол |
- 15 |
0,66±0,36 (0,32–1,34) |
> 0,05 |
|
Возраст > 65 лет |
+ 11 |
1,38±0,46 (0,55–3,45) |
> 0,05 |
|
Балл NIHSS ≥ 10 при поступлении |
+ 3 |
1,09±0,37 (0,52–2,25) |
> 0,05 |
|
Балл Ранкина ≥ 4 при поступлении |
- 100 |
0 |
> 0,05 |
|
Наличие бульбарных нарушений |
+ 42 |
4,23±0,56 (1,4–12,77) |
< 0,05 |
|
Локализация очага инсульта в бассейне ВСА |
+ 8 |
124±0,42 (0,54–2,86) |
> 0,05 |
|
Локализация очага инсульта в ВББ |
- 4 |
0,88±0,42 (0,39–2,01) |
> 0,05 |
|
Сахарный диабет |
- 5 |
0,88±0,42 (0,38–2,01) |
> 0,05 |
|
ХОБЛ |
+ 3 |
1,07±0,41 (0,48–2,4) |
> 0,05 |
|
Время до интубации трахеи* ≥ 1 час |
+ 56 |
6,22±0,56 (2,05–18,8) |
< 0,05 |
|
Трахеостомия ≥ 3 сут от интубации трахеи |
+ 19 |
1,38±0,32 (0,74–8,36) |
> 0,05 |
|
Количество ФБС ≥ 2 |
+ 44 |
3,53±0,44 (1,49–8,36) |
< 0,05 |
|
Время до начала энтерального питания ≥ 3 сут |
+ 61 |
4,23±0,36 (2,07–8,63) |
< 0,05 |
Примечание : * – данный показатель определяет время от появления таких признаков, как снижение уровня сознания ≤ 9 баллов по шкале ком Глазго, бульбарные нарушения, нейрогенная гипервентиляция до выполнения интубации трахеи.
Из таблицы 3 видно, что пол, возраст, локализация и тяжесть инсульта, наличие сопутствующих заболеваний (сахарный диабет, ХОБЛ) достоверно не увеличивали риск развития НП. Так же значимо не оказывали влияния сроки выполнения трахеостомии. Однако выявлены дополнительные факторы риска, наличие которых достоверно увеличивало относительный и абсолютный риски развития НП в остром периоде инсульта. К ним отнесены: время до интубации трахеи ≥ 1 час (АР +56; ОР 6,22 ± 0,56 ДИ 2,05–18,8), количество ФБС ≥ 2 (АР +44; ОР 3,53 ± 0,44 ДИ 1,49–8,36), время до начала энтерального питания ≥3 сут (АР +61; ОР 4,23 ± 0,36 ДИ 2,07–8,63). Кроме того, подтверждена роль бульбарных нарушений в развитии НП (АР +42; ОР 4,23 ± 0,56 ДИ 1,4–12,77). Одним из наиболее значимых факторов риска следует считать время до интубации трахеи, которое четко отражает тот факт, что у пациентов неврологического профиля не следует дожидаться развития ОДН, а необходимо выполнять интубацию трахеи превентивно при развитии определенной очаговой и общемозговой симптоматики.
Указанные факторы риска были учтены при создании в НМХЦ им. Н.И. Пирогова протокола профилактики НП у больных острым инсультом.
Заключение
НП является фактором риска развития неблагоприятного исхода у пациентов с острым инсультом. Отдельно взятые клинические, лабораторные и рентгенологические признаки НП обладают неудовлетворительной чувствительностью, что может обусловливать удлинение сроков принятия решения о коррекции терапии в связи с развитием НП. Учитывая эти обстоятельства, алгоритм диагностики НП должен включать такие методики, комплексное применение которых имеет максимальную чувствительность и специфичность. Этому требованию в большей степени отвечает применение шкалы CPIS, в которой клинические, лабораторные, рентгенологические и бактериологические данные теряют свою исключительность и приобретают примерно равное значение. При этом, по нашим данным, чувствительность метода повышается до 97%, а специфичность 97,9%.
Ценным инструментом в диагностике НПивл является КТ легких. Повысить диагностическое значение КТ при выявлении пневмонии возможно, используя маневр «открытия легких».
Наиболее значимыми факторами риска развития НП у больных острым инсультом являются: время до интубации трахеи ≥ 1 час (АР +56; ОР 6,22 ± 0,56 ДИ 2,05–18,8), количество ФБС ≥2 (АР +44; ОР 3,53 ± 0,44 ДИ 1,49–8,36), время до начала энтерального питания ≥3 сут (АР +61; ОР 4,23 ± 0,36 ДИ 2,07–8,63), бульбарные нарушеня (АР +42; ОР 4,23 ± 0,56 ДИ 1,4–12,77).
Список литературы Диагностика и факторы риска нозокомиальной пневмонии у больных тяжелым инсультом
- Нозокомиальная пневмония, связанная с искусственной вентиляцией легких у хирургических больных./Гельфанд Б.Р. [и др.]. -М.: [б. и.], 2000.
- Нозокомиальная пневмония у взрослых. Российские национальные рекомендации/под. ред. Чучалина А.Г., Гельфанда Б.Р. -М.: [б. и.], 2009. -С. 90.
- Прокоп М. -Спиральная и многослойная компьютерная томография: учеб. пособие для системы послевуз. образования врачей в 2 т./М. Прокоп, под ред. А.В. Зубарева, Ш.Ш. Шотемора. -2-е изд. -М.: МЕДЖпресс-информ, 2009. -Т. 2. -710 с.
- Addington W.R. Assessing the laryngeal cough reflex and the risk of developing pneumonia after stroke: an interhospital comparison/W.R. Addington, R.E. Stephens, K.A. Gilliland//Stroke. -1999. -30. -6. -Р. 1203-1207.
- Beydon I. Can portable chest X-ray examination accurately diagnose lung consodil-ation after major surgery? A comparison with computed tomography scan/I. Beydon, M. Saada, N. Liu [et al.]//Chest. -1992. -102. -Р. 1698-703; 95.
- Bodmann K.F. Nosocomial pneumonia: prevention, diagnosis and treatment/K.F. Bodmann, J. Lorenz, T.T. Bauer [et al.]//Chemother. -J. 2003. -12(2). -Р. 33-44.
- Dellinger R.P. Surviving Sepsis Campaign guidelines for management of severe sepsis and septic shock./R.P. Dellinger, M.M. Levy, J.M. Carlet [et al.]//Crit Care Med. -2004. -32. -Р. 858-873.
- Fàbregas N. Clinical diagnosis of ventilator associated pneumonia revisited: comparative validation using immediate post-mortem lung biopsies./N. Fàbregas [et al.]//Thorax. -1999. -54. -Р. 867-873.
- Gordon C. Dysphagia in acute stroke./C. Gordon, R.L. Hewer, D.T. Wade//BMJ. -1987. -295. -Р. 411-414.
- Guidelines for the management of adults with hospital-acquired, ventilator-associated, and healthcare-associated pneumonia. -Am J Respir Crit Care Med. -2005. -171. -Р. 388-416.
- Hamidon B.B. The Predictors of Early Infection After An Acute Ischaemic Stroke./B.B. Hamidon, A.A. Raymond, M.I. Norlinah, S.B. Jefferelli//Singapore Med J. -2003. -Vol. 44(7). -Р. 344-346.
- Iregui M. Clinical importance of delays in the initiation of appropriate antibiotic treatment for ventilator associated pneumonia./M. Iregui [et al.]//Chest. -2002. -122. -Р. 262-268.
- Johanson W.G. Jr. Nosocomial respiratory infections with gram-negative bacilli. The significance of colonization of the respiratory tract./W.G. Johanson Jr. [et al.]//Ann Intern Med. -1972. -77. -Р. 701-706.
- Lachmann B. Open up the lung and keep the lung open/B. Lachmann//Intensive Care Med. -1992. -Vol. 18, № 6. -P. 319-321.
- Luna C.M. Impact of BAL data on the therapy and outcome of ventilator-associated pneumonia./C.M. Luna [et al.]//Chest. -1997. -111. -Р. 676-685.
- Luna C.M. Resolution of ventilator-associated pneumonia: prospective evaluation of the clinical pulmonary infection score as an early clinical predictor of outcome./C.M. Luna, D. Blanzaco, M.S. Niederman [et al.]//Crit Care Med. -2003. -31 (3). -Р. 676-682.
- Mann G. Swallowing function after stroke: prognosis and prognostic factors at 6 months./G. Mann, G.J. Hankey, D. Cameron//Stroke. -1999. -30. -Р. 744-748.
- Pugin J. Clinical signs and scores for the diagnosis of ventilator-associated pneumonia./J. Pugin//Minerva Anestesiol. -2002. -68 (4). -Р. 261-265.
- Sellars C. Risk factors for chest infection in acute stroke: a prospective cohort study./C. Sellars, L. Bowie, J. Bagg [et al.]//Stroke. -2007. -Vol. 38. -N8. -P. 2284-2291.
- Silver F.L. Early mortality following stroke: A prospective review./F.L. Silver, J.W. Norris, A.J. Lewis [et al.]//Stroke. -1984. -15. -Р. 492-496.
- Wunderink R.G. Radiologic diagnosis of ventilator-associated pneumonia./R.G. Wunderink//Chest. -2000. -117 (4 Suppl 2). -Р. 188-190.


