Диагностика и хирургическое лечение опухолей тонкой кишки
Автор: Стойко Ю.М., Левчук А.Л., Степанюк И.В., Серегин М.В.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.6, 2011 года.
Бесплатный доступ
Представлены современные возможности диагностики и хирургического лечения опухолей тонкой кишки.
Опухоль тонкой кишки, аденокарцинома, саркома, гастроинтестинальные стромальные опухоли, лейомиосаркома, карциноид, лимфома
Короткий адрес: https://sciup.org/140187942
IDR: 140187942 | УДК: 616.341-006-089
Modern diagnostics and surgical treatment of the small intestine tumors
The latest diagnostic and surgical treatment means for the small intestine tumors have been presented.
Текст научной статьи Диагностика и хирургическое лечение опухолей тонкой кишки
Несмотря на достигнутые за последние десятилетия успехи в лечении новообразований тонкой кишки, до настоящего времени их диагностика трудна, поскольку симптомы тонкокишечных опухолей неопределенны и неспецифичны. На тонкую кишку приходится всего 5% всех новообразований желудочно-кишечного тракта, несмотря на ее значительную протяженность (75% длины пищеварительной трубки) [2, 6]. Причем опухоли, как доброкачественные (39,6%), так и злокачественные (60,4% всех новообразований), могут исходить из любой ткани, составляющей стенку тонкой кишки [4, 5]. Наиболее часто злокачественными типами опухолей тонкой кишки являются аденокарцинома и саркома, составляющие 46,2 и 42% в структуре всех опухолей тонкой кишки соответственно [3]. В их симптоматике превалируют клинические проявления тонкокишечной непроходимости. Тогда как для доброкачественных новообразований тощей и подвздошной кишки наиболее патогномоничным симптомом являются рецидивирующие кишечные кровотечения, как правило, интенсивные и хронические, приводящие к анемии со всеми свойственными ей симптомами [7].
Материалы и методы
За последние 6 лет (2004–2010 гг.) нами диагностированы опухоли тонкой кишки у 19 пациентов (табл. 1). Средний возраст больных с доброкачественными опухолями составил 63 года, со злокачественными опухолями – 57 (возрастные колебания от 19 до 82 лет). Мужчин было 16 (84%), женщин – 3 (16%). У 9 пациентов опухоли локализовались в тощей кишке, а у 10 пациентов – в подвздошной кишке. У 11 больных возникли осложнения, которые послужили причиной выполнения экстренных операций. Наиболее частыми клиническими проявлениями доброкачественных опухолей тонкой кишки у 33,3% явились эпизоды кишечных кровотечений, которые носили, как правило, неинтенсивный, но рецидивирующий характер (табл. 2).
Злокачественные опухоли тощей кишки проявлялись клинически у 87% больных. Наиболее частыми симптомами являлись спастические или диффузные боли в животе (63% больных), потеря массы тела (50%), кишечная непроходимость (27,7%), кишечные кровотечения (5,5%), чаще хронические, но иногда и массивные, в результате распада опухоли. Пальпаторно опухоль в животе обнаруживали у 25% больных. У одного пациента злокачественная опухоль подвздошной кишки осложнилась перфорацией и перитонитом. Наиболее частыми симптомами «высокой» тонкокишечной непроходимости являлась локализация опухоли в тощей кишки, а при наличии опухоли в подвздошной кишке были признаки диареи.
Обсуждение полученных результатов
Учитывая относительную редкость выявления опухолей тонкой кишки и разнообразие их гистологической структуры, необходимо охарактеризовать наиболее часто встречающиеся отдельные пять типов опухолей данной локализации.
Аденокарцинома (n=4) является самым распространенным гистологическим типом и составляет 30–50% всех злокачественных опухолей тонкой кишки. Наиболее частыми клиническими проявлениями аденокарциномы, за счет ее экзофитного роста, являются симптомы хронической тонкокишечной непроходимости (рис. 1 А, Б). У 3 пациентов имелось прорастание аденокарциномы в соседние органы (мочевой пузырь, брыжейку поперечноободочной кишки, сигмовидную кишку). В одном случае диагностировано отдаленное метастазирование в печень и забрюшинные лимфатические узлы. У всех больных с аденокарциномой тонкой кишки отмечено повышение уровня онкомаркеров в крови СА 19-9 и РЭА.
Заслуживают внимание по частоте распространенности саркомные опухоли, развивающиеся из клеток мезодермы гладкомышечной и нейрогенной природы. В 1983 году для описания неэпителиальных гастроинтестинальных опухолей (шваномы, лейомиомы и лейомио-
Табл. 1. Морфологическая структура опухолей тонкой кишки
|
Тип опухоли |
Количество |
|
|
абс. |
% |
|
Доброкачественные:
|
Аденома |
1 |
5,2 |
|
Фиброма |
1 |
5,2 |
|
Гемангиома |
2 |
10,4 |
|
Лейомиома |
3 |
15,8 |
|
Невринома |
1 |
5,2 |
|
Липома |
1 |
5,2 |
|
Всего: |
9 |
47,7 |
Злокачественные:
|
Аденокарцинома |
4 |
21,1 |
|
Карциноид |
1 |
5,2 |
|
Ангиосаркома |
1 |
5,2 |
|
Лимфома |
3 |
15,8 |
|
Лейомиосаркома |
1 |
5,2 |
|
Всего: |
10 |
52,6 |
|
Итого: |
19 |
100 |
Табл. 2. Осложнения опухолей тонкой кишки
|
Тип опухоли и вид осложнения |
Количество |
|
|
абс. |
% |
|
|
Злокачественные: |
||
|
Тонкокишечная непроходимость |
5 |
27,7 |
|
Кишечное кровотечение |
1 |
5,5 |
|
Перфорация и параканкрозное воспаление |
1 |
5,5 |
|
Прорастание в соседние органы |
3 |
16,7 |
|
Всего: |
10 |
55,6 |
|
Доброкачественные: |
||
|
Тонкокишечная непроходимость |
1 |
5,5 |
|
Кишечное кровотечение |
6 |
33,3 |
|
Перфорация опухоли |
1 |
5,5 |
|
Всего: |
8 |
44,4 |
|
Итого: |
18 |
100 |

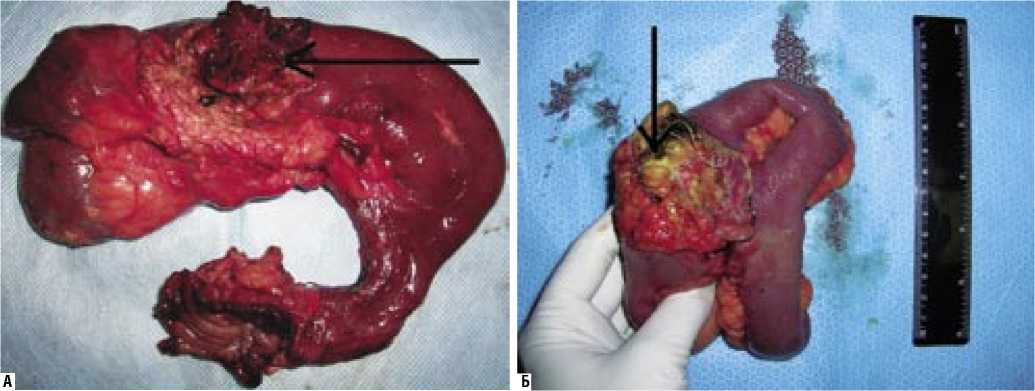
Рис. 1. Аденокарцинома тощей кишки: А – резецированная тощая кишка с опухолью (стрелкой показана опухоль); Б – морфологическая картина (окраска гематоксилином и эозином, ув. х 400). Стрелками обозначено разрастание атипичных желез саркомы) был предложен термин «гастроинтестинальные стромальные опухоли», которые развиваются из клеток Кахаля [1]. Для них характерен иммуногистохимический анализ на наличие экспрессии СД 117. Клинически лейомиосаркома тонкой кишки у одного нашего пациента проявлялась болями в животе, снижением массы тела, тошнотой и рвотой. В этом наблюдении имело место осложнение – перфорация лейомиосаркомы, которая представляла довольно большие размеры (более 10 см) с образованием заворота кишки (рис. 2 А, Б). Как правило, саркоматозные опухоли характеризуются значительной инфильтрацией стенки тонкой кишки, эндофитным ростом и поражением в основном регионарных лимфатических узлов брыжейки.
Карциноид тонкой кишки в нашем наблюдении располагался в стенке подвздошной кишки, небольшого размера (4 x 3) см, со значительной, свойственной ему фибробластной реакцией (специфический фиброз) в брыжейке сегмента пораженной кишки. Вследствие этого длина брыжеечного края кишки уменьшается и сворачивается в петлю, ввиду чего для карциноида на фоне «карциноидного» синдрома характерна клиника кишечной непроходимости (рис. 3 А, Б). Карциноид, диагностированный в наших наблюдениях в одном случае, клинически обусловливал специфический «карциноидный» синдром, характеризующийся триадой симптомов – приливами, диареей и хроническим вальвулитом (поражением трикуспидального клапана сердца и клапана

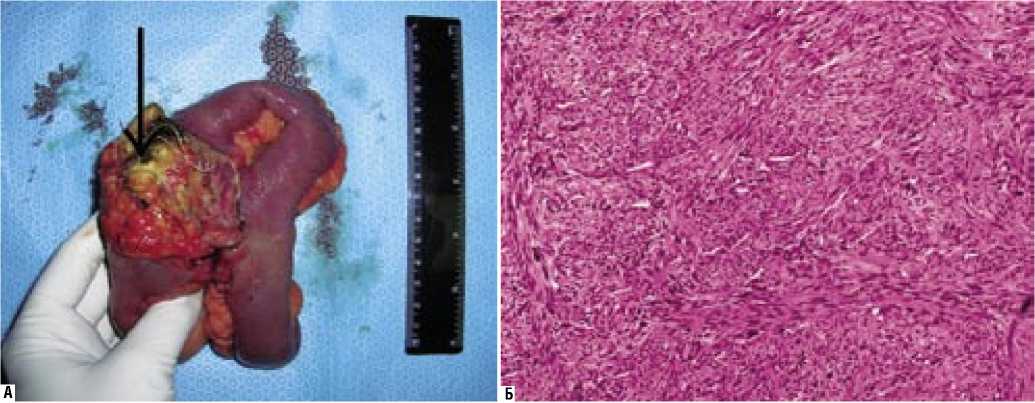
Рис. 2. Лейомиосаркома тонкой кишки с развитием заворота: А – резецированная тонкая кишка с опухолью (стрелкой показана опухоль); Б – морфологическая картина лейомиосаркомы тонкой кишки (окраска гематоксилином и эозином, ув. х 100)
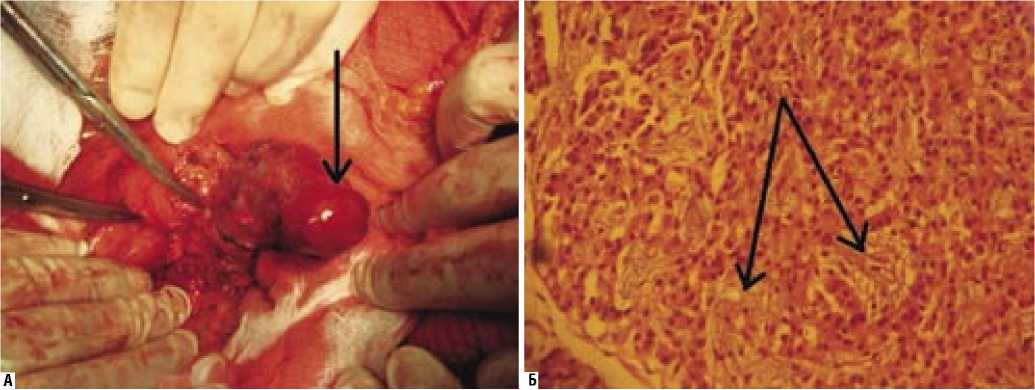
Рис. 3. Карциноид тонкой кишки: А – участок тонкой кишки с опухолью (стрелкой показана опухоль); Б – морфологическая картина карциноида тонкой кишки (окраска гематоксилином и эозином, ув. х 200). Стрелками обозначены мелкие мономорфные клетки с формированием псевдорозеток
легочной артерии). Согласно литературным данным карциноидный синдром сопровождает до 65% пациентов с карциноидом тонкой кишки [1].
Карциноиды являются наиболее распространенными нейроэндокринными опухолями (апудома), исходящими из энтерохромаффинных клеток. Их гистологическое строение впервые было описано LuBarsch O. в 1888 г., а термин «карциноидный» предложен Oberndorfer S. в 1907 г. Наиболее часто (42%) этот вид опухолей желудочно-кишечного тракта встречается в тонкой кишке [7]. Карциноидные опухоли редко метастазируют. Диагноз функионирующего карциноида базируется на определении специфических биохимических маркеров на серотонин: уровень 5-ГИУК и хромогранин А (ХГ-А) в суточной моче.
Лимфомы тонкой кишки развиваются из лимфоидной ткани подслизистого слоя стенки кишки, прорастают в слизистую оболочку с образованием язв. В трех наших наблюдениях лимфома тонкой кишки характеризовалась местным инвазивным ростом с метастазированием в регионарные лимфатические узлы. Клинически лимфомы тонкой кишки проявлялись болями в животе, симптомами тонкокишечной непроходимости и общей интоксикацией. Во всех случаях лимфомы локализовались в проксимальных отделах тощей кишки с поражением протяженных сегментов кишки (более 6 см) (рис. 4 А, Б).
Подавляющее большинство этих опухолей развивалось из В-лимфоцитов, реже встречаются Т-клеточные лимфомы.
Современные методы диагностики опухолей тонкой кишки
Диагностика опухолей тонкой кишки часто не имеет патогномоничной клинической симптоматики.
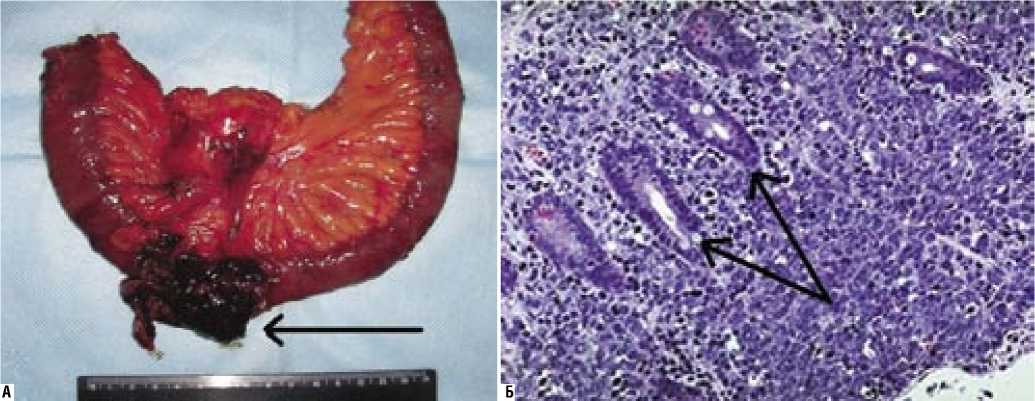
Рис. 4. Лимфома тонкой кишки: А – резецированная тонкая кишка с опухолью (стрелкой показана опухоль); Б – морфологическая картина лимфомы тонкой кишки (окраска гематоксилином и эозином, ув. х 200). Стрелками обозначены зоны нодулярного склероза лимфоидной ткани
Выявление опухолей тонкой кишки нередко происходит случайно, во время оперативного вмешательства, проводимого по поводу какого-либо развившегося осложнения (кишечной непроходимости, инвагинации, заворота кишки, кишечного кровотечения, перитонита на фоне перфорации опухоли). К моменту диагностики злокачественных опухолей тонкой кишки у 36% больных уже имеются метастазы. Основные пути метастазирования опухолей тонкой кишки – гематогенный в печень (89%) и имплантационный (52,4%) с частым поражением большого сальника (32,7%) [1, 7].
Специфических лабораторных изменений в клинических анализах крови и мочи не обнаруживается. При наличии карциноида в моче выявляется повышенный уровень метаболита серотонина – 5-гидроксииндолуксус-ной кислоты. Для аденокарциномы характерно повышение онкологических маркеров крови СА 19-9 и ракового эмбрионального антигена (РЭА). При метастатическом поражении печени повышается карциноэмбриональный антиген - а-фетопротеин. В диагностике гастроинтестинальных стромальных опухолей существенную роль играет наличие специфического маркера KIT-тирозин-киназы СД 117. Для лимфом характерен лейкоцитоз, лимфоцитоз в периферической крови часто с наличием периферического лимфаденита.
Ко всем пациентам, поступившим с клиникой острой или хронической тонкокишечной непроходимости или рецидивирующих кишечных кровотечений, широко применялись рентгенологические методы диагностики: обзорная рентгенография органов брюшной полости, контрастная энтерография с рентгенологическим контролем прохождения бариевой взвеси по кишечнику. У пяти пациентов наличие на обзорной рентгенограмме чаш Клойбера, арок перерастянутых петель тонкой кишки, поперечной гаустрации Кейси позволило диагностировать тонкокишечную непроходимость.
Эндоскопическое исследование проводилось в объеме фиброгастроскопия и фиброколоноскопия с обязательным осмотром всей двенадцатиперстной кишки и 30 см проксимальной части тощей кишки с помощью фиброгастродуоденоскопа, заведенного за связку Трейт-ца, и около 30 см дистального отрезка подвздошной кишки с применением фиброколоноскопа, проведенного за илеоцекальный клапан. Эта методика позволила в трех случаях диагностировать: гемангиому проксимальной части тощей кишки в 10 см от связки Трейтца, лейомиому на расстоянии 8 и 16 см от илеоцекального клапана в дистальном отделе подвздошной кишки.
У пяти пациентов использована возможность прямой визуализации эндоскопической диагностики с помощью «видеокапсулы», которая, проходя по пищеварительному тракту, выполняет фотосъемку (рис. 5 А) с передачей информации на специальное электронное воспринимающее устройство (рис. 5 Б).
Существенным недостатком этого метода является невозможность получения материала для морфологического исследования и недостаточное качество получаемого изображения при наличии непроходимости кишечника.
У троих больных диагноз злокачественной опухоли тонкой кишки был установлен с использованием современной «двухбаллонной тотальной интестиноскопии», позволяющей осмотреть тонкую кишку на всем протяжении и получить биопсийный материал для гистологической верификации и иммунофенотипирования. Кроме этого, у одного пациента с диагностиорованной саркомой тощей кишки, осложненной внутрикишечным кровотечением, выполнен эндоскопический гемостаз раствором «Капрофер».
Скрининговый метод УЗИ органов брюшной полости в 9 случаях помог определить наличие инфильтрата и опухолевидного образования в брюшной полости при
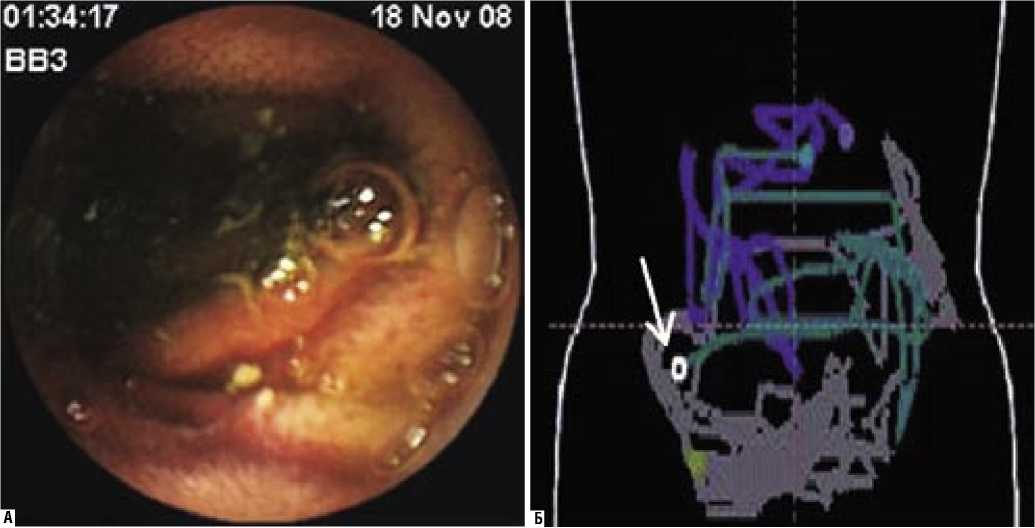
Рис. 5. Эндоскопическая диагностика с помощью «видеокапсулы»: А – эндоскопическое изображение опухоли (липомы) подвздошной кишки с помощью «видеокапсулы»; Б – отображение уровня расположения опухоли (липомы) в подвздошной кишке на электронном воспринимающем устройстве
размерах опухоли более 5–6 см. Однако точную локализацию опухоли тонкой кишки методика ультразвуковой диагностики не дает. УЗИ может быть информативным в оценке размеров опухоли, диагностике поражения регионарных лимфатических узлов или метастатического поражения печени, наличия асцита.
Более перспективным методом комплексной диагностики интрамуральной и лимфогенной распространенности опухолевого процесса, локализованного в проксимальных отделах тощей кишки, примененным к двоим нашим больным с лимфомами, оказалось эндоскопическое ультразвуковое исследование. С помощью ультразвукового датчика на дуоденоскопе определяются глубина опухолевой инвазии, границы опухоли, наличие метастатически измененных лимфатических узлов брыжейки, имеется возможность прицельного контролируемого получения пункционного биопсийного материала в целях морфологической верификации. У одного пациента лимфома тощей кишки диагностирована в 60 см от связки Трейтца во время оперативного вмешательства.
У 10 пациентов с опухолями (5 – доброкачественными, 5 – злокачественными) тонкой кишки диагноз был подтвержден на спиральной компьютерной томографии с применением методики «двойного» контрастирования (прием пероральных водорастворимых контрастных препаратов с одновременным болюсным контрастированием висцеральных сосудов чревной группы) в сочетании с возможностью построения трехмерного изображения (рис. 6). Метод оказался высокочувствителен (до 96%) и специфичен (до 87%), особенно в группе небольших (от 2 до 4 см) доброкачественных опухолей тонкой кишки (гемангиома, лейомиома, фиброма, липома). Данная методика позволяет избежать выполнения более инвазивного метода – ангиографии.
У двух пациентов с рецидивирующими кишечными кровотечениями диагностированы лейомиома и кавернозная гемангиома тощей кишки во время выполнения диагностической лапароскопии. Видеолапароскопия должна шире применяться в диагностической программе поиска источника желудочно-кишечного кровотечения при отсутствии конкретной информации при выполнении фиброгастроскопии, фиброколоноскопии, УЗИ и КТ органов брюшной полости. Диагностическая лапароскопия позволяет выполнить прицельную биопсию патологического образования с последующей гистологической верификацией. Перспективным направлением на современном этапе в хирургическом лечении опухолей тонкой кишки является переход лапароскопии от диагностической к лечебной.
Основные принципы хирургического лечения опухолей тонкой кишки
Доброкачественные опухоли тонкой кишки успешно лечатся хирургическим путем. При небольших доброкачественных опухолях менее 5 см в диаметре, расположенных на противобрыжеечном крае кишки, занимающих не более % окружности тонкой кишки и не нарушающих кровоснабжение сегмента тонкой кишки при их энуклеации, в 7 случаях применена экономная резекция опухолей
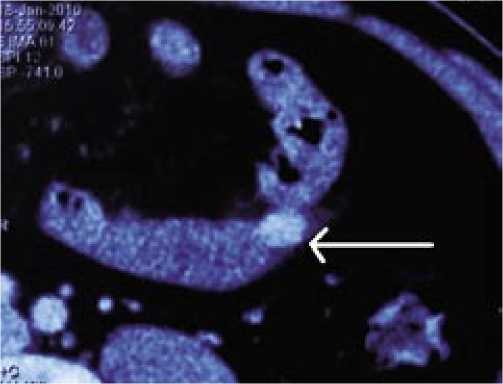
Рис. 6. Компьютерная томография органов брюшной полости больного Д. Стрелкой обозначена опухоль тонкой кишки (лейомиома) размером 2 x 3 см
отступлением от границы инфильтрации и распространения опухоли не менее 2 см (рис. 7 А, Б). Лишь в двух случаях при кавернозных гемангиомах тонкой кишки размерами более 5 и 8 см, стелящихся по стенке кишки и расположенных на брыжеечном ее крае с вовлечением в патологический процесс сосудов, питающих данный сегмент кишечной стенки, была выполнена резекция участка тощей кишки с опухолью с наложением тонкокишечного анастомоза «конец в конец».
Считаем принципиальным и обязательным условием при выполнении вышеуказанных объемов оперативных вмешательств выполнение интраоперационной экспресс-биопсии удаляемой опухоли. В случае подозрения или подтверждения злокачественного морфологического заключения объем оперативного пособия должен быть расширен (отступ от границ опухоли до 15 см в проксимальном и дистальном направлении тонкой кишки с удалением регионарного лимфатического коллектора и большого сальника).
При всех злокачественных опухолях нами выполнено 9 расширенных резекций пораженных участков тонкой кишки с наложением тонкокишечных анастомозов «бок в бок» в виду различных диаметров приводящих и отводящих концов анастомозируемых участков тощей кишки вследствие перерастяжения приводящих отделов кишечника на фоне тонкокишечной непроходимости. В 7 случаях потребовалась назоинтестинальная интубация и декомпрессия тонкой кишки зондом Миллера-Эббота. При нерезектабельной лимфосаркоме тонкой кишки у одного пациента выполнена паллиативная симптоматическая операция – наложение обходного тонкокишечного анастомоза «бок в бок», направленное на ликвидацию тонкокишечной непроходимости.
Всем пациентам, оперированным по поводу злокачественных образований тонкой кишки, в ближайшем послеоперационном периоде применяли различные режимы химиотерапии: при аденокарциномах – 5-фторурацил с цисплатином, при эпителиальных опухолях кишечника (лимфомах) – цикубсимаб в сочетании с авастином, при стромальных опухолях (карциноид) – иматиниб, гливек, соматостатин.
Послеоперационные осложнения отмечены у 5 пациентов (26,4%): у двоих – нагноение послеоперационной раны, у одного – пневмония, у двоих – явления тромбофлебита. Летальных исходов в ближайшем послеоперационном периоде не было.
Отдаленные результаты прослежены у всех больных в срок от одного до трех лет. Все больные в группе доброкачественных образований тонкой кишки после операции чувствуют себя хорошо, летальных исходов не отмечено. В группе злокачественных образований тонкой кишки после операции в течение 1 года у 30% пациентов произошла генерализация ракового процесса, что явилось причиной летального исхода троих больных.
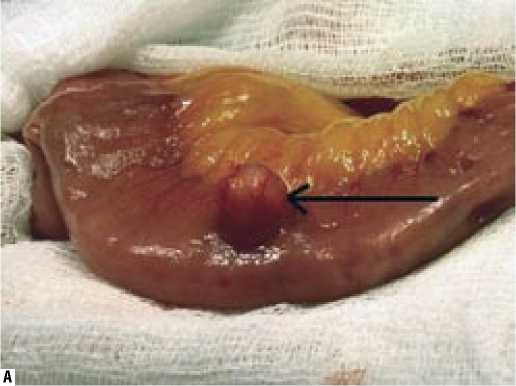
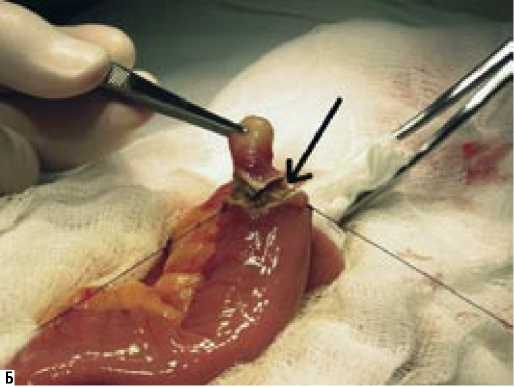
Рис. 7. Участок тонкой кишки с опухолью (стрелкой показана опухоль): А – лейомиома противобрыжеечного края тонкой кишки; Б – экономная краевая резекция участка тощей кишки с лейомиомой

Частичная регрессия опухоли была зафиксирована у 50% (n=5) пациентов, у 20% (n=2) больных отмечена стабилизация онкологического процесса на фоне проведения адъювантной химиотерапии. Клиническое улучшение после проведения хирургического лечения было зарегистрировано у 89% больных.
Заключение
Таким образом, своевременная диагностика опухолей тонкой кишки затруднена из-за отсутствия характерных клинических проявлений, что нередко приводит к ошибкам в интерпретации результатов обследований. Наиболее достоверным и малоинвазивным диагностическим методом выявления опухолей тонкой кишки является спиральная компьютерная томография с болюсным контрастированием. Лапароскопическая ревизия брюшной полости позволяет верифицировать диагностику опухоли тонкой кишки, а в отдельных ситуациях выполнить радикальную операцию. Единственным методом лечения опухолей тонкой кишки остается хирургический. В адьювантной химиотерапии злокачественных опухолей тонкой кишки необходимо шире применить препараты «таргентной» терапии. Прогностическими факторами в лечении пациентов с опухолями тонкой кишки являются: резектабельность опухоли, степень ее дифференцировки, вовлечение серозного покрова кишки в патологический процесс, наличие или отсутствие отдаленных метастазов. Пятилетняя выживаемость при раке тощей и подвздошной кишки достигает 15–20%, при стромальных опухолях – до 35% [3].
Список литературы Диагностика и хирургическое лечение опухолей тонкой кишки
- Горбунова В.А., Орел Н.Ф., Егоров Г.Н. Редкие опухоли APUD-системы (карциноиды) и нейроэндокринные опухоли поджелудочной железы: клиника, диагностика, лечение. М.: Литтерра, 2007. -С. 32.
- Карагюлян С.Р., Данишян К.И., Гржимоловский А.В. Хирургимческое лечение больного с комбинированным опухолевым поражением тонкой кишки//Проблемы гематологии. 2002. -№ 2. -С. 49-52.
- Куликов В.В., Гржимоловский А.В. Опухоли тонкой кишки//Хирургия. 2008. -№ 5. -С. 65-69.
- Янкин А.В. Нейроэндокринные опухоли желудочно-кишечного тракта.//Практическая онкология. 2005. № 4. -С. 6-14.
- Buchman A.L., Wallin A. Videocapsule endoscopy renders obscure gastrointestinal bleeding no longer obscure. Clin. gastroenterd. 2003. -№37. P. 303-306.
- Lev D., Kariv L., Merhav H. Gastrointestinal stromal sarcomas//Br. L. Surg 1999 № 86. -Р. 545-549.
- Modlin M., Shapiro M. Carcinoid tumors and fibrosis: a relation with litle expeanation//Am. L. gastroenterol. 2004. -№ 99. -Р. 1-13.


