Диагностика и лечение фебрильной нейтропении
Автор: Сакаева Д.Д., Борисов К.Е., Булавина И.С., Когония Л.М., Курмуков И.А., Орлова Р.В., Шабаева М.М.
Журнал: Злокачественные опухоли @malignanttumors
Рубрика: Практические рекомендации
Статья в выпуске: 3S2-2 т.13, 2023 года.
Бесплатный доступ
Поддерживающая терапия, противоопухолевая терапия, нежелательное явление, фебрильная нейтропения, антибиотикотерапия, колониестимулирующие факторы
Короткий адрес: https://sciup.org/140302433
IDR: 140302433 | DOI: 10.18027/2224-5057-2023-13-3s2-2-60-68
Текст статьи Диагностика и лечение фебрильной нейтропении
Фебрильная нейтропения (ФН) — неотложное состояние, опасное нежелательное явление противоопухолевой терапии, ведущее к увеличению общей летальности и возрастанию расходов на лечение онкологических больных. При современном лекарственном противоопухолевом лечении развитие ФН прогнозируется у 7,9–11,7% пациентов с атрибутивной летальностью до 11%.
ФН диагностируется в том случае, когда у пациента с нейтропенией развивается фебрильная лихорадка (D70 по МКБ-10). Под нейтропенией понимают уровень нейтрофилов периферической крови≤500 клеток в мкл, либо≤1000 клеток в мкл, если в течение следующих 2 суток вероятно их снижение до≤500 клеток в мкл. В исключительных случаях недоступности определения лейкоцитарной формулы ориентиром может служить количество лейкоцитов≤1000 клеток в мкл.
Фебрильная лихорадка подразумевает хотя бы однократное повышение температуры тела, эквивалентное≥38,3°C при измерении во рту или прямой кишке (соответству-ет≥38,1°C при измерении в подмышечной впадине), либо повышение температуры тела, эквивалентное≥38,0°C при измерении во рту или прямой кишке (соответствует≥37,8°C при измерении в подмышечной впадине), сохраняющееся в течение≥1 часа.
В 90% случаев основной причиной ФН у пациентов с солидными опухолями является бактериальная инфекция. Эмпирическая терапия всегда должна быть направлена на элиминацию бактериальной инфекции.
1. ДИАГНОСТИКА И ОЦЕНКА РИСКОВ НЕБЛАГОПРИЯТНОГО РАЗВИТИЯ ФН
Обязательное обследование при ФН, направленное на оценку тяжести состояния и определение причин лихорадки, включает:
-
• опрос, осмотр и полное физикальное обследование пациента;
-
• общеклинический анализ крови с определением лейкоцитарной формулы;
-
• биохимическое исследование крови с определением глюкозы, креатинина, АЛТ, альбумина, натрия и калия;
-
• бактериологическое исследование крови из периферической вены (исследование подразумевает одновременное использование 2 сред обогащения — аэробной и анаэробной). Если во время развития ФН у пациента уже имеется сосудистый доступ, кровь на стерильность берется и через него (если сосудистый доступ многопросветный, то через каждый отдельный просвет), одновременно с кровью из периферической вены и аналогичным образом.
Необходимость и объем дополнительных исследований определяется врачом в соответствии с данными анамнеза, выявляемыми симптомами, доступностью отдельных методов исследования. При наличии лабораторных возможностей, особенно в период сезонного роста заболеваемости ОРВИ, целесообразно исследование мазков из носо- и ротоглотки на вирусные антигены наиболее частых возбудителей (как правило, методом флюоресцирующих антител). В соответствии с действующими локальными или временными правилами обязательной может быть проверка и на иные инфекции: во время работы над настоящими рекомендациями, например, это исследование мазков из носо- и ротоглотки на наличие вирусной РНК SARS-CoV-2 (методом ПЦР).
При тяжелом общем состоянии пациента показана экстренная госпитализация и дальнейшее лечение в условиях круглосуточного стационара. В остальных случаях оценивается наличие факторов риска неблагоприятного развития ФН. С этой целью используются два прогностических индекса, MASCC и CISNE, позволяющие ранжировать пациентов в группы различного риска. Тяжелое течение заболевания предполагается при индексе риска MASCC<21 или CISNE≥3 (табл. 1,2).
Таблица 1. Шкала MASCC-score и интерпретация результата.
|
Показатель и критерий его оценки |
Балл |
|
Общая выраженность симптомов ФН (сепсиса): нет или легкие/умеренные/тяжелые |
5/3/0 |
|
АД сист. > 90 мм рт ст: да/нет |
5/0 |
|
Без ХОБЛ: да/нет |
4/0 |
|
Без инвазивного микоза в анамнезе: да/нет |
4/0 |
|
Без дегидратации: да/нет |
3/0 |
|
Лихорадка появилась не во время госпитализации: да/нет |
3/0 |
|
Возраст младше 60 лет: да/нет |
2/0 |
|
Интерпретация результата |
Сумма баллов |
|
Низкий риск (дополнительные тяжелые осложнения 8–12%, 28-дневная летальность 1%; в отдельных случаях возможно амбулаторное лечение) |
≥ 21 |
|
Высокий риск (подразумевает госпитализацию) |
16–20 |
|
Крайне высокий риск (подразумевает лечение в ОРИТ) |
≤ 15 |
Таблица 2. Шкала CISNE-score и интерпретация результата.
|
ECOG-PS ≥ 2 |
2 |
|
Стресс-индуцированная гипергликемия |
2 |
|
Хроническое обструктивное заболевание легких |
1 |
|
Хроническое кардиоваскулярное заболевание |
1 |
|
Мукозит ≥ 2 степени по CTCAE |
1 |
|
Моноциты < 200 клеток в мкл |
1 |
|
Интерпретация результата (вероятность смерти) |
Сумма баллов |
|
Низкий риск (28-дневная летальность 1%; в отдельных случаях возможно амбулаторное лечение) |
0 |
|
Высокий риск (подразумевает госпитализацию) |
1–2 |
|
Крайне высокий риск (28-дневная летальность ≥ 13%; подразумевает лечение в ОРИТ) |
3–8 |
Другими важными неблагоприятными прогностическими факторами являются:
• длительность ФН до начала антибиотикотерапии более 1 суток;
• предполагаемая продолжительность нейтропении более 7 дней;
• выявление очага инфекции и соответствующая ему клиническая картина (высокая вероятность сепсиса);
• острое нарушение или декомпенсация функции жизненно-важных органов (высокая вероятность дальнейшего прогрессирования нарушений).
2. ЭМПИРИЧЕСКАЯ АНТИБИОТИКОТЕРАПИЯ2.1. Антибиотики, прием внутрь
Наличие любого из перечисленных факторов является показанием к лечению пациента в условиях круглосуточного стационара, а клиническая нестабильность и острое нарушение или декомпенсация функции жизненно-важных органов — к госпитализации в отделение с расширенными возможностями круглосуточного наблюдения и прикроватного мониторинга (палата интенсивной терапии, отделение реанимации и интенсивной терапии).
Если риск (по шкалам MASSC и CISNE) оценивается как низкий, а другие факторы тяжелого течения или неблагоприятного исхода ФН отсутствуют, дальнейшее лечение может быть организовано в рамках как стационарной, так и амбулаторно-поликлинической помощи. Амбулаторное лечение возможно при условии хорошего контакта с пациентом, постоянного контроля за его состоянием и возможности обеспечения ухода со стороны близких, при необходимости — немедленной связи (для дополнительной консультации врачом и коррекции лечения) и быстрой транспортировки в клинику. Лучший контроль (в том числе лабораторный) обеспечивает лечение в условиях стационара на дому (медицинский патронаж) или дневного стационара. При сомнениях в качестве ухода на дому или иных проблемах, снижающих безопасность, пациенту следует предлагать лечение в условиях круглосуточного стационара.
Антибиотикотерапия является основным методом лечения ФН; раннее начало, достаточная доза и кратность введения антибиотиков позволяют уменьшить период лихорадки, снизить тяжесть проявлений (в том числе обусловленных инфекцией органных повреждений) и атрибутивную летальность, увеличивают вероятность своевременного продолжения противоопухолевого лечения.
Эмпирическая антибиотикотерапия должна быть инициирована как можно раньше, обычно сразу после забора крови на бактериологическое исследование. При первом введении антибиотик широкого спектра действия в достаточной дозе (рекомендуется использовать высшую разовую дозу препарата) вводится внутривенно.
Могут назначаться пациентам, способным принимать препараты внутрь, получающим лечение амбулаторно и не получавшим фторхинолоны в последние 6 недель, например: • моксифлоксацин (по 0,4 г один раз в день);
-
• левофлоксацин (по 0,5 г каждые 12 часов или по 0,75 г один раз в день) и амоксицил-лин/клавуланат (по 0, 875/0,175 г каждые 8 часов или 1,0/0,25 г каждые 12 часов);
-
• ципрофлоксацин (по 0,75 г каждые 12 часов) и амоксициллин/клавуланат (по 0,875/0,175 г каждые 8 часов или 1,0/0,25 г каждые 12 часов);
-
• ципрофлоксацин (по 0,75 г каждые 12 часов) и клиндамицин (по 0,3 г каждые 8 часов).
-
2.2. Антибиотики, парентеральное введение
В отсутствии индивидуальных противопоказаний (например, аллергии) или применения пациентом аналогичного антибактериального средства в последние 6 недель, рекомендуется назначение бета-лактамных антибиотиков широкого спектра действия с высокой активностью в отношении псевдомонад, как правило, в режиме монотерапии, например: • цефепим (по 2,0 г каждые 8 часов, внутривенно);
-
• имипенем/ циластатин (по 0,5 г каждые 6 часов, внутривенно);
-
• меропенем (по 1,0 г каждые 8 часов, внутривенно);
-
• пиперациллин/тазобактам (по 4,5 г каждые 6 часов, внутривенно).
-
2.3. Особые варианты антибиотикотерапии —ФН с выявляемым очагом инфекции
При аллергии на бета-лактамные антибиотики могут использоваться комбинированные схемы, например, азтреонам (по 2,0 г каждые 8 часов, внутривенно) и ванкомицин (по 1,0 г каждые 12 часов, внутривенно).
При выявлении очага инфекции предпочтительно проведение комбинированной антибиотикотерапии: бета-лактамный антибиотик широкого спектра действия с высокой активностью в отношении псевдомонад+антибиотик с активностью в отношении возбудителей, характерных для соответствующего очага:
• при катетер-ассоциированной инфекции — ванкомицин;
• при инфекции кожи, мягких тканей и пневмонии — линезолид;
• при мукозите и энтероколите — амикацин (15–20 мг/кг/сутки внутривенно) и/или метронидазол (по 0,5 г каждые 6 часов внутривенно).
3. КОНТРОЛЬ ЭФФЕКТИВНОСТИ ЛЕЧЕНИЯ
4. ПРИМЕНЕНИЕ Г-КСФ ДЛЯ ПРОФИЛАКТИКИИ ЛЕЧЕНИЯ ФН
Подробный анализ рациональной антибиотикотерапии иных очаговых проявлений бактериальной инфекции выходит за рамки настоящих рекомендаций; в таких случаях эмпирический выбор препаратов и режима их дозирования должен основываться на конкретной клинической ситуации, данных локальных эпидемических исследований и, как правило, является предметом междисциплинарного обсуждения.
Эффективность эмпирической антибиотикотерапии при ФН определяется контролем фебрильной лихорадки. В большинстве случаев раннего назначения антибиотиков широкого спектра действия и отсутствия очага персистирующей инфекции (например, инфицированного венозного доступа, очаговой пневмонии, абсцесса) контроль над лихорадкой достигается в первые 24 часа, а полный контроль — в первые 48 часов лечения.
При полном контроле лихорадки показанием к прекращению антибиотикотерапии является отсутствие признаков инфекции и уровень нейтрофилов периферической крови выше 1000 клеток в мкл. Необходимо помнить, что выявление некоторых возбудителей требует длительного применения антибиотиков даже при полном восстановлении уровня нейтрофилов (например, 3–4 недели при инфекции кровотока, вызванной Staphylococus aureus); подробную информацию можно найти в соответствующих руководствах.
Если лихорадка сохраняется дольше 72 часов на фоне эмпирической антибиотико-терапии, требуется повторное обследование, в том числе бактериологическое. Необходимо повторно оценить возможное наличие очага инфекции (в том числе и любого имплантированного пациенту устройства), рассмотреть клиническую целесообразность использования методов визуализации (например, ЭхоКГ для исследования клапанов сердца, КТ грудной клетки или органов брюшной полости и т. д.). Амбулаторным пациентам рекомендуется госпитализация в круглосуточный стационар; если пациент первоначально получал лечение антибиотиками для приема внутрь, их следует отменить и назначить один из вариантов эмпирической внутривенной антибиотикотерапии. Если к этому времени получен положительный результат первичного бактериологического исследования крови, следует провести коррекцию антибиотикотерапии в соответствии с чувствительностью выявленного возбудителя (антибиотикограммы). В отсутствие положительного результата бактериологического исследования крови полезный ориентир может дать исследование биохимических маркеров бактериальной (прокальцитонин) и грибковой (галактоманнан) инфекций. Если общее состояние не ухудшается до анализа результатов повторного обследования, то необходимости в эскалации эмпирической антибиотикотерапии, как правило, нет. При ухудшении общего состояния, прогресси- ровании органных нарушений — вариант интенсификации лечения следует выбрать по результатам междисциплинарного обсуждения с привлечением специалистов, имеющих более глубокие знания и клинический опыт в области интенсивной терапии и госпитальной инфекции.
Применение препаратов Г-КСФ, уменьшающее продолжительность нейтропении и/или ее глубину, может оказаться полезным методом профилактики или, в отдельных случаях, лечения ФН. Общими правилами являются:
-
• Г-КСФ назначается не ранее, чем через 24 часа по окончании химиотерапии, а прекращается не позднее, чем за 48 часов до начала следующего курса;
-
• введение Г-КСФ продолжается ежедневно до достижения желаемого уровня нейтрофилов периферической крови (как правило, не выше 10000 кл в мкл);
-
• Г-КСФ не применяются для лечения афебрильной нейтропении, при осложнениях и инфекциях, не связанных с нейтропенией (например, внутрибольничная пневмония), а также не назначаются при отсутствии факторов высокого риска развития ФН.
-
4.1. Первичная профилактика ФН
Первичная профилактика целесообразна либо при высоком прогнозируемом риске ФН, либо при существенных негативных последствиях ФН:
-
• при нозологиях и режимах противоопухолевого лечения с высоким риском развития ФН (табл. 3);
-
• истощении (малом резерве) костного мозга, в том числе у пациентов старше 65 лет, или вследствие повторных курсов противоопухолевого лечения;
-
• для обеспечения оптимальной интенсивности лечения в тех случаях, когда редукция доз цитостатиков может негативно влиять на выживаемость.
-
4.2. Вторичная профилактика ФН
-
4.3. Применение колониестимулирующих факторов для лечения фебрильной нейтропении
Пациентам, ранее пережившим ФН, при последующем противоопухолевом лечении профилактическое введение Г-КСФ целесообразно при более чем 10% вероятности повторного эпизода (табл. 4), в том числе, когда по соображениям противоопухолевой эффективности, изменение протокола лечения и редукция доз противоопухолевых препаратов нежелательны. Профилактика Г-КСФ может быть применена при ХЛТ. В настоящее время в клинической практике используются Г-КСФ короткого и пролонгированного действия (табл. 5).
Таблица 3. Нозологии и режимы химиотерапии c высоким (>20%) риском развития ФН.
В общей популяции пациентов с ФН использование Г-КСФ статистически значимо снижает длительность нейтропении на 1–2 дня, не сокращает продолжительность лихорадки и длительность АБ терапии в случае развития ФН и не снижает стоимости лечения одного эпизода ФН.
Однако Г-КСФ могут принести пользу отдельным пациентам, при лечении которых длительность и глубина нейтропении могут иметь решающее значение, в частности при сочетании глубокой нейтропении и выраженных симптомов инфекции, сохраняющихся на фоне активной многокомпонентной антибиотикотерапии.
Таблица 5. Рекомендуемые гранулоцитарные колониестимулирующие факторы.
|
МНН |
Фармакологические свойства |
Форма выпуска |
Режим дозирования и введения |
|
Пролонгированные формы |
|||
|
Эмпэгфилграстим |
Ковалентный коньюгат филграстима с одной молекулой полиэтиленгликоля, пролонгированного действия |
Раствор для п/к введения |
7,5 мг (без учета массы тела) п/к однократно не менее чем через 24 часа после окончания введения химиопрепаратов |
|
Липэгфилграстим |
Гликопегилированный Г-КСФ пролонгированного действия |
Раствор для п/к введения |
6 мг (без учета массы тела) п/к однократно через 24 ч после каждого цикла ХТ |
|
Пэгфилграстим |
Рекомбинантный пегилиро-ванный Г-КСФ (филграстим), конъюгированный с полиэтиленгликолем, пролонгированного действия |
Раствор для п/к введения |
6 мг (без учета массы тела) однократно п/к не ранее чем через 24 часа и не позднее 14 суток после курса ХТ |
|
Обычные формы |
|||
|
Филграстим |
Рекомбинантный человеческий негликолизированный Г-КСФ |
Раствор для п/к и в/в вве дения |
5 мкг/кг массы тела 1 раз/сутки п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до необходимого стабильного АЧН |
|
Ленограстим |
Рекомбинантный человеческий гликолизированный Г-КСФ |
Лиофилизированное сухое вещество для п/к и в/в инъекций во флаконах в комплекте с растворителем |
19,2 млн. МЕ (или 150 мкг) на м² поверхности тела (0,64 млн. МЕ или 5 мкг на кг массы тела) в день п/к или в/в ежедневно через 24–72 часа после последнего дня ХТ до необходимого стабильного АЧН |
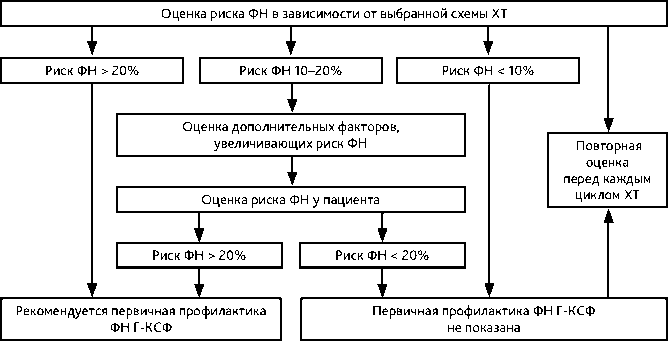
Рисунок 1. Алгоритм для назначения первичной профилактики ФН.
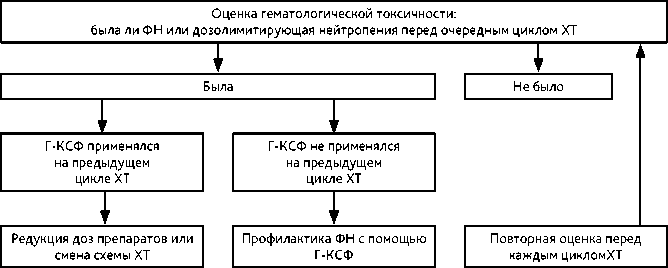
Рисунок 2. Алгоритм принятия решения перед вторым и последующими циклами ХТ.
С целью поддержания дозовой интенсивности терапии, а также профилактики развития фебрильной нейтропении после завершения цитостатической терапии возможно применение Г-КСФ, наиболее распространенным представителем которого является филграстим. Доза и продолжительность терапии филграстимом индивидуальны и определяются его клинической эффективностью, оцениваемой по динамике уровня нейтрофилов. Вместо дозы 5 мкг/кг допустимо применение филграстима в фиксированных суточных дозах 300 мкг или 480 мкг. Возможно досрочное прекращение терапии филграстимом в ситуациях, когда после первоначального падения уровня нейтрофилов отмечается их рост до≥10× 10 9 /л либо, если их снижение после ХТ не наблюдалось, при достижении уровня нейтрофилов≥40–50×10 9 /л.


