Диагностика и лечение рефлюкс-ассоциированных воспалительных заболеваний пищевода и их осложненний
Автор: Ивануса С.Я., Кочетков А.В., Хохлов А.В., Повзун Са, Кобиашвили М.Г., Бояринов Дмитрий Юрьевич, Белевич В.Л., Шушакова О.В., Самусенко И.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.10, 2015 года.
Бесплатный доступ
Представлен опыт лечения пациентов с рефлюкс-ассоциированными воспалительными заболеваниями пищевода и их осложнений.
Рефлюкс-эзофагит, пищевод барретта, пептические стриктуры пищевода, эрозивно-язвенные кровотечения пищевода
Короткий адрес: https://sciup.org/140188394
IDR: 140188394 | УДК: 616.329-009.81-002-06-07-08
Diagnosis and treatment of reflux associated inflammatory diseases of the esophagus and their complications
Experience in treatment of patients with reflux-associated inflammatory diseases of the esophagus and its complications.
Текст научной статьи Диагностика и лечение рефлюкс-ассоциированных воспалительных заболеваний пищевода и их осложненний
Значительное увеличение больных пептическим эзофагитом за последние два десятилетия особенно среди лиц трудоспособного возраста определяет актуальность проводимых исследований [10]. Выявляемость эзофагита у больных с симптомами ГЭРБ составляет 45–80%. Пациенты с ГЭРБ оценивают свое качество жизни хуже, чем больные с ИБС [3, 4]. Широкая распространенность рефлюкс-эзофагита и бесконтрольный прием препаратов приводят к частому развитию осложнений (эрозивно-язвенные кровотечения из пищевода, пептические стриктуры пищевода, пищевод Барретта), частота которых составляет 10–15% [8, 11]. Увеличение за последнее время удельного веса аденокарциномы среди других форм рака пищевода, встречаемость которой в США выросла с 10 до 30 % за последние годы, многие исследователи связывают с ростом количества больных пищеводом Барретта [5]. Ежегодный прирост частоты аденокарциномы пищевода в Европе составляет 4–10% [6].
Развитие и внедрение в клиническую практику новых малоинвазивных методов диагностики и лечения больных с пептическим эзофагитом и его осложненными формами заставляет пересматривать тактику лечения и динамического наблюдения за такими больными.
Внедрение лапароскопических операций для коррекции замыкательной функции кардии привело к увеличению количества оперированных больных не по показаниям, что также сказалось на увеличении неудовлетворительных результатов [7]. До сих пор нет единого мнения, является ли операция методом выбора лечения рефлюкс-ассоциированных воспалительных заболеваний пищевода и их осложнений.
За последние 15 лет в клинике общей хирургии ВМедА и во ВЦЭРМ им. А.М. Никифорова обследовались и лечились 200 больных с рефлюкс-ассоциирован-ными воспалительными заболеваниями пищевода и их осложнений. Преобладали пациенты работоспособного возраста (61,5%), средний возраст – 52,2 года. Неосложненное течение болезни установлено у 48,5%, пищевод Барретта – 20,5%, эрозивно-язвенные кровотечения из пищевода – 19%, пептические стриктуры пищевода – 9% больных.
При обследовании больных на всех этапах использованы современные методы диагностики, включая: суточную рН-метрию, реогастрографию, эндоскопическое исследование с применением осмотра в NBI режиме, режиме i-scan, zoom-эндоскопию, гистологическое и иммуногистохимическое исследование биоптатов слизистой (рис. 1). По разработанному алгоритму обследованы 133 (66,5%) больных, остальные 67 оценены ретроспективно.
Пищевод Барретта диагностирован у 41 пациента. Длинный сегмент более 3 см определен в 15 (36,6%) случаях. У остальных больных диагностирован короткий сегмент. По результатам гистологического исследования у 15 (36,6%) больных выявлен желудочный тип метаплазии, у 23 (56%) – кишечный (рис. 2, 3, 4), у 3 (7,3%) – дисплазия тяжелой степени. Тактика лечения пациентов с пищеводом Барретта зависела от результатов обследования и прежде всего данных гистологического исследования.
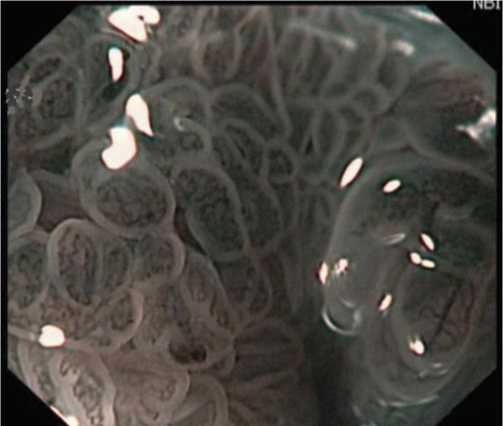
Рис. 3. Пищевод Барретта. Кишечная метаплазия. Цифровая эндоскопия с увеличением в NBI-режиме

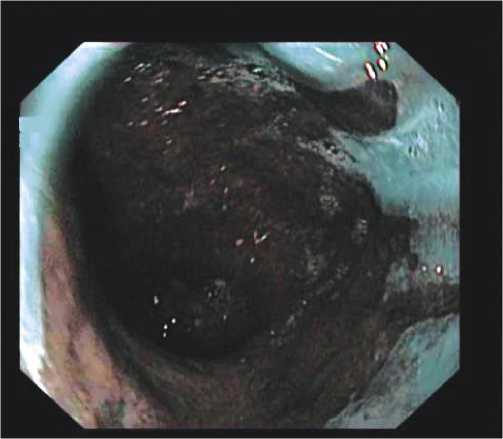
Рис. 1. Гистологическое и иммуногистохимическое исследование биоптатов слизистой
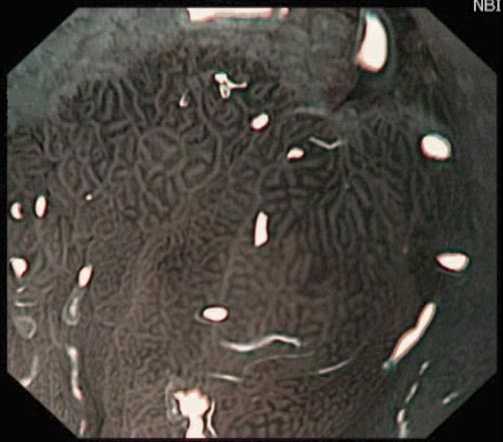
Рис. 2. Пищевод Барретта. Кишечная метаплазия. Цифровая эндоскопия в NBI-режиме
При желудочной метаплазии эндоскопического удаления очагов метаплазии не предпринималось. Оперативное вмешательство выполнено всем пациентам с целью устранения гастроэзофагеального рефлюкса. Из 23 пациентов с кишечной метаплазией в 20 случаях была выполнена аргоноплазменная коагуляция очагов метаплазии слизистой оболочки пищевода с контролем и гистологическим подтверждением восстановления многослойного плоского эпителия пищевода при эзофагоскопии через месяц после операции (рис. 5, 6, 7). В последующем все эти больные были оперированы лапароскопически с целью устранения патологического желудочно-пищеводного рефлюкса. В 3-х наблюдениях
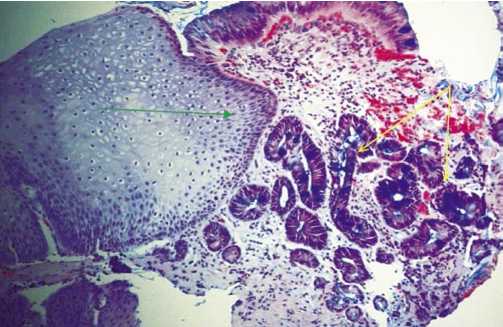
Рис. 4. Биоптат слизистой пищевода. Окраскаальциановым синим. Ув х 100 раз. В препарате на фоне многослойного плоского эпителия пищевода (указан зеленой стрелкой) определяются кишечные крипты с бокаловидными клетками (указаны желтыми стрелками)
при кишечной метаплазии пациенты от оперативного вмешательства отказались на фоне эффективной консервативной терапии, при наблюдении прогрессирования заболевания не выявлено.
В 3 случаях при дисплазии слизистой оболочки пищевода тяжелой степени выполнена резекции измененного участка слизистой максимально на площади до 3 см. После репарации нормальной слизистой оболочки через 1 месяц лапароскопически восстановлена замыкательная функция кардии с хорошим отдаленным результатом.
Эрозивно-язвенные пищеводные кровотечения наблюдались у 38 больных. В 20 случаях причиной развития изменений слизистой явился гастроэзофагеальный рефлюкс. Среди этих больных кровопотеря легкой степени отмечена у 9 (45%) больных, кровопотеря средней степени тяжести – у 4 (20%), тяжелая – у 7 (35%). У 18 пациентов

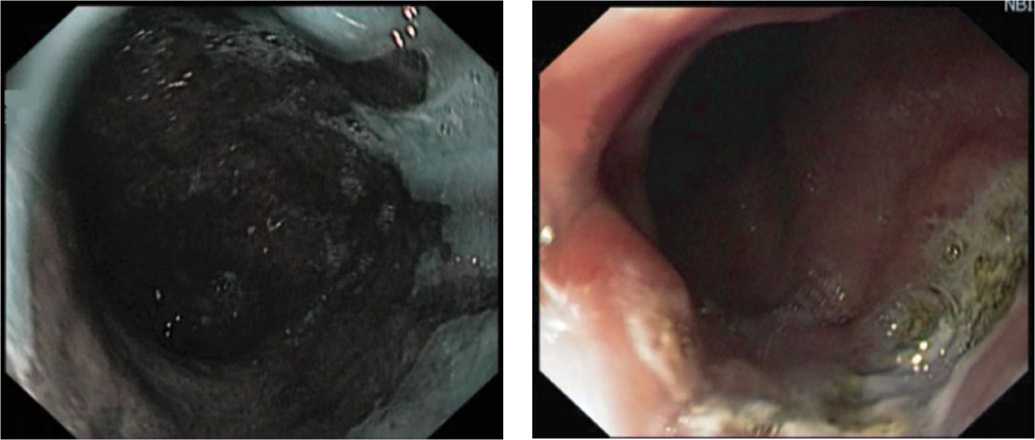
Рис. 5. Цифровая эндоскопия с осмотром в NBI режиме. Пищевод Барретта короткий сегмент. Гистологическое заключение биоптатов: кишечная метаплазия
Рис. 6. Тот же пациент. Выполнено 2 курса аргоно плазменной коагуляции очагов метаплазии
первопричиной явились ишемические изменения слизистой на фоне тяжелого течения основного общесоматического заболевания. По тяжести кровопотери больные распределились следующим образом: легкая степень – 4 (20 %); средняя – 8 (46,6%); тяжелая – 6 (33,4%). Применение эндоскопического гемостаза при эрозивно-язвенных пищеводных кровотечениях потребовалось в 22 (57%) случаях. В 16 (43%) наблюдениях эффективной оказалась консервативная терапия.
Пептические стриктуры диагностированы у 18 пациентов: у 10 – 1 степени, у 5 – 2 ст., у 3 – 3 ст. по классификации Э.А. Годжелло и Ю.И. Галлингера [2]. В 12 (67%) случаях они были признаны функционально незначимыми и не требовали эндоскопической коррекции, в 6 (33%) – показанием к эндоскопическому пособию явилось значимое сужение пищевода. У 2-х больных с протяженными стриктурами использован метод бужирования пищевода по струне-направителю с гибким наконечником, при коротких стриктурах в 4-х случаях – сочетание бужирования и баллонной дилатации. Рецидив развился у 3-х (50%), которые были оперированы в сроки от одного до двух месяцев после повторных курсов эндоскопического бужирования и стихания воспалительных изменений.
Для проведения дифференциальной диагностики недостаточности кардии функционального или органического генеза, а также оценки характера рефлюксата, 80 пациентам была выполнена суточная рН-метрия, которая в 33,3% случаях позволила выявить пациентов с гиперсекреторным типом секреции желудка. Это потребовало проведение длительной антисекреторной терапии. Выявление щелочного рефлюкса в 26,6% наблюдениях позволило заподозрить патологию панкреатобилиарной зоны. Выявление у больных с пищеводом Барретта щелочных или смешанных рефлюксов, считали прогностически
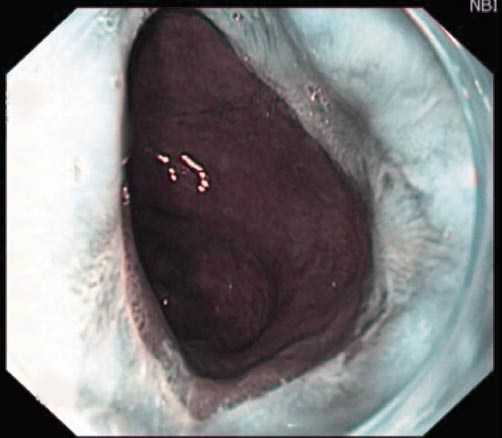
Рис. 7. Осмотр через 6 месяцев. Восстановление нормального сквамозного эпителия пищевода наиболее неблагоприятным фактором, что заставляло использовать более активную тактику лечения.
Недостаточность пищеводного клиренса была отмечена у 67 больных. Во всех случаях диагностировано осложненное течение пептического эзофагита.
По данным импедансометрии, выполненной у 80 пациентов, для неосложненного течения пептического эзофагита был характерен гиперкинетический или спастический тип перистальтики пищевода. Гипокинетический тип перистальтики или атония пищевода отмечены у пациентов с осложненным течением, при этом результаты импедансометрии коррелировали с данными суточной рН-метрии. Изучение моторики пищевода позволило не только
установить причину дисфагии, наблюдавшейся у трети больных, но и прогнозировать развитие ее в послеоперационном периоде. При выявлении гипокинетического типа моторики пищевода явления транзиторной дисфагии в послеоперационном периоде отмечены у всех пациентов.
С целью оценки тяжести течения эзофагита для выявления возможных различий гистологических изменений у больных с разным типом рефлюкса, а также для верификации вида метаплазии и степени дисплазии, подтверждения эффективности разработанного алгоритма лечения, проведено гистологическое исследование 93 биоптатов, взятых у 71 пациента. Использованы стандартные способы окраски и иммуногистохимические методы определения экспрессии Papillomavirus (types 6, 11, 18), HerpesSimplexVirusType 1 (HSVI) и HerpesSimplexVirusType 2 (HSVII), экспрессии Cytomegalovirus (CMV) CloneCCH2 andDDG9.
При изучении биоптатов 30 пациентов с эзофагитом постоянно выявлялся отек собственной пластинки и расширение лимфатических капилляров, что является фактором хронической тканевой гипоксии, препятствующей адекватной пролиферации клеток и, следовательно, нормальной регенерации тканей в условиях повторяющегося воздействия на них повреждающего фактора. Коррекция замыкательной функции кардии приводила к нормализации лимфооттока в этой зоне и тем самым за счет устранения тканевой гипоксии способствовало восстановлению тканевых структур.
У остальных 41 пациентов при исследовании биопта-тов выявлен пищевод Барретта. В 23 случаях диагностирована кишечная метаплазия. У 3 больных наблюдали дисплазию призматического эпителия тяжелой степени.
При сравнительной оценке состояния слизистой оболочки пищевода в зависимости от вида рефлюкса, по данным суточной рН-метрии, выявлены два различных типа ее изменений. В случаях кислотного рефлюкса отмечалась типичная картина пищевода Барретта с желудочной метаплазией, при этом в многослойном плоском эпителии были выявлены койлоциты – так называемые корзинчатые клетки с наличием оптических пустот в околоядерной цитоплазме (рис. 8). Аналогичные клетки описаны в эпителии шейки матки и при хронических вирусных фарингитах у больных с хроническими синуситами [9]. Установлено, что такого рода фенотип эти клетки приобретают в результате паразитирования в них папилломавируса человека, что, в свою очередь, считается облигатным фактором развития рака шейки матки. В наших наблюдениях наличие койлоцитов встречалось у 92% пациентов с кислотными рефлюксами и лишь в 1 случае при наличии смешанного рефлюкса.
При иммуногистохимическом исследовании 10 био-птатов на наличие персистенции в измененном эпителии пищевода цитомегаловируса, вируса герпеса I–II типов, папилломавируса результат оказался отрицательным.
Показания к оперативной коррекции пищеводножелудочного перехода устанавливали при выявлении
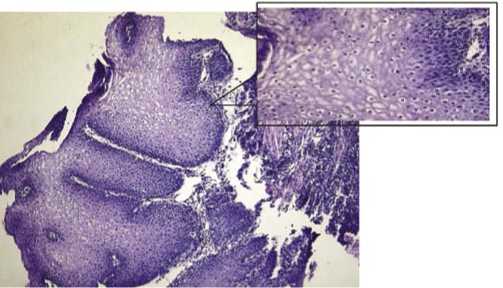
Рис. 8. Рефлюкс-эзофагит. По данным суточной рН-метрии определяется кислотный рефлюкс. Множественные клетки с оптическими пустотами (койлоциты) в составе акантотически измененного многослойного плоского эпителия. Окраска гематоксилином и эозином. Ув. х 60 и х 200
признаков необратимых нарушений замыкательной функции кардии вне зависимоти от наличия осложнений. Оперативные вмешательства по восстановлению замыкательной функции кардии выполнены у 103 пациентов. 90 пациентов оперированы лапароскопическим доступом, 13 – открытым.
Преимущество отдавали полной фундопликации по Nissen-Rosetti, которая выполнена 90 (87,3%) пациентам.
Парциальные фундопликации выполнялись преимущественно в случае симультанного оперативного вмешательства как дополнение к устранению основного заболевания (n = 13). В 2 случаях ваготомия с дренирующей желудок операцией была дополнена выполнением передней крурорафии и фундопексией за правую ножку диафрагмы без выполнения фундопликации, с хорошим отдаленным результатом. В 3 случаях (7,7%) была выполнена конверсия доступа с лапароскопического на открытый в связи с техническими особенностями оперативного вмешательства.
Интраоперационные осложнения развились у 6 (5,8%) больных. В 5 наблюдениях диагностирован правосторонний карбокситоракс, который был связан с повреждением медиастинального листка париетальной плевры. В одном случае отмечена эмфизема области грудной клетки, шеи, лица. Во всех случаях осложнения не повлияли на объем запланированной операции.
Результаты лечения пациентов оценивали через 3, 6, 12 месяцев и далее 1 раз в год.
Для анализа результатов лечения всем пациентам предварительно проводилось анкетирование с помощью опросника sf-36. Всего изучены результаты у 87 больных. Уровень физического благополучия колебался от 10 до 63%, составляя в среднем 44,9%. Уровень психического здоровья колебался от 25 до 76 со средним значением 48,7%.
Через 3 месяца после лечения обследовано 60 больных, уровень психического здоровья составил 55,1%
(колебания от 49 до 68%), физическое здоровье 53,6% (с колебанием значений от 48 до 60%).
Анкетирование 37 пациентов в сроки 6 месяцев после лечения показало значительно лучшие результаты как психического, так и физического здоровья, показатели составили, соответственно, 68,4% и 71, 5%.
В сроки от 12 до 37 месяцев после лечения проведено анкетирование 21 пациента. Максимальный срок наблюдения составил 37 месяцев. Анализ отдаленных результатов показал повышение уровня психического и физического здоровья до 70,8% и 74, 2%, соответственно.
Показатели психического и физического здоровья через 6 месяцев после операции незначительно отличались от показателей в более поздние сроки наблюдения, которые достигают своего максимума в первые 6 месяцев после операции. Рецидив заболевания, обусловленный миграцией фундопликационной манжеты, выявлен у 2 пациентов, в одном случае выполнена рефундопликация.
Ближайшие результаты лечения (через 6 месяцев) оценены у 37 пациентов. Отдаленные результаты в сроки от 12 до 27 месяцев изучены у 21 пациента (табл. 1).
В 6 наблюдениях после устранения метаплазии и дисплазии пищевода выполнялись повторные биопсии для гистологического исследования в сроки до 12 месяцев. Во всех случаях, как по данным эзофагоскопии, так и по данным гистологического исследования, выявлено замещение цилиндрического эпителия многослойным плоским при сохранении умеренных воспалительных изменений слизистой пищевода.
Выводы
-
1. Углубленное обследование больных эзофагитами с определением патогенетических механизмов его развития обеспечивает дифференцированный подход к лечению с получением отличных и хороших результатов у 92% в ближайшем и у 89% больных в отдаленном периоде наблюдения.
-
2. Микроскопические изменения слизистой оболочки пищевода при рефлюкс-эзофагитах существенно различаются в зависимости от типа рефлюкса. Наиболее неблагоприятными в прогностическом отношении являются щелочной и смешанный рефлюксы, сопровождающиеся развитием кишечной метаплазии эпителия пищевода, устранение их с помощью малоинвазивных эндоскопических методов приводит к полной регенерации многослойного плоского эпителия.
-
3. Одним из факторов неудовлетворительной регенерации слизистой оболочки при пищеводе Барретта является тканевая гипоксия, связанная с хроническим отеком ее собственной пластинки вследствие лимфо-стаза, обусловленного нарушением моторики пищевода и функции нижнего пищеводного сфинктера.
-
4. При осложненном течении пептического эзофагита показано двухэтапное лечение с использованием на первом этапе эндоскопического пособия для устранения осложнений, дополненного консервативной
Табл. 1. Результаты ближайших и отдаленных результатов лечения
Список литературы Диагностика и лечение рефлюкс-ассоциированных воспалительных заболеваний пищевода и их осложненний
- Барабанов И.Е. Комплексная оценка результатов лечения больных рефлюксэзофагитом, сочетающимся с другими постгастрорезекци-онными синдромами: автореф. дисс.. канд. мед.наук/И.Е. Барабанов. -СПб., 1992. -21 с.
- Годжелло Э.А. Предупреждение, ранняя диагностика принципы лечения осложнений эндоскопических операций при доброкачественных стенозирующих заболеваниях пищевода/Э.А. Годжелло, Ю.И. Галлингер//Клинич. эндоскопия. -2006. -№2(8). -С. 2-12.
- Гриневич В.Б. Гастроэзофагеальная рефлюксная болезнь и ее внепищеводные проявления: современные представления о диагностике и лечении/В.Б. Гриневич, О.А. Саблин. -СПб., 2004. -С. 10-25.
- Касумов Н.А. Рефлюкс-эзофагит: современное состояние проблемы/Н.А. Касумов//Хирургия. -2007. -№ 4. -С. 62-65.
- Кашин С.В. Пищевод Баррета: принципы эндоскопической диагностики и медикаментозной терапии/С.В. Кашин, И.О. Иваников//Российский журнал гепатологии, гастроэнтерологии, колопроктологии. -2006. -№ 6. -С. 73-77.
- Лукина А.С. Пищевод Барретта/А.С. Лукина//Клинич. эндоскопия. -2008. -№ 1(14). -С. 42-48.
- Солоницын Е.Г. Клинико-эндоскопические особенности и лечебная тактика у больных гастроэзофагеальной рефлюксной болезнью со скользящей грыжей пищеводного отверстия диафрагмы: автореф. дисс. канд.. мед.наук/Е.Г. Солоницын. -СПб., 2007. -22 с.
- Старостин Б.Д. Оптимизация лечения гастроэзофагеальной реф-люксной болезни/Б.Д. Старостин//Рос.журн. гепатологии, гастроэнтерологии, колопроктологии. -2007. -№4. -С. 4-9.
- Ткачук И.В. Клинико-морфологические особенности слизистой оболочки глотки при хронических синуситах: автореф. дис..канд.мед. наук/И.В. Ткачук.-СПб., 1998. -19 с
- Черноусов А.Ф. Результаты фундопликаций при лечении рефлюкс-эзофагита/А.Ф. Черноусов, А.Л. Шестаков, Л.К. Егорова//Весн. хирургической гастроэнтерол. -2009. -№4. -С.64-67.
- Shi G. Lower esophageal sphincter relaxation characteristics using a sleeve sensor in clinical manometry/G.Shi, G.A.Ergun, M.Manka, P.J.Kahrilas//Amer. J. Gastroenterol. -1998. -Vol. 93, N. 12. -P. 2373-2379.
- Wykypiel H. Nissen or partial posterior fundoplication: which antireflux procedure has a lower rate of side effects?/H. Wykypiel, M. Gadenstaetter, A. Klaus, P. Klingler, G.J. Wetscher//Langenbecks Arch Surg. -2005. -Vol. 390, №2. -Р. 141-147


