Диагностика миксомы сердца. МР-томография сердца у больной с миксомой левого предсердия перед хирургическим удалением опухоли
Автор: Меладзе Н. В., Страздень Е. Ю., Власова Э. Е., Королев С. А., Стукалова О. В.
Журнал: Евразийский кардиологический журнал @eurasian-cardiology-journal
Рубрика: Клинический случай
Статья в выпуске: 1, 2020 года.
Бесплатный доступ
Среди большого количества доброкачественных опухолей сердца миксома - наиболее часто диагностируемое внутриполостное новообразование (встречается в 50%). Клиническая картина миксомы крайне разнообразна, часто диагностируется как случайная находка. Обычно диагноз устанавливают по данным эхокардиографии (ЭхоКГ). Магнитно-резонансная томография применяется для обследования больных с подозрением на миксому в случаях, когда данные ЭхоКГ недостаточно информативны, а также перед хирургическим лечением. Приводим клиническое наблюдение пациентки 58 лет с миксомой левого предсердия, которой перед хирургическим удалением миксомы была выполнена МР-томография сердца.
Магнитно-резонансная томография, миксома, сердце, левое предсердие
Короткий адрес: https://sciup.org/143171846
IDR: 143171846 | DOI: 10.24411/2076-4766-2020-10005
MR-tomography of the heart in a patient with left atrium myxoma before surgical treatment
Among the large number of benign tumors of the heart myxoma most frequently diagnosed neoplasm intracavitary (occurs in 50%). The clinical picture of a myxoma is extremely various. Often it is diagnosed as a casual find. Usually the diagnosis is established according to an echocardiography. Magnetic resonance imaging is used for inspection of patients with suspicion on myxoma in cases when information of echocardiography is not enough and before surgical treatment. We present clinical follow-up 58 years old patients with left atrial myxoma, which before surgical treatment has executed a heart MRI.
Текст научной статьи Диагностика миксомы сердца. МР-томография сердца у больной с миксомой левого предсердия перед хирургическим удалением опухоли
Страздень Елизавета Юрьевна Strazden Elizaveta Yurievna врач рентгенолог, заведующая рентгеновским отделением филиала №5 ФГБУ «3 ЦВКГ им. A.А. Вишневского» Минобороны Российской Федерации. Адрес: ул. Госпитальная, д. 3/6, Московская область, Сергиев Посад, Россия, 141307. Tel.: +7496-545-62-59. E-mail: Профиль в ORCID: doctor roentgenologist, head of the X-ray department, Branch №5 FGBU «3-rd Central Military Clinical Hospital named after A.A. Vishnevsky» Ministry of Defense of the Russian Federation, Postal adress: Gospitalnaya str., 3/6, Moscow region, Sergiev Posad, Russia, 141307. Власова Элина Евгеньевна Vlasova Elina Evgenyevna к.м.н., старший научный сотрудник отдела сердечно-сосудистой хирургии ФГБУ «НМИЦ кардиологии» Минздрава России. Адрес: ул. 3-я Черепковская, 15-а, Москва, Россия, 121500. Tел.: +7495-414-6334. E-mail: Профиль в ORCID: Х. PhD in medical Science, researcher in department of cardiovascular surgery, National Medical Research Center of Сardiology. Postal adress: 3-rd Cherepkovskays str., 15-a, Moscow, Russia, 121500. Королев Сергей Владимирович Korolev Sergey Vladimirovich к.м.н., врач-хирург отдела сердечно-сосудистой хирургии ФГБУ «НМИЦ кардиологии» Минздрава России. Адрес: ул. 3-я Черепковская, 15-а, Москва, Россия, 121500. Tел.: +7495-414-63-34. E-mail: Профиль в ORCID: Х PhD in medical Science, doctor in department of cardiovascular surgery, National Medical Research Center of Сardiology. Postal adress: 3-rd Cherepkovskays str., 15-a, Moscow, Russia, 121500. Стукалова Ольга Владимировна Stukalova Olga Vladimirovna к.м.н., старший научный сотрудник отдела томографии «НМИЦ кардиологии» Минздрава России. Адрес: ул. 3-я Черепковская, 15-а, Москва, Россия, 121500. Tел.: +7495-414-63-34. E-mail: Профиль в ORCID: PhD in medical Science, researcher in Tomography Department National Medical Research Center of Сardiology. Postal adress: 3-rd Cherepkovskays str., 15-a, Moscow, Russia,121500. Автор, ответственный за связь с редакцией: Меладзе Нино Вахтанговна к.м.н., младший научный сотрудник отдела томографии ФГБУ «НМИЦ кардиологии» Минздрава России. Адрес: ул. 3-я Черепковская, 15-а, Москва, Россия, 121500. Tел.: +7495-414-63-34. E-mail: meladze_nina@ Профиль в ORCID: Contact for correspondence: Meladze Nino Vakhtangovna PhD in medical Science, researcher in Tomography department, National Medical Research Center of Сardiology. Postal adress: 3-rd Cherepkovskays str., 15-a, Moscow, Russia,121500
Диагностика образований в полости сердца является одним из показаний к проведению МРТ. Это связано с диагностическими возможностями МР-томографии, которая позволяет получить информацию о морфологии и функции сердца, выявить дополнительные образования в полостях сердца, точно определить их локализацию и распространенность. Кроме того, с помощью МР-томография можно определить подвижность опухоли, неинвазивно оценить изменения гемодинамики, вызванные движущейся опухолью, степень обструкции приносящего или выносящего трактов [1].
Миксома является одной из самых распространенных первичных доброкачественных опухолей сердца. Предполагают, что клетки опухоли развиваются из эмбриональной мукоидной ткани или эндотелия с последующей миксоматозной дегенерацией. Миксома может располагаться в любых камерах сердца, но наиболее частой локализацией является ЛП в области овальной ямки межпредсердной перегородки. В правом предсердии миксома встречается не так часто — примерно в 20% случаев. В единичных наблюдениях описывают миксому фиброзных колец, створок или полулунных заслонок клапанов сердца, устьев аорты, или легочной артерии [2]. Известны наблюдения первично-множественного роста миксомы, когда две или более опухоли расположены в одной или нескольких камерах сердца. Примерно у 10 % больных заболевание носит семейный характер, наследуясь по аутосомно-доминантному типу. В таких случаях миксома сердца обычно возникает в молодом возрасте, чаще бывает множественной (30–50 %), может исходить из желудочков (10–15%), сопровождается миксоматозными аденомами молочной железы, опухолями эндокринных органов и пигментацией кожи. Если спонтанные миксомы рецидивируют очень редко, то в случаях семейного заболевания частота их рецидивов составляет 12–22% [3].
Жалобы больных обусловлены тремя патологическими механизмами — эмболией, обструкцией кровотока и конституциональными признаками (в виде снижение массы тела слабость, субфебрильная температура тела, тошнота). Относительно редкое и позднее осложнение миксом — инфекционный эндокардит. Примерно у 10–15% больных протекает бессимптомно и диагноз ставится случайно. Наиболее часто дифференциальный диагноз предсердной миксомы является образование тромба.
Симптомы эмболий возникают у 30–40% пациентов. Поскольку большинство миксом локализуется в левых отделах, около 50% эмболий происходит в экстра- или интракраниальные ар- терии головного мозга, а также в сосуды нижних конечностей, реже — в сосуды кишечника, коронарные и почечные артерии. Эмболии при правосторонних миксомах обычно бессимптомны и приводят лишь к выявляемой инструментально умеренной легочной гипертензии [4]. Симптомы обструкции кровотока при миксоме ЛП обусловлены частичной обтурацией опухолью левого АВ отверстия и реже, устья легочной вены. Как следствие, развиваются легочная и/или венозная, а в ряде случаев артериальная гипертензия и синдром малого сердечного выброса, которые проявляются одышкой, ортопноэ, отеком легких, кашлем, иногда кровохарканьем, сердцебиением, слабостью и периферическими отеками. Часто отмечаются головокружение и преходящая потеря сознания, возможна внезапная смерть. Заподозрить наличие миксомы позволяет изменение степени выраженности этих симптомов в зависимости от положения тела, особенно уменьшение одышки в положении лежа, но установить такую связь удается довольно редко [5].
При объективном обследовании, в частности при аускультации возможно определить стеноз митрального клапана, стеноз клапана аорты, стеноз трехстворчатого клапана, стеноз клапана легочной артерии. При миксомах, локализованных на свободной створке АВ-клапанов, удается выслушать «опухолевый хлопок» — поздний диастолический звук контакта опухоли с эндокардом желудочков. Нередко выслушиваются мезодиастолический и систолический шумы, шум митральной регургитации.
При проведении электрокардиографии (ЭКГ) и рентгенографии органов грудной клетки специфических изменений нет.
Информативным методом диагностики опухолей сердца является трансторакальная и чреспищеводная эхокардиография. Но стандартное трансторакальное эхокардиографическое исследование не всегда в состоянии дать ответ на некоторые вопросы. Это связано с неудовлетворительной визуализацией сердца из-за плохой акустической доступности (в 20–30% случаев), что не позволяет получить диагностически информативное изображение всех интересующих отделов. Также плохая визуализация у довольно значительного количества больных при трансторакальном исследовании вызвана множеством препятствий, которые необходимо преодолеть ультразвуку (кожа, подкожная жировая клетчатка, мышцы). Проведение исследования также затруднено при деформации грудной клетки, узких межреберных промежутках. Повышенная воздушность легочной ткани (например, при эмфиземе легких) — также существенная преграда для ультразвука. Кроме того, в самом сердце присутствуют структуры, мешающие исследованию (выраженный кальциноз, протезированные клапаны).
Чреспищеводная ЭхоКГ в некоторых случаях позволяет получить необходимую дополнительную информацию. Но время исследования ограничено из-за плохой переносимости у большинства пациентов [6, 7], Назначая данное исследование лечащий врач должен четко определить цели и задачи, поставить конкретные вопросы.
Рентгеновская компьютерная томография (РКТ) по сравнению с Эхо-КГ позволяет получить более точную информацию о размерах, локализации, структуре опухоли. РКТ выполняется с контрастным усилением, что позволяет также оценить степень васкуляризации опухоли [8]. РКТ рекомендуют использовать у пациентов, которым по разным причинам невозможно выполнить МРТ: при наличие абсолютных противопоказаний, когда пациент находится в тяжелом состоянии и не может находиться в канале томографа неподвижно и адекватно задерживать дыхание. Важным достоинством РКТ является возможность во время одного исследования не только оценивать камеры сердца, но и получать информацию о состоянии коронарных артерий. К ограничениям РКТ при обследовании больных с уже выявленным образованием сердца можно отнести необходимость контрастирования во всех случаях, а также невозможность получить достаточный объем информации о функциональном состоянии сердца, подвижности опухоли, вызываемых ею нарушениях внутрисердечной гемодинамики [9].
Магнитно-резонансная томография сердца является неинвазивной процедурой, которая в большинстве случаев легко переносится пациентами, при бесконтрастном исследовании сопоставима по времени с эхокардиографией, при этом позволяет достоверно выявить дополнительные образования в полостях сердца, оценить их локализацию, размеры, структуру, наличие обструкции, нарушения гемодинамики. Проведение МРТ сердца пациентам с подозрением на наличие дополнительных образований в полостях сердца, позволяет определить локализацию, уточнить размеры и структуру образований находящейся в полостях сердца, по характеристиках сигнала провести дифференциальную диагностику между миксомой и тромбами, другими опухолями сердца [10].
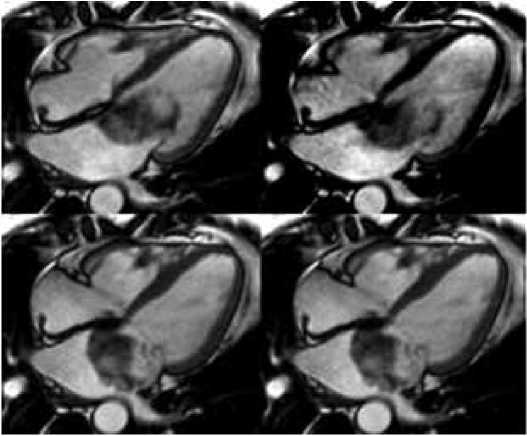
Рисунок 1. Кино-МРТ сердца до хирургического вмешательства. Длинная ось сердца, 4-х камерная проекция, верхний ряд – различные фазы диастолы, нижний – различные фазы систолы. На изображениях в разные фазы диастолы видно, как миксома пролабирует в полость левого желудочка более чем на половину своей длины и обтурирует приносящий тракт левого желудочка
КЛИНИЧЕСКИЙ ПРИМЕР
При амбулаторном обследовании в ИКК им. А.Л. Мясникова у пациентки Л., 58 лет, по данным ЭхоКГ была выявлена миксома левого предсердия (ЛП), пролабирующая в полость левого желудочка (ЛЖ), с развитием стеноза атриовентрикулярного отверстия (АВ) и легочной гипертензии.
Из анамнеза известно, что пациентка считает себя больной в течение полугода, когда появились жалобы на непродуктивный кашель, который пациентка связывала с ОРВИ. Лечилась амбулаторно антибиотиками без четкого клинического эффекта. В течение последних двух месяцев к кашлю присоединились жалобы на слабость, резкое снижение толерантности к физической нагрузке.
Объективно состояние больной относительно удовлетворительное. Кожные покровы чистые, физиологической окраски. Периферических отеков нет. При аускультации легких дыхание везикулярное, отмечались единичные пневмосклеротические хрипы. ЧДД 14 в минуту. Сердечный ритм правильный, ЧСС до 67 в минуту. Артериальное давление на правой руке 120/80 мм рт.ст., на левой руке 118/78 мм рт.ст.
Результаты обследования. По данным рентгенологического исследования грудной клетки увеличения отдельных частей сердца не выявлено (КТИ 47%, при норме до 50%). Легочный рисунок существенно не видоизменен, отмечается диффузный пневмосклероз, уплотнение стенок аорты.
При проведении ЭхоКГ в полости ЛП было выявлено объемное образование округлой формы, однородной структуры, с неровными краями, размером 5,1 х 4,0 х 3,5 см, которое фиксировалось к базальному отделу межпредсердной перегородки (МПП) и пролабировало в диастолу в полость ЛЖ, вызывая обструкцию левого АВ-отверстия. Также отмечалось расширение полости ЛП. ЛЖ был не расширен, сократительная способность его оставалась удовлетворительной. Правые камеры сердца были не расширены.
Перед хирургическим вмешательством для получения дополнительной информации относительно распространенности процесса и инвазии опухоли в стенку сердца (для дифференциальной диагностики от злокачественной опухоли) было проведено МРТ исследование сердца на магнитно-резонансном томографе с напряженностью магнитного поля 3,0 Тл (Achieva), с применением специальной 32-канальной кардиологической катушки. На изображениях в кино-режиме в двухкамерной и четырехкамерной проекциях в полости ЛП визуализировалось объемное образование с четкими, неровными контурами, размером 5,4 х 5,8 см, неоднородное по структуре, с наличием участков повышенной и пониженной интенсивности МР-сигнал на SE и GE последовательностях – участки кровоизлияний и зоны распада.
Кроме того, при кино-МРТ визуализировалось пролабирование опухоли в полость ЛЖ более чем на половину, что приводило к смещению задней створки митрального клапана и обструкции приносящего тракта ЛЖ (рис. 1).
Так как результаты бесконтрастного обследования позволили получить исчерпывающую информацию о состоянии опухоли, исследование с контрастным усилением не выполнялось.
Пациентке было оказано эффективное кардиохирургическое пособие в условиях кардиохирургического отделения в ИКК им. А.Л. Мясникова. При искусственном кровообращении и холодовой и медикаментозной кардиоплегии разрезом вдоль полых вен было вскрыто правое предсердие, рассечена межпредсердная перегородка. При ревизии обнаружена шаровидной формы опухоль на ножке, размерами 6 х 5 см, основание которой крепится к межпредсердной перегородке. Опухоль иссечена в пределах
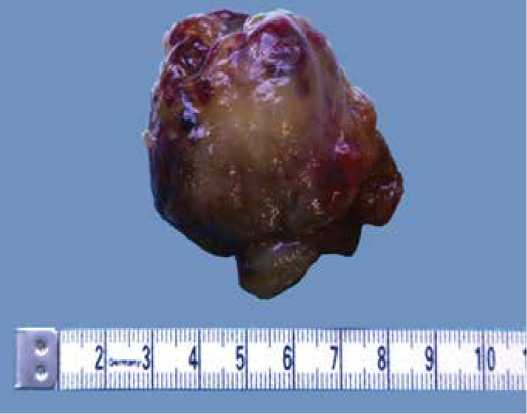
Рисунок 2. Макропрепарат удаленной миксомы сердца
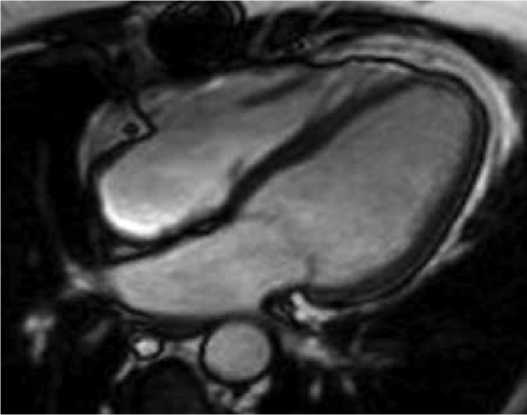
Рисунок 3. Кино-МРТ сердца по длинной оси после успешно проведенного хирургического лечения, 4-х камерная проекция. Дополнительное образование в полости левого предсердия при
настоящем исследовании не определяется здоровых тканей. Выполнена пластика межпредсердной перегородки. Макропрепарат удаленной опухоли представлен на рисунке 2.
По данным гистологического исследования выявлено скопление паукообразных, звездчатых и перстневидных клеток, частично аностомазирующих друг с другом своими отростками. Также в микропрепарате определено большое количество сосудистого типа капилляров, множество очагов кровоизлияния и очагов некроза (что подтверждало данные МРТ). Признаков атипичного роста выявлено не было. Описанная картина характерна для доброкачественной миксомы.
Через четыре недели после оперативного вмешательства для оценки результатов хирургического лечения было повторно выполнено МР-исследование сердца, при котором ранее описываемое образование в полости ЛЖ уже не визуализировалось (рис. 3).
ЗАКЛЮЧЕНИЕ
Несмотря на скудную клиническую картина у 15% пациентов с миксомой предсердия присутствует риск внезапной сердечной смерти [4]. Смерть, как правило, вызвана эмболизацией коронарных артерий и/или легочных артерий. Также летальный исход возможен вследствие обструкции митрального или трехстворчатого клапанов. Поэтому своевременная и точная диагностика данного заболевания так необходима.
При обследовании больного с заподозренным или выявленным внутрисердечным образованием отдается предпочтение следующему диагностическому алгоритму: ЭхоКГ позволяет выявить объемное образование, а МРТ, как уточняющий метод диагностики, детализировать данные ЭхоКГ, особенно перед планирующимся хирургическим лечением [11,12]. При невозможности выполнения МРТ для уточняющей диагностики используется РКТ с контрастированием.
Список литературы Диагностика миксомы сердца. МР-томография сердца у больной с миксомой левого предсердия перед хирургическим удалением опухоли
- Стукалова ОВ Магнитно-резонансная томография сердца с отсроченным контрастированием - новый метод диагностики заболеваний сердца // Российский электронный журнал лучевой диагностики. - 2013. - Т. 3. - С. 7-18.
- Sheppard M.N., Mohiaddin R. Tumors of the heart // Future Cardiology. - 2010. - Vol. 6 (2). - P. 181-193. DOI: 10.2217/fca.09.62
- Burke A.P., Gomez-Roman J.J., Loire R. et al. World Health Organization: Tumours of the lung, pleura, thymus and heart. - Lyon: IARC Press, 2004.
- Lee V., Connolly H., Brown R. Central nervous system manifestations of cardiac myxoma // Arch. Neurol. - 2007. - Vol. 64 (8). - P. 1115-1120. DOI: 10.1001/archneur.64.8.1115
- Rios R.E., Burmeister D.B., Bean E.W. Complications of atrial myxoma // Am. J. Emerg. Med. - 2016. - Vol. 34 (12). - P. 2465.e1-2465.e2. DOI: 10.1016/j.ajem.2016.05.079
- Захарьян Е.А. Миксомы сердца: история изучения, современные методы диагностики и лечения // Крымский терапевтический журнал. - 2012. - Т. 2. - С. 27.
- Приходько В.П., Нуждин М.Д., Логаненко Д.И., Фокин А.А. Современные методы диагностики и хирургического лечения первичных новообразований сердца. - Челябинск, 2012 - 159 с.
- Ю.В. Конради, Д.В. Рыжкова Лучевая диагностика опухолей сердца // Лучевая диагностика и терапия. - 2015. - N 4 (33). - С.28-40.
- Orla Buckley, Rachna Madan, Raymond Kwong, et al. Cardiac Masses, Part 1: Imaging Strategies and Technical Considerations // Am J Roentgenol. - 2011. - Vol. 197(5). - P.837-841.
- DOI: 10.2214/AJR.10.7260
- Abbas A., Garfath-Cox K.A., Brown I.W. et al. Cardiac MR assessment of cardiac myxomas // Br. J. Radiol. - 2015. - Vol. 88 (1045). - P. 20140599.
- DOI: 10.1259/bjr.20140599
- А.В. Ваганов1,2, М.В. Ростовцев1,3, А.А. Ваганов. Лучевая диагностика опухолей сердца // Медицинская визуализация. - 2010. - №2. - С.27-34.
- Hendel RC, Patel MR, Kramer CM, et al. ACCF/ACR/SCCT/ SCMR/ASNC/ NASCI/SCAI/SIR 2006 appropriateness criteria for cardiac computed tomography and cardiac magnetic resonance imaging: a report of the American College of Cardiology Foundation Quality Strategic Directions Committee Appropriateness Criteria Working Group, American College of Radiology, Society of Cardiovascular Computed Tomography, Society for Cardiovascular Magnetic Resonance, American Society of Nuclear Cardiology, North American Society for Cardiac Imaging, Society for Cardiovascular Angiography and Interventions, and Society of Interventional Radiology // J Am Coll Cardiol. - 2006. - Vol. 48. - P.1475-97.


