Диагностика жизнеспособного миокарда до операции и оценка динамики его восстановления после реваскуляризации сердца
Автор: Шевченко Ю.Л., Вахрамеева А.Ю., Вахромеева М.Н., Ульбашев Д.С.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 1 т.20, 2025 года.
Бесплатный доступ
Сохраняющиеся высокие показатели заболеваемости, госпитализации и смертности населения при ИБС, несмотря на поиск новых методов диагностики и лечения, говорят об актуальности проблемы до настоящего времени. Пациенты с ИБС требуют индивидуального комплексного подхода в силу характера и степени выраженности атеросклеротического поражения, наличия потенциально жизнеспособного миокарда, объема и тяжести его гибернации. Внедрение в клиническую практику метода стимуляции экстракардиального неоангиогенеза позволило значительно расширить возможности лечения больных с диффузным поражением коронарного русла. Представлены данные дооперационной визуализации жизнеспособного миокарда у пациентов с тяжелым атеросклеротическим поражением венечного русла, а также динамика его восстановления в послеоперационном периоде в зависимости от выполненного метода хирургической реваскуляризации.Материалы и методы. В проспективное рандомизированное исследование включены данные 140 пациентов с ИБС и диффузным поражением коронарного русла, которым с 2016 по 2023гг. была выполнена реваскуляризация миокарда в отделении сердечно-сосудистой хирургии Клиники грудной и сердечно-сосудистой хирургии им. Святого Георгия ФГБУ «НМХЦ им. Н.И. Пирогова» Минздрава России. I группа (n = 71) - комплексная реваскуляризации; II группа (n = 69) - изолированное коронарное шунтирование. Результаты синхро-ОФЭКТ миокарда и эхокардиографии оценивались на ранних сроках (10-14 суток) и через 6-12 месяцев после операции. Выполнялся сегментарный анализ изменения перфузии и сократимости миокарда. Оценивались основные варианты перфузионно-функционального соответствия. Первичная конечная точка - изменение объема гибернированного миокарда в течение всего периода наблюдения. Вторичные конечные точки - динамика региональной перфузии и сократимости; изменение фракции выброса левого желудочка.Результаты. Объем гибернированного миокарда левого желудочка в раннем послеоперационном периоде уменьшился с 29 [20; 35]% до 17 [10; 25]% в I группе (р function show_abstract() { $('#abstract1').hide(); $('#abstract2').show(); $('#abstract_expand').hide(); }
Ибс, диффузное поражение коронарного русла, комплексная реваскуляризация, гибернация, миокардиальный резерв
Короткий адрес: https://sciup.org/140309956
IDR: 140309956 | DOI: 10.25881/20728255_2025_20_1_11
The diagnosis of viable myocardium before surgery and assessment of the dynamics of its recovery after cardiac revascularization
The continuing high rates of morbidity, hospitalization and mortality of the population with coronary heart disease, despite the search for new diagnostic and treatment methods, indicate the urgency of the problem to date. Patients with coronary heart disease require an individual comprehensive approach due to the nature and severity of atherosclerotic lesions, the presence of a potentially viable myocardium, and the volume and severity of its hibernation. The introduction of the method of stimulation of extracardial neoangiogenesis into clinical practice has significantly expanded the treatment options for patients with diffuse coronary artery disease. The article presents data on preoperative visualization of a viable myocardium in patients with severe atherosclerotic lesions of the coronary bed, as well as the dynamics of its recovery in the postoperative period, depending on the performed surgical revascularization method.Materials and methods. The prospective, randomized study included data from 140 patients with coronary artery disease and diffuse coronary artery disease who underwent myocardial revascularization from 2016 to 2023 at the Department of Cardiovascular Surgery at the Moscow Institute of Thoracic and Cardiovascular Surgery. St. George’s Federal State Budgetary Institution “National Medical and Surgical Center named after N.I. Pirogov” of the Ministry of Health of the Russian Federation. Group I (n = 71) - complex revascularization; group II (n = 69) - isolated coronary bypass surgery. The results of gated-SPECT of the myocardium and echocardiography were evaluated early (10-14 days) and 6-12 months after surgery. Segmental analysis of changes in myocardial perfusion and contractility was performed. The main variants of perfusion-functional compliance were evaluated. The primary endpoint is a change in the volume of the hibernated myocardium during the entire follow-up period. Secondary endpoints are the dynamics of regional perfusion and contractility; changes in the left ventricular ejection fraction.Results. The volume of the hibernated left ventricular myocardium in the early postoperative period decreased from 29[20;35]% to 17[10;25]% in group I (p function show_eabstract() { $('#eabstract1').hide(); $('#eabstract2').show(); $('#eabstract_expand').hide(); }
Текст научной статьи Диагностика жизнеспособного миокарда до операции и оценка динамики его восстановления после реваскуляризации сердца
ИБС до сих пор остается одной из ведущих причин заболеваемости, инвалидизации, смертности населения в России и во всем мире, при этом в настоящее время растет число пациентов с диффузным поражением коронарного русла [1–3].
У трети пациентов с острым инфарктом миокарда (ИМ) развивается выраженная его дисфункция, сердечная недостаточность (СН), снижается качество жизни и уменьшается ее продолжительность [4]. Ремоделирование левого желудочка (ЛЖ) зависит от объема фиброзных изменений сердца и его резервов. В течение первых часов после тяжелого ишемического повреждения активируются различные механизмы, направленные на ограничение зоны некроза и замещение поврежденной ткани миокарда рубцом, при этом некоторые ассоциации кардиомиоцитов могут оставаться жизнеспособными в течение длительного времени и восстанавливать свою функцию после реваскуляризации миокарда [5].
С морфологической и физиологической точки зрения о жизнеспособности кардиомиоцитов можно говорить при сохраненной клеточной структуре и метаболической активности. В клинических же условиях она определяется наличием дисфункционального миокарда в состоянии покоя с возможностью восстановления сократимости при улучшении его перфузии [6; 7].
Известны два основных механизма обратимости ишемической дисфункции миокарда: оглушение и гибернация. Станнинг или оглушение — это транзиторное нарушение функции миокарда, которое возникает после эпизода ишемии или реперфузионного повреждения. Считается, что основной механизм «оглушения» – избыточное накопление кальция в кардиомиоците, изменения в его энергетическом обмене и регуляции окислительных процессов [8]. Гибернация – хроническое потенциально обратимое снижение функции миокарда, связанное с адаптационными изменениями энергетического метаболизма и возможными структурными перестройками в кардиомиоцитах (редукцией миофибрилл, заполнением свободного пространства гликогеном, уменьшением саркоплазматического ретикулума, исчезновением Т-тубул и поперечных канальцев). Восстановление сократимости таких кардиомиоцитов после реваскуляризации зависит от степени тяжести гибернации и выраженности интерстициальных фиброзных изменений [9]. В настоящее время станнинг и гибернация, несмотря на их патофизиологические особенности, представляются общими звеньями одного процесса адаптации к гипоксии [10; 11].
Определение жизнеспособного миокарда играет важную роль в выборе тактики лечения и прогнозирование исходов реваскуляризации [5]. Кроме того, наличие значимого объема гибернированного миокарда у пациентов, которым не выполнялась реваскуляризация, создает субстрат для желудочковых тахиаритмий, что связано с риском внезапной сердечной смерти [12; 13].
Несмотря на то, что многие исследования подтверждают необходимость дооперационной оценки жизнеспособности миокарда, существуют данные, противоречащие этой концепции [14–16]. До сих пор остается много вопросов относительно влияния степени тяжести гибернации и объема жизнеспособного миокарда на тактику лечения и результаты коронарного шунтирования (КШ), особенно у пациентов с диффузным поражением, у которых полный объем реваскуляризации невыполним, и, соответственно, остается риск прогрессирования ишемического повреждения миокарда.
С целью улучшения результатов лечения таких пациентов уже много лет в Клинике грудной и сердечно-сосудистой хирургии имени Святого Георгия КШ дополняется методом стимуляции экстракардиаль-ного неоангиогенеза (методикой «ЮрЛеон») [17; 18]. Представлены данные дооперационного определения объема жизнеспособного миокарда, степени тяжести гибернации, а также динамики его восстановления в послеоперационном периоде в зависимости от выполненного метода хирургической реваскуляризации у пациентов с ИБС и диффузным поражением коронарного русла.
Материал и методы
В проспективное, рандомизированное исследование включены данные 140 пациентов с ИБС и диффузным поражением коронарного русла, которым с 2016 по 2023 гг. была выполнена реваскуляризация миокарда. Рандомизация проводилась с помощью генератора случайных чисел. Пациенты разделены на две группы: в I группу (n = 71) вошли пациенты, которым выполнялась комплексная реваскуляризация (КШ+ЮрЛеон); во II группу (n = 69) – больные, которым проводилось изолированное КШ.
Критериями включения в исследование являлись наличие перенесенного ИМ, подтвержденного инструментальными методами обследования: ЭКГ, ЭхоКГ; гемодинамически значимое атеросклеротическое поражение коронарных артерий; диффузный коронарный атеросклероз (традиционно определяемый как поражение двух и более сегментов одной магистральной артерии, общей протяженностью поражения более 50% всей длины сосуда при наличии гемодинамически значимого сужения просвета и/или малым диаметром дистального русла (менее 2 мм)); информированное согласие пациента на участие в исследовании.
Критериями невключения являлись нестабильная стенокардия; хроническая сердечная недостаточность (ХСН) в стадии декомпенсации; острый ИМ; наличие гемодинамически значимого поражения клапанного аппарата; острое нарушение мозгового кровообращения, а также отказ пациента от исследования.
Критерием исключения явилось отсутствие контрольного исследования через 6–12 месяцев после операции.

Первичная конечная точка — изменение объема гибернированного миокарда в течение всего периода наблюдения. Вторичные конечные точки — динамика региональной перфузии и сократимости; изменение фракции выброса ЛЖ.
По клинико-анамнестическим данным больные обеих групп статистически значимо не отличались (Табл. 1).
По данным селективной коронарографии (КАГ), до операции у 115 (82,1%) пациентов отмечалось 3-х сосудистое поражение, у 19 (13,6%) и 6 (4,3%) больных – поражение 2-х и 1-го коронарных сосудов, соответственно.
У 95 (67,9%) пациентов – окклюзия хотя бы одного коронарного сосуда. Диффузные изменения коронарных артерий, поражение их дистального русла или мелкие (ги-поплазированные) нешунтабельные артерии выявлены у 140 (100%) пациентов.
ЭхоКГ выполнялось на аппарате «General Electric Vivid 7» (USA) до операции, ежедневно при нахождении больного в ОРИТ, 1 раз в 4 суток в отделении, перед выпиской и в отдаленном послеоперационном периоде (6–12 месяцев) при контрольном обследовании. Глобальную систолическую функцию ЛЖ измеряли по формуле Simpson.
С целью диагностики жизнеспособного миокарда и определения его количества до операции всем пациентам была выполнена однофотонная эмиссионная компьютерная томография миокарда ЛЖ в покое, синхронизированная с ЭКГ (синхро-ОФЭКТ). Радиофармпрепарат (РФП) 99m Tc-технетрил вводили внутривенно в дозе 900 МБк. Регистрацию сцинтиграфических изображений проводили на гибридной установке ОФЭКТ/КТ «Discovery NM CT 670 DR» (GE). Для комплексной оценки перфузии и функции миокарда ЛЖ запись перфузионных изображений синхронизировали с ЭКГ пациента по R-зубцу. Оценку перфузии и функции проводили на унифицированных 20-ти сегментарных полярных диаграммах с использованием программы «QGS/QPS», на которых оценивали сегментарный захват РФП. При этом миокардиальные сегменты, в которых накопление РФП было ниже нормы, составляли общую зону гипоперфузии (Рис. 1 А, Б).
При сопоставлении перфузионных полярных диаграмм с функциональными оценивали зоны снижения регионального систолического утолщения миокарда ЛЖ (Рис. 1 В). Каждому сегменту присваивался балл от 1 до 4 (Рис. 1 Г), где 1 балл соответствовал норме; 4 балла – выраженному снижению регионального систолического утолщения миокарда (СУМ). Для оценки динамики изменений, происходящих в миокарде после операции, все миокардиальные сегменты были распределены на три варианта перфузионно-функционального соответствия (ПФС) в зависимости от уровня снижения перфузионных и функциональных показателей.
Дифференциальную диагностику гибернированного миокарда от рубцовых изменений осуществляли в общей
Табл. 1. Клинико-демографическая характеристика пациентов
|
Показатели |
I группа n = 71 |
II группа n = 69 |
Значения р |
|
|
Пол, n (%) |
Муж. |
53 (74,6) |
57 (82,6) |
0,347 |
|
Жен. |
18 (25,4) |
12 (17,4) |
0,347 |
|
|
Возраст, М±SD |
52,4±11,2 |
51,8±12,3 |
0,879 |
|
|
ИМ в анамнезе, n (%) |
71 (100) |
69 (100) |
– |
|
|
Повторный ИМ в анамнезе, n (%) |
9 (12,7) |
10 (14,5) |
0,754 |
|
|
ХСН по NYHA, n (%) |
I ФК |
2 (2,8) |
1 (1,5) |
0,981 |
|
II ФК |
4 (5,6) |
1 (1,5) |
0,380 |
|
|
III ФК |
56 (78,9) |
60 (86,9) |
0,297 |
|
|
IV ФК |
9 (12,7) |
7 (10,1) |
0,838 |
|
|
Артериальная гипертензия, n (%) |
58 (81,7) |
60 (86,9) |
0,533 |
|
|
Сахарный диабет, n (%) |
17 (23,9) |
12 (17,4) |
0,455 |
|
|
Общая ФВ ЛЖ, Мe [Q1; Q3] (%) |
50[47;53] |
51[46;55] |
0,856 |
|
|
Дефект перфузии до операции, Мe [Q1; Q3] (%) |
35 [28;39] |
37 [31;40] |
0,657 |
|
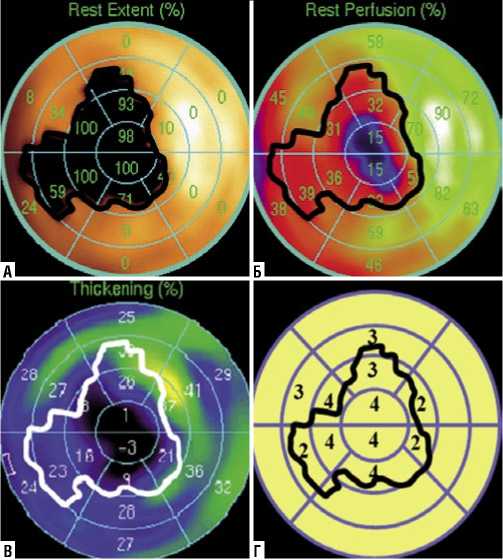
Рис. 1. Оценка перфузионно-функционального соответствия в гипопер-фузируемой зоне миокарда ЛЖ. А – дефект перфузии в покое (гипоперфузируемая зона), Б – сегментарное накопление РФП в гипоперфузируемой зоне, В – региональное СУМ в гипоперфузи-руемой зоне, Г – полуколичественный анализ регионального СУМ в гипоперфузируемой зоне с использованием балльной системы.
зоне гипоперфузии по следующему алгоритму: если в зоне выраженной гипоперфузии отмечалось выраженное снижение регионального СУМ (так называемое «соответствие»), такой миокард расценивался как нежизнеспособный. Если же в зоне выраженной гипоперфузии отмечалось умеренное снижение СУМ (так называемое «несоответствие»), такой миокард расценивался как жизнеспособный (Рис. 2).

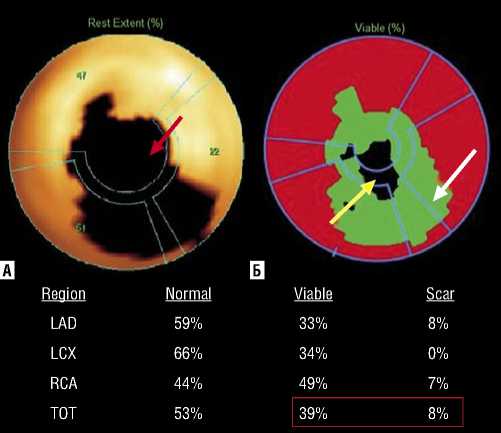
Рис. 2. Оценка объема рубца и жизнеспособного миокарда. На полярной диаграмме (А) визуализируется дефект перфузии (красная стрелка) – 47% от площади миокарда ЛЖ, зона рубца – 8% (задняя стенка с распространением на верхушку ЛЖ – желтая стрелка, Б). Большая часть гипоперфузируемой зоны представлена гиберни-рованным миокардом – 39% (передняя, передне-боковая, задняя, задне-боковая стенки ЛЖ – белая стрелка, Б).
Для более детального анализа все сегменты в зависимости от степени захвата перфузионного индикатора были классифицированы на 5 подгрупп: 1 – 61–74%; 2 – 51–60%; 3 – 41–50%; 4 – 31–40%; 5 – ≤30%
Выделены варианты ПФС в зависимости от исходного уровня перфузии и функциональной активности:
I вариант ПФС – умеренное или выраженное снижение перфузии в сочетании с умеренным снижением функциональной активности – жизнеспособные сегменты миокарда с гибернированными кардиомиоцитами в легкой или средней степени тяжести.
II вариант ПФС – умеренное или выраженное снижение перфузии в сочетании с выраженным снижением функциональной активности – жизнеспособные сегменты миокарда с кардиомиоцитами, находящимися в гибернации средней или тяжелой степени.
III вариант ПФС – выраженное снижение перфузии в сочетании с отсутствием функциональной активности – нежизнеспособные участки миокарда, соответствующие необратимым рубцовым изменениям.
Результаты синхро-ОФЭКТ миокарда ЛЖ оценивались на ранних сроках (10–14 суток) и через 6–12 месяцев после операции. В работе учитывались сцинтиграммы, выполненные в покое.
Для определения объемов гибернированного миокарда ЛЖ и необратимых рубцовых изменений в гипопер-фузируемой зоне использовали программу Corridor 4DM (GE) (США) с автоматическим полуколичественным расчетом процента нормально перфузируемой ткани от общего объема миокарда ЛЖ, зоны гибернированного миокарда и рубца (Рис. 3).
СХЕМА СОПОСТАВЛЕНИЯ ПЕРФУЗИИ И ФУНКЦИИ МИОКАРДА ЛЖ
Перфузия миокарда ЛЖ
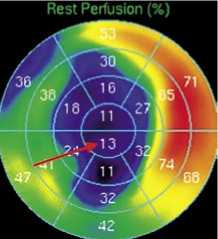
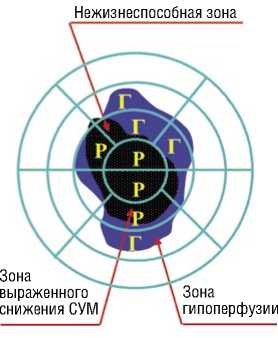
Функция миокарда ЛЖ
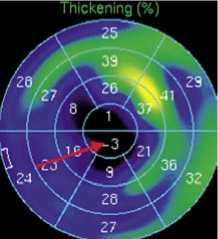
Рис. 3. Алгоритм диагностики жизнеспособного миокарда (Р – рубец, Г – гибернированный миокард, СУМ – систолическое утолщение миокарда).
■ Несоответствие ■ Соответствие
Статистический анализ
Расчет необходимого размера выборки для двусторонней альтернативной гипотезы проводился исходя из мощности 80%, частоты ошибок I рода 5% и допущения о том, что стандартизованный размер эффекта (d Коэна) равен 0.5. Оценка необходимого размера выборки: n = 64 в каждой из групп. Соответствие данных нормальному распределению оценивалось с помощью критерия Колмогорова-Смирнова в программе Statistica 12.
Количественные показатели, имеющие нормальное распределение, описывались с помощью средних арифметических величин (M) и стандартных отклонений (SD). В случае отсутствия нормального распределения количественные данные описывались с помощью медианы (Me) и нижнего и верхнего квартилей [Q1; Q3].
Для суждения о значимости различий количественных переменных в случае распределения, близкого к нормальному, использовали t-критерий Стьюдента. В тех случаях, когда распределение отличалось от нормального, анализ выполнялся с помощью непараметрического критерия Уилкоксона для связанных выборок, для независимых – U-критерия Манна-Уитни. При оценке процентных долей в двух группах проводился анализ четырехпольных таблиц сопряженности с расчетом критерия Хи-квадрат с поправкой Йейтса. Различия считались статистически значимыми при p<0,05.
Результаты
По данным радионуклидной томографии миокарда в покое, у всех 140 пациентов в обеих группах визуали-
зировались зоны гипоперфузии, соответствующие постинфарктным изменениям.
При комплексной оценке перфузионных и функциональных диаграмм было выявлено в двух группах 710 и 690 дисфункциональных сегментов, соответственно. Для более детального анализа все сегменты в зависимости от степени захвата перфузионного индикатора были классифицированы на 5 подгрупп с соответствующей балльной оценкой СУМ (Табл. 2–3).
Варианты ПФС в зависимости от исходного уровня перфузии и функциональной активности:
К I варианту ПФС (умеренное или выраженное снижение перфузии в сочетании с умеренным снижением функциональной активности) относились 427 (60,1%) сегментов (I группа) и 395 (57,2%) сегментов (II группа), т.е. сегменты, в которых уровень накопления РФП колебался от 31 до 74% (подгруппы 1-4), а функциональная активность составляла 2 балла.
Ко II варианту ПФС (умеренное или выраженное снижение перфузии в сочетании с выраженным снижением функциональной активности) включал в себя 229 (32,3%) сегментов в I группе и 240 (34,8%) сегментов во II группе, т.е сегменты 1–5 подгрупп с нарушением СУМ в 3 балла.
III вариант ПФС (выраженное снижение перфузии в сочетании с отсутствием функциональной активности) были отнесены 54 (7,6%) сегмента в I группе пациентов и 55 (8%) сегментов во II группе, т.е. все гипо- и апер-фузируемые сегменты (3-5 подгруппы) с региональным СУМ в 4 балла.
Динамика восстановления гибернированного миокарда
Объем гибернированного миокарда ЛЖ в раннем послеоперационном периоде уменьшился с 29 [20; 35]% до 17 [10; 25]% в I группе (р<0,0001) и с 27 [20; 34]% до 18 [10; 26]% во II группе (р<0,0001) между собой группы статистически значимо не различались (р = 0,25). В отдаленном послеоперационном периоде (6–12 месяцев) в I группе определялось статистически значимо меньший объем гибернированного миокарда: 10 [5; 12]% (I группа), 21 [14; 25]% (II группа) (р = 0,0002).
Сегментный анализ динамики перфузии и функции
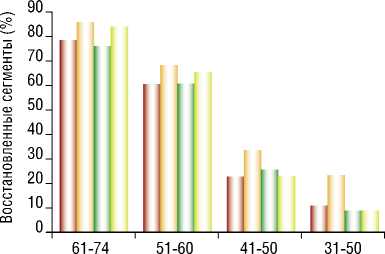
Значимое улучшение сократимости в раннем послеоперационном периоде в I группе отмечалось преимущественно в 1 и 2 подгруппах: 78,8% (n = 160) сегментов (1 подгруппа), 60,3% (n = 132) сегментов (2 подгруппа); через 6–12 месяцев после операции отмечалось восстановление 85,7% (n = 174) сегментов (1 подгруппа) и 68,3% (n = 153) сегментов (2 подгруппа); в 3 подгруппе улучшение функции отмечено в 22,7% (n = 42) сегментов (ранний послеоперационный период) и 33,5% (n = 62) сегментов (отдаленный послеоперационный период); улучшение в 4 подгруппе было в 10,7% (n = 6) сегментов (ранний послеоперационный период) и 23,2% (n = 13) сегментов (отдаленный послеоперационный период); в 5 подгруппе улучшения сократимости выявлено не было (Рис. 4).
Табл. 2. Исходное распределение дисфункциональных сегментов в гипо-перфузируемых зонах в зависимости от уровня накопления РФП в I группе
|
Подгруппы |
Сегментарное накопление РФП, % |
Дисфункциональные сегменты, n |
Всего |
||
|
2 балла |
3 балла |
4 балла |
|||
|
1 |
61–74 |
169 |
34 |
– |
203 |
|
2 |
51–60 |
171 |
53 |
– |
224 |
|
3 |
41–50 |
82 |
99 |
4 |
185 |
|
4 |
31–40 |
5 |
32 |
19 |
56 |
|
5 |
≤ 30 |
– |
11 |
31 |
42 |
|
Всего, n (%) |
427 (60,1) |
229 (32,3) |
54 (7,6) |
710 |
|
Табл. 3. Исходное распределение дисфункциональных сегментов в гипо-перфузируемых зонах в зависимости от уровня накопления РФП во II группе
|
Подгруппы |
Сегментарное накопление РФП,% |
Дисфункциональные сегменты, n |
Всего |
||
|
2 балла |
3 балла |
4 балла |
|||
|
1 |
61–74 |
144 |
36 |
– |
180 |
|
2 |
51–60 |
165 |
70 |
– |
235 |
|
3 |
41–50 |
79 |
94 |
5 |
178 |
|
4 |
31–40 |
7 |
35 |
15 |
57 |
|
5 |
≤ 30 |
- |
5 |
35 |
40 |
|
Всего, n (%) |
395 (57,2) |
240 (34,8) |
55 (8,0) |
690 |
|
Сегментарное накопление РФП (подгруппы)
I I I группа 10-14 сут. п/о I I II группа 10-14 сут. п/о
I группа 6-12 мес. п/о II группа 6-12 мес. п/о
Рис. 4. Динамика изменения сократимости сегментов с различным накоплением РФП в исследуемых группах.
Во II группе в 1 подгруппе отмечалось восстановление 76,1% (n = 137) сегментов (ранний послеоперационный период), 83,9% (n = 151) сегментов (отдаленный послеоперационный период); во 2 подгруппе: 60,9% (n = 143) сегментов (ранний послеоперационный период) и 65,5% (n = 154) сегментов (отдаленный послеоперационный период); в 3 подгруппе улучшение функции составило 25,3% (n= 45) сегментов (ранний послеоперационный период) и 23,0% (n = 41) сегментов (отдаленный послеоперационный период); в 4 подгруп-
пе – 8,7% (n = 5) сегментов (ранний послеоперационный период) и 8,7% (n = 5) сегментов (отдаленный послеоперационный период); в 5 подгруппе улучшения сократимости выявлено не было (Рис. 4). При сравнении между I и II группами отмечена тенденция к улучшению сократимости в отдаленные сроки у пациентов после КШ+ЮрЛеон, в отличие от изолированного проведения КШ, особенно в подгруппах с изначальным накоплением РФП 31–50% и 41–50%.
Степень гибернации клинически определяется скоростью восстановления региональной функции миокарда после полной реваскуляризации. По нашим данным, можно выделить три степени гибернации: легкая (полное восстановление функции «спящего» миокарда в раннем послеоперационном периоде, средняя (полное восстановление в течение 6–12 месяцев), тяжелая (частичное улучшение сократительной способности в течение 12 месяцев) (Рис. 5).
Оценка восстановления функции ассоциаций кардиомиоцитов в зависимости от вариантов ПФС
Сократительная способность миокарда ЛЖ существенно улучшилась при I варианте ПФС: из 427 сегментов в I группе пациентов улучшение сократимости произошло в 72,6% (n = 310) в раннем послеоперационном периоде и в 74,9% (n = 320) в отдаленном послеоперационном периоде. Во II группе пациентов из 395 сегментов улучшение сократимости гибернированного миокарда произошло в 69,4% (n = 274) в раннем послеоперационном периоде и в 64,8% (n = 256) в отдаленном послеоперационном периоде, отмечено ухудшение функции в 18 сегментах. При сравнении групп, отмечены значимые статистические различия в отдаленном послеоперационном периоде (Хи-квадрат с поправкой Йейтса – 9,566, р = 0,002). В сегментах с таким вариантом ПФС кардиомиоциты находились в гибернации легкой или средней степени.
При II варианте ПФС из 229 сегментов в I группе в раннем послеоперационном периоде улучшили сократимость 16,2% (n = 37) сегментов, в течение 6–12 месяцев после операции – 26,6% сегментов (n = 61). Во II группе из 240 сегментов в раннем послеоперационном периоде улучшение сократительной способности отмечено в 18,3% сегментов (n = 44), и в отдаленном – лишь 14,6% сегментов (n = 35). При сравнении групп, отмечены значимые статистические различия в отдаленном послеоперационном периоде (Хи-квадрат с поправкой Йейтса – 9,732, р = 0,002). В сегментах с таким вариантом ПФС кардиомиоциты находились в гибернации средней или тяжелой степени.
Анализ динамики вариантов перфузионно-функционального соотношения показал, что при III варианте ПФС в обеих группах больных ни один сегмент не улучшил сократительную способность после реваскуляризации. Большая часть сегментов была представлена рубцом.
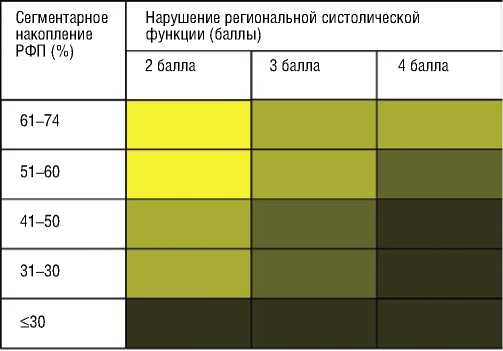
легкая средняя тяжелая нежизне-
□ степень □ степень □ степень ■ способный гибернации гибернации гибернации миокард
Рис. 5. Степени гибернации.
Оценка динамики общей фракции выброса ЛЖ
Общая ФВ в раннем послеоперационном периоде выросла с 50 [47; 53]% до 53 [52; 55]% (I группа) (р<0,0001), с 51 [46; 55]% до 54 [52; 56]% (II группа) (р<0,0001). Группы между собой статистически значимо не различались (р = 0,088). Через 12 месяцев в I группе отмечалось увеличение ФВ ЛЖ до 56 [54; 59] (р<0,0001), во II группе значимых изменений не произошло, ФВ ЛЖ – 53 [51; 57]% (р = 0,46). При сравнении показателей глобальной сократимости миокарда в отдаленные послеоперационные сроки выявлены статистически значимые различия (р<0,0001) (Рис. 6).
В качестве примеров приводим результаты обследования и лечения пациентов с ИБС и диффузным поражением коронарного русла.
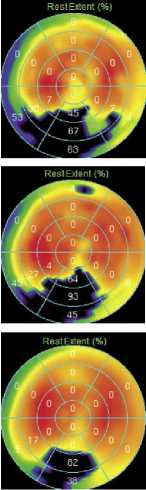
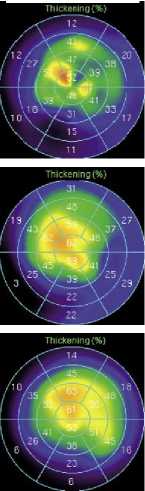
Пациент из I группы. У пациента К., 62 лет до операции, по данным синхро-ОФЭКТ миокарда ЛЖ в покое, визуализировался дефект перфузии в области задней стенки и задней части межжелудочковой перегородки (МЖП) с распространением на задне-боковую стенку ЛЖ. Объем гибернированного миокарда – 24%. На 10 сутки после
% 57^
55_
53 _
51 _
49 _
56%
Рис. 6.
54%
53%
53%
51%
50%
До операции
10-14 сут. 12мес.
после операции после операции
I группа
II группа
Динамика фракции выброса ЛЖ в исследуемых группах.
комплексной реваскуляризации (КШ+ЮрЛеон) при повторном проведении исследования отмечается улучшение перфузии в покое и уменьшение объема гибер-нированного миокарда до 18% (за счет восстановления сегментов, находящихся в легкой степени гибернации). При контрольном обследовании через 12 месяцев после операции отмечена положительная динамика: объем ги-
бернированного миокарда уменьшился до 8% (отмечено восстановление сегментов, находящихся в гибернации средней и тяжелой степени) (Рис. 7).
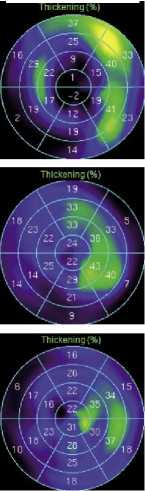
Пациент из II группы. У пациента Т., 65 лет до операции, по данным синхро-ОФЭКТ миокарда ЛЖ в покое, визуализируется дефект перфузии в области верхушки передней стенки и передней части МЖП
До операции
10 сутки после операции
12 месяцев после операции
Перфузия в покое
Региональная функция в покое
Оценка жизнеспособности миокарда ЛЖ в гипоперфузируемой зоне
|
7 |
Region |
Normal |
Viable |
Scar |
|
|
LAD |
99% |
1% |
0% |
||
|
LCX |
76% |
24% |
0% |
||
|
RCA |
21% |
61% |
18% |
||
|
TOT |
73% |
24% |
3% |
|
Region |
Normal |
Viable |
Scar |
|
|
LAD |
99% |
1% |
0% |
|
|
LCX |
91% |
9% |
0% |
|
|
RCA |
46% |
51% |
3% |
|
|
TOT |
82% |
17% |
1% |
|
Region |
Normal |
Viable |
Scar |
||
|
LAD |
100% |
0% |
0% |
||
|
— |
LCX |
100% |
0% |
0% |
|
|
RCA |
60% |
40% |
0% |
||
|
TOT |
92% |
8% |
0% |
Рис. 7. Полярные диаграммы миокарда ЛЖ больного К., 62 л., исходно и в различные сроки после КШ, дополненного методикой ЮрЛеон (пояснение в тексте).
До операции
9 сутки после операции
12 месяцев после операции
Перфузия в покое

Региональная функция в покое
Оценка жизнеспособности миокарда ЛЖ в гипоперфузируемой зоне
|
Region |
Normal |
Viable |
Scar |
||
|
/ A |
LAD |
43% |
54% |
3% |
|
|
r |
LCX |
95% |
5% |
0% |
|
|
RCA |
100% |
0% |
0% |
||
|
\ \ |
|||||
|
TOT |
72% |
27% |
1% |
||
|
Region |
Normal |
Viable |
Scar |
||
|
LAD |
80% |
20% |
0% |
||
|
LCX |
100% |
0% |
0% |
||
|
RCA |
100% |
0% |
0% |
||
|
TOT |
92% |
7% |
1% |
||
|
^7 |
Region |
Normal |
Viable |
Scar |
|
|
Ш |
LAD |
74% |
23% |
3% |
|
|
LCX |
100% |
0% |
0% |
||
|
у |
RCA |
100% |
0% |
0% |
|
|
^7 |
TOT |
89% |
10% |
1% |
|
Рис. 8. Полярные диаграммы миокарда ЛЖ больного Т., 65 л., исходно и в различные сроки после операции КШ (пояснение в тексте).
с распространением на передне-боковую стенку ЛЖ объемом 28% от площади миокарда ЛЖ. Объем гибер-нированного миокарда – 27%. Через 9 дней после КШ отмечается положительная динамика – уменьшение объема гибернированного миокарда до 7% (за счет восстановления сегментов, находящихся в легкой степени гибернации). Через год восстановления сегментов, находящихся в гибернации средней и тяжелой степени не выявлено, отмечена отрицательная динамика (Рис. 8).
Обсуждение
Диагностика гибернированного миокарда до операции и оценка динамики его восстановления после реваскуляризации у пациентов с ИБС на протяжении многих лет остается актуальной проблемой. В отличие от результатов ранних ретроспективных исследований, современные данные не могут строго подтвердить однозначность и необходимость выявления жизнеспособности миокарда у всех пациентов [19–21].
Однако с увеличением количества больных с диффузным поражением коронарного русла, у которых ограничение объема шунтирования является вынужденным решением, появилась особая необходимость индивидуального подхода к визуализации жизнеспособного миокарда ЛЖ и последующему их лечению [22]. Внедрение в клиническую практику метода стимуляции экстракардиального неоангиогенеза «ЮрЛеон» позволило значительно расширить возможности лечения таких больных [23].
Стоит отметить, что не только восстановление функции гибернированного миокарда после операции является основным механизмом, влияющим на прогноз у этой категории пациентов, но и предотвращение дальнейшего его повреждения, а также снижение риска жизнеугрожающих нарушений ритма [16]. Сохраненная общая ФВ ЛЖ при наличии значимой зоны гиберниро-ванного миокарда обеспечивается «мобилизационным режимом» работы оставшихся функционирующих кардиомиоцитов. Переход от «поочередного режима» к «мобилизационному» со временем истощит миокарда, при таких условиях отсутствие своевременной комплексной реваскуляризации приведет в дальнейшем к ухудшению функции сердца, то есть к усугублению тяжести сердечной недостаточности [24–26].
Определение объема жизнеспособного миокарда является недостаточным для формирования оптимального прогноза восстановления функции, необходимо углубленное изучение степени тяжести гибернации, посегментарный анализ перфузии и функции ЛЖ. В нашем исследовании рассмотрены группы пациентов с диффузным поражением венечного русла, у которых шунтирование коронарных артерий в полном объеме ограничено, это увеличивает риск «недостаточности» перфузии для восстановления гибернированного миокарда. Дополнение прямой реваскуляризации миокарда методом «ЮрЛеон» позволило в отдаленные сроки улучшить сократительную способность сердца за счет восстановления зон жизнеспособного миокарда, даже находящегося в более тяжелом состоянии, для восстановление которого необходимо больший временной промежуток. Формирование эктракардиальных коллатералей обеспечило дополнительную перфузию и возможность к улучшению сократимости.
Многолетние и многочисленные наблюдения подтверждают эффективность дополнения КШ методикой экстракардиальной стимуляции неоангиогенеза, в том числе для большего восстановления гибернированного миокарда в отдаленные послеоперационные сроки. Таким образом, прямая хирургическая реваскуляризация, дополненная методом «ЮрЛеон», обеспечивает наиболее оптимальные условия для последующего выхода кардиомиоцитов из состояния гибернации и восстановления нормальной работы сердца.
Современное применение концепции визуализации жизнеспособного миокарда у пациентов с ИБС основано на комплексном подходе к предоперационной диагностике с учетом данных ангиографии для определения анатомического соответствия между жизнеспособными сегментами и сосудами, пригодными для реваскуляризации, то есть для прогнозирования исходов, выбора тактики лечения, и последующей оценки результатов комплексной терапии, особенно это актуально у пациентов с диффузным поражением коронарного русла.
Ограничениями нашего исследования была небольшая выборка пациентов; одноцентровой характер; отсутствие сравнительных данных с результатами позитронно-эмиссионной томографии сердца у пациентов с диффузным поражением коронарного русла при определении объема гибернированного миокарда и динамики его восстановления.
Заключение
Сцинтиграфическая оценка жизнеспособности миокарда является важным критерием выбора тактики лечения больных ИБС, особенно с диффузным поражением коронарного русла. Дополнение коронарного шунтирования методикой стимуляции экстракардиального неоангиогенеза позволяет увеличить восстановление функции большего объема гибернированного миокарда и значительно улучшить отдаленные результаты комплексного лечения пациентов.


