Дифференциальная экспрессия гена NRG1 в церебральных структурах у крыс Wistar при формировании пространственной памяти
Автор: Грудень М.А., Ратмиров А.М., Сторожева З.И.
Журнал: Академический журнал Западной Сибири @ajws
Рубрика: Эксперимент
Статья в выпуске: 1 (72) т.14, 2018 года.
Бесплатный доступ
В релевантных структурах мозга крыс-самцов Wistar, обученных пространственному навыку исследовали экспрессию гена NRG1, белковый продукт которого нейрегулин-1 вовлечен в ряд важных физиологических процессов, в частности в регуляцию процессов нейрогенеза, Показано, что физическая нагрузка и изменение эмоционального состояния в процессе принудительного плавания без обучения в водном лабиринте угнетает на 88 -96% активность гена NRG1 в гиппокампе, префронтальной коре и мозжечке. При этом, формирование пространственной памяти было ассоциировано с восстановлением экспрессии гена NRG1 и образованием специфического межструктурного ансамбля транскрипционной активности гена NRG1. Максимальный уровень экспрессии гена NKG1 обнаружен в коре (на 200%) и мозжечке (460%) у обученных животных с формированной долговременной памяти по сравнению с контролем.
Экспрессии гена nkg1, пространственная память, гиппокамп
Короткий адрес: https://sciup.org/140225987
IDR: 140225987
Differential expression of the NRG1 gene in cerebral structures during the formation of the spatial memory in Wistar rats
Neuroregulin-1, the protein product of NRGlgene expression, is involved in a number of essential physiological processes, notably the regulation of neurogenesis which may have implications in processes of memory formation. Consequently, expression of the NRGlgene was studied in designated brain structures of male Wistar rats that were trained in a spatial memory skill (water maze). It was shown that both the burdens of physical load and emotional state in the form of forced swimming without training in the water maze inhibited at 88 -96% the activity of the NRG1 gene not only in the hippocampus, but also the prefrontal cortex and cerebellum as well. In conjunction with this, the formation of spatial memory was associated with restoration of NRG1 gene expression and the formation of a specific interstructural ensemble of the transcriptional activity of the NKGlgene. In this connection, it was documented that the maximum level of expression of the NRG1 gene was found in the cortex (200%) and cerebellum (460%) in trained animals.
Текст научной статьи Дифференциальная экспрессия гена NRG1 в церебральных структурах у крыс Wistar при формировании пространственной памяти
Исследование процессов долговременной памяти продолжает быть одной из актуальных проблеем нейробиологии [14]. На современном этапе значительное внимание при изучении данного вопроса уделяется процессам нейрогенеза в обеспечении различных видов поведения и памяти c фокусированием на особенностях их генетической регуляции [1, 2, 9]. К настоящему времени большинство экспериментальных работ указанного аспекта посвящены исследованиям экспрессии ранних генов
-
[5 ] или, как в случае генов – регуляторов нейрогенеза, лишь в одной из релевантных церебральных структур – гиппокампе [4]. При этом, имеются единичные данные о структурно-функциональной сопряженности процессов пролиферации / дифференцировки / гибели нервных клеток и механизмов их генетической регуляции в различных структурах мозга у взрослых крыс при формировании долговременной памяти [3, 4].
Теоретический и практический интерес представляет изучение активности генов, кодирующие белки, которые вовлечены в механизмы дифференциации нервных и глиальных клеток, а также другие процессs нейронального развития и пластичности. Интерес вызывает исследования, направленные на изучение особенностей реактивации экспрессии данных генов при формировании долговременной памяти. Одним из интереснейших семейств генов, вовлеченных в данные процессы, являются гены семейства NRG, продуктами которых являются белки нейрегулины, выполняющие разнообразные функции в процессе развития нервной системы [11]. Нейрегулины связаны с эпидермальным фактором роста (Epidermal Growth Factor, EGF). У млекопитающих обнаружено 4 гена NRG – NRG1, NRG2, NRG3, NRG4, каждый из которых кодирует свою группу белков – нейрегулины-1, нейрегулины-2, нейрегулины-3 и нейрегулины-4. Наиболее изученной и разнообразной является группа нейрегулинов-1 (NКG1) [17]. Белок NRG1 является фактором роста, связанным напрямую с развитием и пластичностью нервной системы, при этом, NКG1/erbB сигнальный путь регулирует не только нейрональное развитие, но и миграцию, миелинизацию, а также функционально поддерживает работу синапсов [7]. Обнаружено, что активность генов данного семейства NКG1также вовлечена в ряд патогенетических процессов при нарушениях регуляции нервной системы. Так, NКG1 ген был идентифицирован как часть генома ассоциированная с таким заболеванием как шизофрения, при которой нарушается процессы памяти [18]. Нейрегулины передают свои сигналы клеткам-мишеням, взаимодействуя с трансмембранными рецепторами тирозинкиназы семейства ErbB. В это семейство входят четыре члена - рецептор эпидермального фактора роста (EGF-R, ErbB1, ErbB2, ErbB3 и ErbB4). Рецепторнолигандное взаимодействие с участием NКG1 индуцирует гетеродимеризацию рецепторных мономеров, что, в свою очередь, приводит к активации внутриклеточных сигнальных каскадов и индукции клеточных ответов, включая пролиферацию, миграцию, дифференцировку, выживание или апоптоз. In vivo, функциональные рецепторы NRG1 представляют собой гетеродимеры, состоящие из ErbB2 с молекулой ErbB3 или ErbB4. Ткане-специфическое распределение различных типов рецепторов дополнительно способствует разнообразию и специфич- ности биологических функций этого сигнального пути. Это типичная особенность прохождения сигнала через NRG1/ErbB для контроля последовательных этапов во время развития конкретной системы органов. Например, данный сигнальный путь функционирует на стадии ранней пролиферации, созревании клеток-предшественников, а также при миелинизации клеток Шванна [6].
Исследования вовлеченности гена NКG1 в процессы обучения и памяти немногочисленны. Имеются данные с использованием в качестве модели генетически модифицированных мышей-самцов Akt1 (+/-), NКG (+/-) которые как и двойные мутантные животные сравнивались с их контролями по типу дикого типа (WT). В условиях Akt1 и NКG1 -белкового дефицита обнаружили нарушение эпизодической памяти и социального поведения [10].
Целью настоящей работы явилось сравнительное изучение особенностей экспрессии NRG1 гена в релевантных структурах мозга: гиппокампе, мозжечке и префронтальной коре мозга у половозрелых крыс *Wistar, обученных пространственному навыку в водном лабиринте, а также у подвергнувшихся принудительному плаванию и интактных животных.
Методы исследования.
Эксперименты были выполнены на крысах-самцах Wistar (n=36, 3-х месячного возраста и массой 250,0±15,0 г.), которые содержались в стандартных условиях при свободном доступе к пище и воде, а также 12-ти часовом световом режиме при соблюдении этических норм работы с экспериментальными животными, сформулированных Советом Европейского сообщества об использовании животных для экспериментальных исследований (Директива 86/609/EEC в пересмотре от 14.11.2005). Поведенческие эксперименты на животных были проведены с использованием пространственного водного лабиринта Морриса (Columbus Instruments, USA) по протоколу, описанному ранее [9]. Крысы были разделены на 3 группы: 1 гр. – интактные животные (n=12), 2 гр. – группа «активного контроля-принудительное плавание без платформы » (n=12), 3 гр. — «обученные в водном лабиринте Морриса» животные (n=12). Экспериментальный протокол составлен таким образом, что время принудительного плавания в группе активного контроля соответствовало времени, проведенному в воде обучавшимся животным, т.е. каждому обучавшемуся животному по времени и паттерну плавания соответствовала одна “контрольная” особь. Через 24 ч по окончании поведенческих экспериментов всех крыс декапитировали, извлекали на холоду (+4ºС) структуры мозга: гиппокамп, префронтальную кору и мозжечок, которые использовали для изучения экспрессии гена NRG1 методом ПЦР в режиме реального времени по описанному ранее протоколу [9], применяя в качестве референсного гена – ген β- актина для последующего расчёта относительно
-ΔΔCt уровня экспрессии изучаемых генов по методу 2
-
[12 ]. Уровень экспрессии гена NRG1 в 2-ой и 3-й группах был подсчитан относительно данных их экспрессии у интактных животных. На Рис. 2 экспрессия изучаемого гена NRG1 у обученных животных представлена в % от таковой у животных из группы «активный контроль».
Статистическую обработку полученных результатов проводили по алгоритмам программы “Statis-tica 7,0”. При сравнении нескольких независимых выборок применяли однофакторный непараметрический дисперсионный анализ по методу Крускал-ла-Уолиса (Н-критерий) с последующим post-hoc анализом по U-критерию Манна-Уитни. Критическое значение уровня статистической значимости при проверке нулевых гипотез принималось равным величине 0,05.
Результаты и обсуждение.
В ходе проведенных поведенческих экспериментов по формированию долговременной пространственной памяти показано, что среднее значение времени достижения платформы у крыс во втором и всех последующих сеансах было достоверно ниже, чем в первом ( р <0,01–0,05), а к концу 4-го сеанса обучения (4 день) значения времени достижения платформы были меньше 10 сек ( р <0,01), что свидетельствует о формировании стабильной долго временной пространственной памяти (рис. 1).
В исследованиях транскрипционной активности изучаемого гена NRG1 были обнаружены значимые различия в уровне его экспрессии в гиппокампе, префронтальной коре и мозжечке животных в группах «активного контроля» и «обучения». Так, анализ межструктурной экспрессии гена NRG1 у животных, подвергнувшихся принудительному плаванию в водном лабиринте без платформы документировал подавление активности гена NRG1при принудительном плавании (физической нагрузке в воде) как в гиппокампе, так и мозжечке до 3% и 5% (p<0,01), соответственно, по сравнению с интактными крысами. Выявлено, что в префронтальной коре у этих животных сохраняется 30% (p<0,05) от контроля активных копий NRG1 гена. В группе крыс с формированной долговременной пространственной памятью структурный паттерн экспрессии изучаемого гена NRG1 отличается от такового у животных, которых принуждали к плаванию в водном лабиринте без платформы. Активность гена NRG1 в гиппокампе обученных животных помнящих расположение платформы составила 75% от нативного контроля, а в других церебральных структурах превысила активность гена NRG1 у интактных животных на 200% и 460% (p<0,001) в префронтальной коре в мозжечке, соответственно (рис. 2).
Таким образом, физическая нагрузка в виде принудительного плавания без обучения в водном лабиринте Морриса и эмоциональное состояние животных индуцируют подавление активности NRG1 гена как в гиппокампе, так и в двух других изучаемых структурах (префронтальной коре и мозжечке) взрослых крыс Wistar. 4-х-дневное обучение животных нахождению платформы в водном лабиринте привело к формированию долговременной пространственной памяти, что было ассоциировано с тенденцией возвращения уровня экспрессии гена NRG1 к таковому у интактных крыс и активацией экспрессии данного гена в других двух структурах.
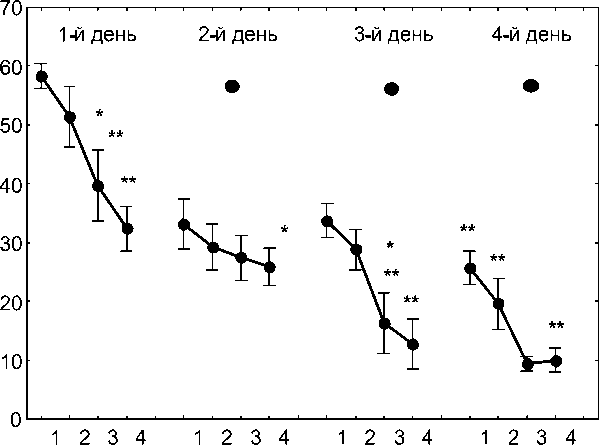
Рис. 1. Формирование долговременной пространственной памяти у половозрелых крыс Wistar в водном лабиринте Морриса (по оси абсцисс – номер пробы, по оси ординат – время достижения платформы (с); * - p <0,05, ** - p <0,01 по сравнению с первой пробой соответствующего дня; • - статистически значимое (p<0,05) снижение среднего значения по всем пробам относительно аналогичного показателя предыдущего дня).
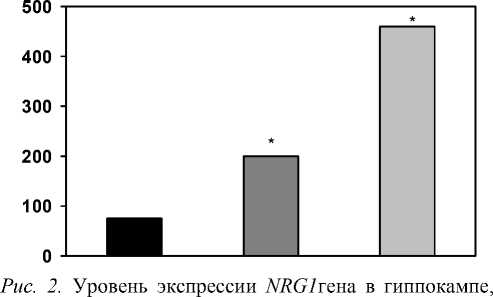
префронтальной коре и мозжечке у обученных пространственному навыку в водном лабиринте
Морриса половозрелых крыс Wistar в % от уровня их экспрессии в соответствующих структурах у животных группы «активного контроля» (по оси абсцисс – структуры мозга, по оси ординат – % от активного контроля. Черный столбик – Гиппокамп, средний – префронтальная кора, светло серый столбик – мозжечок; * p <0,01 по сравнению с гиппокампом).
Можно предположить, что помещение экспериментальных животных в незнакомую ранее им среду (воду) и многодневное нахождение в ней без платформы, олицетворяющую твердую поверхность привело крыс к эмоциональному напряжению и стрессу, вызвало элементы страха и тревожности, а также физическое перенапряжение. Эмоциональная и физическая нагрузка явились негативными сигналами геному, в частности, выразившимися в ингибировании активности гена NRG1 и, вероятно, последующему снижению содержания белка нейре-гулина I. Ранее было показано, что снижение в мозге крыс формы белка нейрегулина I (тип II NRG1) не ведет к нарушению памяти в водном лабиринте Морриса, но имеется дефицит памяти в модели пищевого поведения на визуоскопическую дискриминацию. Крысы со сниженной концентрацией белка NRG1 в данном тесте совершили больше опорных и рабочих ошибок. Эти результаты показывают, что снижение типа II NRG1 в головном мозге может привести к дефициту в визуоскопическом обучении и памяти [15] .
Имеются данные о том, что экспрессия другой изоформы типа I NRG1 в гиппокампе увеличивается при шизофрении [8]. Генная активация влияет на гипокампальные функции и эффекты, вероятно, опосредуются через ингибирующие интернейроны. Тем не менее, данные, полученные с использованием других генетических и фармакологических манипуляций, подчеркивают сложную и плейотроп-ную природу NRG1гена даже в отношении различных изоформ белка. Имеются также данные о том, что NRG1 и его рецепторная тирозинкиназа ErbB4 имеют решающее значение для поддержания ГАМК-ергической активности в другой структуре мозга - амигдале, а ингибирующая нейротрансмис- сия в данной структуре мозга важна для выработки страха и формирования памяти. Нейтрализация эндогенного белка NRG1, ингибирование его синтеза или генетическая изоляция его белкового партнера по сигнальному пути белкаErbB4 в амигдале приводили к уменьшению ГАМК-ергической передачи, влияя на состояние кондиционирования животных, что вероятно, может привести к нарушениям памяти и возникновению тревожности и страза у животных [13]. На основании этих данных, можно предположить участие амигдалы мозга и в наших экспериментах, наряду с другими структурами в формировании эмоционального статуса крыс, подвергавшихся принудительному плаванию и, у которых обнаружено ингибирование экспрессии NRG1 гена во всех исследованных церебральных структурах. Тем не менее, мало известно о вкладе передачи сигналов NRG1/ErbB4 в гиппокампе, ассоциированных с функцией обучения и памяти. Имеются данные по количественному ПЦР в реальном времени оценки уровней мРНК белка NRG1 после фармакологических и генетических манипуляций, где было обнаружено, что пространственное обучение уменьшает экспрессию NRGI гена в гиппокампе. Блокада передачи сигналов NRG1 / ErbB4 в гиппокампе в поле CA1 могла быть связана путем нейтрализации эндогенной активности NRG1, либо ингибирующей / абляционной активности рецептора ErbB4, усиленного Гиппокамп - зависимым пространственным обучением, а также пространственной рабочей памяти и новой памяти распознавания объектов [16]. Таким образом, было подтверждено, что воздействие на сигнальный путь NRG1/ErbB4 выявляет важную роль NRG1/ErbB4 активности в гиппокампе для процессов обучения и памяти. В настоящей работе, было показано, что ингибирование активности NRG1гена происходило в дни адаптации животных к новым условиям выживания, а именно в водной среде, когда происходит модуляция эмоционального их статуса и включаются адаптационные механизмы. Сам процесс формирования долговременной памяти в процессе обучения нахождения скрытой платформы в водном лабиринте в большей степени связан с тенденцией нормализации активности NRG1гена в гиппокампе и резкой активацией экспрессии данного гена в префронтальной коре. Возрастание активности NRG1гена в мозжечке отражает не только увеличение двигательной активности животных на стадии обучения и тестирования, но и вовлеченность данной структуры мозга непосредственно в структурно-функциональные механизмы формирования пространственной памяти. Обнаруженный специфический межструктурный паттерн экспрессии NRG1гена отражает передачу памятного следа первоначально сформированного в гиппокампе другим структурам в процессе его фиксации. Документированные в настоящей работе данные хорошо согла- суются с результатами молекулярно - клеточных исследований, проведенных нами ранее на половозрелых крысах-самцах Wistar в аналогичных экспериментальных условиях. В частности, было показано, что в гиппокампе, префронтальной коре и мозжечке мозга образуются клетки, которые дифференцируются в нейроны и астроциты. При этом, имеются значимые региональные различия выраженности и динамики пролиферации, дифференцировки и апоптотической гибели вновь образованных клеток [3], что тоже может связано с дифференциальной экспрессией NRG1гена, белковый продукт которого является фактором роста.
Таким образом, получены принципиально новые данные о специфической активации NRG1 гена -регулятора нейрогенеза в различных структурах мозга у половозрелых крыс Wistar при формировании и упрочении долговременной пространственной памяти.
Список литературы Дифференциальная экспрессия гена NRG1 в церебральных структурах у крыс Wistar при формировании пространственной памяти
- Грудень М.А., Сторожева З.И., Ратмиров А.М., Шерстнев В.В. Паттерн экспрессии генов Notch2, Numb и Cas8 в релевантных структурах мозга крыс при формировании пространственной памяти//Бюллетень экспериментальной медицины и биологии. -2017. -№ 6. -С. 751-755.
- Грудень М.А, Ратмиров А.М., Соловьева О.А, Шерстнев В.В. Генетическая регуляция активности калиевых каналов типа kir в различных отделах мозга при формировании пространственной памяти у половозрелых крыс//Академический журнал Западной Сибири. -2017. -Т. 13, № 1 (68). -С. 72-73.
- Шерстнёв В.В., Голубева О.Н., Грудень М.А., Сторожева З.И., Гусева Е.В. Нейрогенез и нейроапоптоз в различных отделах зрелого мозга крыс Wistar//Нейрохимия. -2012. -Т. 29, № 3. -С. 206-212.
- Aimone J.B., Li Y., Lee S.W., Clemenson G.D. et al. Regulation and function of adult neurogenesis: from genes to cognition//Physiol. Rev. -2014. -V. 94, № 4. -Р. 991-1026.
- Barry D.N., Commins S. Imaging spatial learning in the brain using immediate early genes: insights, opportunities and limitations//Rev. Neurosci. -2011. -V. 22, № 2. -Р. 131-142.
- Britsch S. The neuregulin-I/ErbB signaling system in development and disease//Adv. Anat. Embryol. Cell. Biol. -2007. -№ 90. -Р. 61-65.
- Chen Y.J., Johnson M.A., Lieberman M.D. et al. Type III neuregulin-1 is required for normal sensorimotor gating,memory-related behaviors, and corticostriatal circuit components//J. Neurosci. -2008. -V. 28, № 27. -Р. 6872-6883.
- Deakin I.H., Nissen W., Law A.J. et al. Transgenic overexpression of the type I isoform of neuregulin 1 affects working memory and hippocampal oscillations but not long-term potentiation//Cereb. Cortex. -2012. -V. 7. -P. 1520-1529.
- Gruden M.A., Storozheva Z.I., Sewell R.D. et al. Distinct functional brain regional integration of Casp3, Ascl1 and S100a6 gene expression in spatial memory.//Behav. Brain Res. -2013. -V.252. -P.230-238.
- Huang C.H., Pei J.C., Luo D.Z. et al. Investigation of gene effects and epistatic interactions between Akt1 and neuregulin 1 in the regulation of behavioral phenotypes and social functions in genetic mouse models of schizophrenia//Front. Behav. Neurosci. -2015. -V. 8. -P. 455-467.
- Krug A., Markov V., Krach S. et al. The effect of Neuregulin 1 on neural correlates of episodicmemory encoding and retrieval//Neuroimage. -2010. -V. 53, № 3. -Р. 985-991.
- Livak K.J., Schmittgen T.D. Analysis of relative gene expression data using real-time quantitative PCR and the 2(-Delta Delta C(T))//Method. Methods. -2001. -V. 25, № 4. -Р. 402-408.
- Lu Y., Sun X.D., Hou F.Q. et al. Maintenance of GABAergic activity by neuregulin 1-ErbB4 in amygdala for fear memory//Neuron. -2014. -V. 84, № 4. -Р. 835-846.
- Pastotter B., Tempel T., Bauml K.T. Long-Term Memory Updating: The Reset-of-Encoding Hypothesis in List-Method Directed Forgetting//Front. Psychol. -2017. -V. 8. -P. 2076.
- Taylor A.R., Taylor S.B., Koenig J.I.The involvement of Type II Neuregulin-1 in rat visuospatial learning and memory//Neurosci. Lett. -2012. -V. 531, № 2. -Р. 131-135.
- Tian J., Geng F., Gao F. et al. Down-Regulation of Neuregulin1/ErbB4 Signaling in the Hippocampus Is Critical for Learning and Memory//Mol. Neurobiol. -2017. -V. 54, № 6. -Р. 3976-3987.
- Willem M. Proteolytic processing of Neuregulin-1//Brain Res. Bull. -2016. -V. 126 (Pt 2). -P. 178-182.
- Zhang Z., Huang J., Shen Y., Li R. BACE1-Dependent Neuregulin-1 Signaling: An Implication for Schizophrenia//Front. Mol. Neurosci. -2017. -V. 10. -P. 302.


