Дифференцированный подход к назначению ингибиторов ангиогенеза при диабетическом макулярном отеке
Автор: Шишкин М.М., Юлдашева Н.М., Антонюк С.В., Юсупов А.Ф., Музаффаров У.Р.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.6, 2011 года.
Бесплатный доступ
Проведено наблюдение за состоянием глаз (n=77) 68 больных сахарным диабетом, у которых диагностирована непролиферативная диабетическая ретинопатия и диабетический отек макулы без (группа I) и с наличием (группа II) признаков витреомакулярных тракций (ВМТ). Методы исследования: визометрия, биомикроофтальмоскопия, флюоресцентная ангиография, оптическая когерентная томография. Всем пациентам интравитреально введен ингибитор ангиогенеза (Бевацизумаб - 2,5 мг). В послеоперационном периоде отмечено улучшение зрительных функций и уменьшение общего объема сетчатки в макулярной области у 71,2% пациентов I группы и у 55,6% пациентов II группы. У пациентов II группы на 10-15-й день наблюдения в 33,3% наблюдений отмечалось ухудшение зрительных функций и усиление тракционного компонента, у пациентов I группы ухудшение также было отмечено, но только в 23,7% наблюдений.
Ингибиторы ангиогенеза, диабетический макулярный отек
Короткий адрес: https://sciup.org/140187967
IDR: 140187967 | УДК: 617.7:616-005.98:616.379-008.64
A differentiated approach to the prescription of angiogenesis inhibitors for diabetic macular edema
Surveillance of the eye (n=77) in 68 diabetic patients diagnosed with nonproliferative diabetic retinopathy, and diabetic macular edema (DME) without (group I) and with presence (group II) of vitreomacular traction (VMT) characters has been conducted. Methods of research are visometry, bio-micro-ophthalmoscopy, fluorescent angiography, optical coherence tomography. All patients have been intravitreally injected angiogenesis inhibitor (bevacizumab - 2,5 mg). Postoperatively, improvement of visual functions has been registered and the decrease in total (G) of the retina in the macular region in 71,2% of patients in group I and in 55,6% of patients in Group II has been mentioned. There had been observed deterioration of visual functions and traction component gain in 33,3% patients in Group II on 10-15th day observation. Deterioration has been registered in patients in group I too, but only in 23,7% of observations.
Текст научной статьи Дифференцированный подход к назначению ингибиторов ангиогенеза при диабетическом макулярном отеке
Диабетический макулярный отек (ДМО) – ведущая причина снижения зрения у больных диабетической ретинопатией (ДР). Данное осложнение наблюдается как на ранних, так и при далеко зашедших стадиях заболевания [1]. Согласно современным представлениям о патогенезе ДМО в основе развития заболевания лежит исчезновение перицитов капилляров, их облитерация, ишемия макулы и, наконец, выброс факторов роста, усиливающих проницаемость сосудов и активирующих пролиферативные процессы [3, 9, 14]. Среди большого количества факторов роста ведущее значение в патогенезе диабетической ретинопатии имеет VEGF – сосудистый эндотелиальный фактор роста [2, 9, 17]. Это стало основанием для разработки группы лекарственных препаратов – ингибиторов ангиогенеза (Пегаптаниб, Бевацизумаб, Ранибизумаб), блокирующих данный фактор и успешно применяемых в последние несколько лет для лечения сосудистой патологии сетчатки [10, 16]. В настоящее время фармакотерапия заболеваний сетчатки, в том числе ДРП, становится альтернативой традиционной лазерной хирургии [5, 11]. Несмотря на то, что Пегаптаниб и Ранибизумаб являются препаратами, специально разработанными для интраокулярного применения, другой препарат из этой группы – Бавацизумаб, по данным ряда исследований, проводимых off-label, не менее эффективен как ингибитор повышенной проницаемости сосудов [4, 7]. Также, по данным некоторых авторов, Бевацизумаб потенциально является более эффективным, чем Пегаптаниб при лечении отечных макулопатий [13, 15]. Кроме того, период полувыведения Бевацизумаба более длительный, что обусловлено его крупной молекулой. Данное свойство дает возможность уменьшить количество повторных инъекций [16]. Определенное значение для пациентов имеет и экономический фактор: стоимость инъекции Бевацизумаба на несколько порядков ниже, чем аналогичных препаратов (Пегаптаниб, Раниби-зумаб). Появление сообщений об осложнениях при лечении Бевацизумабом носит спорадический и неподтвержденный характер [12]. В то же время появились единичные публикации о недостаточной эффективности этих препаратов у некоторых пациентов с ДМО, что авторы связывают с наличием витреомакулярных тракций [2, 8, 15].
Цель исследования
Изучить эффективность ингибитора ангиогенеза Бевацизумаба при различных формах диабетического отека макулы при непролиферативной диабетической ретинопатии.
Материал и методы
Исследование выполнено в период с 2008 по 2009 гг. Под нашим наблюдением находилось 68 пациентов (77 глаз) с непролиферативной формой диабетической ретинопатии и диабетическим макулярным отеком. В работе была использована модифицированная классификация проф. Л.И. Балашевича с соавт. (2004). Возраст пациентов составил в среднем 57,4±13,2 года, длительность сахарного диабета – 14,6±3,9 года. Всем пациентам выпол- няли визометрию, биомикроскопическое исследование сетчатки с бесконтактной линзой (78D), оптическую когерентную томографию (ОКТ) сетчатки и витреоре-тинального интерфейса («Stratus OCT 3000», Carl Zeiss). При ОКТ использовался протокол исследования «Macu-lar Thickness Map». При этом определялись основные морфометрические параметры ДМО: общий объем (ОО) сетчатки и ее толщина в отдельных топографических зонах. Регистрацию выше названных показателей проводили до введения препарата, на 1-е и 10-е сутки и через 1 и 3 месяца. ОКТ выполняли на 10–15-е сутки после введения препарата и по мере необходимости в сроки 1–3 месяца.
По данным проведенных исследований выделили 2 группы пациентов: 50 человек (59 глаз) с ДМО без тракционного компонента составили I группу (рис. 1), во вторую группу вошли 18 человек (18 глаз) с наличием ДМО и признаками тракционного компонента (рис. 2).
Исходная острота зрения исследуемых глаз у пациентов обеих групп не превышала 0,13±0,08. В группе I исходный показатель ОО составил, по данным ОКТ, 8,92±0,13мм3, а в группе II был достоверно выше - 9,74±0,27мм3 (p<0,013). Всем пациентам после ОКТ в условиях операционной под контролем операционного микроскопа вводили Бевацизумаб интравитреально в дозе 2,5 мг иглой 30G через плоскую часть цилиарного тела.
Результаты
При биомикроскопии сетчатки у пациентов обеих групп нами во всех случаях выявлен отек в области макулы в виде диффузного или локального утолщения оптического среза и помутнения сетчатки. У пациентов II группы по данным ОКТ в 100% наблюдений нами были выявлены признаки витреомакулярных тракций. В то же время результаты биомикроскопии позволяли предполагать ВМТ только в 3 (16,7%) случаях по наличию радиальных складок в макуле (рис. 2-а).
После введения препарата через 1 сутки в 47,5% наблюдений пациентов I группы мы отметили улучшение остроты зрения в среднем на 0,25±0,12. У пациентов II группы улучшение данного показателя было отмечено в 44,7%, но не более чем на 0,04±0,01. В то же время у больных II группы в эти же сроки зафиксировано ухудшение зрительных функций в 33,3% наблюдений на 0,07±0,05. У больных I группы ухудшение зрения
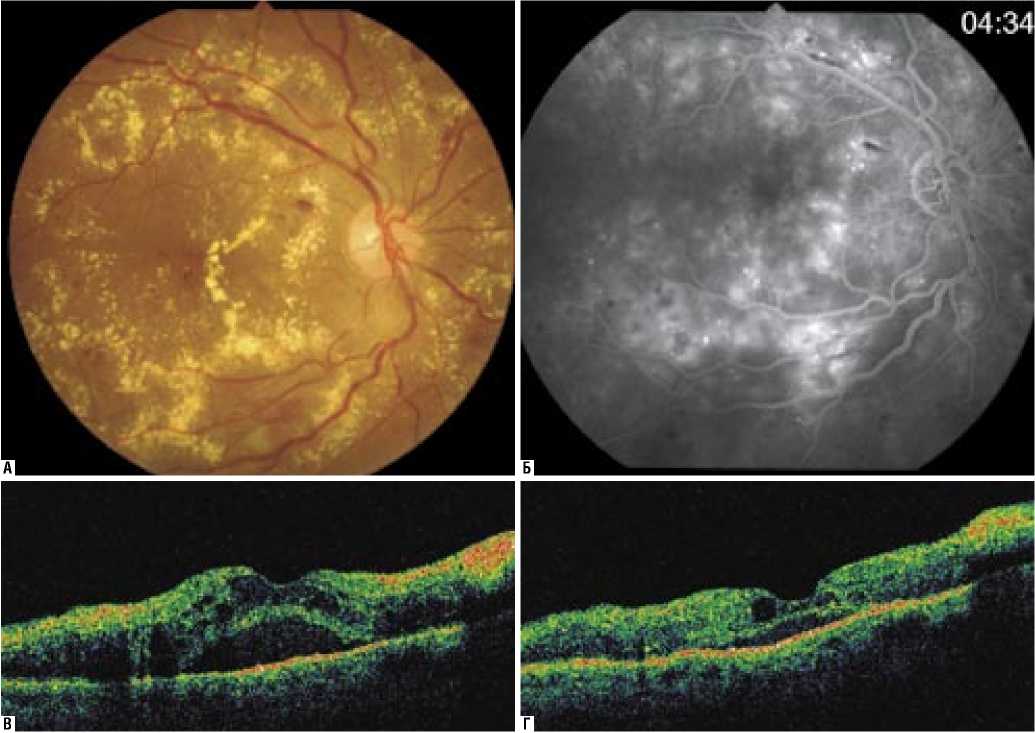
Рис. 1. Пациент А. 54 г. Диагноз – OD: Непролиферативная диабетическая ретинопатия и диабетический макулярный отек без признаков витреомакулярных тракций: А – фото глазного дна; Б – флюоресцентная ангиограмма; В – ОКТ до введения препарата; Г – ОКТ после введения препарата

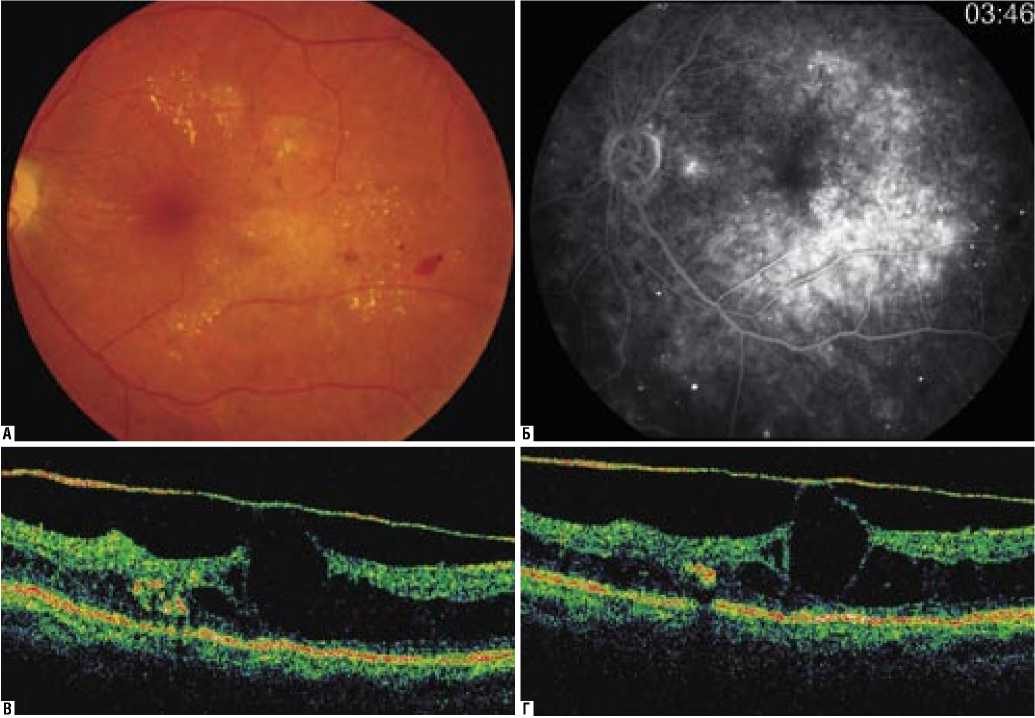
Рис. 2. Пациент К. 62 г. Диагноз – OS: Непролиферативная диабетическая ретинопатия тяжелой стадии и диабетический макулярный отек с горизонтальными витреомакулярными тракциями: А – фото глазного дна; Б – флюоресцентная ангиограмма; В – ОКТ до введения препарата; Г – ОКТ после введения препарата
через 1 сутки произошло только в 23,7% наблюдений до 0,03±0,01.
На 10–15-е сутки после инъекции улучшение зрительных функций на 0,37±0,14 у больных I группы отмечено уже в 71,2% наблюдений, в то время как у пациентов II группы повышение остроты зрения отмечено не более чем на 0,1±0,01 и только в 55,6% наблюдений. Дальнейшего улучшения зрительных функций у пациентов обеих групп не наблюдалось. Процентное соотношение динамики зрительных функций у пациентов обеих групп после инъекции ингибитора ангиогенеза представлено в табл. 1.
Показатели визометрии коррелировали с данными ОКТ, выполненной через 10–15 дней после инъекции.
Уменьшение ОО макулы и толщины сетчатки в отдельных топографических зонах отмечено в обеих группах. При этом только у пациентов I группы (37,3%) зарегистрирована полная резорбция отека макулы с нормализацией ОО до 6,83 ± 0,49 мм3 и формирование контура центральной ямки. У пациентов II группы полной резорбции отека макулы не отмечено ни в одном случае в течение всего срока наблюдения.
У больных I группы отек сетчатки носил равномерный характер и был менее выражен (в среднем на 33,2±12,7 мкм), чем у пациентов II группы. В этой группе отек сетчатки в различных зонах макулы носил неравномерный характер. Сравнительный анализ макулярных карт и томограмм у этих пациентов по-
Табл. 1. Динамика изменения зрительных функций в группах наблюдения после интравитреального введения Bevacizumab
|
Сроки наблюдения |
Группа I (n=59), % |
Группа II (n=18), % |
||||
|
Ухудшение |
Без измений |
Улучшение |
Ухудшение |
Без измений |
Улучшение |
|
|
1 сутки |
23,7% |
28,8% |
47,5% |
33,3% |
22,2% |
44,5% |
|
10–15 сут. |
23,7% |
5,1% |
71,2% |
33,3% |
11,1% |
55,6% |
|
1–1,5 мес. |
18,6% |
81,4% |
– |
38,9% |
61,1% |
– |
|
2,5–3 мес. |
88,1% |
11,9% |
– |
88,9% |
11,1% |
– |

казал, что локальное увеличение толщины сетчатки на 53,7±14,4 мкм соответствует точкам витреомакулярной фиксации. Сказанное выше позволяет предполагать, что локальное увеличение макулярного отека у пациентов II группы после инъекции Бевацизумаба является следствием усиления локального тракционного воздействия стекловидного тела.
Сравнительный анализ динамики морфометрических параметров макулярной зоны, по данным ОКТ, в обеих группах до введения ингибитора ангиогенеза и на 10–15 сутки после введения представлен в табл. 2.
В сроки 1–1,5 месяца в 38,9% наблюдений у пациентов II группы были зарегистрированы рецидивы ДМО, что проявлялось снижением зрительных функций и увеличением толщины сетчатки и ОО в макулярной области (9,11±1,42 мм3). У больных I группы рецидивы в эти же сроки зарегистрированы нами в 18,6% наблюдений, при этом ОО увеличился до 7,94±1,73 мм3 (р≤0,009).
К сроку наблюдения 2,5–3 месяца рецидивы ДМО были зарегистрированы у большинства пациентов I и II групп (78 и 88,9% соответственно). Снижение зрительных функций сопровождалось увеличением ОО до 7,87±1,82 мм3 у пациентов I группы и до 9,07±1,45 мм3 у пациентов II группы. Только в 13 наблюдениях (22%) в группе I и в 2 наблюдениях (11,1%) в группе II зрительные функции к этому сроку наблюдения оставались без изменений.
Назначение повторных инъекций ингибитора ангиогенеза пациентам II группы не дало улучшения зрительных функций и не привело к заметному уменьшению объема сетчатки в 100% наблюдений. В дальнейшем этим больным была рекомендована витреоретинальная хирургия.
Обсуждение
Применение в офтальмологической практике оптической когерентной томографии позволило выделить две основные формы ДМО: с наличием тракционного компонента и без такового [1, 10]. Также этот метод исследования доказал роль стекловидного тела в развитии рефрактерных форм ДМО [10]. Тракции со стороны стекловидного тела не только способствуют рецидивам кровоизлияний, активации пролиферативных процессов, но и обусловливают устойчивость ДМО при лазеркоагуляции и интравитреальном введении стероидов. Эффективность при рефрактерных формах ДМО витректомии также подтверждает роль стекловидного тела в их развитии [2, 8].
ДМО без тракционного компонента – наиболее часто встречающийся вид макулопатий. Согласно полученным нами данным, интравитреальное введение ингибитора ангиогенеза (Бевацизумаб) пациентам с ДМО без тракций наиболее эффективно. В результате нормализуется объем сетчатки в 71,2% наблюдений и улучшаются зрительные функции в среднем на 0,37±0,14.
Согласно нашим наблюдениям ДМО с наличием тракционного компонента при непролиферативной диабетической ретинопатии встречается реже (23,4% наблюдений). Однако именно этот вид макулопатий оказался наиболее устойчивым к лечению ингибиторами ангиогенеза. Витреомакулярный тракционный синдром, наблюдающийся при данном виде макулопатий, может обусловливать рефрактерность данных макулопатий не только при лазеркоагуляции и интравитреальном введении стероидов [5, 13], но и при применении ингибиторов ангиогенеза (по нашим наблюдениям, в 44,4% случаев). Более того, в ряде случаев ингибиторы ангиогенеза могут спровоцировать усиление тракционного компонента, и мы зафиксировали это в 33,3% наблюдений. Частота рецидивов ДМО у пациентов с тракционным компонентом в сроки 1–1,5 месяца выше, чем в глазах без тракций. Увеличение ОО сетчатки и ухудшение зрительных функций у части больных I группы, вероятно, связано с ингибицией VEGF как фактора выживаемости эндотелиальных клеток сосудов, что способствует усилению проницаемости ретинальных сосудов [6].
Выводы
-
1. Оптическая когерентная томография – высокоэффективный неинвазивный метод исследования, позволяющий дифференцировать различные формы диабетического отека макулы.
-
2. Назначение ингибиторов ангиогенеза при ДМО у пациентов с непролиферативной диабетической ретинопатией требует дифференцированного подхода.
-
3. Интравитреальное введение ингибиторов ангиогенеза малоэффективно при диабетическом макулярном отеке с тракционным компонентом.
Табл. 2. Изменения морфометрических ОКТ-параметров сетчатки в сравниваемых группах
|
Топографические зоны макулярной области |
Группа I (n=56), исходный показатель/ показатель после инъекции на 10–15 сут. |
Группа II (n=21), исходный показатель/ показатель после инъекции на 10–15 сут. |
|
Фовеола (мкм) |
294,8±19 / 164,2±17 |
387,3±17 / 281,3±21 |
|
Фовеа (мкм) |
279,8±34 / 192,8±12 |
389,8±23 / 273,2±13 |
|
Перифовеа (мкм) |
315,6±34 / 253,2±23 |
379,7±19 / 295,2±19 |
|
Парафовеа (мкм) |
321,8±23 / 232,4±13 |
381,5±26 / 285,6±31 |
|
ООМ, мм3 |
8,92±1,33 / 6,83±0,49 |
9,74±0,27 / 8,98±1,35 |
Примечания: * – достоверность разницы с показателем до лечения р ≤ 0,01.
Список литературы Дифференцированный подход к назначению ингибиторов ангиогенеза при диабетическом макулярном отеке
- Гацу М.В. Клинико-топографическая классификация диабетических макулопатий/М.В. Гацу, Я.В. Байбородов//Сахарный диабет -2008. -Т. 40, № 3. -С. 20-22.
- Шишкин М.М. Щадящая витреоретинальная хирургия при витреомакулярном тракционном синдроме/М.М. Шишкин, Э.В. Бойко, А.В. Ирхина//I Всероссийский семинар -«круглый стол» «Макула -2004», Ростов на Дону. -С. 23-24.
- Antcliff R.J. The pathogenesis of edema in diabetic maculopathy/R.J. Antcliff, J. Marshall//Semin. Ophthalmol. -1999. -N 14. -Р. 223-232.
- Arevalo J.F. Primary intravitreal bevacizumab (Avastin) for diabetic macular edema: results from the Pan-American Collaborative Retina Study Group at 6-month follow-up/J.F. Arevalo et al.//Ophthalmology. -2007. -N 114. -P. 743-750.
- Bandello F. Triamcinolone as adjunctive treatment to laser panretinal photocoagulation for proliferative diabetic retinopathy/F. Bandello, A. Polito, D.R. Pognuz et al.//Archives of Ophthalmology. -2006. -Vol. 124, N 5. -Р. 643-650.
- Cai J. Activation of Vascular Endothelial Growth Factor Receptor-1 Sustains Angiogenesis and Bcl-2 Expression Via the Phosphatidylinositol 3-Kinase Pathway in Endothelial Cells/J. Cai, S. Ahmad, W. G. Jiang//Diabetes. -2003. -Vol. 52. -P. 2959-2968.
- Caldwell R.B. Vascular endothelial growth factor and diabetic retinopathy: pathophysiological mechanisms and treatment perspectives/R.B. Caldwell et al.//Diabetes Metab. Res. Rev. -2003. -N 19. -Р. 442-455.
- Capone A.Jr. Vitrectomy for refractory diabetic macular edema/A.Jr. Capone, G. Panozzo//Semin. Ophthalmol. -2000. -N 15. -Р. 78-80.
- Ferrara N. Vascular endothelial growth factor basic science and clinical progress/Endocr. Rev. -2004. -N 25. -Р. 581-611.
- Gallemore R.P. Diagnosis of vitreoRetinal adhesions in macular disease with optical coherence tomography./R.P. Gallemore, J.M. Jumper, B.W. McCuen et al.//Retina -2000. -P. 20115-120.
- Hammes H.P. Pericytes and the pathogenesis of diabetic retinopathy/H.P. Hammes//Horm. Metab. Res. -2005. -Vol. 37 (Suppl. 1) -P. 39-43.
- Huang Z.L. Acute Vision Loss after Intravitreal Injection of Bevacizumab (Avastin) Associated with Ocular Ischemic Syndrome/Z.L. Huang, K.H. Lin, Y.C. Lee et al.//Ophthalmologica. -2010. -Vol. 224, N 2. -P. 86-89
- Khalili M.R. Debate on the various anti-vascular endothelial growth factor drugs/M.R. Khalili, H. Hosseini//Indian J Ophthalmol. -2008. -Vol. 56, N 3. P.255-256
- Knudsen S.T. Macular edema reflects generalized vascular hyper рermeability in type 2 diabetic patients with retinopathy/S.T. Knudsen et al.//Diabetes Care 2002. -№ 25. -Р. 2328-2334.
- Moradian S. Intravitreal Bavacizumab in active progressive proliferative diabetic retinopathy/S. Moradian, H. Ahmadiev, M. Malihi et al.//Graef. Arch. Clin. Exp. Ophthalm. -2008. -Vol. 246 (12). -P. 1699-1705.
- Nagpal M. A comparative debate on the various anti-vascular endothelial growth factor drugs: Pegaptanib sodium, ranibizumab and bevacizumab/M. Nagpal, K. Nagpal, P.N. Nagpal//Indian J. Ophthalmol. -2007. -N 55. -P. 437-439.
- Nguyen Q.D. Vascular endothelial growth factor is a critical stimulus for diabetic macular edema/Q.D. Nguyen, S. Tatlipinar, S.M. Shah, et al.//American Journal of Ophthalmology. -2006. -Vol. 142, N 6. -Р. 961-969.


