Дифференцированный подход к выбору тактики диафрагмальной перитонэктомии у больных перитонеальным карциноматозом
Автор: Суров Д.А., Гайворонский И.В., Просветов В.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 2 т.18, 2023 года.
Бесплатный доступ
В статье представлен анализ результатов хирургического лечения 77 пациентов с диссеминированными формами злокачественных опухолей органов брюшной полости и малого таза и наличием перитонеального карциноматоза, оперированных в клинике военно-морской хирургии Военно-медицинской академии имени С.М. Кирова и на ее клинической базе в НИИ скорой помощи имени И.И. Джанелидзе в период с 2019 по 2021 гг. Всем больным выполнялись циторедуктивные оперативные вмешательства, включавшие в себя диафрагмальную перитонэктомию различного объема. Представлена анатомо-хирургическая классификация вторичного опухолевого поражения диафрагмальной брюшины на основе топографоанатомической характеристики локализации опухолевых узлов и вовлечения смежных анатомических структур, размера метастатических узлов, а также глубины опухолевой инвазии. На основе классификации в статье также представлен дифференцированный подход к выбору тактики хирургического лечения пациентов со вторичным опухолевым поражением диафрагмальной брюшины при перитонеальном карциноматозе.
Циторедуктивная хирургия, диафрагмальная перитонэктомия, перитонеальный карциноматоз, дифференцированный подход
Короткий адрес: https://sciup.org/140301990
IDR: 140301990 | DOI: 10.25881/20728255_2023_18_2_46
A differentiated approach to choosing the tactics of diaphragmatic peritonectomy in patients with peritoneal carcinomatosis
The article presents an analysis of the results of treatment of 77 patients of surgical treatment of 77 patients with disseminated forms of malignant tumors of the abdominal cavity and pelvic organs and the presence of peritoneal carcinomatosis operated at the Naval Surgery Clinic of the Kirov Military Medical Academy and at its clinical base at the l.l. Janelidze Research lnstitute of Emergency Medicine in the period from 2019 G. to 2021 All patients underwent cytoreductive surgical interventions, which included diaphragmatic peritonectomy of various volumes. The article presents an anatomical and surgical classification of secondary tumor lesions of the diaphragmatic peritoneum based on the topographic and anatomical characteristics of the localization of tumor nodes and the involvement of adjacent anatomical structures, the size of metastatic nodes, as well as the depth of tumor invasion. Based on the classification, the article also presents a differentiated approach to the choice of tactics for surgical treatment of patients with secondary tumor lesion of the diaphragmatic peritoneum in peritoneal carcinomatosis.
Текст научной статьи Дифференцированный подход к выбору тактики диафрагмальной перитонэктомии у больных перитонеальным карциноматозом
В настоящее время циторедуктивная хирургия диссеминированных форм злокачественных опухолей брюшной полости и малого таза является одной из наиболее актуальных и нерешенных проблем хирургической онкологии [1–4]. Циторедуктивные оперативные вмешательства, направленные на максимально возможное удаление первичной опухоли и ее метастазов, как правило, включают в себя комбинированные резекции различного объема, расширенную лимфодиссекцию и перитонэкто-мию [5]. В качестве дополнительного метода воздействия на резидуальную опухолевую ткань в большинстве случаев выполняют внутрибрюшинную гипертермическую химиоперфузию. Значительное снижение объема опухолевой массы создает благоприятные условия для проведения адъювантной системной лекарственной химиотерапии, эффективность которой, в конечном итоге, во многом определяет отдаленные результаты лечения пациентов, а также качество их жизни. В этой связи достижение оптимальной циторедукции является определяющим фактором прогноза выживаемости больных диссеминированными опухолями брюшной полости и малого таза [6–9]. Одной из наиболее сложных, с точки зрения оперативной хирургии, клинических ситуаций является метастатическое поражение диафрагмальной брюшины, которое наблюдается у 40–70% пациентов с перитонеальным карциноматозом [10; 11]. При этом данные литературы свидетельствуют о значительных технических трудностях выполнения диафрагмальной перитонэктоми, обусловленных морфофункциональными особенностями диафрагмы и ее вариантной анатомии [12; 13]. Кроме того, определяющее значение, с точки зрения особенностей локорегионарного распространения метастатических опухолевых узлов, имеет тесное топографо-анатомическое взаимоотношение органов, расположенных в верхних отделах брюшной полости (печень, селезенка, желудок, абдоминальный отдел пищевода, магистральные сосуды). Принципиальным фактором, определяющим эффективность циторедуктивной хирургии, является сохранение целостности диафрагмы, нарушение которой существенно повышает риски диссеминации опухоли в плевральную полость и ее дальнейшего прогрессирования. Анализ литературы свидетельствует, что в многочисленных отечественных и зарубежных публикациях, прямо или косвенно освещающих проблему диафрагмальной перитонэктомии, как правило, обсуждаются только некоторые ее технические аспекты и оценивается частота осложнений [14; 15]. При этом совершенно очевидно, что повышение безопасности и эффективности сложной в техническом отношении

диафрагмальной перитонэктомии возможно, в первую очередь, за счет применения оперативных приемов, основанных на детальной оценке особенностей регионарного распространения перитонеальных метастазов диафрагмальной брюшины.
Таким образом, попытка систематизации наиболее типичных вариантов метастатического поражения диафрагмальной брюшины и разработка на ее основе персонифицированной хирургической тактики являются возможными направлениями улучшения результатов диафрагмальной перитонэктомии.
Цель
Разработать классификацию вторичного опухолевого поражения диафрагмальной брюшины и предложить дифференцированный подход к хирургическому лечению перитонеального карциноматоза верхнего этажа полости брюшины.
Материалы и методы
Проведен анализ хирургического лечения 77 пациентов с диссеминированными формами злокачественных опухолей органов брюшной полости и малого таза и наличием перитонеального карциноматоза, оперированных в клинике военно-морской хирургии Военно-медицинской академии имени С.М. Кирова и на ее клинической базе в НИИ скорой помощи имени И.И. Джанелидзе в период с 2019 по 2021 гг. Всем больным выполнялись циторедуктивные оперативные вмешательства, включавшие в себя диафрагмальную перитонэктомию различного объема. Были изучены истории болезни пациентов: протоколы операций, фото- и видеоматериалы, результаты гистологических исследований. В группу исследования вошли 71 женщин — (93%) и 6 мужчин — (7%), средний возраст которых составил 58 лет (от 20 лет до 81 года). Локализация первичной опухоли была следующей: яичник — 31 (41%), толстая кишка — 24 (31,8%), матка — 12 (15,5%), органы забрюшинного пространства — 2 (2,6%), желудок — 3 (4,5%), червеобразный отросток — 3 (3,2%), тонкая кишка — 2 (1,3%). Средний индекс РС1 составил 11 (от 7 до 30).
Результаты
Структура оперативных вмешательств при выполнении диафрагмальной перитонэктомии была представлена следующим образом: перитонэктомия (n = 35), резекция диафрагмы (n = 16), резекция глиссоновой капсулы и паренхимы печени (n = 17), спленэктомия (n = 40), резекция сухожильного центра диафрагмы и перикарда (n = 13), парциальная резекция мышечной части диафрагмы (n = 15).
Различный объем поражения брюшины при перитонеальном карциноматозе диктует необходимость выбора определенной тактики хирургического лечения, а также использования соответствующего инструментария и хирургических технологий. Детальная оценка характера метастатического поражения диафрагмальной брюшины и смежных анатомических структур и органов во многом определяет вероятность достижения полной циторедукции.
В большинстве случаев наблюдалось двухстороннее поражение париетальной брюшины мышечной части диафрагмы 65% (n = 50), когда опухолевые диссеминаты локализовались на правом и левом куполах диафрагмы. Реже перитонеальные метастазы локализовались на одном из куполов — 35% (n = 27), при этом у больных раком яичников чаще имело место метастатическое поражение левого купола диафрагмы и селезенки. Другой существенной зависимости расположения перитонеальных метастазов на диафрагмальной брюшине от локализации первичной опухоли выявлено не было. Также не наблюдалось изолированное поражение сухожильного центра. Поражение метастатическими узлами сухожильной части диафрагмы было выявлено при двухсторонней локализации у 57% (n = 23) больных и при односторонней — в 46% (n = 13) наблюдений: слева — 84% (n = 11), справа — 13% (n = 2). Вовлечение в опухолевых процесс селезенки наблюдалось у 60% больных (n = 46), что требовало выполнения спленэктомии. Поражение печени от «просовидных» опухолевых диссеминатов до крупных опухолевых конгломератов (более 2,5 см) наблюдалось у 22% больных (n = 17) (Рис. 1). Наличие дополнительных перитонеальных диссеминатов на капсуле печени и ее связочном аппарате обусловливало необходимость проведения перитонэктомии с выделением капсулы печени и последующим сепарированием её по направлению к диафрагме. После мобилизации пораженного участка глиссоновой капсулы выполняли его тракцию в краниальном направлении с одновременной каудальной ткакцией печени, после чего диссекцию продолжали в направлении диафрагмы. Данный технический
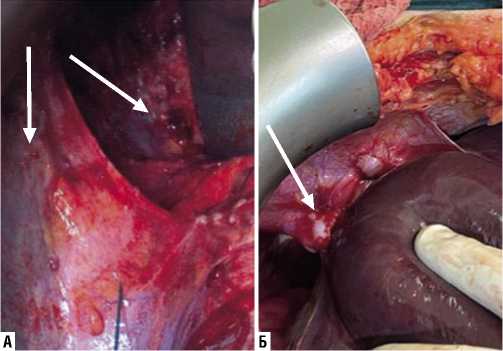
Рис. 1. Интраоперационные фотографии различных вариантов метастатического поражения диафрагмальной брюшины. А — поверхностная опухолевая инвазия диафрагмальной брюшины у пациента с диссеминированным раком толстой кишки (белая стрелка); Б — метастатическое поражение диафрагмальной брюшины с инвазией в мышцу и капсульно-связочный аппарат печени (белая стрелка).

прием обеспечивает достаточный уровень визуального контроля, что уменьшает риски необоснованного повреждения паренхимы печени и печеночных вен, повышая тем самым безопасность вмешательства. В то же время глубокое поражение паренхимы печени, в зависимости от глубины её инвазии, расположения метастаза относительно печеночных вен, требует выполнения атипичной резекции паренхимы печени различного объема.
Исходя из оценки опухолевого поражения, мы определяли размеры опухолевых узлов. В 47,8% (n = 36) случаев размеры опухолевых узлов составили от 1 до 2 мм, в 26% (n = 20) — от 2 мм до 1 см, в 15,4% (n = 12) — от 1 см до 2,5 см, а опухолевые конгломераты более 2,5 см встречались у 13,2% (n = 10) больных. Как правило, размер метастатического узла напрямую зависел от глубины опухолевой инвазии, которая во многом определяет тактику диафрагмальной перитонэктомии.
При изучении гистотопограмм была выявлена различная глубина опухолевой инвазии. Анализ полученных результатов подтвердил зависимость глубины инвазии матастатического узла и его размеров (Рис. 2). Поражение париетальной брюшины до собственной фасции диафрагмы наблюдалось в 52,3% (n = 34) случаев при размере опухолевых узлов от 1 мм до 1 см. Инвазия в мышцу до половины толщины мышечного слоя диафрагмы было выявлено у 31,2 % (n = 20) больных, а трансдиафрагмальное поражение с вовлечением в опухолевые процесс париетальной плевры в — 16,4% (n = 12) наблюдений.
Клинический опыт свидетельствует, что поверхностное опухолевое поражение, вовлекающее только брюшину, не вызывает особых технических сложностей, и в этом случае выполняется классическая перитонэкто-мия, техника которой детально была детально описана P. Sugarbaker ещё в конце 90-х гг. (Рис. 3). Диафрагмальная перитонэктомия имеет определенные отличия от других этапов циторедуктивной операции. Отсутствие жировой клетчатки и рыхлой соединительной ткани между брюшиной и диафрагмой требует постоянной тракции мобилизуемого листка париетальной брюшины и тщательного гемостаза, создающего условия для качественной визуализации плоскости диссекции. Одним из наиболее важных технических аспектов диафрагмальной перитонэктомии является её непрерывное продолжение в каудальном направлении с последующей мобилизацией париетальной брюшины левого латерального канала с этапной интраоперационной оценкой необходимости выполнения резекции органов и анатомических структур (селезенка, надпочечник, почка). Перитонэктомия правого купола диафрагмы также сопряжена с рядом технических трудностей, связанных с необходимостью устойчивой экспозиции плоскости диссекции с целью снижения рисков ятрогенного повреждения печени, нижней полой вены (НПВ) и печеночных вен.
При инвазии опухолевого узла в мышечный слой, не превышающей по глубине прорастания 50% толщины диафрагмы, выполняется парциальная резекция её мы-
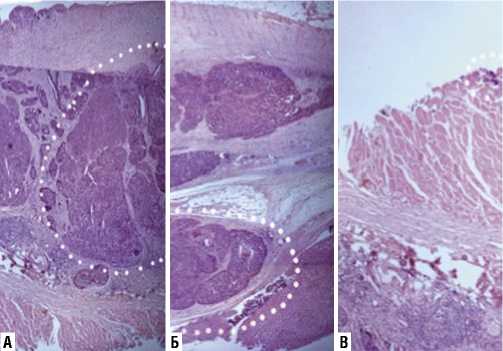
Рис. 2. Различная степень поражения диафрагмальной брюшины при карциноматозе: А — опухолевая инвазия всех слоев диафрагмы; Б — метастазы, поражающие капсулу печени и «area nuda»; В — поверхностные метастазы на диафрагме со стороны брюшной полости. Гистологические препараты, изготовленные после выполненной диафрагмальной перитонэктомии. Окраска гематоксилин и эозин, увеличение х 200.
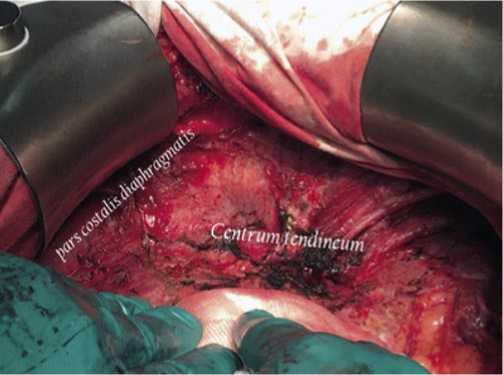
Рис. 3. Вид операционного поля после выполненной перитонэктомии мышечного и сухожильного отделов диафрагмы при поверхностной перитонеальной инвазии.
шечного слоя, что позволяет избежать необоснованной перфорации диафрагмы и вскрытия плевральной полости на стороне вмешательства. Трансдиафрагмальная инвазия перитонеальных диссеминатов требует резекции всей толщины диафрагмы. Необходимо добиваться тщательного гемостаза и перевязки диафрагмальных сосудов, а также четкого визуального контроля для недопущения ранений магистральных сосудов, повреждения легких, печени и пищевода. Резекция диафрагмы в зависимости от глубины и площади опухолевого поражения требует соблюдения мер профилактики попадания в плевральную полость крови и асцитической жидкости, что неизбежно может привести к прогрессированию опухолевого процесса в плевральной полости (Рис. 4). Дефект ушивается отдельными узловыми швами. При обширных дефектах,

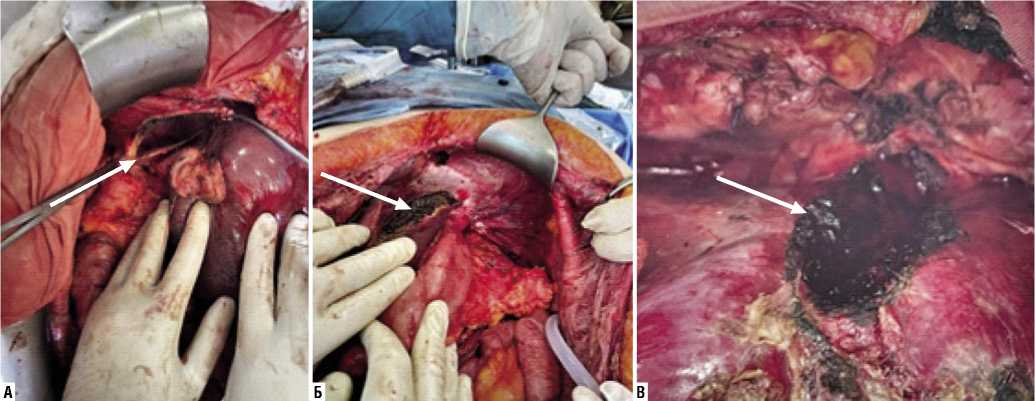
Рис. 4. Интраоперационные фотографии циторедуктивных операций. А — резекция правого купола диафрагмы с резекцией и глиссоновой капсулы (белая стрелка); Б — вид после перитонэктомии левого купола диафрагмы, спленэктомиии и атипичной резекции; В — вид после резекции сухожильного центра и нижней стенки перикардиальной сумки (белая стрелка).
в ряде случаев, не представляется возможным выполнить их закрытие, что требует применения синтетических материалов.
Одними из наиболее трудных локализаций опухолевого поражения являются: area nuda и область ретропе-ченочного сегмента нижней полой вены (НПВ), которые требуют мобилизации печени, сопряженной с высокими рисками её ятрогенных повреждений и ранений НПВ, инвазия в перикард и сухожильный центр диафрагмы, что требует достижения максимальной экспозиции операционного поля, для предотвращения ранения сердца и магистральных сосудов.
Таким образом, на наш взгляд, классификация метастатического поражения диафрагмы при перитонеальном карциноматозе должна включать в себя топографоанатомическую характеристику локализации опухолевых узлов и вовлечения смежных анатомических структур, размеров метастатических узлов, а также глубины опухолевой инвазии.
Анатомо-хирургическая классификация вторичного опухолевого поражения диафрагмальной брюшины.
-
I. Локализация опухолевых узлов:
-
1. Одностороннее поражение мышечной части диафрагмы:
-
1а. правый купол диафрагмы;
-
1б. левый купол диафрагмы;
-
1в. двустороннее поражение диафрагмы;
-
2. Сухожильный центр диафрагмы;
2а. сочетанное поражение мышечной части и сухожильного центра диафрагмы.
-
II. Размер опухолевых узлов:
-
1. 1–2 мм, («просовидное обсеменение»);
-
2. от 2 мм до 1 см;
-
3. от 1 см до 2,5 см;
-
4. более 2,5 см.
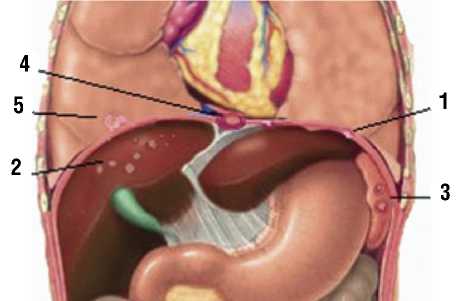
Рис. 5. Схема метастатического поражения диафрагмы и смежных анатомических структур при перитонеальном карциноматозе. 1 — диафрагма; 2 — капсула и паренхима печени; 3 — селезенка; 4 — перикард; 5 — легкое.
-
III. Глубина опухолевой инвазии (Рис. 6):
-
1. поражение брюшины до собственной фасции диафрагмы;
-
2. инвазия до 50% толщины мышечного слоя диафрагмы;
-
3. инвазия более 50% толщины мышечного слоя диафрагмы;
-
4. инвазия опухолью всех слоев диафрагмы с вовлечением диафрагмальной плевры (трансдиафрагмальная инвазия).
-
IV. Вовлечение в опухолевых процесс смежных органов и анатомических структур (Рис. 5):
-
1. диафрагма;
-
2. печень (глиссонова капсула и её паренхима);
-
3. селезенка;
-
4. перикард;
-
5. легкое;
-
6. нижняя полая вена.
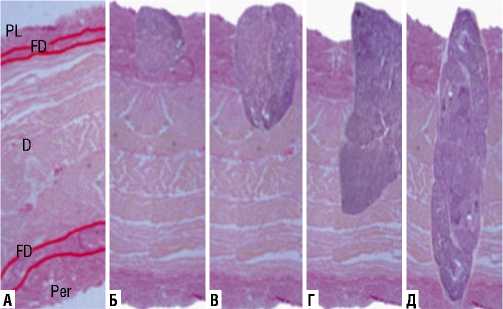
Рис. 6. Иллюстрация опухолевого поражения диафрагмальной брюшины в зависимости от глубины инвазии: А — красным цветом обозначены границы между слоями диафрагмы (Per — брюшина; FD — диафрагмальная фасция, являющаяся продолжением f. еndoabdominalis; D — мышечный слой диафрагмы; FD — диафрагмальная фасция; PL — плевра). Б — указано поражение брюшины до собственной фасции диафрагмы; В — поражение, затрагивающее до 50% толщины диафрагмы; Г — опухолевая инвазия достигает более 50% толщины диафрагмы; Д — трансдиафрагмальное опухолевое поражение с вовлечением плевры.
Табл. 1. Дифференцированный подход к выбору тактики хирургического лечения пациентов со вторичным опухолевым поражением диафрагмальной брюшины при перитонеальном карциноматозе
|
Характер опухолевого поражения диафрагмальной брюшины |
Хирургическая тактика |
|
Опухолевая инвазия брюшины до собственной фасции диафрагмы |
Стандартная диафрагмальная перитонэктомия |
|
Опухолевая инвазия до 50% толщины мышечного слоя диафрагмы |
Перитонэктомия; парциальная резекция диафрагмы; ушивание дефекта мышечного слоя |
|
Опухолевая инвазия опухоли более 50% толщины мышечного слоя диафрагмы |
Перитонэктомия; резекция участка диафрагмы, ушивание раны диафрагмы; дренирование плевральной полости |
|
Опухолевая инвазия в капсулу глиссона |
Перитонэктомия; глиссонэк-томия |
|
Опухолевая инвазия в паренхиму печени |
Перитонэктомия; резекция печени |
|
Опухолевая инвазия в селезенку |
Перитонэктомия; спленэктомия |
|
Инвазия в сухожильный центр диафрагмы и перикард |
Перитонэктомия; резекция сухожильного центра диафрагмы; резекция перикарда; ушивание раны перикарда |
|
Опухолевая инвазия нижней полой вены |
Перитонэктомия; резекция стенки нижней полой вены; ушивание дефекта нижней полой вены |
Ввиду различных (по своей локализации, глубине инвазии и размерам опухолевых узлов) вариантнов метастатического поражения диафрагмальной брюшины при перитонеальном карциноматозе, можно предложить следующую дифференцированную тактику хирургического лечения (табл. 1).
Выводы
Разработанная классификация поражения диафрагмы при перитонеальном карциноматозе в полной мере отражает её основные варианты, локализацию метастатических очагов, их размеры, глубину инвазии и может быть применена для выбора рациональной тактики диафрагмальной перитонэктомии.
Предложенная дифференцированная тактика диафрагмальной перитонэктомии является рациональной, безопасной и отвечает требованиям достижения оптимальной циторедукции у больных карциноматозом брюшины.
В целях повышения безопасности диафрагмальной перитонэктомии и достижения полной циторедукции необходима тщательная стратификация больных и предоперационная оценка характера метастатического поражения диафрагмы, а также смежных анатомических структур и органов.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Дифференцированный подход к выбору тактики диафрагмальной перитонэктомии у больных перитонеальным карциноматозом
- Ганцев Ш.Х., Ганцев К.Ш., Кзыргалин Ш.Р. и др. Перитонеальный канцероматоз при злокачественных новообразованиях различных локализаций. Достижения и перспективы // Креативная хирургия и онкология. — 2021. — Т.11. — №2. — С.149-156. [Ganev ShKh, Ganev KSh, Kzyrgalin ShP, et al. Peritoneal carcinomatosis in malignant neoplasms of various localizations. Achievements and prospects. Creative surgery and oncology. 2021; 11(2): 149-156. (In Russ.)]
- Ганцев Ш.Х., Забелин М.В., Ганцев К.Ш. и др. Перитонеальный кан-цероматоз: мировые научные школы и современное состояние вопроса // Креативная хирургия и онкология. — 2021. — Т.11. — №1. — С.85-91. [Ganev ShKh, Zabelin MV, Ganev KSh, et al. Peritoneal carcinomatosis: world scientific schools and the current state of the issue. Creative surgery and oncology. 2021; 11(1): 85-91. (In Russ.)].
- Майстренко Н.А., Хватов А.А., Учваткин Г.В. и др. Экзентерация малого таза в лечении местно-распространенных опухолей // Вестник хирургии имени И.И. Грекова. — 2014. — Т.173 — №6.- С.37-42. [Maistrenko NA, Khvatov AA, Uchvatkin GV, et al. Pelvic exenteration in the treatment of locally advanced tumors. Bulletin of Surgery named after I.I. Grekov. 2014; 173(6): 37-42. (In Russ.)]
- Соболев Д.Д., Каприн А.Д., Хомяков В.М. и др. Опыт комбинированного лечения больных местно-распространенным и диссеми-нированным раком желудка с использованием методики гипертермической интраоперационной внутрибрюшной химиотерапии // Research'n Practical Medicine Journal. 2015. [Sobolev DD, Kaprin AD, Khomyakov VM,et al. Experience of combined treatment of patients with locally advanced and disseminated gastric cancer using hyperthermic intraoperative intraperitoneal chemotherapy. Research'n Practical Medicine Journal. 2015. (In Russ.)]
- Sugarbaker PH. Prevention and Treatment of Peritoneal Metastases: a Comprehensive Review. Indian J. Surg. Oncol. 2019; 10(1): 3-23.
- Шелехов А.В., Дворниченко В.В., Радостев С.И. и др. Циторедуктив-ные операции в лечении рака яичников 3С стадии: сравнительный анализ результатов // Вопросы онкологии. — 2019. — Т.65. — №1. — С.142-146. [Shelekhov AV, Dvornichenko VV, Radostev SI, et al. Cytoreductive operations in the treatment of ovarian cancer of stage 3C: comparative analysis of results. Questions of oncology. 2019; 65(1): 142-146. (In Russ.)]
- Bogani G, Ditto A, Martinelli F, et al. Surgical Techniques for Diaphragmatic Resection During Cytoreduction in Advanced or Recurrent Ovarian Carcinoma: A Systematic Review and Meta-analysis. Int J Gynecol Cancer. 2016; 26(2): 371-80.
- Farrell R. Peritonectomy and hyperthermic intraperitoneal chemotherapy for advanced epithelial ovarian cancer: What gynaecological oncologists really think. Aust N Z J Obstet Gynaecol. 2019; 59(3): 457-462.
- Spiliotis J, Kopanakis N, Prodromidou A, et al. Peritoneal sarcomatosis: Cytoreductive surgery and hyperthermic intraperitoneal chemotherapy. Surg Innov. 2021; 28(3): 394-395.
- Nagai T, Oshiro H, Sagawa Y, et al. Pathological Characterization of Ovarian Cancer Patients Who Underwent Debulking Surgery in Combination with Diaphragmatic Surgery: A Cross-Sectional Study. Medicine (Baltimore). 2015; 94(50): e2296.
- Ahmed S, Levine EA, Randle RW, et al. Significance of diaphragmatic resections and thoracic chemoperfusion on outcomes of peritoneal surface disease treated with cytoreductive surgery (CRS) and hyperthermic intraperitoneal chemotherapy (HIPEC). Ann Surg Oncol. 2014; 21(13): 4226-31.
- Tozzi R, Ferrari F, Nieuwstad J, et al. Tozzi classification of diaphragmatic surgery in patients with stage IIIC-IV ovarian cancer based on surgical findings and complexity. J Gynecol Oncol. 2020; 31(2).
- Zapardiel I, Peiretti M, Zanagnolo V, et al. Diaphragmatic surgery during primary cytoreduction for advanced ovarian cancer: peritoneal stripping versus diaphragmatic resection. Int J Gynecol Cancer. 2011; 21(9): 1698703.
- Stepanyan A, Malakyan Z, Alaverdyan A, et al. Right upper quadrant peritonectomy. Answering frequently asked questions. Int J Gynecol Cancer. 2021; 31(9): 1305-1306.
- Sullivan BJ, Bekhor EY, Carpiniello M, et al. Diaphragmatic Peritoneal Stripping Versus Full-Thickness Resection in CRS/HIPEC: Is There a Difference? Ann Surg Oncol. 2020; 27(1): 250-258.


