Дифференцированный подход в эндоскопическом лечении больных с окклюзией БДС
Автор: Шабунин А.В., Бедин В.В., Нечипай А.М., Коржева И.Ю., Чернов М.В., Комиссаров Д.Ю.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 4 (50), 2016 года.
Бесплатный доступ
В статье представлены результаты эндоскопического лечения больных с механической желтухой, обусловленной окклюзией БДС. Описаны методики дифференцированного подхода в современных возможностях эндоскопического лечения больных с данной хирургической патологией.
Механическая желтуха, окклюзия бдс
Короткий адрес: https://sciup.org/142211267
IDR: 142211267
Текст научной статьи Дифференцированный подход в эндоскопическом лечении больных с окклюзией БДС
Синдром механической желтухи, развивающийся на фоне острой окклюзии БДС, в настоящее время занимает первое место по распространенности у пациентов с заболеваниями билиопанкреатодуоденальной зоны [1, 5]. Среди заболеваний, вызывающих непроходимость внепечёночных желчных протоков, важное место занимают патологические изменения в области большого дуоденального сосочка (БДС). Последние имеют широкий спектр:
-
1) воспалительные заболевания: острые и хронические па-пиллиты с наличием или без гиперпластических процессов,
-
2) доброкачественные опухоли, 3)злокачественные опухоли [2, 6, 8].
По данным литературы, рак БДС составляет 11,7-24,5% от всех злокачественных опухолей, приводящих к механической желтухе [5]. Аденома БДС отмечается лишь у 0,15% эндоскопических исследований по поводу механической желтухи, а у больных с постхолецистэктомическим синдромом (ПХЭС) эта цифра колеблется от 1,8 до 9,6% [5].
Доброкачественный стеноз БДС выявляется у 4–40% больных при первичных и у 11–84% больных - при повторных операциях на желчевыводящих путях и поджелудочной железе [9].
Достаточно часто заболевания БДС сочетаются с желчнокаменной болезнью (ЖКБ), холедохолитиазом. ЖКБ встречается, в среднем, у каждого десятого жителя планеты, а холедохолитиаз, как ее осложнение, имеется у 5–20%, частота резидуального холедохолитиаза остается высокой и составляет 1,5—10% [6].
Благодаря внедрению в медицинскую практику современных неинвазивных методов обследования органов брюшной полости: УЗИ, КТ и МРТ, полученные результаты позволяют в кратчайшие сроки установить причину и характер билиарной и/или панкреатической гипертензии [3, 4].
Однако, на этапе оказания экстренной помощи, вне зависимости от причины острой окклюзии БДС, основной задачей, подлежащей решению, является декомпрессия билиарного тракта эндоскопическими транспапиллярными способами [7].
Цель работы: оценить современные технические возможности различных эндоскопических ретроградных вмешательств в лечении больных с механической желтухой и синдромом окклюзии БДС, включая высокоинформативные визуализационные возможности ЭУС.
Материалы и методы
За период 2015г. – июнь 2016 г. в эндоскопическом отделении ГКБ имени С.П. Боткина выполнено 687 ретроградных вмешательств, 152 (22%) из которых – в экстренном и срочном порядке. Ведущими жалобами пациентов являлись: изменение цвета кожи, мочи и кала у 590 (85,9%) больных и боли в эпигастрии и правом подреберье — у 445 (64,8%). Слабость отмечали 80 (12%) больных. Жалобы на озноб, иногда повторяющийся в течение суток, повышение температуры тела, пот, боли в правом подреберье предъявляли 134 (19,6%) больных. Кроме перечисленных жалоб у больных имелись диспепсические расстройства, проявляющиеся анорексией — у 54 (8%); тошнотой, рвотой – у 57 (8,3%). Длительность желтухи варьировала от 1,5- 2 дней до 1,5-2месяцев. У большинства больных длительность желтушного периода находилась в пределах от 1 недели до 1,5 месяцев. Из общего числа 687 больных, которым выполнено эндоскопическое вмешательство по поводу механической желтухи, 63 (9,2%) пациента к моменту поступления в стационар ранее были оперированы по поводу ЖКБ.
Согласно диагностическому алгоритму, перед проведением рентген-эндоскопических вмешательств всем больным проводили клиническое исследование, включающее лабораторную диагностику (общий и биохимический анализы крови, свертывающая система) и неинвазивные методы обследования (трансабдоминальное УЗИ (редко КТ или МРХПГ), обзорные рентгеновские снимки ОГК и брюшной полости).
Используя УЗИ, причина механической желтухи была выявлена в 52% случаев (357 пациентов). Следующим шагом в диагностическом алгоритме у всех больных явилась ЭГДС (687 больных). Исследование проводили с помощью эндоскопов фирмы «Olympus» (EXERA II). В процессе исследования обращали внимание на деформации желудка и ДПК, а также косвенные признаки функционирования двенадцатиперстной кишки и желчевыводящих путей: дуодено-гастральный рефлюкс желчи, множественные лимфоангиоэктазии на слизистой ДПК, отражающие застой в системе лимфооттока (так называемый симптом «манной крупы»), отсутствие желчи в ДПК. Основной задачей выполнения гастродуоденоскопии у больных с механической желтухой была визуальная оценка состояния БДС (его размеров, формы, рельефа слизистой оболочки, наличие опухолевидных образований на поверхности ампулы и в области устья сосочка), морфологическая верификация обнаруженных изменений, а также выявление сопутствующих заболеваний слизистой оболочки верхних отделов пищеварительного тракта.
В результате выполнения ЭГДС характерные визуальные изменения БДС были обнаружены у 202 (29,4%) больных, сопутствующая патология верхних отделов пищеварительного тракта: язвенная болезнь желудка и двенадцатиперстной кишки была выявлена у 93 пациентов (13,5%), эрозивные гастродуодениты – у 324 (47%) , дивертикулы ДПК – у 67 (10%).
Далее гастроскоп с торцевой оптикой заменяли на дуо-деноскоп с боковым расположением оптической системы и проводили прицельный осмотр слизистой зоны БДС. Использовали эндоскопы фирмы «Olympus» (Япония). Прицельная биопсия БДС выполнялась стандартными биопсийными щипцами из прилагаемых к дуоденоскопам стандартных наборов эндоскопических инструментов. Катетеризация устья БДС и контрастирование протоковых систем выполнялась катетерами разных фирм-производителей (Olympus, EndoFlex, Boston Sientific). Рентгеновское исследование проводили на аппарате фирмы «АРХМ-РЕНЕКС», оснащенным электронно-оптическим преобразователем.
В качестве рентгеноконтрастных средств использовали водорастворимый йодсодержащий препарат (телебрикс 35М). Количество вводимого контраста в желчные пути составляло не более 10 мл.
В 57 (37,5%) из 152 случаев показанием для ургентных вмешательств явился синдром острой окклюзии БДС вслед- ствие папиллолитиаза и развившийся на ее фоне острый билиарный панкреатит (эндофото 1). В 31 (20,4%) случае причиной окклюзии БДС были его злокачественные новообразования (эндофото 2), в 64 (42,1%) – доброкачественные поражения (аденома БДС -12 больных (7,9%) (эндофото 3), папиллостеноз и СТОХ -33 пациента (21,7%) (фото 2), папиллит- 21 (12,5%) (эндофото 4).
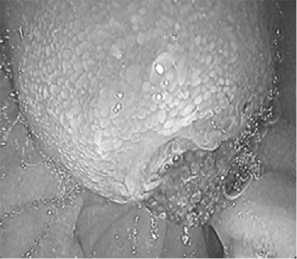
Эндофото 1: Острая окклюзия устья БДС конкрементом
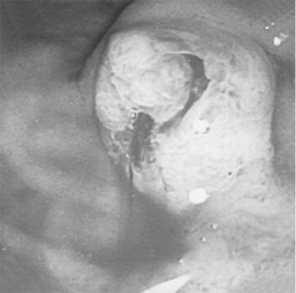
Эндофото 2: Рак БДС
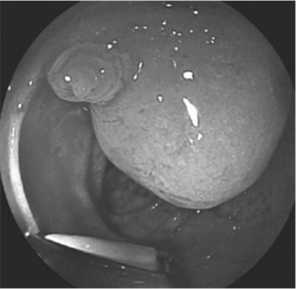
Эндофото 3: Аденома БДС
При всех заболеваниях БДС, сопровождающихся билиарной обструкцией, в качестве первого этапа лечения применяли ЭПСТ, направленную на адекватную декомпрессию желчевыводящих протоков.
Выбор метода ЭПСТ и инструментов зависел от локализации, формы папиллы и анатомических особенностей
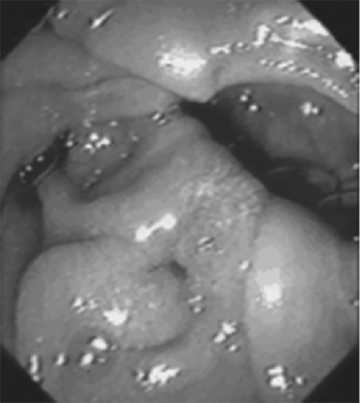
Эндофото 4: Папиллит БДС
-
1) адекватная медикаментозная седация больного и релаксация перистальтики ДПК (в/в наркоз);
-
2) правильное позиционирование БДС;
-
3) выбор оптимального способа рассечения БДС в каждом конкретном случае;
-
4) четкое следование анатомическим ориентирам;
-
5) постоянный контроль за натяжением струны и длиной разреза при выполнении типичной ЭПСТ и обязательный контроль за глубиной разреза при выполнении нетипичной ЭПСТ;
-
6) использование режима Endocut (чередование режимов «разрез» и «коагуляция») при рассечении папиллы.
Использовали два варианта рассечения папиллы: па-пиллотомию, когда рассекали только «розетку» сосочка, и папиллосфинктеротомию, при которой разрез проходил по интрамуральной части холедоха, проксимальнее папиллы. Длина разреза во многом определялась характером патологических изменений желчных протоков и папиллы и зависела от вида, формы и протяженности продольной складки двенадцатиперстной кишки, и составляла от 8 до 30 мм, чаще - от 10 до 13 мм. При этом стремились разрушить нижний сфинктер Бойдена, сфинктер ампулы, сохраняя верхний, что, собственно, является профилактикой дуоденобилиарного рефлюкса. Использовали три основных способа ЭПСТ: канюляционный, неканюляционный и смешанный. Методика канюляционной ЭПСТ заключалась в канюляции устья БДС папиллотомом так, чтобы его режу-
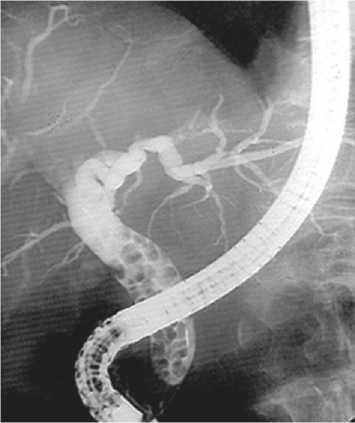
Фото 1: ЭРХПГ. Множественный холедохолитиаз
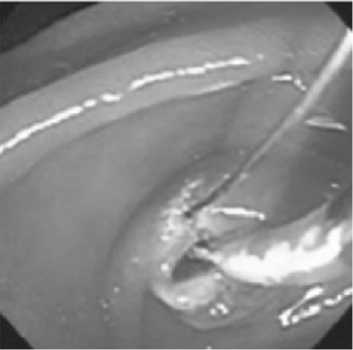
Эндофото 5: Методика канюляционной ЭПСТ
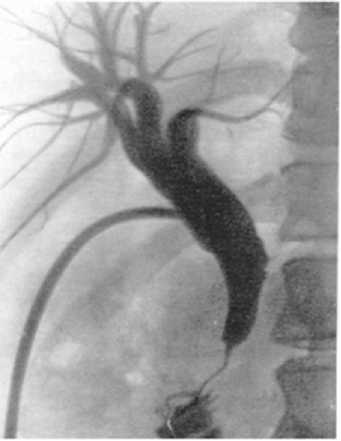
Фото 2: ЭРХПГ. Папиллостеноз и стеноз ТОХ
интрамурального отдела холедоха (продольной складки нисходящего отдела двенадцатиперстной кишки), характера заболевания, варианта предыдущей операции и цели настоящей операции.
Основными принципами адекватного проведения операции ЭПСТ явились:
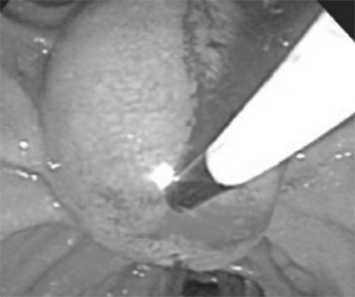
Эндофото 6: Методика неканюляционной ЭПСТ
щая часть была обращена в сторону холедоха, что соответствует 11-12 часам поля зрения дуоденоскопа (эндофото 5). При вколоченном в БДС камне, когда ввести папиллотом в устье не преставилось возможным, использовали нека-нюляционный способ ЭПСТ. Папиллотомом игольчатого типа осуществляли разрез от устья БДС по центру продольной складки двенадцатиперстной кишки непосредственно над вклиненным камнем (эндофото 6). Смешанный способ ЭПСТ включал сочетание двух первых: папиллотомом игольчатого типа рассекали «розетку» сосочка до отверстия, способного пропустить папиллотом типа Демлинга или Сома. Затем осуществляли канюляционную ЭПСТ.
При выполнении ЭПСТ применяли смешанный режим коагуляции и резки с преобладанием резки. Адекватность ЭПСТ контролировали непосредственно после ее завершения по величине разреза и скорости эвакуации контрастного вещества из холедоха. Длина папиллотомного разреза максимально возможно приближалась к диаметру общего желчного протока, а скорость эвакуации контрастного вещества составляла не ниже 3 мл/мин.
В 29% случаев папиллолитиаза для рассечения «крыши» БДС применялась атипичная папиллотомия игольчатым ножом с последующей инструментальной экстракцией конкрементов или с их самопроизвольным отхождением в просвет ДПК; в 12% – выполнена канюляционная папил-лосфинктеротомия и в 59% – атипичная папиллотомия была дополнена канюляционной папиллосфинктеротоми-ей. Во всех случаях после рассечения папиллы выполняли ЭРПХГ. В 69% случаев выявлен множественный холедохо-литиаз и при первичном вмешательстве удалены все рентгеноконтрастные конкременты (фото 1). В 31% случаев, после длительно протекающих и незавершенных литоэкстракций, были установлены билиарные пластиковые стенты. Впоследствии этим больным вторым или третьим этапом завершали транспапиллярную литоэкстракцию.
В 5-х наблюдениях результаты рентгенологических методов диагностики не позволили однозначно оценить при- чины и уровни окклюзии дистальной части ОЖП: этим больным непосредственно перед ретроградным вмешательством выполнили эндоскопическую ультрасонографию, по результатам которой были диагностированы рентгеннега-тивные и по этой причине недоступные для визуализации конкременты в терминальной части холедоха (фото 3 и 4).
Кроме того, эндосонография у 58 (8,4%) пациентов до ЭРХПГ позволила провести дифференциальный диагноз между аденомой и аденокарциномой БДС при внутриампу-лярном их расположении, 34 пациентам (5%) со стенозом ТОХ, выполненная через 2-3 дня после декомпрессии, ЭУС дополнила информацию об этиологии заболевания (фото 5).
Результаты и их обсуждение: в раннем послеоперационном периоде у 64% больных с острым билиарным панкреатитом в течение 1-3 суток отмечена регрессия явлений последнего с полным или частичным купированием болевого синдрома и снижением уровня амилаземии. В 32% случаев наблюдалась транзиторная амилаземия (до 1500 ед/л), сохранявшаяся до 3-х суток, что объяснялось длительностью догоспитального этапа болезни (70%) или электротравмой устья панкреатического протока (30%). Этой категории больных на 2–е сутки после декомпрессионного ретроградного вмешательства было выполнено стентирование главного панкреатического протока. Лечение острого билиарного панкреатита ограничилось консервативной терапией, панкреатические стенты были удалены через 2-3дня (после нормализации лабораторных показателей). У 4-х больных (3,6%) в послеоперационном периоде развился панкреоне-кроз, который впоследствии потребовал неоднократного оперативного лечения (оментобурсостомия, некрсекве-стрэктомия), в последующем 2 из 4 пациентов умерли от гнойно-септических осложнений.
У 17 (81%) больных с папиллитом была выполнена не-канюляционная ЭПСТ для разрешения острой окклюзии БДС. 2 (9,5%) пациентам удалось заканюлировать устье БДС и рассечь папиллу, не затрагивая интрамуральную часть
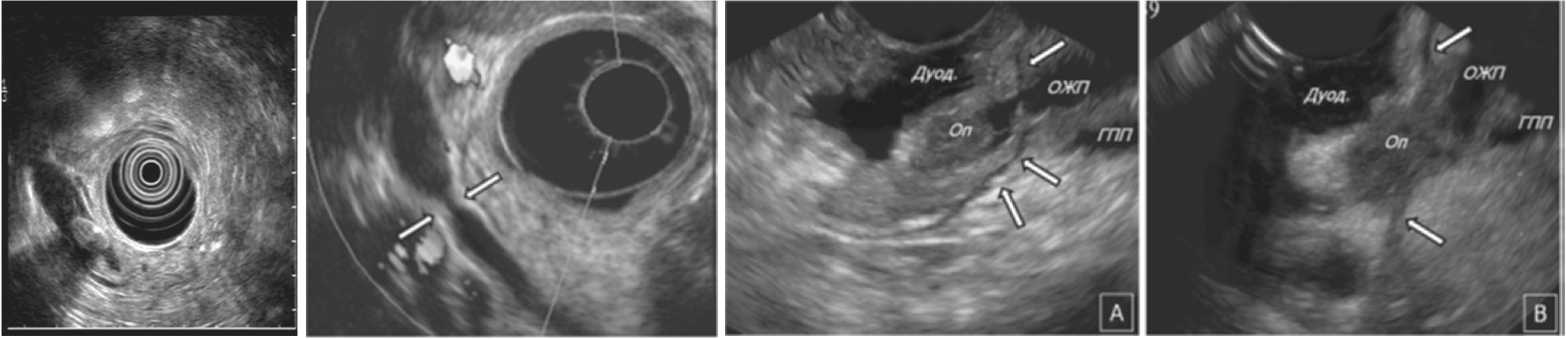
Фото 3: ЭндоУЗИ: Фото 4: ЭндоУЗИ. A B
Холедохолитиаз Рубцовый стеноз ОЖП Фото 5: Опухоль БДС. ЭндоУЗИ.
А – аденома БДС, опухоль не выходит за пределы подслизистого слоя двенадцатиперстной кишки; В – аденокарцинома БДС, опухоль инфильтрирует мышечный слой стенки двенадцатиперстной кишки, терминальный отдел холедоха и паренхиму поджелудочной железы
ОЖП. У 2-х (9,5%) из 21 папиллит разрешился консервативно.
При внутриампулярных опухолях (аденоме) у 12 больных была выполнена неканюляционная ЭПСТ для биопсии и декомпрессии желчных протоков.
При раке БДС 22 пациентам после биопсии опухоли выполнялась смешанная ЭПСТ, 10- канюляцию холедоха удалось выполнить после атипичной (неканюляционной) ЭПСТ, после - всем пациентам были установлены пластиковые стенты. Из 32 больных только 7 (22%) были радикально оперированы (операция ПДР), 23 некурабельным пациентам через 2-3 недели после декомпрессии выполнена замена пластикового стента на СМР металлический стент.
При доброкачественных стенозах папиллы и ТОХ (23 пациента) для достижения декомпресии применили типичные и смешанные способы ЭПСТ, баллонную дилятацию с последующим пластиковым эндопротезированием холедоха. При раке ТОХ канюляция осуществлялась в основном после типичной ЭПСТ, исследование заканчивали стентированием ОЖП.
Общая летальность среди больных с острой окклюзией БДС составила 1,8%.
Выводы
Эндоскопические транспапиллярные вмешательства являются методом выбора в лечении больных с острой окклюзией БДС и механической желтухой, направленным на восстановление естественного желчеоттока и устранение билиарной и панкреатической гипертензии. Оправдано стремление к выполнению радикальной холедохолитоэк-стракции у пациентов с множественным холедохолитиазом при синдроме острой окклюзии БДС. В подобных клинических ситуациях необходимо проводить билиодуоденальное стентирование с целью снижения риска повторных вмешательств, и, как следствие, улучшения прогноза заболевания. Больным с длительным (более суток) анамнезом билиарного панкреатита (с лечебной целью) или с ятрогенной электротравмой устья панкреатического протока (с профилактической целью) необходимо одномоментно стентировать ГПП на 1-2 дня до нормализации клинико-лабораторных показателей. Более широкое внедрение в клиническую практику ЭУС для уточняющей диагностики причин острой окклюзии терминальной части холедоха и БДС позволит оптимизировать алгоритм диагностики и лечения больных с механической желтухой.
Список литературы Дифференцированный подход в эндоскопическом лечении больных с окклюзией БДС
- Гальперин Э. И., Ветшев П. С. Руководство по хирургии желчных путей. М.; 2006.
- Guitron A., Huerta F., Macias M. et al. Management of difficult cases of biliary litiasis. Rev. Gastroenterol. Mex. 2015; 60 (3): 140-144.
- Савельев В. С. 50 лекций по хирургии. М.; 2003.
- Гальперин Э. И., Котовский А. Е. Лечение больных желчнокаменной болезнью, осложненной механической желтухой и холангитом. В кн.: Пленум эндоскопической хирургии. СПб.; 2003.
- Ветшев П. С. Диагностический подход при обтурационной желтухе. Рос. журн. гастроэнтерол., гепатол., колопроктол. 2009; 6: 18-24.
- Гвоздик В.В., Гвоздик Вл.В., Амеличкин М.А. и др. Эндоскопическое лечение гнойного холангита при холангиолитиазе. Материалы XI Московского международного конгресса по эндоскопической хирургии: Москва, 18-20 апреля 2007г. -С. 125-126.
- Снегирев Ю.В., Гвоздик Вл.В., Трошкин В.В. и др. Эндоскопическая папиллотомия: виды и клиническое применение. Материалы XI Московского международного конгресса по эндоскопической хирургии: Москва, 18-20 апреля 2007г. -С. 361-362.
- Старков Ю.Г., Солодинина Е.Н., Шишин К.В., Плотникова JI.C. Роль эндоскопической ультрасонографии в хирургии. Материалы XI Московского международного конгресса по эндоскопической хирургии: Москва, 18-20 апреля 2007г. -С. 378-380.
- Maguchi H., Takahashi K., Katanuma A. Endoscopic management of biliary and pancreatic ducts strictures//Digestive Endoscopy. 2004. -Vol. 16.-P. 34-38.
- Samardzic J., Latic F., Kraljik D. et al. Treatment of common bile duct stones, is the role of ERCP changed in era of minimally invasive surgery? Med. Arh. 2010; 64 (3): 187-188.


