Дифференцированный подход в лечении больных с повреждением печени при абдоминальной травме
Автор: Шабунин А.В., Бедин В.В., Греков Д.Н., Тавобилов М.М., Цуркан В.А., Дроздов П.А.
Журнал: Московский хирургический журнал @mossj
Статья в выпуске: 4 (50), 2016 года.
Бесплатный доступ
Цель: Улучшить результаты лечения больных с повреждением печени при абдоминальной травме. Материалы и методы: До мая 2014 года травма печени являлась показанием к оперативному вмешательству, вне зависимости от степени повреждения печени. За этот период пролечено 173 больных. У всех больных выполнено оперативное вмешательство. С мая 2014 года по июль 2016 48 больных применен дифференцированный подход к лечению. «Открытые» оперативные вмешательства выполнены 26 больным (54,2%), неоперативное лечение применено 22 больным (45,8%). Результаты: Применение дифференцированного подхода в лечении больных с повреждением печени позволило уменьшить как послеоопера-ционную (12,7% против 11,5%) так и общую летальность у больных второй группы по сравнению с первой группой (12,7% против 6,25%), а также уменьшить среднее время пребывания больного в стационаре (17,76 против 7,23 дней) и среднюю кровопотерю (1365 мл против 1230 мл). Заключение: Применение дифференцированного подхода в лечении больных с травмой печени позволяет уменьшить общую летальность, сократить время пребывания больных в стационаре и уменьшить затраты на лечение.
Повреждение печени, дифференцированный подход, оперативное вмешательство
Короткий адрес: https://sciup.org/142211274
IDR: 142211274
Текст научной статьи Дифференцированный подход в лечении больных с повреждением печени при абдоминальной травме
Травмы печени относятся к наиболее тяжёлым, сложным для диагностики и лечения абдоминальным повреждениям. Они составляют около трети всех травм органов брюшной полости, наиболее частой причиной закрытых травм печени является автодорожная травма, процент которой достигает 40 [1,2], основной контингент пострадавших, это мужчины трудоспособного возраста. Общая послеоперационная летальность при повреждениях печени достигает 10-15% и увеличивается до 40-50% у больных с IV и V степенью по AAST [3, 4].
При травме печени особенно важен фактор времени. Диагностика и лечение должны быть проведены с минимальной затратой времени и максимальной эффективностью. Если простыми, безопасными, довольно информативными методами можно быстро и достоверно установить точный диагноз, не обязательно прибегать к более сложным методам диагностики [5, 6].
В течение последнего столетия подходы к лечению тупой травмы печени изменились от наблюдения и выжидатель- ной тактики в начале 1900 годов до, в большей части, оперативной агрессии, и в настоящее время до избирательных операций и неоперативному подходу по показаниям [7, 8].
Современная парадигма неоперативного лечения (НОЛ) травм печени у взрослых была стимулирована удачным опытом неоперативного лечения с повреждением солидных органов у детей. Преимущества этого подхода в исключении напрасной лапаротомии, воспалительных интраабдоми-нальных осложнений, уменьшения количества трансфузий, ранней выписке и снижение затрат не лечение. Начиная с 1990-х годов, было опубликовано большое количество статей по этой теме, которые показывали возможность успешного лечения больных с травмой печени у 80-94% без оперативного лечения [9, 10, 11]. Результатом этих публикаций стали обновленные рекомендации Европейского общества хирургов и травматологов (EAST) для НОЛ тупой травмы печени (ТТП) и селезенки.
НОЛ ТТП в настоящее время это метод лечения у гемодинамически стабильных пациентов независимо от степени травмы и возраста больных. Больные, подверженные НОЛ,
должны быть обеспечены возможностями для мониторинга, периодической клинической оценке и возможности немедленного использования операционной. Пациенты же с нестабильной гемодинамикой и перитонеальными симптомами должны быть немедленно подвержены операции.
Компьютерная томография с контрастным усилением это «золотой» стандарт для установления степени травмы и определения дальнейшей тактики лечения [12]. Ангиографическое исследование с эмболизацией сосудов, чрескожное дренирование, эндоскопическая ретроградная пан-креатохолангиография и лапароскопия остаются важным дополнением в НОЛ ТТП [13].
Материал и методы
С января 2008 по июль 2016 года в ГКБ им. С.П. Боткина находились 941 больной с травмой органов брюшной полости. Из них 734 мужчины (78%) и 207 женщин (22%). Открытая травма была у 427 больных (45,4%), закрытая у 514 больных (54,6%). Средний возраст больных составил 36,16±9,32 лет.
Травма печени была диагностирована у 221 больного (23,4%). Закрытая травма печени - 102 больных (46,2%), открытая травма печени - 82 больных (37,1%), изолированная травма печени - 37 больных (16,7%).
Для определения тяжести повреждения печени и прогнозирования динамики кровотечения использовали классификацию травмы паренхиматозных органов, предложенную E.Moore (1986 год). Для определения тяжести повреждения печени выполняли компьютерную томографию (КТ) органов брюшной полости с внутривенным контрастированием. Распределение больных по тяжести повреждения печени было следующим: I степень - 55 больных (24,9%), II степень - 69 больных (31,2%), III степень -64 больных (28,9%), IV степень - 28 больных (12,7%), V степень - 5 больных (2,3%) (Диаграмма 1).
До мая 2014 года диагностированная травма печени являлась показанием к оперативному вмешательству, вне зависимости от степени повреждения печени. В эту группу вошли 173 больных (78,3%). Открытое оперативное вмешательство выполнено у большинства больных - 156 пациентов (90,2%), лапароскопическая остановка кровотечения - 17 больных (9,8%).
При выполнении открытого оперативного вмешательства мы выполняем широкую срединную лапаротомию для проведения полноценной ревизии органов брюшной полости. Доступ можно расширить по Рио-Бранко, либо до торокаофре-нолапаротомии. При операциях на печени всегда используем ранорасширители типа
«Сигала». При продолжающимся кровотечении на первом этапе проводим тампонаду раны печени, затем накладываем турникет на печеночно-двенадцатиперстную связку. При необходимости выполняем полную сосудистую изоляцию печени с наложением турникетов на нижнюю полую вену выше печеночных вен и выше устья почечных вен. Перед выполнением ревизии раны печени проводим ее мобилизацию, заключающуюся в пересечении связочного аппарата печени и вывихивании правой доли печени из ее ложа путем отделения от париетальной брюшины. Ревизия раны печени заключается в удалении сгустков, выявлении источника кровотечения и выполнениие гемостаза. Источником кровотечения чаще всего являются дефекты в венах, относящихся либо к системе печеночных вен, либо к системе воротной вены. Знание этого аспекта может помочь избежать осложнений, таки как ишемия и некроз, либо блок оттока определенного участка печени. Поэтому, по возможности отдаем предпочтение ушиванию дефекта в вене атравматичной нитью 4-0 или 5-0. Нежизнеспособные участки печеночной паренхимы удаляются по типу атипичной резекции. Большие размозженные участки печени стараемся не ушивать, а выполняем гемостаз и желчестаз раневой поверхности и проводим адекватное дренирование данной области. Дренирование с использованием марлевых тампонов нежелательно, т.к. это может привести к повторному кровотечению после их удаления и к инфицированию данной области. Только в случае временной остановки кровотечения и планировании больного на отсроченную операцию можно использовать данный прием. Показаниями к холецистостомии считаем большие по площади повреждения печеночной паренхимы, наличие желчи в ране и центральные повреждения печени. При небольших разрывах печени дефект в ней ушиваем с обязательным использова-
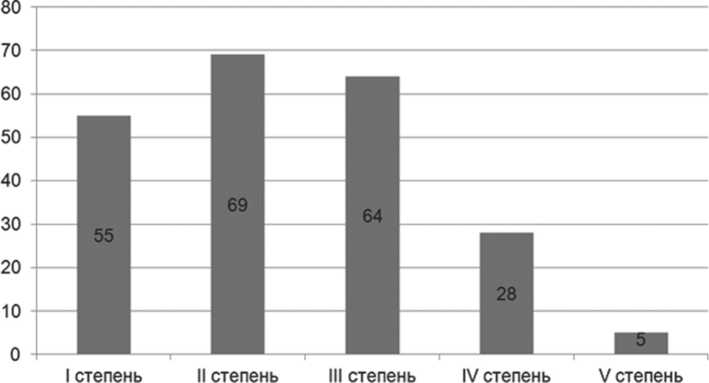
Диаграмма 1. Распределение больных по тяжести повреждения печени согласно классификации AAST
нием только атравматичной рассасывающей нити. По показаниям укладываем или тампонируем рану гемостатическими губками или пленками, которые также используем и при поверхностных разрывах без ушивания печени. При повреждениях, протекающих с массивным кровотечением, которые не удается остановить перечисленными выше методами и, самое главное, сопровождающиеся нестабильной гемодинамикой мы используем тактику под названием «damage control surgery». Данный прием применен у 14 больных. Суть ее заключается в сокращенном оперативном вмешательстве и временной интраабдоминальной тампонаде для сохранения жизни пострадавшему, находящемуся в критическом состоянии, с последующим выполнением специализированной реконструктивно-восстановительной операции и окончательным устранением последствий тяжелой сочетанной травмы.
С мая 2014 года мы стали применять новый алгоритм лечения больных с тупой травмой печени, суть которого в первую очередь, заключается в определении стабильности статуса пациента и степени тяжести травмы по данным проведенного обследования. При отсутствии признаков продолжающегося кровотечения больные распределялись в группу НОЛ, для проведения которой пациенты госпитализировались в реанимационное отделение, где проводились противошоковые мероприятия, динамическая оценка изменение статуса больного, динамическое УЗИ каждые 4 часа. При необходимости, по показаниям выполнялись дренирования под контролем УЗИ; ЭРХПГ, ангиография с эмболизацией, лапароскопия. Любые сомнения в неэффек-
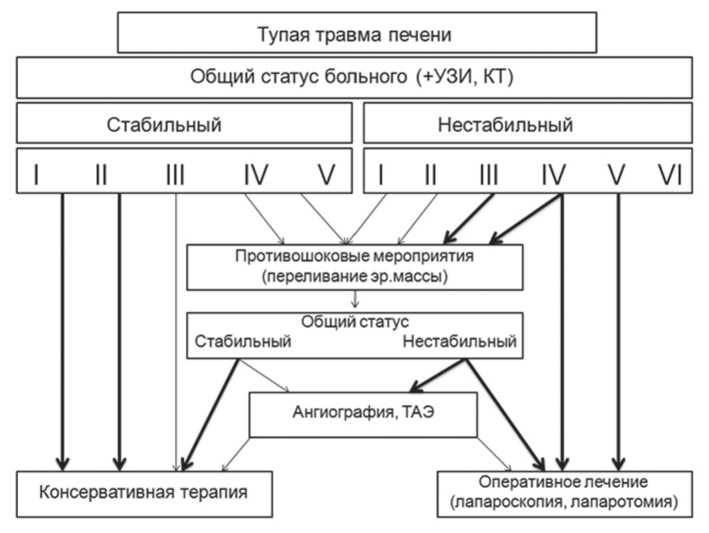
Схема 1. Алгоритм диагностики и лечения больных с повреждением печени
тивности консервативного лечения являлись показанием к операции (схема 1).
Показанием к применению рентгенэндоваскулярных методик является наличие экстравазации контрастного препарата в полость гематомы при КТ органов брюшной полости (рисунок 1). Эмболизацию сосудов выполняем стальными микроспиралями.
Показанием к ЭРХПГ, санации холедоха является билиарная гипертензия на фоне гемобилии с явлениями механической желтухи, которая не купируется проведением консервативной терапии.
Дренирования жидкостных скоплений печени выполняем при подозрении на их инфицирование.
Больным, которым применен дифференцированный подход, составили вторую группу, в нее вошли 48 больных. «Открытые» оперативные вмешательства выполнены 26 больным (54,2%), НОЛ применено 22 больным (45,8%). Из них ангиография с эмболизацией сосудов потребовалась 9 больным, ЭРХПГ с ревизией и санацией общего желчного протока 1 больному, дренирование инфицированных жидкостных скоплений под УЗ-контролем 2 больным.
Результаты
Средняя кровопотеря у больных I группы составила 1365 ± 845 мл: от 300 до 4100 мл. Осложнения были у 72 больных (43,1%). Из них специфических у 24 больных (14,0%). У 5 больных наблюдались сочетание нескольких осложнений. Среди специфических осложнений наиболее часто встречались: желчный свищ - 9; инфицированная билома - 6; абсцесс печени – 11; внутрибрюшное кровотечение - 5.
Послеоперационная летальность составила 12,7% (22 больных). Основной причиной смерти явилась полиорганная недостаточность на фоне геморрагического шока. Общая летальность составила 12,7%. Средняя длительность госпитализации в первой группе составила 17,76±8,75 дня.
о второй группе экстренное оперативное вмешательство в первый час от момента поступления в стационар потребовалось 15 больным (31,25%). У 33 (68,75%) больных, учитывая отсутствие явных явлений продолжающегося кровотечения на момент поступления в стационар, начато проведение консервативной терапии. У 11 больных (22,9%), при динамическом наблюдении отмечена отрицательная динамика, как по результатам инструментального обследования (нарастание свободной жидкости в брюшной полости), так и клинически (нестабильность гемодинамики на фоне проведения инфузионно-трансфузионной
терапии). Этим больным выставлены показания к «открытому» оперативному вмешательству.
Оперативные вмешательства выполнялись по вышеперечисленным принципам. Средняя кровопотеря составила 1230 ± 545 мл. Осложнения были у 13 больных (50%). Специфические осложнения у 7 больных (26,9%). Их них: желчный свищ у 3 больных, внутрибрюшной кровотечение у 2 больных, абсцесс печени у 2 больных. Послеоперационная летальность составила 11,5% (3 больных).
Ангиография с эмболизацией сосудов выполнена 9 больным. Во всех случаях удалось выявить источник кровотечения и выполнить селективную эмболизацию, что позволило избежать оперативного вмешательства (рис. 2-3). Эмболизация выполнялась в первые сутки после поступления в стационар. Средний период госпитализации составил 5,97±2,64 дня. Послеоперационных осложнений и летальности не было.
НОЛ без применения миниинвазививных и «открытых» вмешательств была проведена у 13 больных. Среди больных, которым применен данный метод лечения летальности не было. Средний срок госпитализации составил 3,27±2,32 дня.
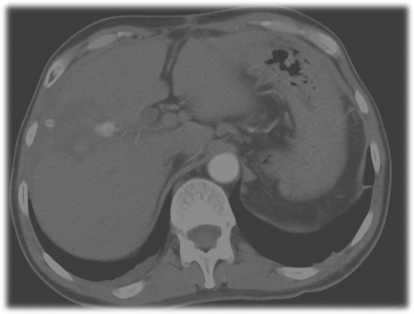
Рис. 1. МСКТ органов брюшной полости с внутривенным контрастированием. Травма печени класс IV по AAST. Экстравазация контраст- ного препарата в полость гематомы
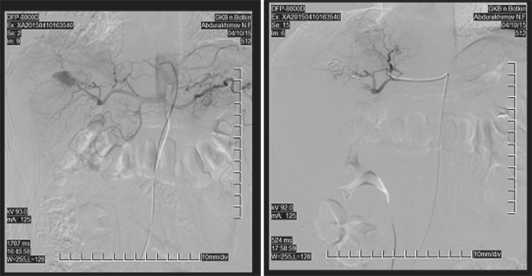
Рис. 2-3. Ангиография. Травма печени класс IV по AAST. Экстрава-зация контрастного препарата в полость гематомы. Артериальная эмболизация
Общая летальность во второй группе составила 6,25% (3 больных). Средняя длительность госпитализации 7,23±2,56 дня.
Обсуждение
В группе, где был применен дифференцированный подход в лечении больных с ТТП, оперативная активность составила - 54,2%. Остальным пациентам проведено либо строго консервативное лечение, либо им были использованы миниинвазивные способы лечения (эмболизация, ЭРХПГ, дренирование).
При сравнении двух групп, послеоперационные осложнения (43,1% против 50%) были выше у оперированных больных второй группы. Это объясняется тем, что оперированные больные второй группы имели значительно более тяжелые повреждения печени, что не позволило применить консервативные методы лечения. Однако, применение дифференцированного подхода в лечении больных с ТТП позволило не только незначительно уменьшить послеоопера-ционную (12,7% против 11,5%) но и значительно уменьшить общую летальность у больных второй группы по сравнению с первой группой (12,7% против 6,25%), а также уменьшить среднее время пребывания больного в стационаре (17,76 против 7,23 дней) и среднюю кровопотерю (1365 мл против 1230 мл).
Активное внедрение в широкую клиническую практику высокоинформативных методов диагностики, таких как КТ органов брюшной полости с внутривенным контрастированием, ультразвуковых аппаратов экспертного класса, ангиографии позволяют с высокой точностью классифицировать травматические повреждения печени и определять дальнейшую тактику лечения у больных с тупой травмой печени.
Решающими факторами, определяющими эффективность НОЛ, являются, во-первых, правильный отбор, во-вторых, - неоднократное и частое обследование в первые 2-3 суток после травмы.
В настоящее время УЗИ используют как скрининговый метод, позволяющий выявить морфологические изменения печени и проследить за их динамикой. Иногда, по разным причинам, УЗИ малоинформативно, в таких случаях используется КТ с внутривенным контрастированием. Отрицательная динамика, выявленная этими методами, служит показанием к доплерографии (УЗДГ) и ангиографии, причем последняя является не только диагностической, но и лечебной процедурой, позволяющей осуществить гемостаз эндоваскулярными методами. Эндоваскулярные методы гемостаза основаны на введении в поврежденный сосуд склерозирующих веществ, эмболов, баллонов, спиралей, создающих механическое препятствие кровотоку с последующим тромбозом, что приводит к окклюзии просвета.
Использование минимально инвазивных методов лечения, таких как ангиография с эмболизацией сосудов,
ЭРХПГ, дренирование под УЗ-контролем позволяют повысить процент успешного лечения при НОЛ.
Применение данного алгоритма лечения возможно только в многопрофильных стационарах с наличием высокоинформативных исследований (экспертное УЗИ, КТ) и ангиографической бригады, способной выполнить селективную эмболизацию сосудов.
Выводы
Применение дифференцированного подхода в лечении больных с травмой печени позволяет уменьшить общую летальность, сократить время пребывания больных в стационаре и уменьшить затраты на лечение.
Список литературы Дифференцированный подход в лечении больных с повреждением печени при абдоминальной травме
- Абакумов, М.М. Повреждения живота при сочетанной травме/М.М. Абакумов, Н.В. Лебедев, В.И. Малярчук -М.: Медицина, 2005. -С. 176.
- Гуляев, А.А. Видеолапароскопия при закрытой травме живота/А.А. Гуляев //Эндоскопическая хирургия -2006. -№ 2. -С. 36-37.
- Борисов, А.Е. Диагностика и хирургическое лечение изолированных и сочетанных травматических повреждений печени/А.Е. Борисов //Вестн. хирургии. -2007. -№ 4 (166). -С. 35-39.
- Гуманенко, Е.К. Военно-полевая хирургия/Е.К. Гуманенко. -М.: ГЭОТАР-Медиа, 2008. -С. 763.
- Радыгина М.В., Ярцев П.А., Кирсанов И.И., Левитский В.Д. Видеолапароскопическая диагностика и лечение повреждений печени при травме живота///Анналы хирургической гепатологии. -2008. -№3. -С. 228-229.
- Бойко В.В., Тарабан И.А., Замятин П.Н., Черняев Н.С. Современные аспекты диагностики и хирургического лечения 11. повреждений печени///Харювська хiрургiчна школа. -2010. -№6. C. 94-101.
- Урман М.Г., Субботин А.В. Хирургическая тактика при травме печени и развившихся внутрибрюшных осложнениях. Вестник хирургии. 2009. № 3. С. 72-75.
- Эргашев О.Н., Гончаров А.В., Прядко А.С., Виноградов Ю.М. Повреждение печени у пострадавших с тяжёлой сочетанной травмой. Вестник хирургии. 2011. № 6. С. 52-55.
- Carrillo EH, Spain DA, Wohltmann CD, Schmieg RE, Boaz PW, Miller FB, et al. Interventional techniques are useful adjuncts in nonoperative management of hepatic injuries. J Trauma. 1999;46:619-622.
- Shapiro MB, Nance ML, Schiller HJ, Hoff WS, Kauder DR, Schwab CW. Nonoperative management of solid abdominal organ injuries from blunt trauma: impact of neurologic impairment. Am Surg. 2001;67:793-796
- Velmahos GC, Toutouzas KG, Radin R, Chan L, Demetriades D. Nonoperative treatment of blunt injury to solid abdominal organs: a prospective study. Arch Surg. 2003;138:844-851.
- Fang J, Chen R, Wong Y, Lin B, Hsu Y, Kao J, et al. Pooling of contrast material on computed tomography mandates aggressvie management of blunt hepatic injury. Am J Surg. 1998;176:315-319.
- Johnston JW, Gracias VH, Reilly PM. Hepatic angiography in the damage control population. J Trauma.2001;50:176.


