Диизобутилены. Конкурентные превращения в процессах олигомеризации изобутилена и алкилирования ароматических субстратов на сульфокатионитах
Автор: Шураев Максим Васильевич, Таразанов Сергей Вячеславович, Крымкин Никита Юрьевич, Нестерова Татьяна Николаевна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Статья в выпуске: 6-2 т.15, 2013 года.
Бесплатный доступ
Выполнена олигомеризация изобутилена и алкилирование фенола на перспективном промышленном катализаторе Amberlyst 36 Dry. Установлено, что при температурах выше 373 К наряду с основным превращением протекает деструкция тетрамеров изобутилена и алкильных заместителей в молекулах трет -октилфенолов. Олигомеризация сопровождается изомеризацией алкенов.
Олигомеризация, изобутилен, диизобутилены, сульфокатионит, фенол, конкурентные превращения
Короткий адрес: https://sciup.org/148202590
IDR: 148202590 | УДК: 66.095.261.4:66.095.253
Diizobutilene. Competitive transformations in processes of oligomerization the isobutylene and alkylation the aromatic substrate on sulfokationite
The oligomerization of isobutylene and phenol alkylation on the perspective industrial Amberlyst 36 Dry catalyst is executed. It is established that at temperatures above than 373 K on a row with the main transformation destruction of tetramer of isobutylene proceeds and the alkilnykh of deputies in molecules tret-oktilphenols. Oligomerization is accompanied by isomerization of alkenes.
Текст научной статьи Диизобутилены. Конкурентные превращения в процессах олигомеризации изобутилена и алкилирования ароматических субстратов на сульфокатионитах
Топливное направление переработки нефти предполагает использование ряда процессов, позволяющих получать синтез-газ, ароматические углеводороды, нафтены, олефины, идущие на дальнейшую переработку в нефтехимическую продукцию. Продукты олигомеризации олефинов применяются как компоненты моторных топлив, исходные вещества для производства пластификаторов, лекарственных препаратов, смол, моющих средств, смазок, присадок к маслам и топливам. Продукты димеризации олефинов нашли применение для получения высших алкилфенолов, которые стали одними из важнейших полупродуктов в нефтехимии и промышленном органическом синтезе. Применение алкилфенолов обусловлено их легкой окисляе-мостью, интересно их использование в качестве антиокислителей для авиационных топлив, смазочных масел, различных жиров и других важных компонентов. Олигомеризация олефинов направлена на получение углеводородов, обладающих важными свойствами. В работе [1] нами приведен состав продуктов олигомеризации изобутилена и превращений триметилпентенов (ТМП). Многообразие получаемых продуктов указывает на протекание конкурентных превращений при олигомеризации изобутилена. В данной работе рассматриваются превращения продуктов олигомеризации в различных средах.
Шураев Максим Васильевич, аспирант Таразанов Сергей Вячеславович, аспирант Крымкин Никита Юрьевич, аспирант
диизобутилены, сульфокатионит, фенол, конку-
Экспериментальная часть. Условия проведения олигомеризации изобутилена и превращений димеров приведены в [1]. Алкилирование фенола ТМП выполнено в изотермическом реакторе идеального смешения, в рубашке которого кипел теплоноситель (бензол, толуол или ацетон). Во всех экспериментах использовали сульфокатионит Amberlyst 36 Dry. Фенол произведен ОАО «НК «РОСНЕФТЬ» ООО «Новокуйбышевский завод масел и присадок» и имел содержание основного вещества 99,5% масс. Фенол и катализатор помещались в реакционную часть. Количество сульфокатионита составляло 15±1% масс. от массы фенола и алкена. Смесь катализатора и фенола выдерживали в течение 1 часа при температуре кипения теплоносителя. Затем в реактор вводились ТМП в соотношении 1моль ТМП на 6 моль фенола.
Продукты алкилирования фенола анализировали методом газовой жидкостной хроматографии на программно-аппаратном комплексе «Хроматэк-аналитик» на базе хроматографа «Кристалл-2000М» с пламенно-ионизационным детектором и кварцевой капиллярной колонкой с привитой фазой SE-30 – 50 м х 0,25 м, давление на входе – 3 атм., газ-носитель – гелий, объем пробы 0,1 мкл, время анализа – 36 минут, точность поддержания температуры в термостате колонок ±0,2 К.
Обсуждение результатов. Олигомеризация изобутилена протекает с образованием продуктов, подробно рассмотренных нами в работе [1]. На рис.1 представлено изменение концентрации продуктов олигомеризации изобутилена в зависимости от времени контакта. Накоплению димеров следует увеличение концентрации тримеров и тетрамеров изобутилена.
тетрамеров изобутилена существенна. Тримеры образуются в незначительных количествах, не более 1% масс. за время контакта 115 мин. (рис. 4).
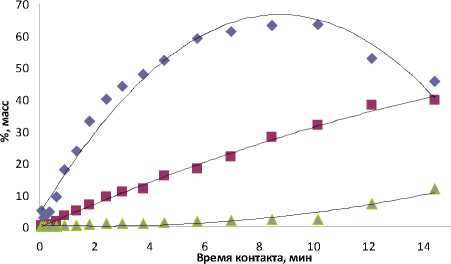
Рис. 1. Продукты олигомеризации изобутилена при 318 К, в зависимости от времени контакта: ♦ - димеры, ■ – тримеры, ▲ – тетрамеры, % масс.
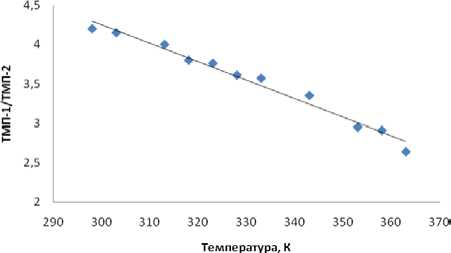
Рис. 3. Соотношение концентраций триметилпентенов
Уже при минимальном времени контакта 0,15 мин. в реакционной массе присутствуют тримеры и тетрамеры изобутилена (рис. 1), однако их концентрация незначительна и составляет менее 0,3% масс. для тримеров и 0,02% масс. для тетрамеров. Увеличение температуры приводит к снижению концентрационного уровня димеров с 60% масс. (рис. 1) до 30% масс. (рис. 2), при этом концентрация тетрамеров увеличивается до 20% масс.
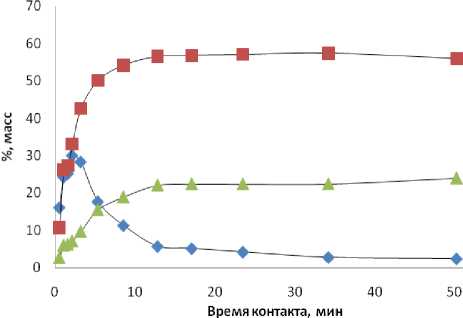
Рис. 2. Выход продуктов олигомеризации изобутилена при 343 К: ♦ - димеры, ■ – тримеры, ▲ – тетрамеры, % масс.
Помимо олигомеризации изобутилена протекает изомеризация димеров. Соотношение концентраций основных представителей диизобутиленов быстро стабилизируется. В диапазоне 293-368 К постоянное значение достигается за время контакта от 1 до 5 мин. в зависимости от температуры реакции (рис. 3), полученные значения близки к приведенным в работах [2, 3].
Наряду с последовательной олигомеризацией изобутилена протекает димеризация ТМП. В мягких условиях (323 К) скорость образования
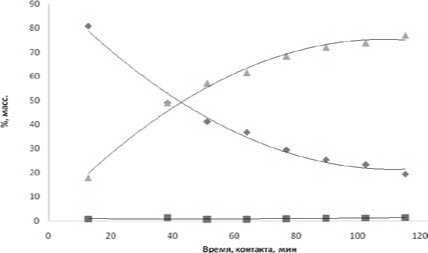
Рис. 4. Превращения ТМП при 323 К: ♦ - димеры, ■ – тримеры, ▲ – тетрамеры, % масс.
С увеличением температуры до 373 К при времени контакта более 10 мин. протекает деструкция тетрамеров с образованием тримеров, которые в данном случае преобладают над другими компонентами реакционной массы. За время контакта 55 мин. концентрация тримеров увеличивается до 50% масс., а концентрация тетрамеров не превосходит 20% масс. (рис. 5).
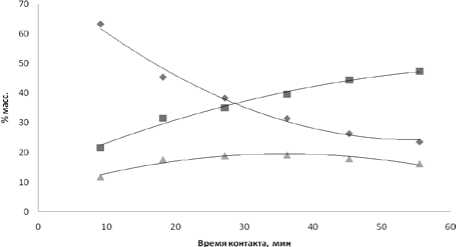
Рис. 5. Превращения ТМП при 403 К: ♦ -димеры, ■ – тримеры, ▲ – тетрамеры, % масс.
Увеличение температуры до 403 К приводит к дальнейшей деструкции тетрамеров. Степень деструкции достигает 90%. Схожая картина наблюдается при алкилировании фенола диизобутиленами на Amberlyst 36 Dry. Получение октилфенолов при относительно невысоких температурах (329 К; 353 К) сопровождается образованием примесей 4- трет -бутилфенола и 2- трет -бутилфенола (рис. 6). Однако при повышении температуры до 383 К картина резко меняется, за время реакции 250 мин. Концентрация трет -бутилфенолов увеличивается до 50 % масс. (рис. 7). Увеличение концентрации ТБФ связано с деструкцией алкильного заместителя октилфенолов. Данные подтверждаются резким снижением концентрации октилфенолов с повышением температуры (рис. 8).
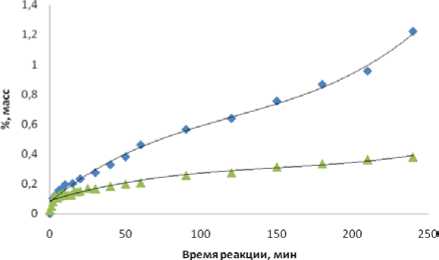
Рис. 6. Изменение концентрации трет бутилфенолов при изменении температуры реакции: ▲ –329 К; ♦ - 353 К
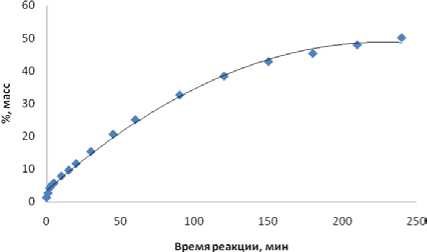
Рис. 7. трет -Бутилфенолы при 383 К
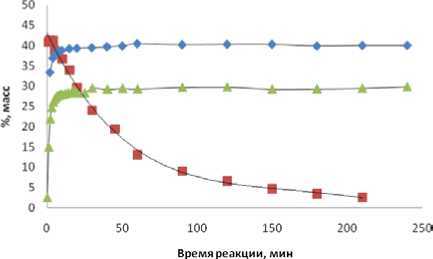
Рис. 8. Концентрация трет -октилфенолов при алкилировании фенола: ▲ – 329 К, ♦ - 353 К; ■ – 383 К
Помимо алкилирования фенола димерами и деструкции октилфенолов протекают превращения димеров. Выше сообщалось, что при 323 К на Amberlyst 36 Dry в значительном количестве реакционная масса представлена тетрамерами изобутилена (рис. 4). Аналогично, даже в присутствии высокоактивного фенола, протекает олигомеризация димеров изобутилена (рис. 9). Тетрамеры образуются в начальный момент времени, при максимальной концентрации димеров в реакционной массе. Увеличение времени реакции ведет к снижению их концентрации.
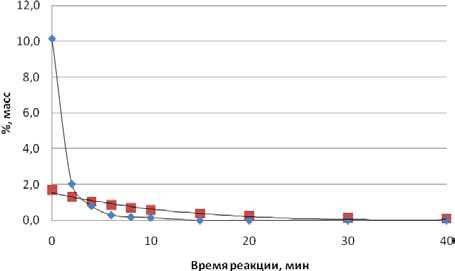
Рис. 9. Концентрация димеров и тетрамеров при 353 К: ♦ - димеры, ■ – тетрамеры % масс.
Выводы:
-
1. Экспериментально установлено, что при 343 К и выше максимальная концентрация тримеров и тетрамеров достигает 60 и 20% масс. соответственно.
-
2. В диапазоне 293-368 К соотношение концентраций диизобутиленов достигает постоянного значения за время контакта от 1 до 5 мин.
-
3. При 373 К и выше основные превращения сопровождаются значимой деструкцией тетрамеров изобутилена и алкильного заместителя в трет -октилфенолах.
Список литературы Диизобутилены. Конкурентные превращения в процессах олигомеризации изобутилена и алкилирования ароматических субстратов на сульфокатионитах
- Шураев, М.В. Олигомеризация изобутилена. Идентификация компонентов реакционной массы/М.В. Шураев, Т.Н. Нестерова, Е.В. Головин//Известия Самарского научного центра Российской академии наук. 2013. В печати.
- Karinen, R.S. Reaction Equilibrium in the Isomerization of 2,4,4-Trimethyl Pentenes/R.S. Karinen, M.S. Lylykangas, A.O.I. Krause//Ind. Eng. Chem. Res. 2001. 40. P. 1011-1015.
- Gallaway, W.S. Murray, M.J. Isomerization of Certain Olefins by Silica Gel at Room Temperature/W.S. Gallaway, M.J. Murray//J. Am. Chem. Soc. 1948. 70. P. 2584-2586.


