Динамическая МРТ - новый метод диагностики рака простаты
Автор: Китаев Сергей Вячеславович, Круглина Руслана Вячеславовна, Нестеров Сергей Николаевич
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Статья в выпуске: 1 т.4, 2009 года.
Бесплатный доступ
Методом динамической МРТ обследовано 50 больных с повышением уровня сывороточного ПСА. Выявлено 71 подозрительных очагов контрастного усиления. Распределение контрастного вещества в очагах проявлялось тремя типами динамических кривых. Первый тип (линейного усиления) наблюдался в 23 очагах, второй (раннее усиление в течение 1-2 мин с последующим плато) - в 24 очагах. Третий тип кривой (раннее усиление в течение 1-2 мин с последующим вымыванием контрастного вещества) - в 24 очагах. В аденокарциноме чаще (18 случаев) встречался 3 тип динамической кривой, что подтверждено критерием z (z= 3.953, p
Рак простаты, динамическая мрт, трансректальная биопсия
Короткий адрес: https://sciup.org/140187721
IDR: 140187721 | УДК: 616.65-006:
Текст научной статьи Динамическая МРТ - новый метод диагностики рака простаты
Рак простаты (РП) по частоте занимает второе место среди злокачественных заболеваний у мужчин, и c начала 90-х годов отмечается стойкая тенденция к увеличению его выявляемости среди средней возрастной группы [7]. Наиболее общепринятыми скрининговыми методами диагностики РП наряду со стандартным пальцевым исследованием считается определение уровня ПСА (простатспецифического антигена) сыворотки и трансректальное ультразвуковое исследование (ТРУЗИ). Хотя чувствительность и специфичность диагностики при сочетании трех методов (ТРУЗИ, пальцевое исследование и ПСА) достигает, соответственно, 90% и 85%, выявление рака при биопсии составляет всего 33% [8, 9, 10, 11]. С одной стороны, проблема состоит в низкой специфичности скрининговых методов и трудностях дифференциальной диагностики, с другой – отрицательный результат биопсии может быть объяснен ее неселективностью. Даже при использовании самой современной расширенной мультифокальной биопсии при традиционных методах отбора пациентов, процент выявленных раков по результатам некоторых исследователей [3] составляет всего 38%. Тем не менее, при повторной биопсии, выполненной прицельно из участков, которые при проведении трансректальной МРТ подозрительны на рак, процент подтверждения диагноза значительно выше [5].
Таким образом, становится очевидной необходимость введения дополнительных критериев добиопсий-ной диагностики РП с применением новых лучевых методов. В работах по изучению возможностей стандартной методики МРТ с поверхностной катушкой в диагностике локализованных форм рака было показано, что чувствительность метода зависит от степени дифференцировки опухоли. Вместе с тем, существуют исследования, в которых указывается, что в случаях обильной васкуляризации органа чувствительность ТРУЗИ в диагностике рака повышается с 75 до 81%, а специфичность с 40 до 77% [2]. В этой связи представляет интерес изучение особенностей фармакокинетики контрастного вещества при динамической МРТ с болюсным контрастированием [6]. В известных нам источниках все авторы отмечают раннее и интенсивное накопление контрастного препарата в раковой опухоли, однако для дифференциальной диагностики используются фармакокинетические параметры, расчет которых требует очень тщательного сбора данных, и громоздких вычислений, хорошо работающих в экспериментальной модели, но неосуществимых в клинической практике. Причем данные различных авторов достаточно противоречивы [4, 13, 15, 16, 17]. Таким образом, можно сказать, что на сегодняшний день нет универсальных рекомендаций, касающихся техники проведения и критериев оценки результатов динамической МРТ простаты.
Цель исследования – оценка возможностей динамической МРТ с болюсным контрастированием в диагностике локализованных форм РП и дифференциальной диагностике с доброкачественными изменениями.
Материал и методы
Обследовано 50 пациентов, у которых на основании повышения уровня ПСА крови в пределах от 3.8 нг/мл до
68 нг/мл высказано подозрение на РП. Средний возраст составлял 67 ± 8 лет. У всех больных МРТ проводилась до диагностической пункции. Магнитно-резонансную томографию выполняли на томографе с напряженностью магнитного поля 1.5 Т с использованием поверхностной катушки для тела. После стандартных режимов исследования всем пациентам проводили динамическую контрастную МРТ с болюсным контрастированием по описанной ниже методике.
До введения контрастного вещества выполняли нативный скан. Время выполнения одного скана в зависимости от количества срезов составляло от 14 до 16 с. После введения контрастного вещества выполняли серию динамических сканов: на 30, 70, 100 и на 300 с. По мере реконструкции каждого скана осуществлялось автоматическое вычитание преконтрастного скана из каждого постконтрастного с построением субтракционных изображений.
Субтракционные изображения оценивали на предмет наличия накапливающих контрастное вещество участков. Особое внимание уделяли участкам с ранним (в 1–2 минуту после введения контрастного вещества) интенсивным усилением сигнала. При обнаружении таких очагов изучали динамику контрастного усиления путем построения кривой «интенсивность – время». Для этого в области подозрительного очага выбирали зону интереса округлой или полицикличной формы, соответствующей форме очага. Градиент контрастного усиления оценивали в относительных единицах (процентах) в автоматическом режиме при построении кривой по формуле:
si№,^lz5ELixX№ , SIpre где SI – максимальная интенсивность сигнала в абсолютных единицах: post – после введения контрастного вещества, pre – до введения контрастного вещества. При оценке динамической кривой обращали внимание на максимальный градиент усиления интенсивности сигнала, на время наступления этого максимального градиента и его устойчивость. Таким образом, каждый раз мы фиксировали один из трех типов кривых динамики контрастного усиления патологического очага. Это: I тип (линейный) – персистирующее усиление сигнала в очаге; II тип (плато) – раннее усиление, остающееся устойчивым при последнем измерении; III тип (вымывание) – раннее усиление с последующим вымыванием контрастного вещества из очага. Контрастное усиление в очаге считалось устойчивым, если интенсивность сигнала от него при последнем измерении не менялась более чем на 10%.
Проекционное расположение каждого подозрительного участка накопления контрастного вещества отмечали на коронарной диаграмме с целью последующего выполнения прицельной биопсии. Результаты биопсии сопоставляли с результатами МРТ. При этом подсчитывали количество очагов накопления контрастного вещества с линейной динамикой контрастного усиления, с плато и вымыванием, имеющих место при доброкачественных изменениях (простатит, железисто-стромальная гиперплазия) и при РП. С помощью критерия z сравнивали доли встречаемости каждой кривой динамики контрастного усиления при доброкачественных изменениях и раке. Отличия считались достоверными при p<0,05.
Кроме изучения динамики контрастного усиления, сравнивали отличия средних относительного градиента максимальной интенсивности сигнала при доброкачественных изменениях (простатит, железисто-стромальная гиперплазия, ПИН) и раке. Для этого использовали критерий Стьюдента с 95% доверительным интервалом.
Результаты
При МРТ простаты в Т2/tse последовательности у 50 больных было выявлено 71 подозрительных на рак очагов. Однако, в большинстве из них вероятность опухолевого поражения расценивалась как сомнительная или маловероятная. Только у 11 пациентов изменения, выявленные в T2/tse последовательности, расценивались как сильно подозрительные. В ходе выполнения динамической МРТ у всех без исключения пациентов наблюдался один и тот же образец контрастного усиления, а именно: контрастное вещество накапливалось в центральной (парауретральной) зоне железы по узловому типу. В нормальной неизмененной периферической зоне железы контрастное вещество не накапливалось или накопление имело легкий диффузный характер с линейной динамикой усиления в случаях застоя секрета или хронического простатита (рис. 1, 2). В последнем случае участку усиления в динамической МРТ соответствовала зона гипоинтенсивности в Т2/tse.
На фоне описанного усиления у 50 пациентов в области периферической или переходной зон были выявлены очаги накопления контрастного вещества в количестве 71, подозрительные на рак. Очаги считали подозрительными
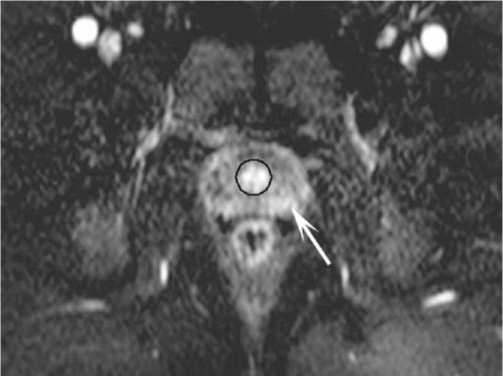
Рис. 1. Контрастирование простаты у больного хроническим простатитом. Усиление сигнала от парауретральных отделов (обведено). В периферической зоне усиление сигнала незначительное, носит диффузный характер (стрелка)
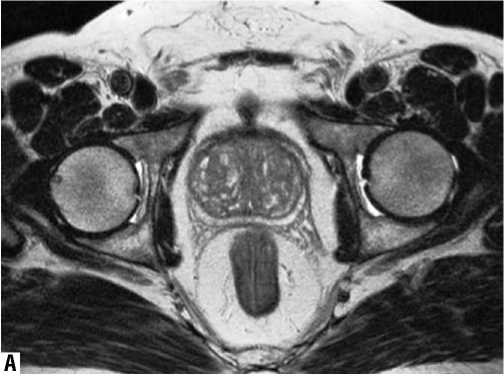
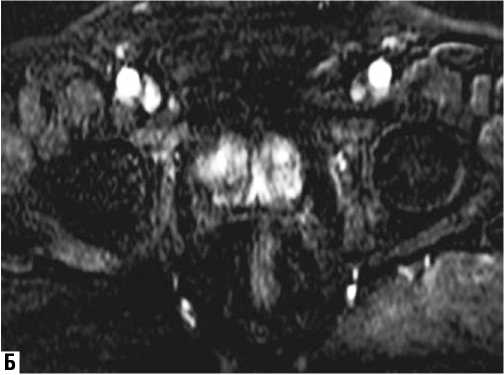
Рис. 2. Контрастирование простаты у больного ЖСГ. А – T2/tse, Б – T1/tfl с контрастированием (субтракционное изображение). Узлы гиперплазии интенсивно и негомогенно накапливают контрастное вещество. Периферическая зона «чистая»
при наличии одного или более из перечисленных ниже признаков (рис. 3):
-
– локализация в области периферической или переходной зоны;
-
– раннее (с первой минуты) и интенсивное (с градиентом усиления более 100%) усиление интенсивности сигнала;
– наличие гипоинтенсивного сигнала от очага в Т2/tse.
В последующем была выполнена селективная трансректальная биопсия всех 50 подозрительных очагов. Доброкачественные изменения выявлены в 29 пробах, аденокарцинома – в 42.
Изучение динамики накопления контрастного препарата в очагах позволила выделить 3 типа кривых интенсивность-время: 1-й тип (рис. 4) – линейный или близкий к нему, означающий непрерывное накопление контрастного вещества; 2-й тип (рис. 4) – раннее и интенсивное усиление (в 1–2 минуту) с последующим плато (отсутствием динамики); 3-й тип (рис. 5) – раннее интенсивное усиление с последующим вымыванием контрастного вещества, начиная со 2–3 минуты («wash out»). Сопоставление различных типов кривых с гистологическим исследованием материала, полученного после пункционной биопсии или радикальной простатэктомии, представлены в таблице 1. Между частотой различных типов динамических кривых различий не было. Первый тип кривой выявлен в 23 очагах, второй – в 24 и третий – в 24. Из них доброкачественные изменения, к которым относилась фиброзно-мышечная и железисто-стромальная гиперплазия, были выявлены в 42 пробах, а рак – в 29. При этом для рака был более характерен 3-й тип кривой (18 случаев), что подтверждено критерием z для парных сравнений с 95% доверительным интервалом.
В 6 очагах с аденокарциномой наблюдался линейный (персистирующий) тип динамики усиления, в 5 – плато. В 2 очагах, где также наблюдался 3-й тип кривой, была выявлена простатическая интраэпителиальная неоплазия
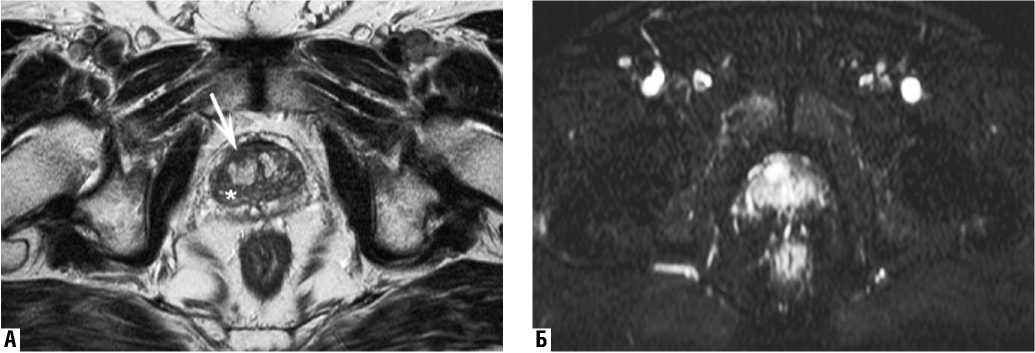
Рис. 3. Рак простаты. В Т2/tse импульсной последовательности (А) в правой доле определяется гипоинтенсивный очаг (стрелка). На динамической МРТ (Б) в опухолевом узле наблюдается раннее и интенсивное накопление контрастного вещества
Mean Curve across (6 ima 14-13 ima 14; rel 6 ima 14) norm
Scaling: Factor=1.0 0ffset=0.0 SP F20.3
Average of mean values: 1: 76.89 2: 51.90 3: 78.93
Average of areas: 1: 0.89 2:0.42 3: 1.29
Normal Time 1.36
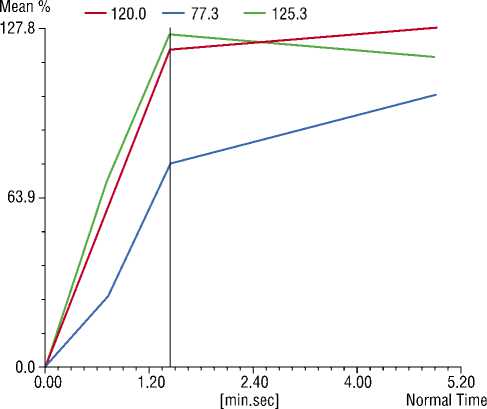
Рис. 4.
Mean Curve across (6 ima 13-16 ima 13: rel 6 ima 13) diff
Scaling: Factor=1.0 0ffset=0.0
Average of mean values: 1: 102.20 2: 87.97
Average of areas: 1: 0.312:1.74
SP F27.0
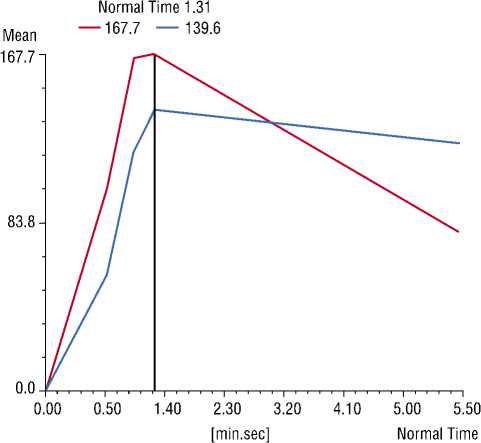
Рис. 5. Третий тип кривой «wash out». Максимальная интенсивность сигнала достигается к концу второй минуты. Затем наблюдается постепенное вымывание
Динамические кривые «интенсивность-время». Точечная и сплошная линии представляют тип кривой «плато». Пунктирная линия представляет персистирующее усиление сигнала с течением времени близкое к линейной зависимости (линейный тип кривой)
Табл. 1.
|
Гистологическое заключение |
Типы динамических кривых |
Всего |
||
|
I II |
III |
|||
|
Аденокарцинома |
6 |
5 |
18 |
29 |
|
Доброкачественный процесс (всего) |
17 |
19 |
6 |
|
|
– простатит |
9 |
4 |
– |
42 |
|
– ПИН* |
– |
1 |
3 |
|
|
– ЖСГ |
8 |
14 |
3 |
|
|
Критерий z для парных сравнений |
z=1.425 (p>0.05) |
z=2.2 (p>0.05) |
z=3.953 (p<0.05) |
|
* – простатическая интраэпителиальная неоплазия
Сравнение частоты различных типов динамических кривых при раке ПЖ и доброкачественных изменениях
(ПИН) – ложно положительные результаты. В 3 случаях в аденокарциноме наблюдалось диффузное усиление периферических отделов железы с линейным типом кривой, а в одном – раннее интенсивное усиление с последующим плато. Все четыре очага были неверно расценены нами как проявления простатита (ложно отрицательный результат). Таким образом, количество истинноположительных МРТ-заключений составило 25, ложноотрицательных – 4, истинноотрицательных – 40, ложноположительных – 2.
У всех пациентов с 2-ым и 3-им типом динамической кривой максимальный прирост интенсивности сигнала приходился на временной отрезок 1–2 мин. Среднее значение максимального градиента усиления сигнала (в %) при раке и доброкачественных изменениях не отличалось и составило 101 ± 18 и 102 ± 26, соответственно.
Чувствительность динамической МРТ с контрастированием в диагностике рака простаты составила 86%, специфичность – 95%, общая точность – 92%, предсказательная ценность положительного результата – 93%, предсказательная ценность отрицательного результата – 91%.
Обсуждение
Большинство работ, посвященных динамической МРТ с болюсным контрастированием в диагностике различных заболеваний, основаны на двухкомпонентной модели фармакокинетики хелатов гадолиния [14]. Данная модель описывает обмен контрастным препаратом между двумя компонентами: плазмой крови и экстрацеллюлярным пространством. Введенное в вену контрастное вещество, пройдя малый круг, попадает в аорту. В первую минуту исследования доминирующую роль в усилении патологического очага играет сосудистая составляющая. То есть, интенсивное накопление контрастного вещества в первую минуту исследования объясняется хорошей васкуляризацией образования. Общеизвестен факт, что злокачественные опухоли продуцируют эндотелиальный фактор роста, индуцирующий рост в опухоли патологической сосудистой сети, представленной широкими прямыми капиллярами с повышенной проницаемостью эндотелия [12]. Другой характерной особенностью патологической сосудистой сети является наличие артериовенозных шунтов.
На 2-ой минуте достигающее капилляров контрастное вещество выходит в интерстиций. Таким образом, с появлением контрастного вещества в интерстиции в усилении сигнала будут участвовать уже обе компоненты. С этого момента они будут находиться в состоянии непрерывного обмена контрастным веществом по прин- ципу химического градиента. Очевидно, что чем больше емкость интерстициального пространства, тем меньшая порция контрастного вещества попадет обратно в кровоток и будет элиминироваться почками. Это, в свою очередь, меньше отразится на общем пуле контрастного вещества, участвующего в дальнейшем изменении интенсивности сигнала (с 3–5 минуты).
Однако, данная особенность фармакокинетики не может объяснить раннее вымывание контрастного вещества, которое в наших исследованиях начиналось уже со второй минуты. Мы считаем, что именно наличие артериовенозных шунтов объясняет механизм раннего снижения интенсивности сигнала в 3-ем типе динамической кривой.
К сожалению, обильная васкуляризация с повышенной проницаемостью капилляров характерна не только для злокачественных процессов. Аденома простаты также хорошо кровоснабжается и при контрастном усилении также демонстрирует очаги раннего и интенсивного накопления контрастного вещества. Аденома также может содержать артериовенозные шунты, поэтому диагностика рака в центральной или переходной зоне продолжает оставаться проблемой. В дифференциальной диагностике помогает редкая частота рака, локализованного только в центральной зоне простаты (по данным литературы [18] всего в 5%). Также, третий тип кривой мы наблюдали в трех очагах с простатической интраэпителиальной неоплазией (ПИН), которая представляет собой внутри-ацинарную пролиферацию эпителиоцитов и относится к предраковым состояниям. По данным литературы [1] у 50% пациентов, в биоптате которых обнаруживается ПИН, при повторной биопсии выявляется рак.
Два ошибочных предположения об отсутствии рака у пациентов с хроническим простатитом можно объяснить недостаточной скоростью введения контрастного вещества на этапе освоения методики, когда наблюдалось диффузное усиление всех отделов железы, и ошибками в выделении области интереса.
По поводу 2-го и 3-го типов кривых, все-таки имевших место при раке, но встречавшихся достоверно реже, можно сказать, что своего максимального градиента усиления аденокарцинома достигала всегда быстрее по сравнению с нормальной тканью, что позволяло визуализировать ее достаточно четко. Мы надеемся, что наше предположение подтвердится и в дальнейшем на большем количестве наблюдений.
Выводы
-
1. Динамическая МРТ является высокоинформативным методом первичной диагностики рака предстательной железы. С вероятностью, превышающей 95%, можно утверждать, что для рака более характерен 3-й тип кривой динамики контрастного усиления («wash out»).
-
2. По градиенту максимального усиления интенсивности сигнала, доброкачественные изменения предстательной железы (хронический простатит, гиперплазия) и рак не имеют достоверных различий, поэтому данный
-
3. Полученные результаты могут служить надежным основанием для внедрения в клиническую практику прицельной трансректальной биопсии из подозрительных участков железы, обнаруженных после проведения динамической МРТ.
критерий нельзя использовать в дифференциальной диагностике.
Список литературы Динамическая МРТ - новый метод диагностики рака простаты
- Александров В.П., Карелин М.И. Рак предстательной железы. СПб.: Издательский дом СпбМАПО, 2004. -148 с.
- Гажонова В.Е. Значение ТРУЗИ с УЗ-ангиографией в дифференциальной диагностике гипоэхогенных участков предстательной железы//Мед. Виз. 2000. -№4. -С. 28-33.
- Назаренко Г.И., Хитрова А.Н., Головатенко-Абрамов К.В. и др. Возможности МРТ с динамической цистовезикулопростатографией в дифференциальной диагностике рака предстательной железы и простатита//Мед. Виз. -2005. -№3. -С. 88-99.
- Barentsz J.O., Engelbrecht M., Jager G.J. et al. Fast dynamic gadolinium-enhanced MR imaging of urinary bladder and prostate cancer//J. Magn. Reson. Imaging. -1999. -Vol. 10, №3. -P. 295-304.
- Beyersdorff D., Taupitz M., Winkelmann B. et al. Patients with a history of elevated prostate-specific antigen levels and negative transrectal US-guided quadrant or sextant biopsy results: value of MRI//Radiology. 2002. V. 224. P. 701-706.
- Buckley D.L., Roberts C., Parker G.J. et al. Prostate cancer: evaluation of vascular characteristics with dynamic contrast-enhanced T1-weighted MR Imaging -Initial Experience//Radiology. 2004. V. 233. P. 709-715.
- Campbell's urology/P.C. Walsh. 8th ed. Philadelphia etc.: Saunders, 2002. V. 4. P. 2623-3952.
- Cornud F., Belin X., Piron D. et al. Color Doppler-guided prostate biopsies in 597 patients with elevated serum PSA level: impact of Gleason score for nonpalpable lesions//Urology. 1997. V. 49. N 15. P. 709-715.
- Ellis W.J., Brawer M.K. Repeat prostate needle biopsy: who needs it?//J. Urol. 1995. V. 153. P. 1496-1498.
- Keetch D.W., Catalona W.J., Smith D.S. Serial prostatic biopsies in men with persistently elevated serum prostate specific antigen values//J. Urul. 1994. V. 151. P. 1571-1574.
- Kravchic S., Cytron S., Peled R. et al. Using gray-scale and two different techniques of color Doppler sonography to detect prostate cancer//Urology. 2003. V. 61. №5. P. 977-981.
- Lewin M., Bredow S., Sergeyev N., et al. In vivo assessment of vascular endothelial growth factor-induced angiogenesis//Int. J. Cancer. 1999. V. 83. P. 798-802.
- Padhani A.R., Gapinski C.J., Macvicar D.A. et al. Dynamic contrast enhanced MRI of prostate cancer: correlation with morphology and tumor stage, histological grade and PSA//Clin. Radiol. 2000. V. 55. P. 99-109.
- Port R.E., Knopp M.V., Hoffmann U. et al. Multicompartment alalysis of gadolinium chelate kinetics: blood-tissue exchange in mammary tumors as monitored by dynamic MR imaging//J. Magn. Res. Imaging. 1999. V. 10. N 3. P. 233-241.
- Rouviere O., Raudrant A., Ecochard R. et al. Enhancement patterns of prostate cancer in dynamic MRI//Eur. Radiol. 2003. V. 13. P. 931-942.
- Preziosi P., Orlacchio A., Di Giambattista G. et al. Enhancement patterns of prostate cancer in dynamic MRI//Eur. Radiol. 2003. V. 13. N 5. P. 925-930.
- Schlemmer H.P., Merkle J., Grobholz R. et al. Can preoperative contrast-enhanced dynamic MR imaging for prostate cancer predict microvessel density in prostatectomy specimens?//Eur. Radiology. 2004. V. 14. N 2. P. 309-317.
- Walsh P.C. Prostate cancer tumor volume: measurement with endorectal MR and MR spectroscopic imaging//J. Urol. 2002. V. 168. №4. P. 1640.


