Динамика эффективности фиксации CO 2 штаммом Bracteacoccus minor при различной доступности азота
Автор: Кочубей А.В., Мальцева И.А., Мальцев Е.И., Яковийчук А.В.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Ботаника
Статья в выпуске: 4, 2024 года.
Бесплатный доступ
Чрезмерное выделение и накопление углекислого газа в атмосфере является серьезной проблемой, имеющей ряд негативных экологических последствий, включая глобальное потепление. Для борьбы с этими последствиями используются различные подходы, при этом основное внимание уделяется сокращению выбросов углекислого газа и достижению нулевого углеродного баланса. В дополнение к сокращению добычи и использованию ископаемых видов топлива в качестве потенциального решения рассматривается биосеквестрация. Микроводоросли особенно перспективны в этом отношении, поскольку они могут служить поглотителями углекислого газа при использовании в биотехнологических процессах. Некоторые штаммы микроводорослей, например, из рода Bracteacoccus Tereg, были изучены на предмет их способности синтезировать ценные продукты, хотя способность поглощать углекислый газ данными объектами не изучалась, в частности при изменении концентрация доступного азота в питательной среде. В ходе исследования было установлено, что высокие уровни биодоступного азота увеличивают среднюю скорость поглощения углекислого газа, в то время как максимальное поглощение происходит, когда культура выходит из lag-фазы. Скорость фиксации углекислого газа и его количество, поглощенное Bracteacoccus minor (MZ-Ch31), напрямую зависят от продуктивности биомассы и концентрации хлорофилла.
Биосеквестрация, биомасса, продуктивность, хлорофилл, среда культивирования, bbm, 3n bbm, f, f2
Короткий адрес: https://sciup.org/147247240
IDR: 147247240 | УДК: 551.4 | DOI: 10.17072/1994-9952-2024-4-366
Dynamics of CO2 fixation efficiency by Bracteacoccus minor strain with different nitrogen availability
The excessive release and accumulation of carbon dioxide in the atmosphere is a major global issue with several negative environmental consequences, including global warming. Various approaches are used to eliminate these negative effects, with the main focus being on reducing carbon dioxide emissions and achieving a zero-carbon balance. In addition to decline fossil fuel mining and use, biosequestration is being considered as a potential solution. Microalgae are particularly promising in this regard, as they can serve as sinks for carbon dioxide when used in biotechnological processes. Some strains of microalgae from the genus Bracteacoccus Thereg, have been studied for their ability to synthesize valuable products. However, the ability to absorb carbon dioxide by these objects has not been studied, in particular, when the concentration of available nitrogen in the nutrient medium changes. The study found that high levels of bioavailable nitrogen increase the average rate of absorption of carbon dioxide, while maximum absorption occurs when the culture leaves the lag-phase. The rate of carbon dioxide fixation and its amount absorbed by Bracteacoccus minor (MZ-Ch31) directly depend on biomass productivity and chlorophyll concentration.
Текст научной статьи Динамика эффективности фиксации CO 2 штаммом Bracteacoccus minor при различной доступности азота
Увеличение объемов использования ископаемой энергии на основе углерода, уничтожение лесов и другие изменения в землепользовании привели к еще большему количеству отходов в виде парниковых газов, а также к снижению способности планеты поглощать их [White, 2012]. Проблема эмиссии углекислого газа в атмосферу приобретает все более глобальные масштабы [Li et al., 2023], что связано в первую очередь с индустриализацией, увеличением численности населения и использованием ископаемой энергии [White, 2012]. Накопление парниковых газов имеет ряд негативных экологических последствий, одно из которых – глобальное потепление [Venkata Mohan et al., 2016; Zhu et al., 2016; Sangeetha et al., 2022], а также ряд сопутствующих проблем, что в комплексе стало серьезной угрозой для экологической устойчивости и безопасности человечества в целом [Ma et al., 2022]. В связи с этим все более актуальной становится стратегия нулевого углеродного баланса [Ma et al., 2022]. По вопросам изменения климата и снижения выбросов парниковых газов разработан ряд регламентирующих документов международного статуса, в которых Российская Федерация является стороной взаимодействия [Cherepovitsyna, Dorozhkina, Kostyleva, 2023].
Большие перспективы по снижению эмиссии углекислого газа может иметь биосеквестрация. Она предполагает возможность снижения эмиссии углекислого газа путем восстановления различного рода экосистем или введения в эксплуатацию не возделываемых территорий, акваторий и др. Однако данные мероприятия обычно продолжительны во времени, а для лесных экосистем требуют десятилетий. Ввиду данных ограничений микроводоросли выглядят как довольно перспективный объект биосеквестрации, а их использование в данном контексте становится все шире [Cheah et al., 2015; Zhu et al., 2016; Ma et al., 2022; Zhao et al., 2022; Li et al., 2023]. Известен положительный опыт применения некоторых штаммов микроводорослей для снижения выбросов CO 2 с дымовыми газами. Поглощение CO 2 клетками водорослей усиливается при синтезе вторичных метаболитов [Venkata Mohan et al., 2016]. Спектр синтезируемых микроводорослями метаболитов очень широк [Barkia, Saari, Manning, 2019; Dolganyuk et al., 2020; Coulombier, Jauffrais, Lebouvier, 2021; Ramos-Romero et al., 2021]. Объемы биомассы микроводорослей, выращиваемой для целей биотехнологических производств, постоянно растут.
Широко распространенной практикой активизации биосинтеза ценных метаболитов является культивирование в стрессовых условиях, в том числе выращивание в средах с ограниченной доступностью азота [Rios et al., 2015; Mudimu et al., 2017; Zhang et al., 2018; Janssen, Wijffels, Barbosa, 2019; Chen et al., 2022; Şirin, Serdar, 2024]. И хотя накопление вторичных метаболитов сопряжено с усилением поглощения CO 2 , сами процессы биосеквестрации при ограничении азота исследованы мало [Farooq, 2022]. Однако они представляют значительный интерес с точки зрения достижения нулевого углеродного баланса.
В качестве биотехнологических объектов интенсивно исследуются представители рода Bracteacoccus Tereg, что связано с их способностью синтезировать при определенных условиях культивирования каротиноиды, липиды и ценные жирные кислоты [Ratha et al., 2013; Minyuk, Chelebieva, Chubchikova, 2014; Mamaeva et al., 2018; Maltsev et al., 2020; Chekanov et al., 2022; Lukavský et al., 2022; Malik et al., 2022]. В этом аспекте один из представителей – Bracteacoccus minor (Chodat) Petrova исследован довольно слабо, хотя является космополитным видом и довольно широко распространен. Эффективность поглощения CO 2 данным видом пока не изучалась, хотя его широкое распространение в сочетании с биотехнологическим потенциалом может стать основой разработки проектов, объединяющих в себе решение проблем секвестрации углекислого газа и получения ценных метаболитов в промышленных масштабах.
Цель – изучить динамику биофиксации CO 2 штаммом Bracteacoccus minor (MZ-Ch31) в условиях различной доступности азотного питания.
Материалы и методы исследований
Выделенный из почвы штамм Bracteacoccus minor MZ-Ch31 (насаждение Robinia pseudoacacia L., парк им. Горького, г. Мелитополь, Россия), выращивали на стандартной среде BBM (Bischoff and Bold, 1963). Штамм в культуре поддерживается при 15±2°C в пробирках, освещенных белыми диодами с интенсивностью света 120 Лк и режимом освещения 16:8 ч (свет/темнота) на среде BBM. Для эксперимента клетки иннокулировали в 150 мл свежей среды BBM. При наступлении экспоненциальной фазы роста (через 5 дней) эту культуру использовали для постановки эксперимента. В качестве реакторов использовались плоскодонные колбы объемом 250 мл с герметичными крышками и системой обеспечения постоянства состава газовоздушной смеси в колбе. Культуры аэрировали воздухом с помощью аквариумного компрессора Hailea ACO-308 (Hailea, China). Воздух подавали через стеклянную трубку с внутренним диаметром 4 мм со скоростью 0.1 л мин-1. Для предотвращения бактериального загрязнения культуры использовали бактериальный вентиляционный фильтр (GSV, Italy) диаметром 40 мм, который устанавливался в разрыв между компрессором и стеклянной трубкой. Это позволило поддерживать культуру в альгологически чистом состоянии. Выращивание штамма проводили в стандартных условиях: интенсивность света – 5000 Лк; режим освещения – 16:8 ч (свет/ темнота); температура окружающей среды – 20±1°С. Начальная концентрация – 2.89×105 клеток мл-1.
Для постановки эксперимента использовали стандартную и модифицированную по содержанию азота среду BBM. Исследовали 4 варианта питательной среды, обозначенные как группа-1, группа-2, группа-3, группа-4. Группы отличались между собой содержанием в питательной среде общего азота (N) в форме нитратов (NO 3 –). Концентрации подбирались в соответствии с содержанием N в широко применяемых средах культивирования (3N BBM, BBM, F, F2). Соответственно концентрация азота в группах составляла: группа-1 – 0.124 г л-1; группа-2 – 0.04 г л-1; группа-3 – 0.025 г л-1; группа-4 – 0.012 г л-1. Группа-2 выступала в качестве контрольной, т.к. имела стандартное для среды BBM содержание азота.
Плотность биомассы (B) определяли гравиметрически, путем выдерживания 1 мл биомассы в сушильном шкафу на протяжении 6 часов при 120°С и последующим взвешиванием сухого остатка.
Рост микроводорослей оценивали путем измерения сухого веса (СВ). Измеренный сухой вес выражали в г л - 1 . Объемная продуктивность биомассы (P) рассчитывалась по формуле в соответствии с источником [Morais, Costa, 2007]:
Р (г СВ л-1 день-1) = У, где X1 – сухой вес (г СВ л-1) во время t1 (день), и X2 – сухой вес (г СВ л-1) во время t2 (день).
Биофиксацию СО 2 (F) рассчитывали на продуктивность биомассы (Р) по уравнению [Morais, Costa, 2007] с уточнениями:
F — pQ м— )
, где Р – продуктивность биомассы (г СВ л-1 день-1), C C – содержание С в биомассе (%), M (CO 2 ), (MC) – молярная масса CO 2 и С соответственно.
Содержание углерода в биомассе Bracteacoccus minor принимали равным 48.5%, что соответствует среднему значению для различных зеленых микроводорослей [Harwati, Willke, Vorlop, 2018].
Содержания хлорофиллов -a, -b (Chl a, b) определяли по методу [Yang et al., 1998]. Экстракцию пигментов из микроводорослей проводили 80.0% ацетоном. Для этого 10 мг отделенных от среды центрифугированием (10 мин. при 3 000 об/мин-1, 530 g) клеток подвергали 3-кратному замораживанию- размораживанию с целью разрушения клеточных оболочек. После чего добавляли 4 мл ацетона с целью создания соотношения биоматериал-экстрагент 1:40 (масса: объем) и дополнительно гомогенизировали биомассу путем растирания с кварцевым песком. Полученную смесь герметично закрывали и оставляли на 24 часа при температуре 25°С в темном месте для полной экстракции пигментов. Далее ацетоновый экстракт отделяли от осадка центрифугированием при 10 000 об/мин-1 (6 000 g) и температуре 4°С на протяжении 10 мин. Анализировали интенсивность поглощения экстракта пигментов на спектрофотометре Ulab 102 (China) при длинах волн: 663.6; 646.6 нм, что соответствует максимуму поглощения для Chl a и Chl b. Расчеты проводили по следующей формуле:
.
Содержание суммы хлорофиллов выражали в мг г-1 СВ путем преобразования расчетных единиц µг мл-1 с учетом коэффициента разведения и навески сухой биомассы.
Все измерения проводились минимум в трех повторностях, на графиках и в таблицах приведены средние величины и ошибки средней которые высчитывали по ANOVA с применением встроенных функций программы Microsoft Excel (v. 1903). Достоверными считали различия при p≤0.05. Корреляционный анализ проводили с применением встроенной функции попарных корреляций Пирсона в программном обеспечении IBM SPSS Statistics v. 27. Достоверными считали корреляции при уровне значимости p≤0.10.
Результаты
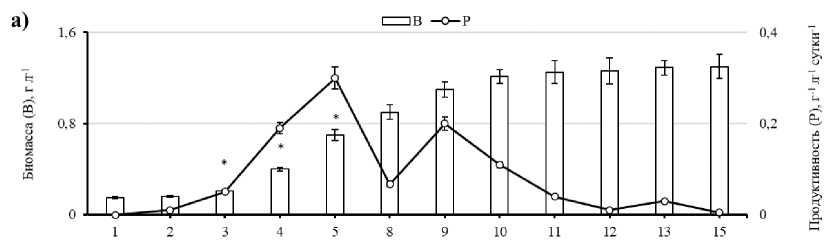
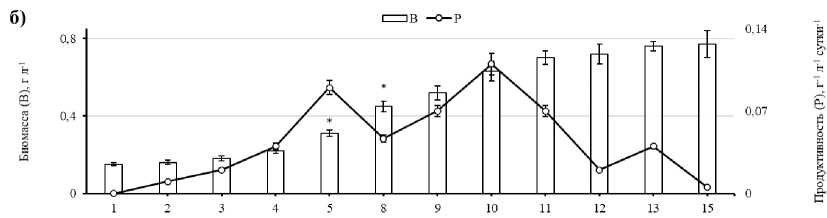
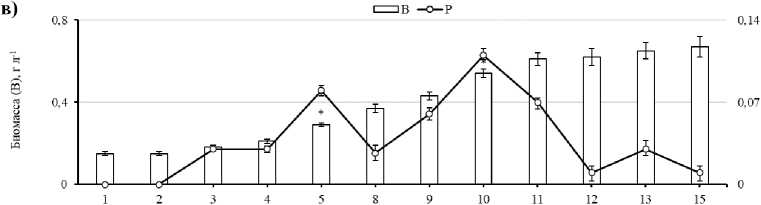
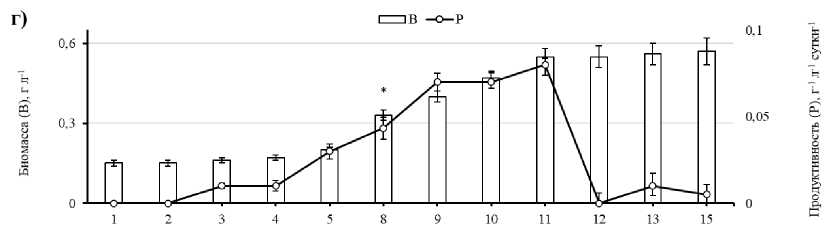
В ходе эксперимента плотность биомассы Bracteacoccus minor (MZ-Ch31) в контрольной группе (группа-2) на 15 сутки культивирования достигла 0.77 г СВ л-1, максимальный прирост биомассы наблюдался между 4–5 и 5–8 сутками (0.11 и 0.14 г СВ л-1) (рис. 1б). Более низкое содержание доступного азота в питательной среде (3 и 4 группа) сопровождалось уменьшением накопления биомассы штаммом и удлинением lag-фазы (рис. 1в, 1г). Наиболее сильно снижалась концентрация биомассы при минимальной концентрации азота в среде культивирования (группа-4) и составляла – 0.57 г СВ л-1, при этом lag-фаза была максимальной и длилась 8 суток (рис. 1г).
Время культивирования, суток
Время культивиров ания, суток
Время культивирования, суток
-.SMH^OhLKd) qlooHaHXMABOdu
Время культивиров ания, суток
Рис. 1. Скорость роста (B), продуктивность (P) и биофиксация CO 2 (F) Bracteacoccus minor (MZ-Ch31) при культивировании в различных вариантах эксперимента:
а) – 0.124; б) – 0.04; в) – 0.025; г) – 0.012 г л-1. * – разница достоверна относительно предыдущего значения на уровне p≤0.05
[Growth rate (B), productivity (P) and bio-fixation of CO 2 (F) Bracteacoccus minor (MZ-Ch31) during cultivation in various experimental variants:
-
а) – 0.124; б) – 0.04; в) – 0.025; г) – 0.012 g L-1. Note: * – the difference is significant relative to the previous value at the p≤0.05 level]
В группе-4 между 11–12 сутками культивирования прирост биомассы не был отмечен, а максимальный достоверный прирост (0.13 г СВ л-1; p≤0.05) установлен между 5 и 8 сутками. Стоит отметить, что по мере снижения концентрации азота достоверные приросты биомассы смещаются на более поздние сроки.
Ограничение доступности азота в среде лимитирует рост и деление клеток, приводит к удлинению lag-фазы, сокращению логарифмической фазы и выходу на стационарную стадию роста культуры раньше относительно контроля. При повышении концентрации азота до 0.124 г л-1 (группа-1), что в 3.1 раза больше относительно стандартной BBM, отмечено наибольшее накопление биомассы среди всех исследованных экспериментальных групп. Максимальный прирост биомассы был между 4–5 сутками и составлял 0.30 г СВ л-1 (p≤0.05). Также в группе-1 установлена максимальная в эксперименте плотность биомассы 1.30 г СВ л-1 и самая короткая lag-фаза – 3 суток. Следует отметить, что плотность биомассы имела прямую зависимость от содержания азота в среде культивирования, что подтверждено коэффициентом корреляции (r=1.0; p≤0.05).
.HHIX3ъeOu j - (巴 ^оо KHIIEJXHtHg
Время культивирования, суток
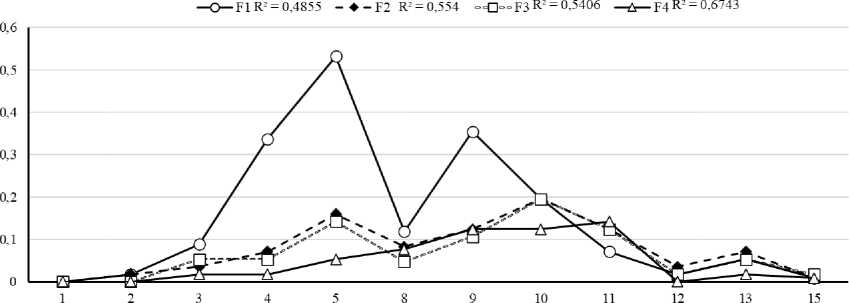
Рис. 2. Биофиксация CO 2 (F) Bracteacoccus minor (MZ-Ch31) при культивировании в различных вариантах эксперимента:
концентрация азота в среде: F1 – 0.124; F2 – 0.04; F3 – 0.025; F4 – 0.012 г л-1. R2 – величина достоверности аппроксимации (полиноминальная линия тренда)
[Bio-fixation of CO 2 (F) Bracteacoccus minor (MZ-Ch31) during cultivation in various experimental variants: Nitrogen concentration in medium: F1 – 0.124; F2 – 0.04; F3 – 0.025; F4 – 0.012 g L-1. Note: R2 – approximation accuracy (polynomial trend line)]
Максимальная среди исследованных групп продуктивность биомассы установлена для группы-1 с наибольшим содержанием азота в питательной среде. Она достигала максимального значения (0.3 г СВ л-1сутки-1) на 5 день культивирования с дальнейшим снижением до минимума в конце эксперимента. В стандартной среде BBM (группа-2) максимум продуктивности составлял 0.11 г СВ л-1 сутки-1, так же, как и в группе-3. В эксперименте с минимальным количеством азота в среде (группа-4) максимум продуктивности приходился на 10 сутки – 0.08 г СВ л-1 сутки-1.
Стоит отметить, что при культивировании штамма в экспериментальных группах 1 – 3 наблюдался рост продуктивности с двумя пиками, в группе-1 – на 5 и 9 сутки, в группе-2 – на 5 и 10 сутки. Далее происходило резкое снижение продуктивности, связанное, очевидно, с нарастающим истощением питательных компонентов в среде и замедлением роста и деления клеток. В группе-4 пик продуктивности приходится на 11 сутки с дальнейшим резким снижением.
Ежедневные показатели биофиксации CO 2 в контрольной группе (группа-2) снижались по мере старения культуры (рис. 2). Максимальная эффективность поглощения СО 2 штаммом в стандартной среде BBM (группа-2) наблюдалась на 10 сутки и составляла 0.2 г CO 2 л-1 сутки-1, а минимальная – на 2 и 15 сутки культивирования, что связано с низким приростом биомассы. В группе-1 максимум фиксации CO 2 составлял 0.53 г CO 2 л-1 на 5 сутки роста. Это самый высокий показатель в эксперименте (рис. 1а). В группе-4 максимальное поглощение было значительно ниже – всего 0.14 г CO 2 л-1 сутки-1 и отмечено на 11 сутки культивирования.
Средняя скорость биофиксации углекислого газа за весь период культивирования снижалась с уменьшением концентрации азота в питательной среде (r=1.0; p≤0.05) (табл. 1). В группе-4 она была наименьшей. Также минимальным в этой группе было и общее количество утилизированного за 14 суток эксперимента CO 2 . Относительно контрольной группы данные показатели были меньше в 1.6 раз. Повышение концентрации азота в питательной среде приводит к повышению как средней скорости биофиксации CO 2, так и общего количества поглощенного углекислого газа почти в 2 раза относительно стандартной среды BBM.
Таблица 1
Биомасса и биофиксация CO2 Bracteacoccus minor MZ-Ch31 в различных вариантах эксперимента (M±SD; n = 3)
[Biomass and bio-fixation of CO2 Bracteacoccus minor MZ-Ch31 in various experimental variants (M±SD; n = 3)]
|
Варианты эксперимента |
Биомасса на 14 сутки, г СВ л-1 |
Содержание хлорофиллов ( a, b ) на 14 сутки, мг г-1 СВ |
Средняя скорость биофиксации CO 2 за 14 суток, г CO 2 л-1 день-1 |
Утилизированный CO 2 за 14 суток, г л-1 |
Содержание азота в среде, мг л-1 |
|
Группа-1 |
1.3±0.03# |
2.34±0.24*# |
0.16 |
1.8±0.17# |
0.124 |
|
Группа-2 (BBM) |
0.77±0.17* |
1.72±0.18* |
0.08 |
0.93±0.06* |
0.040 |
|
Группа-3 |
0.67±0.07 |
1.13±0.12*# |
0.07 |
0.81±0.06 |
0.025 |
|
Группа-4 |
0.57±0.03# |
0.58±0.07*# |
0.05 |
0.58±0.05*# |
0.012 |
Примечание. * – разница достоверна относительно предыдущей группы на уровне p≤0.05; # – разница достоверна относительно группы-2 (BBM) на уровне p≤0.05.
Содержание хлорофиллов ( a, b ) определяли в конце эксперимента на 14 сутки. Стоит отметить, что снижение концентрации азота в среде привело к уменьшению содержания хлорофиллов (r=1.000; p≤0.01). Результаты корреляционного анализа показали (табл. 2), что содержание хлорофиллов может быть одним из показателей секвестрационных характеристик штамма, так как для Bracteacoccus minor MZ-Ch31 установлена прямая (достоверная) корреляционная зависимость между концентрацией хлорофилла, параметрами биофиксации и утилизированного CO 2 . Это обусловлено тем, что фотосинтез сопровождается поглощением углекислого газа и является основным метаболическим шлюзом, обеспечивающим накопление прекурсоров для биосинтеза первичных и вторичных метаболитов, необходимых для роста и деления клеток.
Обсуждение
Скорость поглощения CO 2 для Bracteacoccus minor (MZ-Ch31) хорошо коррелирует с ростом биомассы, поскольку более высокое поглощение CO 2 в фотоавтотрофных условиях приводит к высокой продуктивности биомассы. Такая же зависимость установлена для Chlorella sp. и, как предполагают авторы, заметное увеличение продуктивности биомассы может быть объяснено усиленной фотосинтетической активностью и функцией ключевых фотоавтотрофных ферментов [Butti, Venkata Mohan, 2018]. Скорость биофиксации углекислого газа у Bracteacoccus minor MZ-Ch31 имела прямую зависимость от концентрации хлорофиллов в клетке (r = 0.918; p≤0.10). Азотное голодание в качестве инструмента повышения биофиксации CO 2 неэффективно, поскольку приводит к снижению общего количества биомассы, а также количества хлорофиллов.
Таблица 2
Результаты корреляционного анализа [The results of the correlation analysis]
|
Показатели |
B |
Chl |
F |
CU |
N |
|
|
B |
Корреляция Пирсона |
1 |
0.918* |
0.999*** |
0.999*** |
1.000*** |
|
знач. (двухсторонняя) |
0.082 |
0.001 |
0.001 |
<0.001 |
||
|
Chl |
Корреляция Пирсона |
0.918* |
1 |
0.918* |
0.923* |
0.908* |
|
знач. (двухсторонняя) |
0.082 |
0.082 |
0.077 |
0.092 |
||
|
F |
Корреляция Пирсона |
0.999*** |
0.918* |
1 |
1.000*** |
0.998** |
|
знач. (двухсторонняя) |
0.001 |
0.082 |
<0.001 |
0.002 |
||
|
CU |
Корреляция Пирсона |
0.999*** |
0.923* |
1.000*** |
1 |
0.997** |
|
знач. (двухсторонняя) |
0.001 |
0.077 |
0 |
0.003 |
||
|
N |
Корреляция Пирсона |
1.000*** |
0.908* |
0.998** |
0.997** |
1 |
|
знач. (двухсторонняя) |
<0.001 |
0.092 |
0.002 |
0.003 |
||
Примечания: B – биомасса Bracteacoccus minor MZ-Ch31 на 14 сутки, г СВ л-1; Chl – содержание хлорофиллов (a, b) на 14 сутки, мг г-1 СВ; F – средняя скорость биофиксации CO2 за 14 суток, г CO2 л-1 день-1; CU – утилизированный CO2 за 14 суток, г л-1; N – содержание азота в питательной среде, мг л-1; n = 4. * – корреляция достоверна на уровне p≤0.10; ** – корреляция достоверна на уровне p≤0.05; *** – корреляция достоверна на уровне p≤0.01.
Максимальная описанная на данный момент способность поглощать углекислый газ установлена для Chlorella vulgaris – от 3.45 г CO 2 л-1 день-1 до 6.24 г CO 2 л-1 день-1, Aphanothece microscopica Nageli – 5.44
г CO 2 л-1 день-1 [Fan et al., 2008; Ho et al., 2011]. Также высокие значения отмечены для Nannochloropsis gaditana – 1.7 г CO 2 л-1 день-1 [Adamczyk, Lasek, Skawińska, 2016], Synechocystis aquatilis SI-2 – 1.5 г CO 2 л-1 день-1 [Murakami, Ikenouchi, 1997]. В среднем биофиксация CO 2 для представителей микроводорослей различных филогенетических и экологических групп варьирует от 0.02 до 6.24 г CO 2 л-1 день-1 [Ho et al., 2011]. Большая вариативность данных может быть следствием как индивидуальных особенностей видов водорослей, так и условий культивирования, включая исходную концентрацию биомассы водорослей. Для Bracteacoccus minor (MZ-Ch31) в условиях нашего эксперимента наибольшее поглощение углекислого газа было 0.53 г CO 2 л-1 день-1, среднее – 0.16 г CO 2 л-1 день-1. Дальнейшие исследования позволят получить более полные характеристики биофиксации CO 2 штаммом.
Заключение
Скорость биофиксации и общее количество поглощенного CO 2 Bracteacoccus minor (MZ-Ch31) зависит от концентрации азота в питательной среде. Повышение доступности азота увеличивает среднюю скорость поглощения углекислого газа с 0.05 г CO 2 л-1 сутки-1 до 0.16 г CO 2 л-1 сутки-1. Максимум поглощения углекислого газа соответствовал 0.53 г CO 2 л-1 сутки-1 и был достигнут в момент выхода культуры с lag-фазы. Скорость биофиксации и количество поглощенного углекислого газа Bracteacoccus minor (MZ-Ch31) прямо зависит от концентрации биомассы (r= 0.999 и r= 0.999; p≤0.01) и хлорофиллов (r= 0.918 и 0.923; p≤0.10).
Список литературы Динамика эффективности фиксации CO 2 штаммом Bracteacoccus minor при различной доступности азота
- Adamczyk M., Lasek J., Skawinska A. CO2 biofixation and growth kinetics of Chlorella vulgaris and Nannochloropsis gaditana // Applied Biochemistry and Biotechnology. 2016. Vol. 179, № 7. P. 1248-1261.
- Barkia I., Saari N., Manning S.R. Microalgae for high-value products towards human health and nutrition // Marine drugs. 2019. Vol. 17, № 5. Art. 304.
- Butti S.K., Venkata Mohan S. Photosynthetic and lipogenic response under elevated CO2 and H2 conditions - high carbon uptake and fatty acids unsaturation // Frontiers in Energy Research. 2018. Vol. 6. Art. 27.
- Cheah W.Y. et al. Biosequestration of atmospheric CO2 and flue gas-containing CO2 by microalgae // Bio-resource technology. 2015. Vol. 184. P. 190-201.
- Chen X. et al. Nitrogen starvation enhances the production of saturated and unsaturated fatty acids in Aurantio-chytrium sp. PKU#SW8 by regulating key biosynthetic genes // Marine drugs. 2022. Vol. 20, № 10. Art. 621.
- Chekanov K. et al. Differential responses to UV-A stress recorded in carotenogenic microalgae Haemato-coccus rubicundus, Bracteacoccus aggregatus, and Deasonia sp. // Plants. 2022. Vol. 11, № 11. Art. 1431.
- Cherepovitsyna A.A., Dorozhkina I.P., Kostyleva V.N. Sequestration and use of carbon dioxide: the essence of technology and approaches to the classification of the projects // Russian Journal of Industrial Economics. 2023. Vol. 15, № 4. P. 473-487.
- Coulombier N., Jauffrais T., Lebouvier N. Antioxidant compounds from microalgae: a review // Marine drugs. 2021. Vol. 19, № 10. Art. 549.
- Dolganyuk V. et al. Microalgae: A promising source of valuable bioproducts // Biomolecules. 2020. Vol. 10, № 8. Art. 1153.
- Fan L.-H. et al. Evaluation of a membrane-sparged helical tubular photobioreactor for carbon dioxide biofixation by Chlorella vulgaris // Journal of Membrane Science. 2008. Vol. 325, № 1. P. 336-345.
- Farooq W. Maximizing energy content and CO2 bio-fixation efficiency of an indigenous isolated micro-alga Parachlorella kessleri HY-6 through nutrient optimization and water recycling during cultivation // Front. Bioeng. Biotechnol. 2022. Vol. 10, № 9. Art. 804608.
- Harwati T.U., Willke T., Vorlop K.D. Characterization of the lipid accumulation in a tropical freshwater microalgae Chlorococcum sp. // Bioresource Technology. 2018. Vol. 121. P. 54-60.
- Ho S.-H. et al. Perspectives on microalgal CO2-emission mitigation systems - A review // Biotechnology Advances. 2011. Vol. 29, № 2. P. 189-198.
- Janssen J.H., Wijffels R.H., Barbosa M.J. Lipid production in Nannochloropsis gaditana during nitrogen starvation // Biology. 2019. Vol. 8, № 1. Art. 5.
- Li S. et al. Production of sustainable biofuels from microalgae with CO2 bio-sequestration and life cycle assessment // Environmental research. 2023. Vol. 227. Art.115730.
- Lukavsky J. et al. The alga Bracteacoccus bullatus (Chlorophyceae) isolated from snow, as a source of oil comprising essential unsaturated fatty acids and carotenoids // Journal of Applied Phycology. 2022. In Review. preprint. DOI: 10.21203/rs.3.rs-2125780/v1.
- Ma Z. et al. Microalgae-based biotechnological sequestration of carbon dioxide for net zero emissions // Trends in biotechnology. 2022. Vol. 40, № 12. P. 1439-1453.
- Malik S. et al. Characterization of a newly isolated self-flocculating microalga Bracteacoccus pseudomi-nor BERC09 and its evaluation as a candidate for a multiproduct algal biorefinery // Chemosphere. 2022. Vol. 304. Art. 135346.
- Maltsev Y.I. et al. Biotechnological potential of a new strain of Bracteacoccus bullatus (Sphaeropleales, Chlorophyta) as a promising producer of omega-6 polyunsaturated fatty acids // Russian Journal of Plant Physiology. 2020. Vol. 67. P. 185-193.
- Mamaeva A. et al. Simultaneous increase in cellular content and volumetric concentration of lipids in Bracteacoccus bullatus cultivated at reduced nitrogen and phosphorus concentrations // Journal of Applied Phy-cology. 2018. Vol. 30. P. 2237-2246.
- Minyuk G.S., Chelebieva E.S., Chubchikova I.N. Secondary carotenogenesis of the green microalga Bracteacoccus minor (Chodat) Petrova (Chlorophyta) in a two-stage culture // International Journal on Algae. 2014. Vol. 16, № 4. P. 354-368.
- Morais M.G., Costa J.A.V. Carbon dioxide mitigation with Chlorella kessleri, Chlorella vulgaris, Scenedesmus obliquus and Spirulina sp. cultivated in flasks and vertical tubular photobioreactors // Biotechnol. Lett. 2007. Vol. 29. P. 1349-1352.
- Mudimu O. et al. Screening of microalgae and cyanobacteria strains for a-tocopherol content at different growth phases and the influence of nitrate reduction on a-tocopherol production // Journal of Applied Phycology. 2017. Vol. 29. P. 2867-2875.
- Murakami M., Ikenouchi M. The biological CO2 fixation and utilization project by rite (2) - screening and breeding of microalgae with high capability in fixing CO2 - // Energy Conversion and Management. 1997. Vol. 38. P. 493-497.
- Ramos-Romero S. et al. Edible microalgae and their bioactive compounds in the prevention and treatment of metabolic alterations // Nutrients. 2021. Vol. 13, № 2. Art. 563.
- Ratha S.K. et al. Exploring nutritional modes of cultivation for enhancing lipid accumulation in microalgae: Exploring nutritional modes of cultivation // Journal of Basic Microbiology. 2013. Vol. 53, № 5. P. 440450.
- Rios L.F. et al. Nitrogen starvation for lipid accumulation in the microalga species Desmodesmus sp. // Applied biochemistry and biotechnology. 2015. Vol. 175, № 1. P. 469-476.
- Sangeetha M. et al. Biosequestration of carbon dioxide using carbonic anhydrase from novel Streptomy-ces kunmingensis // Archives of microbiology. 2022. Vol. 204, № 5. Art. 270.
- §irin P. A., Serdar S. Effects of nitrogen starvation on growth and biochemical composition of some microalgae species // Folia microbiologica. 2024. Vol. 69, № 4. Р. 889-902.
- Venkata Mohan S. et al. A circular bioeconomy with biobased products from CO2 sequestration // Trends in biotechnology. 2016. Vol. 34, № 6. P. 506-519.
- White W.A. Biosequestration and ecological diversity. Boca Raton: CRC Press, 2012. 250 p.
- Yang C.-M. et al. Methods for the determination of the chlorophylls and their derivatives // Taiwania. 1998. Vol. 43, № 2. P. 116-122.
- Zhang W.W. et al. Enhancing astaxanthin accumulation in Haematococcus pluvialis by coupled light intensity and nitrogen starvation in column photobioreactors // Journal of microbiology and biotechnology. 2018. Vol. 28, № 12. P. 2019-2028.
- Zhao Y. et al. Screening and application of Chlorella strains on biosequestration of the power plant exhaust gas evolutions of biomass growth and accumulation of toxic agents // Environmental science and pollution research international. 2022. Vol. 29, № 5. P. 6744-6754.
- Zhu X. et al. An informatics-based analysis of developments to date and prospects for the application of microalgae in the biological sequestration of industrial flue gas // Applied microbiology and biotechnology. 2016. Vol. 100, № 5. P. 2073-2082.


