Динамика перфузии миокарда в рубцовой ткани по данным стресс-МРТ у пациентов, подвергаемых эндоваскулярной реканализации хронической окклюзии правой коронарной артерии
Автор: Курбатов Владислав Петрович, Обединский Антон Андреевич, Обединская Наталья Ростиславовна, Пономарев Дмитрий Николаевич, Покушалов Евгений Анатольевич
Журнал: Патология кровообращения и кардиохирургия @journal-meshalkin
Рубрика: Ишемическая болезнь сердца
Статья в выпуске: 3 т.19, 2015 года.
Бесплатный доступ
Актуальность Хронические окклюзии коронарных артерий в большинстве случаев ассоциируются с наличием постинфарктного кардиосклероза в заинтересованном бассейне кровоснабжения. Этот факт ставит под сомнение целесообразность чрескожного коронарного вмешательства при данной патологии. Магнитно-резонансная томография (МРТ) сердца является наиболее точным методом верификации ишемии миокарда и определения объема постинфарктного кардиосклероза (ПИКС). Представляет интерес изучение значения данной методики для оценки перфузии в зоне ПИКС до и после реканализации хронической окклюзии коронарной артерии. Цель Оценить перфузию рубцовой ткани в заинтересованном бассейне кровоснабжения до и после ЧКВ при наличии хронической окклюзии правой коронарной артерии (ХО ПКА) по данным МРТ с отсроченным контрастированием и фармакологическим стресс-тестом. Материал и методы Проспективное рандомизированное исследование включает две группы пациентов с ХОПКА и ПИКС. В первой группе провели успешное чрескожное коронарное вмешательство, вторая группа получала только консервативную терапию. Всем пациентам выполняли МРТ с отсроченным контрастированием и стресс-тестом исходно и через 2 мес. результаты При контрольной МРТ в первой группе отметили достоверное снижение среднего количества сегментов рубцовой ткани с наличием стресс-дефекта перфузии с 2,84 (1,64) до 2,00 (1,61), средняя разница составила -0,84 сегмента, 95% ДИ для разницы -1,23___-0,46, р
Постинфарктный кардиосклероз, стресс-мрт, чрескожное коронарное вмешательство, хроническая окклюзия правой коронарной артерии, сто of right coronary artery
Короткий адрес: https://sciup.org/142140688
IDR: 142140688 | УДК: 616.127-089:616.24
Dynamics of myocardial perfusion in scar tissue according to stress CMR in patients with coronary artery disease undergoing endovascular recanalization office CTO of right coronary artery
Objective. The aim of the study was to evaluate the perfusion of scar tissue in the concerned basin blood supply before and after PCI in the presence of CTO RCA by using CMRI with delayed contrast enhancement and pharmacological stress test. Methods. The results of prospective randomized study involving two groups of patients with the presence of СТО coronary arteries and PIC (scar) are presented. The first group was with successful PCI, the second group received only conservative therapy. Delayed contrast-enhanced CMRI with a stress test was performed in all patients at baseline and after 2 months. Results. Group 1 had a significantly reduced mean number of segments with the presence of stress perfusion defects in the scar tissue during the control cardiac MRI, from 2.84 (1.64) to 2.00 (1.61), the mean difference was -0.84, 95% CI for the difference -1.23... -0.46, р
Текст научной статьи Динамика перфузии миокарда в рубцовой ткани по данным стресс-МРТ у пациентов, подвергаемых эндоваскулярной реканализации хронической окклюзии правой коронарной артерии
Доказано, что магнитно-резонансная томография (МРТ) сердца с отсроченным контрастированием является наиболее точным методом для верификации и определения объема постинфарктного кардиосклероза (ПИКС) [3, 4]. Крупные исследования (CE-MARC) и многочисленные работы доказали, что МРТ c фармакологическим стресс-тестом обладает высокой чувствительностью и специфичностью в выявлении дефектов перфузии миокарда [5, 6], с этой целью используется фармакологическая проба с аденозином.
В научной литературе отсутствуют рандомизированные клинические исследования относительно применения МРТ с аденозиновым стресс-тестом для определения нарушений перфузии в зоне ПИКС до и после реканализации ХОКА, что определяет необходимость данной работы.
Цель исследования: оценить перфузию рубцовой ткани в заинтересованном бассейне кровоснабжения до и после ЧКВ при наличии хронической окклюзии правой коронарной артерии (ХО ПКА) по данным МРТ с отсроченным контрастированием и фармакологическим стресс-тестом.
Материал и методы
За период с октября 2010 г. по апрель 2014 г. на базе центра эндоваскулярной хирургии и лучевой диагностики ФГБУ «ННИИПК им. акад. Е.Н. Мешалкина» Минздрава России обследовали 72 пациента с наличием ХО ПКА, которым выполняли чрескожную транслюминальную коронарную ангиопластику (ЧТКА) со стентированием. Критерии включения: стабильная стенокардия напряжения I–IV функционального класса (ФК), правый тип кровоснабжения сердца по данным селективной коронарографии, отсутствие хирургически значимого атеросклеротического поражения других коронарных артерий (стенозы менее 65%). Допускалось наличие ранее стентированных артерий без признаков значимого рестеноза и высокого риска ишемии миокарда по данным МРТ с аденозиновым стресс-тестом.
Среди обследованных больных были выделены две группы пациентов. В первую группу вошли 39 пациентов, которым была выполнена успешная ЧКВ ХО ПКА. Во вторую группу включены 33 пациента, не подвергающиеся оперативному лечению, находящиеся исключительно на консервативной терапии. Пациенты в обеих группах сопоставимы по демографическим показателям и исходной тяжести состояния.
Всех пациентов обследовали на магнитнорезонансном томографе Initial Achieva 1,5 Т, Philips (Голландия).
Стандартный протокол исследования предусматривал сканирование в области сердца в аксиальной плоскости в режимах с черной (TSE_BBsense) и белой (M2D_B_TFE) кровью толщиной среза 8 мм, интервалом 0,8 мм. При этом позиционирование срезов проводили в стандартной последовательности. Морфологию левого желудочка (ЛЖ), в частности его форму, толщину стенок и показатели сократимости, оценивали в кинорежиме B_TFE в двух-, трех- и четырехкамерных плоскостях, а также по короткой оси сердца, при необходимости выполняли дополнительный срез через выходной тракт ЛЖ. Наличие отека миокарда ЛЖ диагностировали в плоскости по короткой оси на Т2_BB_ SPIR.
Для выявления и оценки распространенности рубцовых изменений миокарда ЛЖ анализировали отсроченное накопление контрастного вещества в плоскости по короткой оси, в двух- и четырехкамерной плоскостях в режиме Т1_TFE_SPIR и 3DT1_TFEPSIR. Время задержки сатурационного импульса TFE Prepulse для подавления сигнала от миокарда выбирали на серии предварительного просмотра в режиме LookLoсker или IR_TFE_LL.
Для детальной оценки сократимости и массы миокарда ЛЖ просматривали серию срезов в коронарной плоскости с использованием программ Philips MR Cardiac Explorer или Philips MR Cardiac Analysis. Перфузию миокарда исследовали на трех уровнях в плоскости по короткой оси сердца, проходящей через середину расстояния между кольцом митрального клапана и серединой ЛЖ, через середину ЛЖ, а также на середине расстояния между верхушкой и серединой ЛЖ.
Для проведения стресс-перфузии миокарда использовали стандартный протокол [7]. Миокардиальную перфузию ЛЖ оценивали с использованием 17-сегмен-тной схемы (АНА, 2002). Согласно европейским рекомендациям по стабильной стенокардии напряжения, клинически значимой ишемией миокарда для стресс-МРТ являлся дефект перфузии в двух и более сегментах [8], что соответствует 10% и более объема миокарда [9]. Сумму стресс-индуцированных сегментов учитывали в соответствии с кровоснабжением бассейна правой коронарной артерии. Три врача отделения лучевой и функциональной диагностики оценивали дефекты перфузии независимо друг от друга.
Для верификации наличия ХОКА, а также определения коллатералей и морфологии окклюзированного сосуда всем больным проводили диагностическую коронарографию по стандартной методике M.P. Judkins на моноплановой ангиографической установке «Aдван-ткс LCV» или биплановой ангиографической установке «Aдванткс LC/LP» (Дженерал электрик, США).
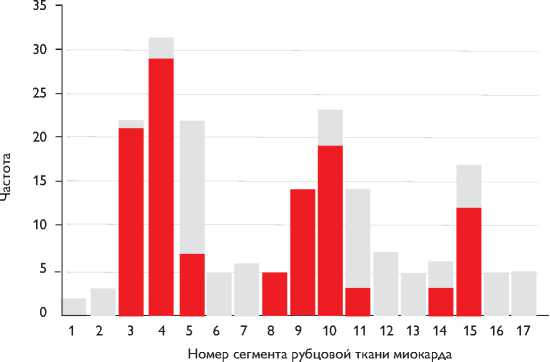
■ Стресс-дефект перфузии
Рис. 1. Исходное распределение рубцовой ткани и стресс-дефектов перфузии миокарда по сегментам в первой группе
Все пациенты получали антиангинальную терапию: нитраты, бета-блокаторы или антагонисты кальция в индивидуальных дозировках. При наличии показаний (артериальная гипертензия (АГ), выраженная сердечная недостаточность, гиперхолестеринемия) назначались также диуретики, ингибиторы ангиотензин-превращающего фермента и статины. Кроме того, все пациенты длительно принимали препараты ацетилсалициловой кислоты в индивидуальных дозировках.
Для статистической обработки данных использовали методы описательной статистики, параметрические и непараметрические статистические методы. Для обзора серийных измерений применяли регрессионный анализ повторных измерений. Для межгруппового анализа качественных признаков применяли критерий хи-квадрат Пирсона либо точный тест Фишера. Количественные признаки сравнивали с применением теста Манна – Уитни. Для внутригруппового анализа количественных и качественных признаков
■ Стресс-дефект перфузии
ll. -ll -I
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17
Номер сегмента рубцовой ткани миокарда
Рис. 2. Распределение рубцовой ткани миокарда и стресс-дефектов перфузии по сегментам в первой группе через 2 мес. после стентирования правой коронарной артерии на этапах исследования применяли тесты Фридмана и МакНемара соответственно. Количественные характеристики представлены как медиана (25-й; 75-й процентили), если не указано иное. Качественные признаки представлены как число (%). Статистический анализ выполнен с применением программного обеспечения R Core Team (2013). R: A language and environment for statistical computing. R Foundation for Statistical Computing, Vienna, Austria. URL:
Результаты и обсуждение
Согласно данным стандартного обследования, ПИКС был зафиксирован у 24 (64,9%) в первой и 22 (68,8%) пациентов во второй группах, достоверных межгрупповых различий не обнаружено (р = 0,81). В то же время, по данным МРТ, наличие рубцовой ткани хотя бы в одном сегменте миока б рда зафиксировали у 35 (89,7%) в первой и 27 (81,8%) пациентов во второй группах (р = 0,49). Исходно 14 (19,4%) пациентов в двух группах имели рубцовую ткань в области 4 сегментов. Локализация рубца в пределах трех и двух сегментов отмечалась в 9 (12,5%) случаях. Всего у 72 пациентов зафиксировано 285 сегментов рубцовой ткани миокарда, из них 200 (70,2%) сегментов имели дефект перфузии.
В первой группе рубцовая ткань охватывала область четырех сегментов в 6 (15,4%) случаях, у 5 пациентов в каждом случае рубец занимал 6, 7, и 8 (12,6%) сегментов. Во второй группе также наиболее часто – в 8 (21,1%) случаях – встречалась локализация рубцовой ткани в области 4 сегментов. Распространение рубца на область 3 и 2 сегментов миокарда было отмечено в 7 (21,9%) и 5 (15,6%) случаях соответственно. Достоверных межгрупповых различий количества сегментов рубцовой такни миокарда не обнаружено (р = 0,51).
В двух группах наиболее часто рубцовая ткань располагалась в области четвертого – в 54 (75,0%) случаях, десятого – в 42 (58,3%), третьего – в 35 (48,6%) и пятнадцатого сегмента – в 23 (31,9%) случаях . Стресс-дефект перфузии этих сегментов зарегистрирован в 51 (70,8%), 38 (52,8%), 35 (100,0%) и 18 (25,0%) случаях соответственно.
В первой и второй группах преобладающей локализацией рубцовой ткани являлись четвертый (29 (74,4%) и 25 (73,5%) случаев), десятый (23 (58,9%) и 19 (55,9%) случаев), третий (22 (56,4%) и 14 (41,2%) случаев) и пятнадцатый (17 (43,6%) и 6 (17,4%) случаев)
Стресс
Покой
Отсроченное контрастирование
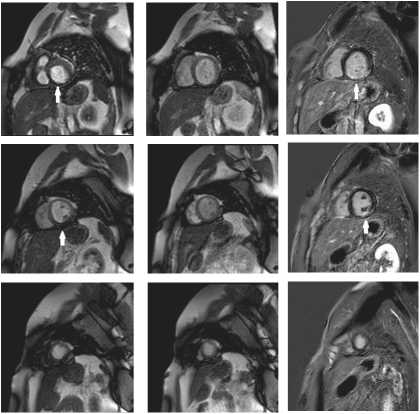
б
Рис. 3. МРТ сердца со стресс-тестом (а) и отсроченным контрастированием миокарда (б) до ЧКВ сегменты соответственно. Дефект перфузии отмечался в 21 (53,8%), 19 (48,7%), 21 (53,8%) и 12 (30,8%) случаях в первой группе и в 24 (70,6%), 19 (100,0%), 13 (100,0%) и 6 (100,0%) случаях во второй группе. Статистически достоверных межгрупповых различий в исходном характере распределения сегментов рубцовой ткани, демонстрирующих стресс-дефект перфузии, не обнаружено (р = 0,67).
При контрольной МРТ через 2 мес. в первой группе отмечено достоверное снижение среднего количества сегментов рубцовой ткани, демонстрирующих стресс-дефект перфузии, с 2,84 (1,64) до 2,00 (1,61), средняя разница составила –0,84 сегмента, 95% ДИ для разницы –1,23… –0,46, р<0,01. Динамика количества сегментов со стресс-дефектом перфузии в первой группе представлена на рис. 1 и 2. Во второй группе при контрольной МРТ через 2 мес. после рандомизации среднее (стандартное отклонение) количество сегментов с дефектом перфузии осталось неизменным и составило 2,36 (1,61); р = 0,91.
При межгрупповом сравнении количества сегментов, демонстрирующих стресс-дефект перфузии при контрольной МРТ через 2 мес. после рандомизации, статистически достоверных различий не обнаруже-
Стресс
Покой
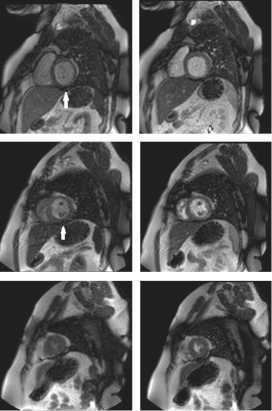
Рис. 4. МРТ сердца со стресс-тестом ( а ) и отсроченным контрастированием миокарда ( б ) после ЧКВ
Отсроченное контрастирование
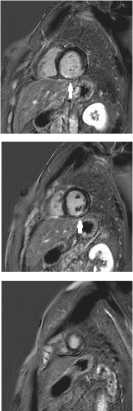
б
но. Среднее (стандартное отклонение) составило 2,00 (1,57) в первой и 2,33 (1,63) во второй группах. Средняя разница (первая – вторая группа) составила –0,33 сегмента, 95% ДИ для разницы –0,41… 1,08, р = 0,37. Этот факт объясняется тем, что среднее количество сегментов рубцовой ткани с дефектом перфузии исходно было выше в первой группе (2,84, (1,64)), чем во второй группе (2,36 (1,61)), хотя достоверных различий не было (р = 0,51).
Таким образом, ЧКВ при ХО ПКА улучшает перфузию миокарда в сегментах с рубцовыми изменениями, по данным МРТ с фармакологическим стресс-тестом (рис. 3 и 4). Заключение коррелирует с результатами исследований в молекулярной и клеточной биологии. Доказано, что постинфарктный рубец состоит из фенотипически трансформированных фибробластоподобных клеток, называемых миофибробластами [10, 11]. Эти клетки питаются посредством неососудов и находятся в постинфарктной зоне. Постинфарктный рубец – метаболически активная ткань, васкуляризированная и способная сокращаться [12, 13]. Развитие обратимой миокардиальной дисфункции называется «гибернирующим миокардом» [14]. Гибернация миокарда – защитный механизм, с помощью которого возможно частично восстановить сократительную функцию в области повреждения [15]. Опыты на крысах показали, что при микроскопическом исследовании сердца в определенных случаях наблюдаются небольшие островки живого миокарда в зоне ПИКС. Эти участки способствуют сохранению формы и объема левого желудочка [16]. Таким образом, возможно предположить, что ЧКВ при ХО ПКА способно уменьшить постинфарктное ремоделирование сердца и прогрессирование сердечной недостаточности.
Выводы
Согласно результатам исследования, эндоваскулярная реканализация ХО ПКА у больных постинфарктным кардиосклерозом улучшает перфузию в зоне ПИКС. Метод МРТ с аденозиновым стресс-тестом целесообразно использовать для диагностики регресса ишемии в зоне ПИКС после успешной реканализации коронарных артерий.
Список литературы Динамика перфузии миокарда в рубцовой ткани по данным стресс-МРТ у пациентов, подвергаемых эндоваскулярной реканализации хронической окклюзии правой коронарной артерии
- De Wood M.A., Spores J., Notske R. et al.//N. Engl. J. Med. 1980. Vol. 303. P. 897-902.
- Olivari Z., Rubartelli P., Piscione F. et al.//J. Am. Coll. Cardiol. 2003. Vol. 41. P. 1672-1678.
- Осиев А.Г., Кретов Е.М., Найденов Р.А. и др.//Патология кровообращения и кардиохирургия 2013. № 3. С. 46-49.
- Kim R.J., Fieno D.S., Parrish T.B. et al.//Circulation. 1999. Vol. 100. P. 1992-2002.
- Greenwood J.P., Maredia N., Younger J.F. et al.//Lancet. 2012. Vol. 379. P. 453-456.
- Nandalur K.R., Dwamena B.A., Choudhri A.F. et al.//J. Am. Coll. Cardiol. 2007. Vol. 50. P. 1343-1353.
- Курбатов В.П., Гензель Н.Р., Обединский А.А. и др.//Радиология практика. 2012. № 4. С. 27-34.
- Montalescot G., Sechtem U., Achenbach S. et al.//Eur. Heart J. 2013. Vol. 34. P. 2949-3003.
- Davies R.F., Goldberg A.D., Forman S. et al.//Circulation. 1997. V. 95. P. 2037-2043.
- Sun Y., Weber K.T.//J. Mol. Cell Cardiol. 1996. Vol. 28. P. 851-858.
- Vracko R., Thorning D.//LabInvest. 1991. Vol. 65. P. 214-227.
- De Mey J.G.R., Fazzi G.E.//Hypertension. 1996. Vol. 28. P. 696.
- Gabbiani G., Hirschel B.J., Ryan G.B., et al.//J. Exp. Med. Vol. 67. P. 719-734.
- Camici P.G., Prasad S.K., Rimoldi O.E. et al.//Circulation. 2008. Vol. 117. P. 103-114.
- Ross J.Jr.//Circulation. 1991. Vol. 83. P. 1076-1083.
- lhaddad I.A., Kloner R.A., Hakim I. et al.//Am. Heart. J. 1996. Vol. 131. № 3. P. 451-457.


