Динамика проницаемости кишечника у онкологических больных в периоперационном периоде
Автор: Карпенко А.Ю., Цветков Д.С., Киселевский М.В.
Журнал: Сибирский онкологический журнал @siboncoj
Рубрика: Лабораторные и экспериментальные исследования
Статья в выпуске: 6 (66), 2014 года.
Бесплатный доступ
Слизистая оболочка кишечника является защитным барьером организма, препятствующим проникновению в системный кровоток бактериальных агентов и их токсинов, вызывающих развитие воспалительной реакции. В работе оценена динамика кишечной проницаемости у онкологических и кардиохирургических больных в периоперационном периоде с помощью метода неметаболизируемых сахаров (лактулоза-маннитол). Выявлено, что уровень экскреции лактулозы и маннитола повышен у онкологических больных с развившимися послеоперационными осложнениями как до, так и после операции, что свидетельствует о повышенной кишечной проницаемости у данной группы пациентов. Можно предположить, что проникающий, вследствие повышенной кишечной проницаемости, в кровь бактериальный липополисахарид индуцирует ответ эффекторов врожденного иммунитета, на фоне уже активированной иммунной системы приводит к развитию системной воспалительной реакции. Поэтому оценка трансинтестинальной проницаемости может рассматриваться в качестве прогностического фактора неблагоприятного течения раннего постоперационного периода у онкологических больных.
Проницаемость кишечника, онкологические больные, послеоперационные осложнения
Короткий адрес: https://sciup.org/14056476
IDR: 14056476 | УДК: 616-006:616.33-006.6-089:612.017
Dynamic of intestinal permeability in cancer patients during perioperative period
Intestinal mucosa is a barrier, preventing bacteria and it’s derivate from penetrating to organism, where it triggers inflammation. In this study the dynamic of intestinal permeability in cancer and cardio surgery patients during perioperative period is evaluated using dual sugar test (lactulose-mannitol). Lactulose and mannitol excretion ratio is increased in group of cancer patients with postoperative complications before and after surgery. This indicates an increased intestinal permeability in these patients. Probably increased permeability cause bacterial lipopolysaccharide translocation into blood, where it induces effectors of innate immunity, leading to system inflammation reaction due to already activated immunity. According to this, evaluation of intestinal permeability can be considered as a prognostic factor of unfavorable early postoperative period in cancer patients.
Текст научной статьи Динамика проницаемости кишечника у онкологических больных в периоперационном периоде
У онкологических больных в периоперационном периоде часто наблюдается увеличение содержания в крови бактериального эндотоксина – липополисахарида (ЛПС). Энтеротоксемия может быть обусловлена не только поступлением бактерий и их токсинов из первичного очага воспаления, но и усилением их транслокации через слизистые оболочки. Слизистая оболочка кишечника формирует эффективный барьер для микроорганизмов и токсинов [12]. Нарушение этого защитного механизма в случае увеличения кишечной проницаемости может привести к чрезмерной транслокации кишечных бактерий и/или их токсинов в окружающие ткани и отдаленные органы [14]. Транзиторная бактериемия встречается довольно часто и сопровождает не только инвазивные, но и многие неинвазивные манипуляции и процедуры. Экспериментально было показано, что трансинтестинальное перемещение бактерий и токсинов наблюдается у пациентов с ожогами, шоком, обструкцией кишечника и после расширенных операций [7, 10, 13, 15, 17].
Следовательно, стрессовое воздействие на организм пациента во время операционного вмешательства может приводить к изменению барьерной функции слизистых оболочек, прежде всего кишечника, и вызывать поступление в кровь бактерий и/ или их токсинов, что, в свою очередь, инициирует каскад воспаления вследствие активации эффекторов врожденного иммунитета. Изучение механизмов такой инверсии иммунных реакций организма является в настоящее время одной из важнейших задач биомедицинских исследований, решение которой позволит понять патогенез развития послеоперационных гнойно-септических осложнений, а также выявить прогностические маркеры и разработать меры профилактики. Оценка целостности кишечного барьера является эффективным методом для диагностики и мониторинга степени повреждения слизистой оболочки кишечника. С этой целью широко используется измерение уровня экскреции с мочой неметаболизируемых сахаров, вводимых перорально [1, 11, 16].
Целью исследования являлось изучение изменения кишечной проницаемости у онкологических больных в периоперационном периоде.
Материал и методы
Кишечную проницаемость оценивали с помощью определения экскреции лактулозы и манни-тола. Для этого больным перорально давали 30 мл 1,5 % раствора маннитола (4,5 г маннитола) и 30 мл препарата «Дюфалак» (20 г лактулозы), после чего в течение 6 ч собирали мочу, измеряли общий объем диуреза и отбирали пробу для дальнейшего исследования. Полученные пробы мочи хранили при –70ºС.
У онкологических пациентов пробы мочи собирали за сутки до операции, на 1, 2 и 5-е сут после операции с целью оценки динамики трансинтестинальной проницаемости. У кардиохирургических больных мочу собирали накануне и на 1-е сут после операции для сравнения исходных показателей кишечной проницаемости и влияния хирургического вмешательства.
Определение концентрации лактулозы проводили по методу Селиванова [12], маннитола – по методу Corcoran и Page [9]. Высчитывали процент экскретированных с мочой аналитов по следующей формуле:
Cl = [D × k × V/m] × 100 %, где D – оптическая плотность; k – коэффициент, полученный с помощью калибровочной кривой, равный 5,7337 для лактулозы и 0,586 для манни-тола; V – объем диуреза, мл; m – масса аналита, мг (20 000 мг лактулозы, 4 500 мг маннитола).
Статистическую обработку полученных результатов проводили с использованием критериев непараметрической статистики пакета Statistica 10. Для межгруппового сравнения применяли критерий Манна – Уитни (р<0,05), для внутригруппового – Вилкоксона (р<0,05). В качестве описательной статистики использовали медиану и размах квартилей (25 ÷75 %).
Результаты исследования
Онкологические больные ретроспективно были разделены на 2 подгруппы: 1) с развившимися послеоперационными осложнениями (у 8 из 24 пациентов возникли следующие послеоперационные осложнения: острый панкреатит (n=6), пневмония (n=2), сепсис (n=1)); 2) без осложнений (n=16).
На начальном этапе проводилось сравнение показателей трансинтестинальной проницаемости в обеих группах до и через 1 сут после операции. При исследовании уровня выведения лактулозы оказалось, что на дооперационном этапе уровень экскреции данного сахара у онкологических больных с осложнениями был значимо выше, у кардиохирургических пациентов и онкологических больных без осложнений. После операции этот показатель значимо возрастал у кардиохирургических пациентов и у онкологических больных без осложнений. В группе онкологических больных с осложнениями исследуемый параметр имел недостоверную тенденцию к увеличению (p=0,06), однако существенно (p<0,05) превышал аналогичные показатели у онкологических больных без осложнений и кардиохирургических пациентов. Процент выведения лактулозы в группе онкологических больных без осложнений значимо не отличался от
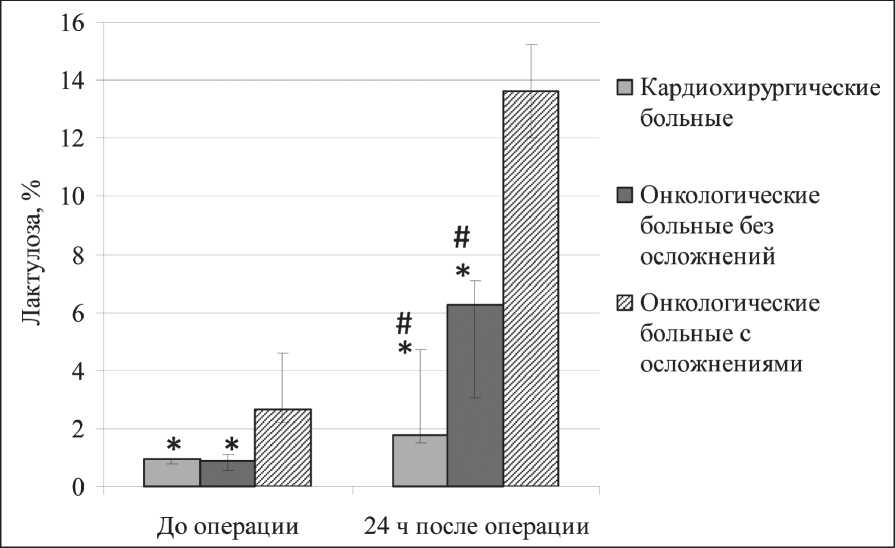
Рис. 1. Выведение лактулозы накануне и через 1 сут после операции у кардиохирургических больных, онкологических пациентов без послеоперационных осложнений и с осложнениями. Данные представлены в виде медианы и размаха квартилей; * – значимое межгрупповое отличие от показателей онкологических больных с осложнениями по критерию Манна – Уитни (p<0,05); # – значимое внутригрупповое отличие от показателей до операции по критерию Вилкоксона (p<0,05)
такового у кардиохирургических пациентов как до, так и после операции (рис. 1).
Процент выведения маннитола в группе онкологических больных с послеоперационными осложнениями исходно также значимо превышал показатели кардиохирургических больных и онкологических пациентов без осложнений. Экскреция маннитола у онкологических больных с послеоперационными осложнениями значимо увеличивалась через 1 сут после операции. Этот показатель значимо не отличался у кардиохирургических больных и онкологических пациентов без осложнений до и после операции; хирургическое вмешательство также не приводило к достоверному изменению данного параметра в указанных группах (рис. 2).
Таким образом, результаты исследования согласуются с имеющимися литературными данными о повышении трансинтестинальной проницаемости в ответ на хирургическое вмешательство [7]. Рассматриваемое явление наблюдалось не только в группе онкологических больных, у которых в ходе операции нарушалась целостность желудочно-кишечного тракта, но и во время кардиохирургических вмешательств, не оказывающих непосредственного влияния на состояние кишечной стенки.
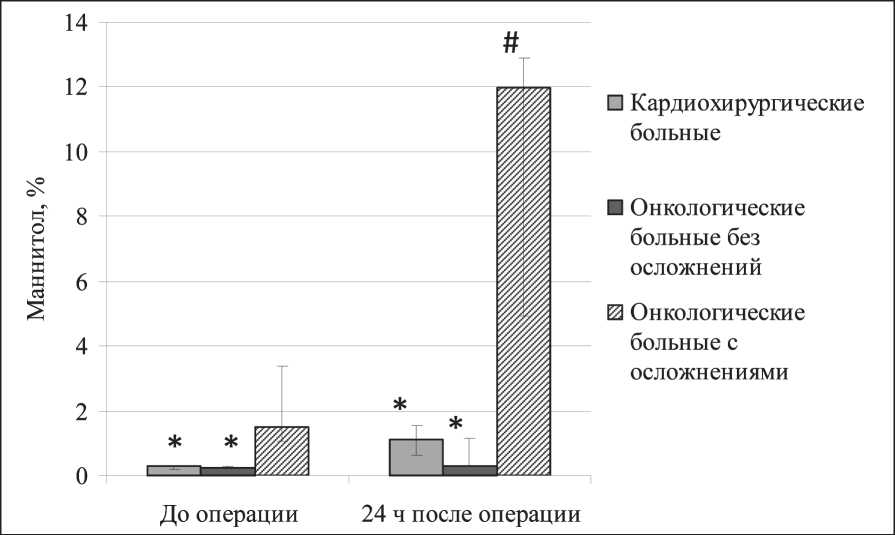
Рис. 2. Выведение маннитола накануне операции и на 1-е сут после операции у кардиохирургических больных и онкологических пациентов без послеоперационных осложнений и с таковыми. Данные представлены в виде медианы и размаха квартилей; * – значимое межгрупповое отличие от показателей онкологических больных с осложнениями по критерию Манна – Уитни (p<0,05); # – значимое внутригрупповое отличие от показателей до операции по критерию Вилкоксона (p<0,05)
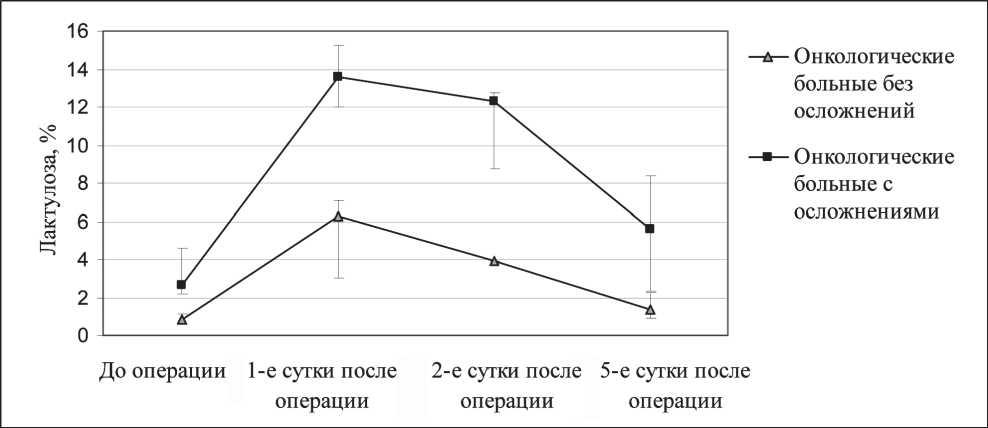
Рис. 3. Изменение уровня лактулозы, экскретированной с мочой в периоперационном периоде, у пациентов без послеоперационных осложнений и с таковыми. Данные представлены в виде медианы и размаха квартилей; * – значимое отличие между группами по критерию Манна – Уитни
Показатели кишечной проницаемости в группе онкологических больных без осложнений не отличались от таковых у кардиохирургических пациентов как до, так и после операции. Это позволяет предположить, что локализация опухоли в органах желудочно-кишечного тракта сама по себе не влияет на трансинтестинальную проницаемость. Однако исследуемые параметры были повышены в группе онкологических больных с послеоперационными осложнениями, что наблюдалось уже на дооперационном этапе.
У онкологических больных исследовалась динамика экскреции маннитола и лактулозы в раннем послеоперационном периоде. При изучении уровня выведения лактулозы было установлено, что уровень ее экскреции в группе пациентов с осложнениями остается повышенным в течение 5 сут после операции, в то время как у больных без осложнений этот параметр на 5-е сут послеоперационного периода не отличается от исходных значений (рис. 3). Значения экскреции маннитола в группе с осложнениями были значимо выше, чем у пациентов без осложнений, только до и через 1 сут после операции, однако в последующем (2–5-е сут после операции) значимых отличий не выявлено (рис. 4). Такая динамика показателей свидетельствует о повышенной проницаемости кишечной стенки у пациентов с послеоперационными ослож-
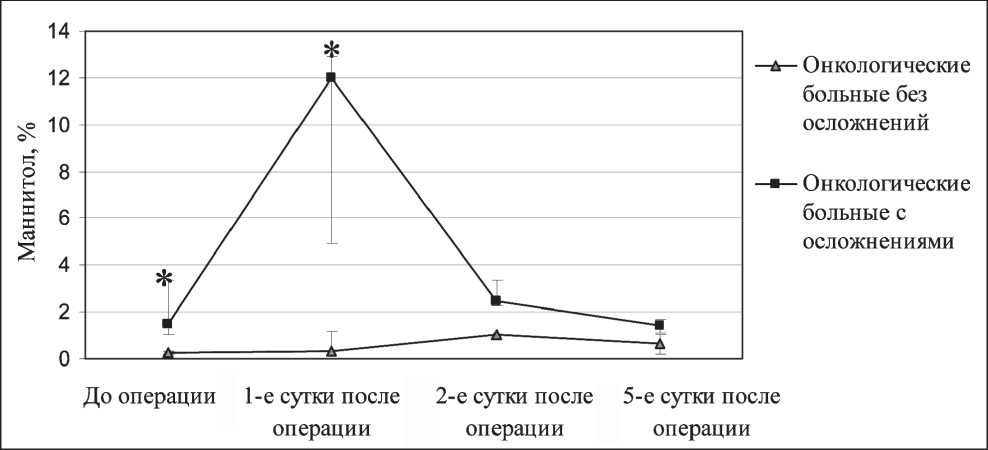
Рис. 4. Изменение уровня лактулозы, экскретированной с мочой в периоперационном периоде, у пациентов без осложнений и с таковыми. Данные представлены в виде медианы и размаха квартилей; * – значимое отличие между группами по критерию Манна – Уитни
СИБИРСКИЙ ОНКОЛОГИЧЕСКИЙ ЖУРНАЛ. 2014. № 6
нениями, что наблюдается уже на дооперационном этапе. В связи с этим трансинтестинальная проницаемость может рассматриваться как прогностический фактор развития послеоперационных гнойно-септических осложнений.
Обсуждение
Измерение экскреции с мочой неметаболизи-руемых сахаров, введенных перорально, широко используется для исследования кишечной проницаемости как при различных патологических процессах, так и в здоровом организме. Метод двух сахаров основан на том, что небольшие молекулы (маннитол, рамноза) проходят через слизистую оболочку кишечника трансцеллюлярным путем, а большие молекулы (лактулоза, целлобиоза) – па-рацеллюлярным путем, через плотные контакты. Таким образом, возрастание уровня экскреции лактулозы свидетельствует о повышении проницаемости плотных контактов.
Межклеточные плотные контакты представляют собой комплекс из нескольких белков, формирование которого регулируется множеством факторов. Имеются данные об изменении числа плотных контактов в ответ на действие интерферона γ, фактора некроза опухоли α, интерлейкинов 1, 4, 6, 10, различных факторов роста. Механизмы такой регуляции связывают с влиянием вышеперечисленных цитокинов на реорганизацию актинового цитоскелета, что ведет к изменению структуры плотных контактов [8].
Известно, что для онкологических больных характерно повышенное содержание в крови различных цитокинов [3, 5], влияющих на систему межклеточных контактов и, соответственно, на проницаемость кишечника. Это, наряду с последующим стрессовым воздействием расширенного хирургического вмешательства, может стать причиной транслокации бактерий и/или их токсинов через кишечную стенку в системный кровоток, что может привести к развитию системной воспалительной реакции в раннем послеоперационном периоде.
Результаты настоящей работы свидетельствуют о повышенной кишечной проницаемости у онкологических больных с послеоперационными осложнениями в сравнении с кардиохирургическими пациентами и группой онкологических больных без осложнений. Это согласуется с данными других авторов о повышенном уровне ЛПС и некоторых цитокинов у онкологических больных с сепсисом [2, 4]. Можно предположить, что проникающий вследствие повышенной кишечной проницаемости в кровь ЛПС, посредством толлподобных рецепторов индуцирует ответ эффекторов врожденного иммунитета [6], что на фоне уже активированной иммунной системы приводит к развитию системной воспалительной реакции. Поэтому оценка трансинтестинальной проницаемости может рассматриваться в качестве прогностического фактора неблагоприятного течения раннего постоперационного периода у онкологических больных.
Выводы
В работе показано, что уровень экскреции лактулозы в группе онкологических больных с послеоперационными осложнениями выше, чем у пациентов без осложнений до операции, на 1-е и 5-e сут после операции. Уровень экскреции маннитола у онкологических пациентов с послеоперационными осложнениями выше, чем таковой у больных без осложнений, до операции и на 1-е сут после операции. Уровень экскреции лактулозы и маннитола у онкологических больных с послеоперационными осложнениями превышает показатели кардиохирургических пациентов как до операции, так и на 1-е сут после. Показатели трансинтестинальной проницаемости онкологических больных не отличаются от таковых в группе кардиохирургических пациентов до операции и через 24 ч после нее.


