Динамика содержания аквапоринов плазмалеммы и тонопласта подсемейств PIP и TIP в ходе роста растяжением клеток колеоптилей проростков риса, различающихся скоростью роста в условиях нормоксии и затопления
Автор: Кирпичникова А.А., Смирнов П.Д., Данелия Г.В., Емельянов В.В., Шишова М.Ф.
Журнал: Сельскохозяйственная биология @agrobiology
Рубрика: Механизмы адаптации
Статья в выпуске: 3 т.60, 2025 года.
Бесплатный доступ
Колеоптили злаков характеризуются достаточно ограниченным временным интервалом развития и выполняют защитную функцию. У гидрофитного злака риса посевного (Oryza sativa L.) за счет способности клеток колеоптилей к росту растяжением осуществляется защита проростка от недостатка кислорода при затоплении. Резкое удлинение клеток сопровождается интенсивной вакуолизацией. Этот процесс обусловлен усилением транспорта воды через плазмалемму и тонопласт, который осуществляется посредством транспортеров группы аквапоринов. В работе нами впервые приведены данные, позволившие выявить изменения представленности аквапринов семейств PIP1 и TIP1 в клетках колеоптилей проростков риса, развивающихся в условиях нормоксии и затопления. Цель работы состояла в оценке динамики содержания аквапоринов с преимущественной локализацией в плазмалемме и тонопласте клеток колеоптилей в процессе роста растяжением у риса при аэрации и дефиците кислорода. Использовали семена двух сортов риса отечественной селекции - Аметист (медленно растущий) и Кубань 3 (быстро растущий). Семена поверхностно стерилизовали и проращивали (по 50 шт.) в гидропонных условиях в темноте при 29 °С на стеклянных мостках (контрольные растения) или создавали условия затопления в банках объемом 750 мл с использованием 4 % питательного раствора Кнопа. Для определения длины клеток центральной части колеоптилей изготавливали микропрепараты. Их фотосъемку выполняли с помощью светового микроскопа Leica DM 2500 и фотокамеры Leica DFC450 C («Leica Microsystems GmbH», Германия) при увеличении ×20. Общую микросомальную фракцию получали из клеток колеоптилей проростков при температуре 4 °С. Содержание белка в пробах определяли по микрометоду Брэдфорда с использованием красителя Coumassie Brilliant Blue G250. Поглощение красителя, сорбированного на белках, измеряли на планшетном спектрофотометре SPECTROstar Nano («BMG Labtech», Германия) при λ = 595 нм. Концентрацию белка в пробах определяли на основе калибровочного графика, построенного с использованием раствора яичного альбумина на 150 мМ сахарозе и 10 мМ Tris-MES. Белки разделяли методом денатурирующего электрофореза в 10 % полиакриламидном геле. Содержание аквапоринов PIP1 с преимущественной локализацией на плазмалемме и TIP1 с преимущественной локализацией на тонопласте в составе общей микросомальной фракции оценивали посредством иммуноблот-анализа с использованием специфичных поликлональных антител. Проведенный микроскопический анализ длины клеток центральной части колеоптилей выявил завершение роста у проростков сорта Кубань 3 на 5-е сут развития в аэробных условиях. Удлинение клеток колеоптилей у сорта Аметист было незначительным за весь тестируемый период. При затоплении у колеоптилей сорта Кубань 3 отмечали почти 2-кратное удлинение клеток уже на 3-и сут прорастания по сравнению с контролем. Более интенсивный рост при затоплении сохранялся до 7-х сут прорастания. У сорта Аметист на 3-и сут выявленные различия были не столь велики, как у сорта Кубань 3, однако к 5-м сут длина клеток увеличивалась почти в 3 раза. В процессе удлинения клеток происходило изменение содержания белка во фракции клеточных эндомембран. Вследствие значительного увеличения размеров клеток на 5-е сут после прорастания происходило почти 3-кратное снижение концентрации белка микросомальной фракции. Этот процесс продолжался, хоть и не столь интенсивно и дальше, к 7-м сут развития проростка. Снижение содержания белка было отмечено как для сорта Кубань 3, так и для сорта Аметист. При недостатке кислорода (затопление) оно оказалось менее интенсивным. С помощью иммуноблоттинга показана неравная динамика накопления белков аквапоринов подсемейств PIP1 и TIP1 как при аэробном развитии проростков риса, так и при недостатке кислорода. У проростков сорта Кубань 3 в отличие от сорта Аметист накопление аквапоринов PIP1 соответствовало изменению интенсивности удлинения клеток колеоптилей. Однако независимо от сорта и количества кислорода при прорастании содержание вакуолярных аквапоринов TIP1 постепенно увеличивалось. Полученные данные указывают на различия функционального значения аквапоринов плазмалеммы и тонопласта в процессе роста растяжением клеток колептилей в условиях нормоксии и недостатка кислорода.
Аквапорины, затопление, колеоптили, рис
Короткий адрес: https://sciup.org/142246196
IDR: 142246196 | УДК: 633.18:581.1:576.32/.36:577.24 | DOI: 10.15389/agrobiology.2025.3.445rus
The plasma membrane and tonoplast PIP and TIP aquaporins abundance during the elongation growth of coleoptile cells of rice seedlings with different growth rates under normoxia and submergence
Coleoptiles of cereals are characterized by a rather limited time interval of development and perform a protective function. In the hydrophytic cereal rice (Oryza sativa L.), the ability of coleoptile cells to grow by elongation protects the seedling from oxygen deficiency during flooding. Sharp Cell elongation is accompanied by intense vacuolization. This process is due to increased water transport through the plasma membrane and tonoplast, which is carried out by special transporters of the aquaporin group. In the presented work, for the first time, data were obtained that made it possible to reveal a crosslink between changes in the amount of plasma membrane aquaporins of the PIP1 and TIP1 subfamilies and the intensity of cell elongation in coleoptiles of rice seedlings both under normoxia and hypoxia and to reveal the unequal functional significance of plasma membrane and tonoplast aquaporins during cell elongation. The aim of the work was to evaluate the dynamics of the content of aquaporins with predominant localization in the plasma membrane and tonoplast of coleoptile cells during elongation growth in rice under aeration and oxygen deficiency. Seeds of two rice varieties of domestic selection were used: Amethyst (slow-growing) and Kuban 3 (fast-growing). The seeds were surface sterilized and germinated (50 pcs.) under hydroponic conditions in the dark at 29 °С on glass walkways (control plants) or flooded in 750 ml jars using 4 % Knop nutrient solution. Micropreparations were made to determine the length of the cells in the central part of the coleoptiles. They were photographed using a Leica DM 2500 light microscope and a Leica DFC450 C camera (Leica Microsystems GmbH, Germany) at a magnification of 20×. The total microsomal fraction was obtained from coleoptile cells of seedlings at a temperature of 4 °С. The protein content in the samples was determined by the Bradford micromethod using the Coumassie Brilliant Blue G250 dye. The absorption of the dye adsorbed on the proteins was measured on a SPECTROstar Nano plate spectrophotometer (BMG Labtech, Germany) at λ = 595 nm. The protein concentration in the samples was determined based on a calibration graph constructed using a solution of egg albumin in 150 mM sucrose and 10 mM Tris-MES. The proteins were separated by denaturing electrophoresis in 10% polyacrylamide gel. The content of aquaporins PIP1 with predominant localization on in the plasma membrane and TIP1 with predominant localization in the tonoplast in the total microsomal fraction was estimated by immunoblot analysis using specific polyclonal antibodies. Microscopic analysis of the length of cells in the central part of coleoptiles revealed the completion of growth in the seedlings of the Kuban 3 variety on the 5th day of development under aerobic conditions. Elongation of coleoptile cells in the Ametist variety was low intense throughout the tested period. When flooded, coleoptiles of the Kuban 3 variety showed almost 2-fold elongation of cells already on the 3rd day of germination compared to the control. More intensive growth under flooding persisted until the 7th day of germination. In the Ametist variety, the differences revealed on the 3rd day were not as great as in the Kuban 3 variety, but by the 5th day the cell length increased almost 3 times. During cell elongation, the protein content in the fraction of cellular endomembranes changed. Due to a significant increase in cell size on the 5th day after germination, there was an almost 3-fold decrease in the concentration of protein in the microsomal fraction. This process continued, although not so intensively, further, by the 7th day of seedling development. A decrease in protein content was noted for both the Kuban 3 and Ametist varieties. Under oxygen deficiency (flooding), it was less pronounced. Using immunoblotting, unequal dynamics of accumulation of proteins of the PIP1 and TIP1 subfamilies aquaporins was shown both during aerobic development of rice seedlings and under oxygen deficiency. The accumulation of PIP1 aquaporins corresponded to a change in the intensity of coleoptile cell elongation. The effect was more visible in the Kuban 3 variety seedlings. However, regardless of the variety and amount of oxygen during germination, the content of vacuolar aquaporins TIP1 gradually increased. The obtained data indicate differences in the functional significance of aquaporins of the plasmalema membrane and tonoplast in the process of elongation growth of coleptile cells under normoxia and oxygen deficiency conditions.
Текст научной статьи Динамика содержания аквапоринов плазмалеммы и тонопласта подсемейств PIP и TIP в ходе роста растяжением клеток колеоптилей проростков риса, различающихся скоростью роста в условиях нормоксии и затопления
На ранних этапах развития у злаков, многие из которых относятся к ценным сельскохозяйственным культурам, формируется особый ювенильный орган — колеоптиль. Он представляет собой модифицированный лист, функция которого заключается в защите от действия стрессовых факторов: изменения температуры, обезвоживания и даже негативного действия гербицидов (1, 2). Защитный эффект во многом определяется длиной колеоптиля. У риса посевного ( Oryza sativa L.), обладающего способностью прорастать в условиях недостатка кислорода (затопление), эта защитная функция приобретает новое значение: резкое ускорение роста колеоптиля обеспечивает возможность снабжения развивающегося проростка кислородом (3). Этот процесс рассматривают в рамках одной из стратегий адаптации растительных организмов к недостатку кислорода, известной как синдром «избегания» (low-oxygen escape syndrome, LOES) (4). Она свойственна разным видам гидрофитных растений (5). В ряде скрининговых исследований было продемонстрировано, что длина колеоптиля проростка риса положительно коррелирует с устойчивостью к недостатку кислорода (6, 7).
Механизмы, лежащие в основе первичных этапов роста клеток колеоптиля в аэробных условиях, описываются теорией кислого роста, предложенной более полувека назад (8, 9). Согласно ей, фитогормон ауксин активирует Н+-АТФазу плазмалеммы, что приводит к закислению клеточных стенок и активации механизмов, обеспечивающих рост клетки в длину (10). Логично предположить, что этот же механизм лежит и в основе роста клеток колеоптилей риса при затоплении. Тем не менее данные литературы по этой теме весьма ограничены (11). Отметим, что еще одной характерной особенностью роста растяжением служит интенсивная вакуолизация, опосредованная транспортом воды в вакуоль. Движущей силой этого потока Н 2 О становится осмотическое давления в вакуолярной системе (11, 12). Его величина определяется накоплением в вакуоли осмотически активных ионов и метаболитов, в том числе сахаров, амино- и органических кислот, ионов К+ и др.
Интенсивный транспорт воды через биологические мембраны осуществляется с участием трансмембранных белков аквапоринов (13, 14). К этой группе относят транспортеры, локализованные в плазмалемме (plasma membrane intrinsic proteins, PIP) и тонопласте (tonoplast intrinsic proteins, TIP) (14, 15). Накоплено достаточно много данных о роли аквапоринов в обеспечении роста различных органов растительного организма, а также при действии факторов, приводящих к обезвоживанию (11, 15). Однако данных об участии аквапоринов в обеспечении роста растяжением в норме и при недостатке кислорода не хватает для подтверждения их физиологической значимости в реализации этого процесса (11, 14, 15). Один из немногих примеров заключается в увеличении гидростатической проницаемости клеточных мембран при изменении экспрессии генов ZmPIPs и ZmTIPs на этапе прорастания (16).
Аквапорины относят к высококонсервативному семейству MIP (major intrinsic proteins). Они идентифицированы у всех живых организмов, кроме термофильных архей и ряда бактерий (15, 17), и представляют собой семейство мембранных транспортных белков, функционирующих как селективные каналы для транспорта воды, а также некоторых других молекул, в том числе газов (15, 18). У зеленых растений ( Viridiplantae Cavalier-Smith, 1981), 446
особенно у высших, аквапорины кодируются достаточно большими семействами генов. Полагают, что появление таких семейств в эволюции растений обусловлено необходимостью эффективно регулировать водный гомеостаз в изменяющихся условиях окружающей среды при прикрепленном образе жизни (17, 19). У риса насчитывается 33 гена, кодирующих аквапо-рины (16).
Результаты анализа экспрессии генов аквапоринов подсемейств PIP и TIP указывают на их участие в обеспечении роста осевых органов на разных этапах развития растительного организма, в том числе на этапе прорастания (15). Однако данные об участии в аквапоринов в обеспечении роста колеоптилей риса отсутствуют.
В настоящей работе впервые приведены данные, которые позволили выявить соответствие между изменением содержания аквапоринов плазмалеммы подсемейства PIP1 и интенсивностью роста растяжением клеток колеоптилей риса при прорастании как в условиях нормоксии, так и гипоксии.
Цель исследования состояла в оценке динамики представленности аквапоринов с преимущественной локализацией в плазмалемме и тонопласте в процессе роста растяжением клеток колеоптилей риса в условиях аэрации и дефицита кислорода.
Методика. В лабораторном эксперименте (2022-2024 годы) использовали семена двух сортов риса отечественной селекции — Аметист (медленно растущий) и Кубань 3 (быстро растущий) (7).
Семена поверхностно стерилизовали в течение 15 мин 50 % раствором гипохлорита натрия, 10 раз промывали стерильной водой и далее замачивали 1 ч в горячей воде (55 ° С). После этого семена (по 50 шт.) проращивали в гидропонных условиях в темноте при 29 ° С на стеклянных мостках (контрольные растения) или создавали условия затопления в банках объемом 750 мл (7, 20) с использованием 4 % питательного раствора Кнопа. Количество кислорода измеряли с помощью анализатора растворенного кислорода Эксперт-009 («Эконикс-Эксперт», Россия). Этот показатель в гипоксическом растворе не превышал 0,5-0,6 мг/л. Растворы и посуду для работы с растениями предварительно стерилизовали.
Для определения длины клеток колеоптили фиксировали в смеси этанол: формалин: ледяная уксусная кислота в соотношении 100:7:7, через 2 нед растительный материал отмывали 70 % этанолом и сохраняли при 4 °С. Для изготовления постоянных препаратов пробы обрабатывали с применением модифицированной стандартной цитологической схемы проводки через этанол/изопропанол. В качестве заменителя ксилола был использован реактив Bioclear («BIO-OPTICA Milano», Италия). После обезвоживания пробы заливали в блоки гомогенизированной парафиновой среды His-tomix («BioVitrum», Россия). Далее изготавливали срезы толщиной 20 мкм при помощи ротационного микротома Accu®-Cut™ SRM 200 («Sakura Fin-etek Europe», Нидерланды). Регидратирование и окрашивание проводили по модифицированной схеме через BioClear, изопропанол и этанол. После регидратации в 70 % этаноле срезы окрашивали 0,5 % раствором сафранина в 50 % этаноле (21). Окрашенные препараты заключали в поливиниловый спирт Mowiol («Sigma-Aldrich», США) по методике «Polysciences, Inc.» (США, .
Фотосъемку и исследование препаратов выполняли с помощью светового микроскопа Leica DM 2500 («Leica Microsystems GmbH», Германия) и фотокамеры Leica DFC450 C («Leica Microsystems GmbH», Германия) при увеличении ½20. Морфометрию клеток проводили на полученных изображениях при помощи пакета FIJI, версия 2.9.0 . В каждом варианте исследовали по 5 препаратов по 25 клеток на каждом.
Общую микросомальную фракцию получали из клеток колеоптилей проростков при температуре 4 ° С (22). Навеску растительного материала (1 г) гомогенизировали в среде, содержавшей 330 мМ сахарозы, 50 мМ Tris-HCl, 5 мМ EDTA, 5 мМ аскорбиновой кислоты, 5 мМ DTT (pH 7,8). Полученный гомогенат центрифугировали 10 мин при 100 g, далее скорость увеличивали до 3000 g (5 мин) и затем до 17000 g (15 мин, 4 ° С) (центрифуга MPW-350R, «MPW Med. Instruments», Польша). Осадок гомогенизировали в среде, содержащей 300 мМ раствор сахарозы на 10 мМ буфере Tris-Mes (pH 7,2). Супернатант центрифугировали 60 мин при 100 000 g (центрифуга Avanti J-30I, «Beckman Coulter», США). Осадок (общая микросомальная фракция, ОМФ) гомогенизировали в среде, содержавшей 300 мМ раствор сахарозы на 10 мМ буфере Tris-Mes (pH 7,2). Содержание белка в пробах определяли по микрометоду Брэдфорда (23) с использованием красителя Coumassie Brilliant Blue G250 («Sigma-Aldrich», США). Поглощение красителя, сорбированного на белках, определяли на планшетном спектрофотометре SPECTROstar Nano («BMG Labtech», Германия) при X = 595 нм. Концентрацию белка в пробах определяли на основе калибровочного графика, построенного с использованием раствора яичного альбумина на 150 мМ сахарозе и 10 мМ Tris-MES (pH 7,2).
Белки разделяли методом денатурирующего электрофореза в 10 % полиакриламидном геле (24). Перед нанесением на электрофорезные гели пробы выравнивали по содержанию белка. Белок из общей микросомальной фракции осаждали 20 % ТХУ и затем растворяли в загрузочном буфере. На дорожку геля наносили 20 мкг белка. Для контроля разделения белков на геле использовали маркеры молекулярной массы PageRuler™ Prestained Protein Ladder («Thermo Fisher Scientific», США). Электрофоретическое разделение белков проводили в буфере Tris-глицин (25 мМ Tris, 192 мМ глицин, 0,1 % SDS, pH 8,3) в системе Mini-PROTEAN («Bio-Rad», США) при 4 ° С по протоколу производителя.
Содержание аквапоринов PIP1 и TIP1 в составе общей микросомальной фракции клеток колеоптилей риса оценивали с помощью иммуноблоттинга. Для этого гели промывали трансфер-буфером и проводили блот-перенос на нитроцеллюлозную мембрану (0,45 мкм, «Bio-Rad», США) в системе Mini-PROTEAN («Bio-Rad», США) в течение 1 ч при 100 В и 250 мА по протоколу производителя. После переноса мембрану обрабатывали блокирующим буфером (1 ч) и в течение ночи инкубировали в этом буфере, содержащем первичные кроличьи антитела, специфичные для ак-вапоринов PIP1;1-5 (AS09 489, «Agrisera», Швеция) и TIP1;1-2 (AS09 493, «Agrisera», Швеция). После этого мембраны отмывали 5 раз по 5 мин в 25 мл блокирующего буфера. Вторичные поликлональные противокроличьи козьи антитела, меченные пероксидазой хрена (AS09 602, «Agrisera», Швеция) растворяли в 25 мл блокирующего буфера с добавлением молока. Мембрану, обрабатывали раствором с вторичными антителами при 37 °С в течение 1 ч на качалке. Затем мембраны промывали и проявляли с помощью 3,3-диаминбензидина, растворенного в фосфатно-солевом буфере (pH 5,8). Пероксидаза хрена вторичных антител окисляет диаминобензидин и вызывает его полимеризацию, в результате чего на мембране образуется окрашенный осадок (пятно). Мембрану сканировали, с помощью компьютерной программы PhotoM, версия 1.31 измеряли оптическую плотность и площадь пятен, соответствующих аквапоринам на нитроцеллюлозной мембране. Эти значения перемножали и использовали для полуколичественной оценки содержания аквапоринов.
Все эксперименты по иммуноидентификации проводили в 3-кратной биологической и 4-кратной аналитической повторностях. Статистическую обработку данных осуществляли с помощью GraphPad Prism 8.0.1 для Windows . На рисунках приведены средние значения величин (M) и их стандартные ошибки (±SEM). Значения, отмеченные разными буквами, статистически значимо различались при p < 0,05 (взвешенное среднее Тьюки).
Результаты. Ранее при анализе интенсивности роста сортов и линий риса из коллекции ФНЦ риса (г. Краснодар) были отобраны два контрастных по исходной скорости роста сорта — Кубань 3 (быстро растущий) и Аметист (медленно растущий) (7). Последующий анализ роста колеоптилей подтвердил сохранение этой закономерности и на этапе прорастания как в контрольных условиях, так и при гипоксии (20).
В настоящей работе при аэробном развитии длина клеток центральной зоны колеоптилей у сорта Кубань 3 увеличивалась почти в 2 раза и достигала максимума на 5-е сут, тогда как у сорта Аметист она увеличивалась не столь значительно (рис. 1).
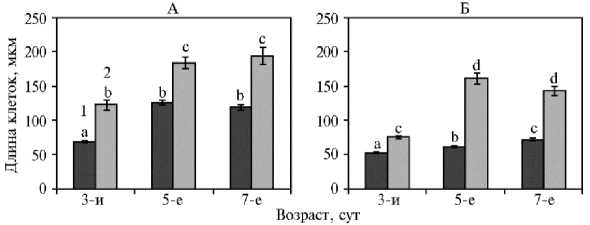
Рис. 1. Длина клеток центральной части колеоптилей у проростков риса ( Oryza sativa L.) сортов Кубань 3 (А) и Аметист (Б) в условиях нормоксии (1) и при затоплении (2) ( N = 5, n = 25, M ±SEM; лабораторный опыт) . Значения, отмеченные разными буквами (a-d), статистически значимо различаются (взвешенное среднее Тьюки, p < 0,05).
Изменение условий прорастания (снижение количества кислорода) приводило к значительному изменению длины клеток. В колеоптилях сорта Кубань 3 отмечали почти 2-кратное удлинение клеток уже на 3-и сут прорастания по сравнению с контролем. Более интенсивный рост при затоплении сохранялся до 7-х сут прорастания. У сорта Аметист на 3-и сут выявленные различия были не столь велики, как у сорта Кубань 3, однако к 5-м сут длина клеток увеличивалась почти в 3 раза. Ранее обусловленные сортовыми особенностями различия в интенсивности удлинения колеоптилей риса были показаны в нескольких работах (25, 26). Полагают, что длина колеоптиля коррелирует с устойчивостью сорта риса к затоплению. R. Narsai с соавт. (27) показали, что при прорастании зерновок риса деление клеток в колеоптилях в значительной степени прекращалось после 2,5-3 сут набухания, в результате чего их популяция насчитывала около 80 000 клеток при нормоксии и около 55 000 в условиях затопления (27). То есть через 3 сут после прорастания рост колеоптилей почти полностью зависит от удлинения клеток, а не от деления. В связи с этим расшифровка механизмов роста колеоптилей за счет растяжения клеток в условиях гипоксии приобретает особое значение.
Полученные данные указывают на существенное различие в интенсивности роста растяжением клеток колеоптилей у риса в норме и при затоплении. Реализация роста растяжением тесно сопряжена с вакуолизацией, а следовательно, с транспортом воды через плазмалемму и тонопласт.
Следующий этап нашей работы заключался в детектировании белков аквапоринов подсемейств PIP1 и TIP1 в мембранах клеток колеоптилей риса. В контрольных аэробных условиях наибольшим содержанием белка отличались мембраны клеток самых молодых из протестированных проростков (рис. 2). Причем содержание белка в клетках колеоптилей оказалось приблизительно равным как у быстро растущего, так и у медленно растущего сорта. Дальнейшее развитие проростка в условиях нормоксии приводило к существенному снижению количества белка в мембранной фракции на 5-е сут и небольшому добавочному снижению на 7-е сут (рис. 2, А).
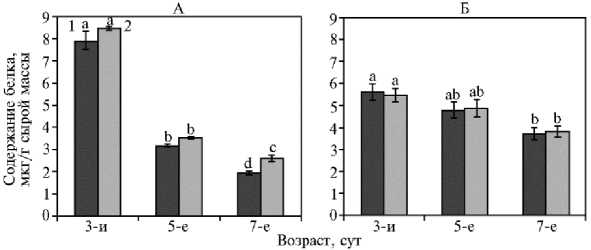
Рис. 2. Содержания белка в общей микросомальной фракции клеточных мембран, полученных из клеток колеоптилей проростков у риса ( Oryza sativa L.) сортов Кубань 3 (1) и Аметист (2) в условиях нормоксии (А) и при затоплении (Б) ( N = 3, n = 4, M ±SEM; лабораторный опыт) . Значения, отмеченные разными буквами (a-c), статистически значимо различаются (взвешенное среднее Тьюки, p < 0,05).
При развитии в условиях затопления содержание белка в клетках колеоптилей проростков обоих сортов было снижено более чем на 30 % по сравнению с контролем. Этот эффект отмечали как для сорта Кубань 3, так и для сорта Аметист (см. рис. 2, Б). Однако снижение содержания белка с возрастом при гипоксии происходило гораздо медленнее, чем при нор-моксии, и на 7-е сут даже достигало несколько больших значений, нежели в условиях нормоксии. Ранее было показано, что в условиях недостатка кислорода (гипоксия и аноксия) наблюдается общее снижение активности синтетических процессов, в том числе синтеза белка (28, 29). Тем не менее часть энергетических резервов клетки тратится на синтез индуцированных недостатком кислорода белков. В первую очередь это касается, например, ферментов альтернативных путей дыхания и метаболизма сахарозы (30-32). Для колеоптилей было продемонстрировано накопление ряда экспансинов (33). В ряде работ указывалось на возможную роль аквапоринов в процессе адаптации растений к затоплению. Однако в этих публикациях преимущественно анализировали роль аквапоринов корневой системы (14). Данные о роли аквапоринов в процессе роста растяжением клеток колеоптилей при недостатке кислорода практически отсутствуют.
В нашей работе идентификацию аквапоринов плазмалеммы и тонопласта проводили с использованием специфичных поликлональных антител, выработанных против аквапоринов подсемейства PIP1 с преимущественной локализацией на плазмалемме и подсемейства TIP1 с преимущественной локализацией на тонопласте.
На рисунке 3 представлены сканированные изображения блотов.
Антитела против TIP1 взаимодействовали с белками, обладающими молекулярной массой около 26 кДа. Эти антитела реактивны против аквапори-нов тонопласта TIP1;1 и TIP1;2. Антитела против PIP1 выявили две полосы белков с молекулярной массой 25 и 28 кДа. Вероятно, это связано с тем, что антитела взаимодействуют со всеми изоформами PIP1 белков — PIP1;1, 1;2, 1;3, 1;4 и 1;5. Полученные данные свидетельствуют об изменении содержания целевых белков в мембранах интереса (плазмалемма или тонопласт). Очевидно, что изменения происходили как в процессе развития проростков в нормальных условиях, так и при действии стрессового фактора — затопления. Причем эти изменения были неодинаковыми для белков PIP1 и TIP1.
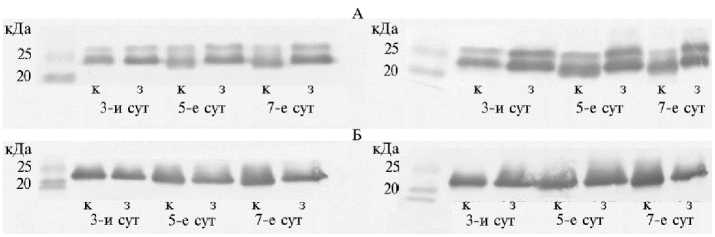
Рис. 3. Изображения иммуноблотов аквапоринов плазмалеммы (PIP1) (А) и тонопласта (TIP1) (Б) фракции мембран из колеоптилей проростков риса ( Oryza sativa L.) сортов Аметист (слева) и Кубань 3 (справа) в условиях нормоксии (к) и затопления (з) .
Цифровизация результатов, полученных с помощью иммуноблоттинга, позволила провести полуколичественный анализ этих изображений (рис. 4). Для аквапоринов PIP1 значения для пятен с массой 25 и 28 кДа на одной дорожке электрофореграммы суммировали.
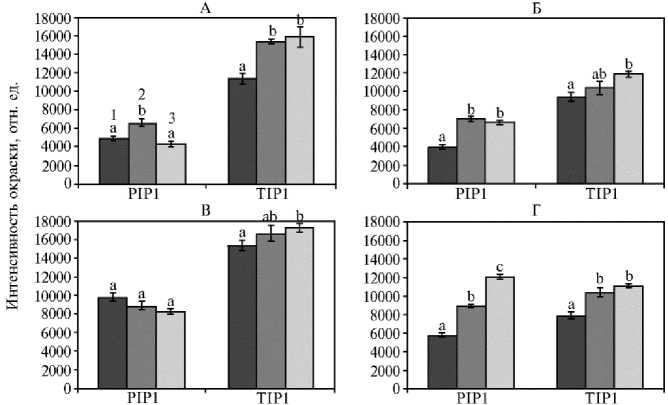
Рис. 4. Содержание аквапоринов PIP1 и TIP1 в общей микросомальной фракции мембран клеток колеоптилей у проростков риса ( Oryza sativa L.) сортов Кубань 3 (А, В) и Аметист (Б, Г) в условиях нормоксии (А, Б) и при затоплении (В, Г) на 3-и (1), 5-е (2) и 7-е сут (3) ( N = 3, n = 4, M ±SEM; лабораторный опыт) . Значения, отмеченные разными буквами (a-c), статистически значимо различаются (взвешенное среднее Тьюки, p < 0,05).
В контрольных условиях максимальное содержание аквапоринов, локализованных на плазмалемме, было детектировано на 5-е сут развития проростков независимо от сорта риса. Тем самым этап наиболее интенсивного удлинения клеток соответствовал максимальному накоплению аквапо-ринов плазмалеммы. Для сорта Кубань 3 наиболее ярко выявлялась нелинейность изменения содержания аквапоринов PIP1, что, по-видимому, связано с большей амплитудой активности роста, также отличающейся нелинейностью. Косвенным подтверждением роли аквапоринов PIP1 в развитии колеоптилей может служить экспрессия кодирующих их генов. Имеются лишь несколько исследований, выявивших экспрессию этих генов на самых ранних этапах развития у злаков. Так, было показано, что нокаутные мутанты риса по гену OsPIP1;3 характеризовались резким снижением скорости прорастания и, напротив, повышение экспрессии этого гена усиливало процесс прорастания, предшествующий развитию проростка (34). Экспрессия генов аквапоринов PIP1 была выявлена у колеоптилей проростков кукурузы (16). При выращивании проростков в условиях затопления уже на 3-и сут отмечали увеличение содержания белков PIP1 по сравнению с контролем для обоих протестированных сортов. В дальнейшем количество ак-вапоринов PIP1 в мембранах клеток у сорта Кубань 3 статистически значимо не менялось и было выше контрольных значений. В клетках проростков сорта Аметист наблюдали последовательное, фактически 2-кратное, увеличение содержания белка интереса в составе микросомальной фракции. Отметим, что для клеток колеоптилей сорта Аметист характерно значительное усиление роста по сравнению с таковым в нормоксических контрольных условиях. Можно заключить, что и в условиях недостатка кислорода изменение содержания белков PIP1 согласуется с изменением роста.
Отметим, что выявленные различия между сортами с неодинаковой скоростью роста — Кубань 3 и Аметист могут быть обусловлены активностью аквапоринов. Следует учитывать возможность посттрансляционной регуляции аквапоринов. Известно, что активность транспортеров меняется при снижении рН, при изменении уровня АФК и концентрации Са2+ (35, 36). Эти изменения были зарегистрированы при недостатке кислорода (37, 38). Следовательно, активность транспортеров может меняться без изменения их количества в составе клеточных мембран.
Что касается белков аквапоринов TIP1, то независимо от сорта и условий выращивания происходило постепенное увеличение их содержания на протяжении эксперимента. Можно предположить, что их накопление отражает активную вакуолизацию клеток как в норме, так и при действии затопления. Следует подчеркнуть, что большим накоплением TIP1 отличались микросомы из клеток колеоптилей проростков сорта Кубань 3. Как и в случае с аквапоринами PIP1 можно сослаться лишь на данные литературы о наличии экспрессии белков TIP1 в колеоптилях на ранних этапах прорастания проростков кукурузы (16).
Таким образом, детекция с помощью иммуноблоттинга позволила нам не только продемонстрировать динамику содержания аквапоринов мембран, но и выявить ее различия у представителей разных подсемейств.
К сожалению, даже при интенсивном развитии протеомного подхода данные о возможном нелинейном изменении содержания различных белков в процессе роста растяжением в нормоксических условиях практически отсутствуют. На микросомальной фракции из клеток этиолированных колеоптилей ржи было показано изменение всего для 8 белков, в том числе уменьшение содержание белка субъединицы В Н+-АТФазы тонопласта в процессе старения этого органа (39). Изменение содержания именно этой субъединицы протонной АТФазы тонопласта в зависимости от стадии развития колеоптиля было выявлено и на клетках проростков риса (40). Показано, что его максимальное содержание характерно для клеток на этапе интенсивного роста. В культуре клеток арабидопсиса удлинение клеток сопровождалось изменением содержания 392 белков (41). К числу накапливающихся белков были отнесены не только АТФаза Р-типа, но и ряд аквапо-ринов подсемейства PIP2.
Приведенные результаты получены на разных модельных объектах, разными методами, при разных условиях развития. В связи с этим их прямое сравнение с полученными нами данными невозможно. Тем не менее совокупно они указывают на возможность динамических изменений в белковых профилях мембран как плазмалеммы, так и тонопласта в процессе роста растяжением.
Особый интерес представляют выявленные нами различия в динамике аквапоринов разных подсемейств. Они обеспечивают различия в интенсивности потоков воды на границе внешняя среда/цитозоль и цито-золь/вакуоль при растяжении клетки и сопровождающей его вакуолизации. Показано, что в процессе развития колеоптиля в воздушной среде общее удлинение клеток заканчивается на 5-е сут, а процессы, связанные с ваку-олярной системой, еще продолжаются. В связи с этим, по-видимому, максимальное содержание отмечено для плазмалеммного PIP1 именно на 5-е сут, а последовательное накопление аквапоринов вакуолярного подсемейства TIP1 продолжалось до 7-х сут. В условиях затопления и рост, и вакуолизация продолжаются на 7-е сут, что может служить причиной линейного накопления обоих исследованных аквапоринов.
Целесообразно в дальнейшем провести детектирование аквапоринов не только с использованием общемикросомальной фракции, но и очищенных мембранных препаратов, особенно с последующим применением про-теомных технологий. Перспективным представляется анализ экспрессии генов, кодирующих белки аквапоринов PIP1 и TIP1 в клетках колеоптилей риса как при нормоксии, так и затоплении. Полученные данные позволят расширить представления о механизмах роста растяжением, которые могут представлять собой новые критерии повышения устойчивости к недостатку кислорода при создании новых сортов риса и других сельскохозяйственных культур (42, 43). Важность подобной задачи возрастает в связи расширением затопляемых площадей вследствие потепления климата. Кроме того, на основе выявления различий в интенсивности роста колеоптилей возможна разработка новых дешевых способов тестирования уже существующих коллекционных сортов отечественной и зарубежной селекции.
Итак, полученные нами данные еще раз продемонстрировали, что рост растяжением представляется комплексным этапом развития растительной клетки. Его динамика в контрольных условиях (нормоксия) носила нелинейный характер с максимумом на 5-е сут развития проростков риса. Она отличалась от таковой при действии стрессора — недостатка кислорода. Рост в условиях затопления продолжался до 7-х сут, что обусловливало выполнение физиологической роли колеоптиля — достижения воздушной среды. В процессе развития проростков наблюдалось постепенное старение колеоптилей по мере завершения их защитной функции. Этот процесс сопровождался снижением содержания общего белка в клеточных мембранах. Однако это снижение было не столь выраженным в гипоксических условиях, когда рост клеток еще продолжался. Проведенный анализ убедительно показал, что изменение содержания аквапоринов подсемейства PIP1 положительно согласуется с динамикой роста клеток колептилей риса в условиях нормоксии. Однако при недостатке кислорода (при затоплении), когда рост растяжением превращается в этап адаптационного развития, характер накопления белков менялся и не удалось выявить соответствия между динамикой роста клеток и накоплением аквапоринов плазмалеммы у обоих протестированных сортов, хотя в условиях гипоксии во все сроки наблюдения уровень аквапоринов PIP1 был повышен.


