Динамика уровня тропонина Т после радиочастотной абляции устьев легочных вен у больных с фибрилляцией предсердий
Автор: Линчак Р.М., Догадова Т.В., Свешников А.В., Вахромеева М.Н., Недбайкин А.М., Ким К.Ф., Трифонов С.И.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Статья в выпуске: 1 т.5, 2010 года.
Бесплатный доступ
Радиочастотная аблация (РЧА) устьев легочных вен - наиболее эффективный метод лечения больных с фибрилляцией предсердий - сопровождается повышением тропонинов крови в 100% наблюдений. У части пациентов после процедуры появляется болевой синдром в грудной клетке с чертами ангинозного приступа и изменения на ЭКГ, что требует проведения дифференциальной диагностики с инфарктом миокарда. В статье приводятся результаты детального анализа клинической картины, лабораторных и инструментальных данных, призванных ответить на данный вопрос.
Тропонин, фибрилляция предсердий, радиочастотная аблация
Короткий адрес: https://sciup.org/140187784
IDR: 140187784 | УДК: 616.141/12-008.313.2:615.849
Troponin elevations after radiofrequency catheter ablation pulmonary vein for atrial fibrillation
Characteristics of clinical, instrumental findings and troponin T dynamic in patients after radiofrequency ablation pulmonary vein for atrial fibrillation.
Текст научной статьи Динамика уровня тропонина Т после радиочастотной абляции устьев легочных вен у больных с фибрилляцией предсердий
К настоящему времени накоплено достаточно данных, показывающих, что повышение тропонинов (Тн) в крови – наиболее специфичных маркеров повреждения миокарда – определяется не только при инфаркте миокарда (ИМ), но и при целом ряде заболеваний и вмешательств, не связанных с ишемической болезнью сердца (ИБС) [14].
Как известно, тропониновый комплекс кардиомиоцита состоит из трех субъединиц – Тн I, Т и С [4, 13]. Последний представлен не только в кардиомиоцитах, но и в мышечных клетках других тканей, в силу чего не является кардиоспецифичным и не применяется для диагностики повреждения миокарда. В отличие от Тн С, тропонины T и I определяются исключительно в кардиомиоцитах, причем большая их часть находится в связанном виде с сократительным аппаратом клеток. Существует также цитозольный пул несвязанных Тн (около 6–8%), высвобождение которого обуславливает раннее повышение Тн в крови даже при обратимом повреждении мембраны кардиомиоцитов. Когда же повреждение становится необратимым, внутриклеточный ацидоз и активация протеолитических ферментов приводят к разрушению контрактильного аппарата с последующим высвобождением связанных с последним Тн [2, 5]. Специфичность сердечных Тн весьма высока и составляет 90–94% [1, 5, 6, 11].
Одной из причин повышения Тн в крови является возникновение «малых повреждений миокарда» при эндоваскулярных кардиохирургических вмешательствах, в частности, РЧА аритмогенных очагов [10, 11]. По данным литературных источников, изоляция устьев легочных вен, проводящаяся по поводу фибрилляции предсердий (ФП), сопровождается увеличением уровня Тн в 70–100% наблюдений [6–13, 15]. При этом степень подобного повышения превышает норму в 3–20 раз [6, 7, 9]. Некоторые авторы указывают на наличие ассоциации между степенью гипертропонинемии и количеством аппликаций, а также длительностью процедуры [7, 13], в то же время в других исследованиях подобной взаимосвязи не обнаружено [8, 11].
По данным литературных источников [8, 13], а также по нашим собственным наблюдениям, во многих случаях после РЧА у пациентов отмечается болевой синдром в грудной клетке, зачастую сопровождающийся динамикой сегмента ST-T на ЭКГ, что обуславливает актуальность дифференциальной диагностики, и в первую очередь, с ИМ.
Все это побудило нас к собственному исследованию, целью которого явилось изучение особенностей клинической картины, динамики лабораторных и инструментальных параметров у пациентов после РЧА устьев легочных вен, имеющих повышение уровня Тн Т в крови.
Материал и методы
Обследовано 66 пациентов (44 мужчины и 22 женщины, средний возраст 56,4±9,6 года) с фибрилляцией предсердий, перенесших оперативное вмешательство – РЧА устьев легочных вен. В качестве основного диагноза верифицировались гипертоническая болезнь, постмио-кардитический кардиосклероз, ИБС, а также идиопатические формы ФП.
В раннем послеоперационном периоде оценивалась клиническая картина, в которой особое внимание уделялось наличию и характеристикам болевого синдрома в грудной клетке (его характер, локализация, длительность, иррадиация, эффект от проводимой терапии).
Всем пациентам проводилось количественное исследование уровня кардиального Тн Т (аппарат Cardiac Reader, Roche) через 30–60 мин., 12–16 часов и на 5, 10 сутки после РЧА.
В этом же временном интервале регистрировали ЭКГ в 12 стандартных отведениях. Оценивали динамику сегмента ST (депрессия более 1 мм) и зубца Т (негативация более чем на 1 мм).
Выполняли эхокардиографическое (ЭхоКГ) исследование на аппарате VIVID 7 в М-, В-режимах при поступлении пациентов в стационар и через 12–24 часа после РЧА. Оценивали показатели глобальной и локальной сократительной способности миокарда в покое. Признаки утраты жизнеспособности миокарда по данным ЭхоКГ признаны одним из критериев инфаркта миокарда консенсусом ESC/ACC/AHA/WHF от 2007г. [14].
На 2–3 сутки после манипуляции выполняли сцинтиграфическое исследование миокарда левого желудочка (ЛЖ) с использованием радиофармпрепарата (РФП) «пирфотех», патологическая фиксация которого в настоящее время также признана одним из критериев острого очагового поражения миокарда (консенсус экспертов ESC/ACC/AHA/WHF, 2007).
Пациентам, имевшим упоминание об ИБС в анамнезе, а также 3 и более факторов риска ИБС, в предоперационном периоде выполняли коронароангиографию (КАГ).
Результаты исследования
При оценке клинической картины в ближайшем послеоперационном периоде отмечено появление боли в грудной клетке у 12 пациентов (18%), причем у 10 (15%) из них большинство характеристик болевого синдрома оказались весьма типичными для стенокардии.
Изучение концентрации Тн Т у обследованных больных до оперативного вмешательства не выявило отклонений от нормы ни в одном наблюдении. Однако уже через 30–60 мин. после РЧА в крови всех больных отмечено повышение концентрации Тн, при этом средний уровень Тн Т составил 0,69±0,3 нг\мл (рис. 1). Через 12–16 часов концентрация Тн Т в крови достигала максимума повышения – 0,75±0,6нг\мл – и в последующем постепенно снижалась. К 5-м суткам после операции средний уровень Тн Т составил 0,22±0,15 нг\мл. И к этому времени у 30 больных (45%) отмечена нормализация концентрации Тн Т. На 10-е сутки исследования только у 2 пациентов (3%) сохранялась гипертропонинемия, средний уровень которой составил 0,04±0,01нг\мл.
Анализ данных ЭКГ в послеоперационном периоде выявил динамику сегмента ST и/или зубца Т у 11 пациентов (17%). В подавляющем большинстве наблюдений изменения проявлялись в виде уменьшения амплитуды зубца Т или его негативации в грудных отведениях V2-V6 (рис. 2). У некоторых больных помимо изменений зубца Т регистрировалось появление депрессии сегмента ST до 1,0–1,5 мм в тех же отведениях. При этом у 7 пациентов (11%) отсутствовали признаки атеросклеротического поражения коронарных артерий по данным коронароан-
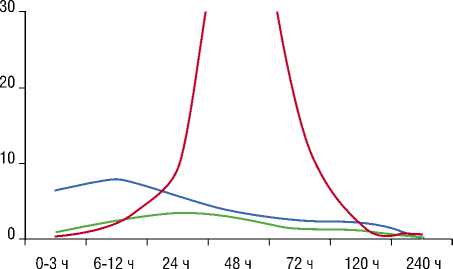
---РЧА — non-Q-l/IM ---Q-ИМ
Рис. 1. Динамика концентрации Тн Т в крови у пациентов, перенесших РЧА, и у пациентов с ИМ (адаптировано из ESC Clinical Practice Guidelines, 2007)
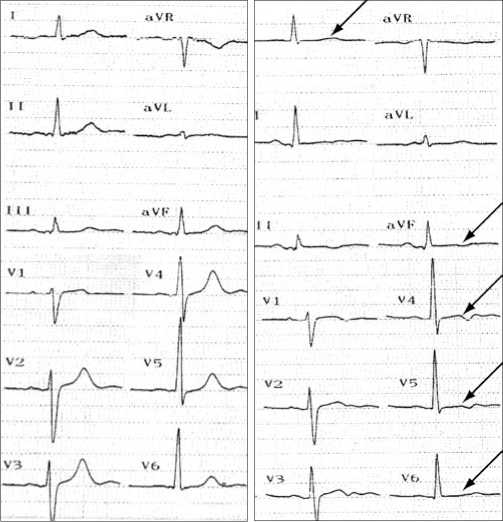
Рис. 2. ЭКГ пациента Д., 52 лет с фибрилляцией предсердий: А. – до РЧА; Б. – появление сглаженных и слабоотрицательных зубцов Т в отведениях V2–V6 (указано стрелками)
гиографии. Вышеописанные изменения ЭКГ сохранялись на протяжение от 3 суток до нескольких месяцев.
По данным ЭхоКГ как исходно, так и в послеоперационном периоде, ни у одного из обследованных пациентов не выявлялось признаков нарушения локальной сократительной способности миокарда ЛЖ.
При сцинтиграфии миокарда ЛЖ у 64 пациентов (97%) не было установлено патологического накопления РФП «пирфотех» в проекции ЛЖ, что исключало острый некроз. У 1 пациента (1,5%) отмечалось диффузное накопление РФП в области ЛЖ при отсутствии очаговой фиксации, что трактовалось нами как проявление хронической ишемии. При КАГ у этого больного верифици- ровалось двухсосудистое атеросклеротическое поражение венечных артерий (стенозы более 50%).
Всем пациентам, имевшим упоминание об ИБС в анамнезе (24 больных, 36%) и/или более 3 факторов риска ИБС (11 больных, 17%), выполняли КАГ. По результатам исследования у 4 пациентов (6%) верифицировано атеросклеротическое поражение коронарных артерий: у 3 (4,5%) – гемодинамически незначимые (до 50%) стенозы; у 2 (3%) – стенозы более 50%.
Обсуждение результатов
Повышение Тн Т и/или I в крови регистрируется при некрозе всего лишь 1 г сердечной мышцы, что обусловливает чрезвычайно высокую (до 98–98%) чувствительность гипертропонинемии в диагностике повреждений миокарда [4]. Однако факт увеличения концентрации Тн не является абсолютным свидетельством ИМ и может определяться при целом ряде других патологических состояний, как связанных, так и не связанных с поражением сердечной мышцы [14]. Это определяет значимо меньшую (до 90–94%) диагностическую специфичность повышения Тн [2, 4, 5].
Одной из причин увеличения тропонинов вне связи с ИБС является РЧА аритмогенного очага, в частности, устьев легочных вен, проводящаяся у пациентов с пароксизмаль-но-персистирующей формой ФП. Литературные данные, посвященные изучению этого вопроса, к настоящему времени весьма немногочисленны. Большинство авторов свидетельствуют о высокой частоте выявления гипертро-понинемии (70–100%) у подобного контингента больных [6–13], при этом степень повышения Тн превышает норму в 3–20 раз [6, 7, 9]. Мы получили сходные данные – гипер-тропонинемия выявлялась нами в 100% наблюдений после РЧА, а средний максимум повышения Тн Т превысил 99-й перцентиль верхнего референсного уровня в 7,5 раз.
Следует отметить, что в изученной нами литературе исследование динамики Тн в крови проводилось только лишь в течение первых 24 часов после вмешательства [7–10]. Нами прослежена динамика активности Тн Т в крови на протяжение 10 суток после РЧА, что позволило произвести сравнительный анализ с таковой при остром ИМ, как с Q-зубцом, так без Q-зубца на ЭКГ (рис. 1). Интересно, что в отличие от ИМ, повышение уровня Тн Т в крови регистрировалось в более ранние сроки – уже через 30-60 минут после завершения РЧА. Пик концентрации Тн Т в крови достигался к 12 часам послеоперационного периода и превышал норму в 7,5 раз, тогда как для Q-ИМ характерно более позднее достижение пика концентрации – через 24 часа – и более значимая пиковая концентрация Тн Т – до 50 норм. При не-Q ИМ повышение уровня Тн Т в крови наступает также в более поздние, чем при РЧА, сроки; максимум такого повышения регистрируется через 24–36 часов и степень гиперферментемии не превышает 3–4 норм.
У каждого шестого обследованного нами пациента в послеоперационном периоде регистрировался болевой синдром, характерный для ИБС (с локализацией в области грудины или слева от нее, давящего или жгучего характера, с иррадиацией в межлопаточную область). Однако следует отметить, что в большинстве случаев нитропрепараты, в отличие от ненаркотических анальгетиков, не оказывали купирующего эффекта. У 2 пациентов также наблюдался болевой синдром в грудной клетке, однако его характер не имел схожих черт с типичным ангинозным приступом (точечные колющие боли в области IV межреберья, усиливающиеся при движениях, вдохе). Таким образом, частота возникновения кардиалгии у больных после РЧА весьма высока, и в большинстве случаев характер боли имеет схожие с ангинозным синдромом характеристики. Этот факт обусловливает актуальность дифференциальной диагностики гипертропонинемии, в первую очередь, с ИМ, особенно у тех лиц, в анамнезе которых прослеживается упоминание об ИБС.
В нашем исследовании установлено появление динамики на ЭКГ ишемического характера у каждого шестого пациента. В большинстве наблюдений изменения ST-T верифицировались у больных с болевым синдромом в грудной клетке после РЧА. A.S. Manolis и соавт. (1999) удавалось обнаруживать нарушения процессов реполяризации после РЧА лишь у больных с синдромом предвоз-буждения желудочков, которые трактовались авторами как «феномен сердечной памяти».
С целью исключения острого повреждения миокарда ЛЖ выполняли ЭхоКГ и сцинтиграфию миокарда с РФП «пирфотех». Основа последнего исследования заключается в формировании прочных соединений фосфата и кальция, избыток которого появляется при остром некрозе миокарда [3]. У всех обследованных нами пациентов в послеоперационном периоде не обнаруживалось нарушений локальной сократимости миокарда и зон патологической фиксации «пирфотеха», что свидетельствовало об отсутствии очагового повреждения миокарда ЛЖ. Сходные данные приводят и другие авторы [10, 11, 13]. Лишь у одного пациента по результатам сцинтиграфии миокарда верифицировалось диффузное накопление РФП по всему миокарду ЛЖ. У данного больного не наблюдалось болевого синдрома в грудной клетке, динамики на ЭКГ и нарушений локальной сократимости миокарда ЛЖ. Некоторые литературные источники объясняют подобные сцинтиграфические признаки явлением хронической ишемии миокарда, сопровождающейся образованием диссеминированных мелкоточечных некрозов [3]. В пользу этого предположения свидетельствуют также и данные КАГ, выявившей у данного больного двухсосудистое поражение коронарного русла (гемодинамически значимые стенозы правой коронарной артерии до 85% и передней межжелудочковой артерии до 75%). Следует также отметить, что в доступной литературе мы не обнаружили работ, в которых описывались бы результаты сцинтиграфии миокарда у больных с гипертро-понинемией после РЧА устьев легочных вен.
По данным КАГ, выполненной пациентам с болевым синдромом в грудной клетке и динамикой на ЭКГ, у всех обследованных лиц, кроме одного, отсутствовали призна- ки гемодинамически значимого коронарного атеросклероза, что, в совокупности с данными ЭхоКГ и сцинтиграфии миокарда, позволило исключить связь гипертропонине-мии с острым очаговым поражением миокарда ЛЖ. Лишь у одной больной из вышеописанной группы по данным КАГ обнаружена осложненная атеросклеротическая бляшка в проксимальной трети передней нисходящей коронарной артерии, формирующая критический стеноз просвета сосуда до 98%. Вместе с тем, по данным ЭхоКГ и сцинтиграфии миокарда у этой пациентки, признаков нарушения жизнеспособности миокарда не было выявлено. Несмотря на это, состояние было расценено как острый ИМ, и произведено экстренное чрескожное коронарное вмешательство – стентирование передней нисходящей коронарной артерии. Возможно, такой диссонанс между результатами КАГ и неинвазивных визуализирующих методик объясняется различной чувствительностью методов. Известно, что очаги патологической фиксации РФП при сцинтиграфии миокарда появляются лишь при некрозе более 10 г миокарда, а локальное нарушение кинетики ЛЖ – при потере более 20% жесткости ЛЖ [2, 4].
Таким образом, результаты собственного исследования позволяют нам сделать вывод о том, что в подавляющем большинстве случаев гипертропонинемия после РЧА устьев легочных вен ассоциирована с появлением множественных мелкоочаговых некрозов миокарда левого предсердия в местах РЧА. К подобным выводам приходят и другие авторы [10, 11]. Вместе с тем, мы полагаем, что пациентам с отягощенным ишемическим анамнезом и/или с наличием более 3 факторов риска сердечно-сосудистых осложнений в предоперационном периоде следует выполнять КАГ для оценки состояния коронарного русла. ИМ верифицирован нами лишь у 1 больной (1,5%), однако и в этом случае при наличии большинства критериев ИМ (повышение Тн, болевой синдром, динамика на ЭКГ, ангиографические признаки осложненной гемодинамически значимой атеросклеротической бляшки в коронарной артерии) некоторые признаки этого заболевания (потеря жизнеспособного миокарда по данным ЭхоКГ и сцинтиграфии миокарда с «пирфотехом») отсутствовали. Все это свидетельствует о необходимости продолжения подобных работ и накопления клинического материала.
Выводы
-
1. Повышение уровня ТнТ в крови у больных с фибрилляцией предсердий, перенесших РЧА, регистрируется в 100% случаев. В отличие от инфаркта миокарда повышение концентрации ТнТ наблюдается уже через 30–60 минут после РЧА, достигает пика раньше – к 12 часам после операции и сохраняется повышенной на протяжении менее длительного, чем при ИМ, срока. Максимальная степень повышения ТнТ после РЧА превышает норму в 7,5 раз, что больше, чем у больных с non-Q ИМ и меньше – чем у пациентов с Q-ИМ.
-
2. Болевой синдром в грудной клетке в раннем послеоперационном периоде после РЧА устьев легочных
-
3. Изменения на ЭКГ ишемического характера (депрессия сегмента ST более 1 мм и негативация зубца Т более чем на 1 мм) в послеоперационном периоде выявляются у каждого шестого пациента. При этом признаки утраты жизнеспособности миокарда ЛЖ по данным ЭхоКГ и сцинтиграфии миокарда не зафиксированы ни у одного из обследованных пациентов.
-
4. Гипертропонинемия у больных после РЧА устьев легочных вен в подавляющем большинстве наблюдений ассоциирована с множественными очагами повреждения миокарда левого предсердия, образующимися во время процедуры. Частота ИМ после РЧА невысока, его диагностика весьма сложна и требует применения всего комплекса диагностических процедур, включая КАГ.
вен отмечается у каждого пятого пациента, при этом у каждого шестого больного большинство характеристик боли соответствуют ангинозному приступу.
Список литературы Динамика уровня тропонина Т после радиочастотной абляции устьев легочных вен у больных с фибрилляцией предсердий
- Егорова М.О., Золотухина Е.З., Теряева Н.Б. и др. Характер изменения маркеров повреждения миокарда при процедуре радиочастотной абляции у больных с аритмиями//Биохимия. -2002. -№20. -С. 3-5.
- Черепахина А.Д., Рудакова Т.Л. Сравнительная характеристика тропонина Т и I в диагностике инфаркта миокарда и других форм повреждения миокарда//Ученые записки СПБГМУ им. Акад. И.П. Павлова. -2001. -Т. 8, №2. -С. 18-20.
- Чернов, В.С. Сцинтиграфия миокарда в ядерной кардиологии/В.С. Чернов, Ю.Б. Лишманов. -Т.: Издательство Томского Университета, 1997. -267 с.
- Шалаев, С.В. Тропонины в кардиологической практике: пособие для врачей/С.В. Шалаев, Е.С. Петрик, А.В. Панин. -М.: МЗ РФ, 2001. -24 с.
- Bednarek J., Tomala I., Majewski J. Biochemiczne wskazniki uszkodzenia mi^snia sercowego po ablacji RF.//Kardiol. Pol. -2004. -60. Р. 339-341.
- Beukema W.P., Elvan A., Sie H.T. Successful Radiofrequency Ablation in Patients With Previous Atrial Fibrillation Results in a Significant Decrease in Left Atrial Size.//Circulation. -2005. -112. Р. 2089-2095.
- Haegeli L.M., Kotschet E., Byrne J. Cardiac injury after percutaneous catheter ablation for atrial fibrillation.//Europace. -2008. -10. Р. 273-275.
- Katritsis D., Hossein-Nia M., Anastasakis A. et al. Use of troponin-T concentration and kinase isoforms for quantitation of myocardial injury induced by radiofrequency catheter ablation.//European Heart Journal. -1997. -18(6). Р. 1007-1013.
- Katritsis D.G., Hossein N.M., Anastasakin A. et al. Miocardial injury induced by radiofrequency and low energy ablation: a quantitative study of CK isoforme, CK-MB and troponin T concentrations.//PACE. -1998. -21. Р. 1406-1410.
- Madrid A.H., del Rey J.M., Rubi J. et al. Biochemical markers and cardiac troponin I release after radiofrequency catheter ablation: approach to size of necrosis.//Am. Heart J. -1998. -136. Р. 948-955.
- Manolis A. S., Vassilikos V., Maounis T. et al. Detection of myocardial injury during radiofrequency catheter ablation by measuring serum cardiac troponin I levels: procedural correlates.//J. Am. Coll. Cardiol. 1999. -34. Р 1099.
- Shilkin A., Danilo J.P. et. al. The evolution and resolution of long-term cardiac memory.//Circulation. 1998. -97. Р. 1810.
- Shyu K.G., Lin J.N., Chen J.J. et. al. Use troponin T, creatine kinase and its isoform to monitor myocardial injury during radiofrequency ablation for supraventricular arrhythmia.//Cardiology. 1996. -87. -Р. 392-395.
- Thygesen K., Alpert J.S., White H.D. et al. On behalf of the Joint ESC/ACC/AHA/WHF. Task Force for the Redefinition of Myocardial Infarction.//Eur. Heart J. -2007. -28 (20). -Р. 25-38.


