Дисперсия реполяризации как предиктор жизнеугрожающих желудочковых аритмий при экспериментальном сахарном диабете малого стажа
Автор: Е.Н. Седякина, А.С. Цветкова, А.В. Дуркина, М.А. Гонотков, Я.Э. Азаров, А.О. Овечкин
Журнал: Ульяновский медико-биологический журнал @medbio-ulsu
Рубрика: Биологические науки
Статья в выпуске: 4, 2024 года.
Бесплатный доступ
Сахарный диабет (СД) является хорошо известным фактором риска сердечно-сосудистых заболеваний (ССЗ) и сам по себе может вызывать нарушение метаболизма миокарда, окислительный стресс, воспаление, апоптоз кардиомиоцитов, структурное ремоделирование, желудочковую дисфункцию и летальные аритмии. Цель. Поиск модели сахарного диабета, при которой увеличивается частота индуцируемых ишемией/реперфузией миокарда желудочковых аритмий, а также изучение электрофизиологических свойств миокарда желудочков в найденных моделях СД. Материалы и методы. Исследование проведено на 32 крысах с неконтролируемым стрептозото-циновым СД длительностью 4 нед. (малый стаж) и 8 нед. Контрольную группу составили 23 крысы. При эпикардиальном картировании измеряли параметры деполяризации и реполяризации, а также дисперсию реполяризации миокарда желудочков. Ишемию и реперфузию миокарда левого желудочка вызывали перевязкой коронарной артерии с целью провокации желудочковой тахикардии и/или фибрилляции желудочков (ЖТ/ФЖ). Результаты. Продолжительность реполяризации была значительно выше в обеих группах крыс с диабетом по сравнению с контролем, но дисперсия реполяризации отличалась от контроля только в группе с сахарным диабетом продолжительностью 4 нед. В этой же группе реперфузи-онные желудочковые аритмии развивались значимо чаще по сравнению с группой со стажем диабета 8 нед. Выводы. Частота развития реперфузионной ЖТ/ФЖ была выше у крыс с СД длительностью 4 нед., что, возможно, связано с большей дисперсией длительности реполяризации миокарда левого желудочка в этой группе.
Сахарный диабет, реполяризация, желудочковые аритмии, реперфузия
Короткий адрес: https://sciup.org/14132312
IDR: 14132312 | DOI: 10.34014/2227-1848-2024-4-133-143
Repolarization dispersion as a predictor for life-threatening ventricular arrhythmias in short-term experimental diabetes mellitus
Diabetes mellitus (DM) is a well-known risk factor for cardiovascular diseases (CVDs). It can cause myocardial metabolic dysfunction, oxidative stress, inflammation, cardiomyocyte apoptosis, structural re-modeling, ventricular dysfunction and lethal arrhythmias. The aim of this study was to find a model for diabetes mellitus increasing the frequency of ventricular arrhythmias induced by myocardial ischemia/reperfusion and to study the electrophysiological properties of the ventricular myocardium in the obtained models. Materials and Methods. The study was conducted on 32 rats with uncontrolled streptozotocin-induced diabetes mellitus lasting 4 (short-term) and 8 (long-term) weeks. The control group consisted of 23 rats. During epicardial mapping, depolarization and repolarization parameters, and ventricular myocardial repolarization dispersion were measured. Left ventricular myocardial ischemia and reperfusion were caused by coronary artery ligation to provoke ventricular tachycardia and/or ventricular fibrillation. Results. The repolarization duration was significantly higher in both groups of rats with diabetes mellitus compared to the control. However, the repolarization dispersion differed from the control only in the group with short-term diabetes mellitus (4 weeks). In this group, reperfusion ventricular arrhythmias developed significantly more often compared with the group with long-term diabetes mellitus (8 weeks). Conclusions: The incidence of reperfusion-induced ventricular tachycardia and/or ventricular fibrillation was higher in rats with short-term diabetes mellitus (4 weeks). It may be due to greater dispersion of left ventricular myocardial repolarization in this group.
Текст научной статьи Дисперсия реполяризации как предиктор жизнеугрожающих желудочковых аритмий при экспериментальном сахарном диабете малого стажа
Введение. Сахарный диабет (СД) является хорошо известным фактором риска сердечно-сосудистых заболеваний (ССЗ) и сам по себе может вызывать нарушение метаболизма миокарда, окислительный стресс, воспаление, апоптоз кардиомиоцитов, структурное ремоделирование, желудочковую дисфункцию и летальные аритмии. Эти изменения в совокупности составляют концепцию диабетической кардиомиопатии (ДКМП) [1, 2]. ДКМП является причиной более высокого риска внезапной сердечной смерти у лиц с сердечно-сосудисты1ми заболеваниями по сравнению с лицами без СД [3, 4]. Несмотря на то что желудочковые аритмии при СД, включая желудочковую тахикардию и фибрилляцию желудочков (ЖТ/ФЖ), являются результатом раз-личны1х сердечно-сосудистых патологий, электрическое ремоделирование вследствие ДКМП вносит большой вклад в аритмогенез [5, 6].
Удлинение фазы реполяризации потенциалов действия в желудочковых кардиомиоцитах можно рассматривать как явление, приводящее к развитию либо re-entry либо ранней постдеполяризации в диабетическом сердце [6, 7]. Это происходит в результате сочетания изменений токов K+, Na+ и Ca2+ при диабете [5, 8–10].
Несмотря на имеющиеся успехи в изучении электрического ремоделирования при диабетической кардиомиопатии [9–13] результаты экспериментальных исследований по воспроизведению желудочковых аритмий у животных остаются противоречивыми. Имеются сообщения о безуспешных попытках разработать модель с высоким уровнем аритмического исхода у животных с индуцированным СД [14, 15]. Возможными причинами такой устойчивости к развитию желудочковых аритмий называют диабетическое прекондиционирование миокарда желудочков к влиянию ишемии/ре-перфузии [14] или выраженное повреждение миокарда в экспериментах с продолжительным (более месяца) некорригируемым СД.
Цель исследования. Поиск модели СД, при которой увеличивается частота индуцируемых ишемией/реперфузией миокарда желудочковых аритмий, а также изучение электрофизиологических свойств миокарда желудочков у крыс с разным стажем экспериментального СД.
Материалы и методы. Экспериментальная модель. Эксперименты проведены на 55 крысах-самцах линии «Вистар» (возраст 6– 10 нед.). Исследование выполнено в соответствии с Руководством по уходу и использованию лабораторных животных (8-е издание, National Academies Press (США), 2011 г.) и принципами Директивы 2010/63/EU Европейского парламента о защите животных, используемых в научных целях, и одобрено этическим комитетом Института физиологии Коми научного центра Уральского отделения РАН. У 32 крыс СД индуцировали однократной внутривенной инъекцией стрептозотоцина (60 мг/кг массы тела), растворенного в холодном цитратном буфере (pH 4). Концентрацию глюкозы в венозной плазме измеряли сначала через 24 ч после инъекции, затем один раз в неделю с помощью глюкометра OneTouch (LifeScan, Швейцария). Контрольную группу составили 23 самца того же возраста. Всех животных содержали в стандартных лабораторных клетках и кормили стандартным кормом при постоянном доступе к пище и воде. В дальнейшем крысы с СД были разделены на
2 группы в зависимости от длительности диабета: СД короткий (16 крыс с малым стажем диабета – 4 нед.) и СД длительный (16 крыс с длительностью СД 8 нед.).
Электрофизиология. Запись ЭКГ-отведений от конечностей (КТ-07-3/12, «ИНКАРТ», Санкт-Петербург, Россия) осуществлялась с частотой 1028 Гц, динамическим диапазоном ±310 мВ. Компьютерные измерения длительности комплекса QRS, RR, QT и Tpeak-Tend (от самого раннего Tpeak до самого позднего Tend в отведениях от конечностей) проводились на записанных в цифровом формате ЭКГ.
Запись униполярных электрограмм с поверхности эпикарда проводилась у крыс после анестезии внутримышечной инъекцией тела-зола (15 мг/кг массы тела, Zoetis Manufacturing & Research Spain, S.L., Ctra. de Camprodon, s/n., Finca La Riba, Vall de Bianya, 17813, Же-рона, Испания). Животных интубировали, затем им проводили механическую вентиляцию легких и выполняли срединную торакотомию. Температуру сердца поддерживали на уровне 37–38 °С путем орошения теплым физиологическим раствором и подогрева окружающего воздуха. Униполярные электрограммы регистрировались с поверхности эпикарда правого и левого желудочков с использованием квадратной матрицы из 64 электродов (8×8 отведений, межэлектродное расстояние 0,5 мм) с помощью специально разработанной 128-канальной системы записи (16 бит; полоса пропускания 0,05–1000 Гц; частота 4000 Гц). В каждом эпикардиальном отведении время активации (AT) и время реполяризации (RT) определяли как минимум dV/dt во время комплекса QRS и максимум dV/dt во время зубца T соответственно по отношению к началу комплекса QRS. В качестве продолжительности потенциала действия рассчитывали интервал активации-реполяризации (ARI) – разницу между RT и AT. В анализе использовалась средняя длительность ARI по всем отведениям. За дисперсию реполяризации (DOR), являющуюся предиктором односторонней блокады проведения, принимали разницу между максимальным и минимальным значениями RT. После записи электрограмм в исходном состоянии левую переднюю нисходящую коронарную артерию лигировали для развития ишемии в течение 5 мин, после чего следовал 5-минутный период реперфузии, обеспечиваемый ослаблением лигатуры. Анализировали частоту возникновения эпизодов желудочковой тахикардии и/или фибрилляции желудочков (ЖТ/ФЖ), индуцированных ишемией и/или реперфузией.
Скорость проведения (CV) измеряли с помощью изохронных карт активации при электростимуляции (400 уд./мин, 2 мА, 2 мс) свободных стенок левого и правого желудочков. CV рассчитывали как расстояние, пройденное через матрицу (в продольном направлении (CVL) и в поперечном (CVT)), деленное на разницу между временем активации в месте стимуляции и самым ранним временем активации на противоположной стороне матрицы.
Исследование длительности потенциала действия (ПД) кардиомиоцитов. Выделение кардиомиоцитов проводили у 16 крыс из группы СД малого стажа, 12 крыс из группы СД длительного стажа и 13 контрольных крыс. После электрофизиологического картирования перед изъятием сердца внутрибрюшинно вводился гепарин (5000 МЕ/мл), разведенный в 0,9 % NaCl. Изолированное сердце промывали в течение 10 мин ретроградной перфузией через аорту по системе Лангендорфа аэрированным (95 % O2, 5 % CO2) и модифицированным бескальциевым раствором Тироде следующего состава (мМ): 125 NaCl, 4 KCl, 1,7 NaH2PO4, 25,2 NaHCO3, 0,55 MgCl2, 4,9 пирувата натрия, 20.5 таурина, 11.11 ммоль/л глюкозы и 1 мг/мл бычьего сывороточного альбумина; рН 7,4, 37 °С. Затем перфузию осуществляли раствором Tироде того же состава с добавлением коллагеназы II типа (0,6 мг/мл, Sigma Aldrich, США), протеазы (0,06 мг/мл, Sigma Aldrich, США) и 10 мкМ CaCl2 в течение 30–35 мин для выделения желудочковых кардиомиоцитов. По окончании ферментативной перфузии желудочки разрезали на мелкие кусочки. Клетки отделяли от кусочков фильтрованием через сетку с порами (200 мкм) в растворе Kraft-Brühe, содержащем (мМ): 30 KCl, 50 глутаминовой кислоты,
30 KH2PO4•2H2O, 3 MgSO4•7H2O, 0,5 EGTA, 10 глюкозы, 20 таурина и 20 HEPES; рН 7,2.
Регистрацию записи мембранного потенциала проводили методом patch-clamp в режиме current-clamp при температуре 22–24 °C с помощью Axopatch 200B (Axon Instrument). Желудочковые кардиомиоциты помещали в экспериментальную камеру RC26 (Warner Instrument Corp.). Пипетки изготавливали из боросиликатного стекла (Sutter Instruments) в пуллере HEKA типа PIP 6 (HEKA Electronics).
Для регистрации использовали стандартные растворы: внешний – NaCl 150; KCl 5,4; MgCl2 1,2; HEPES 5; CaCl2 1,8 (pH 7,4, 24 °С, доводили с помощью 5М раствора NaOH); пипеточный – KCl 140; MgCl2 1; EGTA 5; HEPES 10; MgАТФ 4; Na2ГТФ 0,03 (рН 7,2, 24 °С, доводили с помощью 5М раствора KOH).
Статистический анализ. Для статистического анализа использовались IBM SPSS Statistics версии 23.0 и GraphPad Prism 8.0.1 (GraphPad Software, Бостон, Массачусетс, США). Данные представлены в виде медиан и интерквартильных интервалов (IQR). Непараметрические критерии сравнения использовались в связи с отсутствием нормального распределения данных. Тест Крускала – Уоллиса использовался для сравнения контрольной группы, групп короткого и длительного СД. Далее для попарного сравнения использовался U-критерий Манна – Уитни. Частоту реперфузионных аритмий в группах контроля и СД сравнивали, используя точный критерий Фишера. Статистически различия считались значимыми при р<0,05.
Результаты. Как и ожидалось, у крыс с СД уровень глюкозы в плазме венозной крови был выше, чем у контрольных. Так, в контрольной группе показатель гликемии натощак составил 5,7 (IQR 5,3–6,5) ммоль/л против 31,4 (IQR 20,5–33,3) ммоль/л в группе короткого СД и 31,0 (IQR 25,9–33,1) ммоль/л в группе длительного СД (р<0,001 в обоих сравнениях).
На ЭКГ у крыс с сахарным диабетом наблюдалось значимое увеличение интервала RR, длительности QТ и интервала Tpeak-Tend (рис. 1).
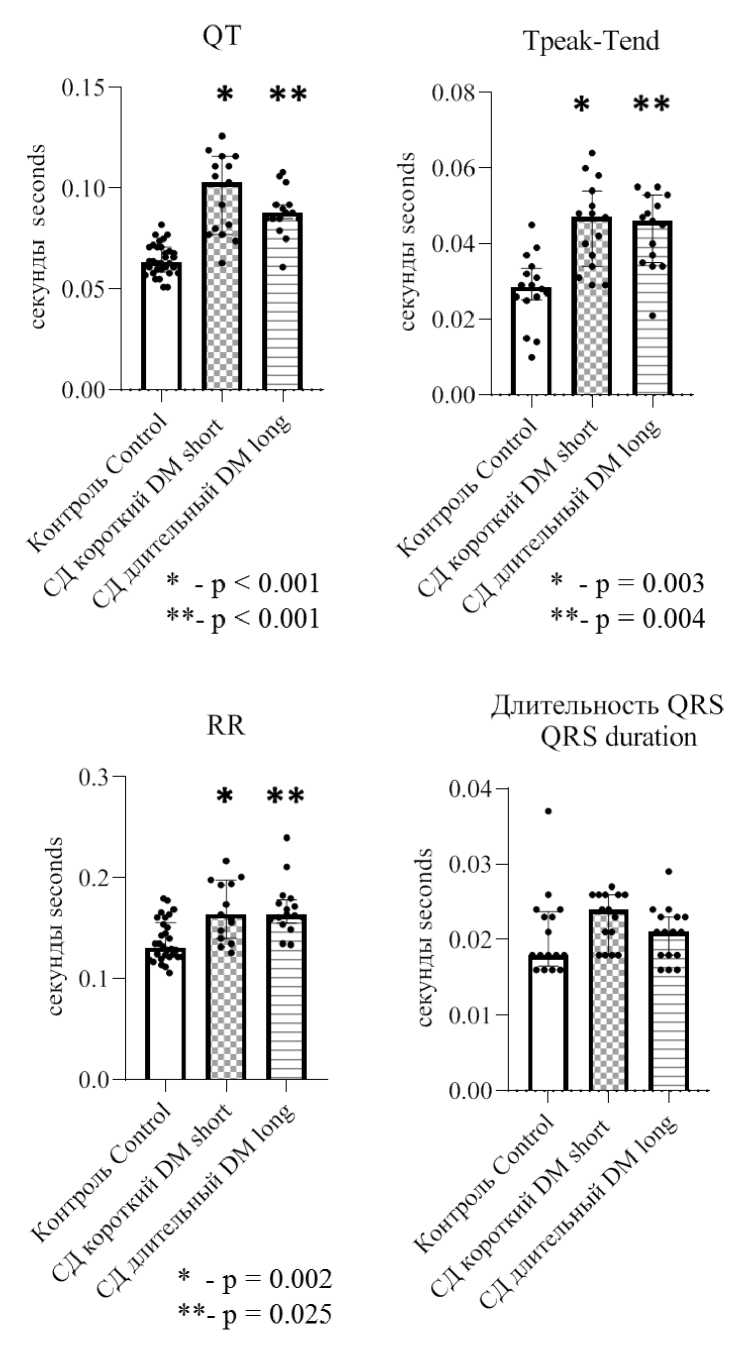
Рис. 1. Сравнение показателей ЭКГ в группах животных (U-критерий Манна – Уитни) Fig. 1. Comparison of ECG parameters in different animal groups (Mann – Whitney U test)
При оценке электрофизиологических параметров верхушки левого желудочка в исходном состоянии (до ишемии/реперфузии) время активации и дисперсия реполяризации значимо отличались от контрольной группы только у животных с коротким стажем СД (рис. 2). Время окончания реполяризации и интервал активации-реполяризации левого желудочка были значимо выше в обеих группах животных с СД по сравнению с контролем (рис. 2).
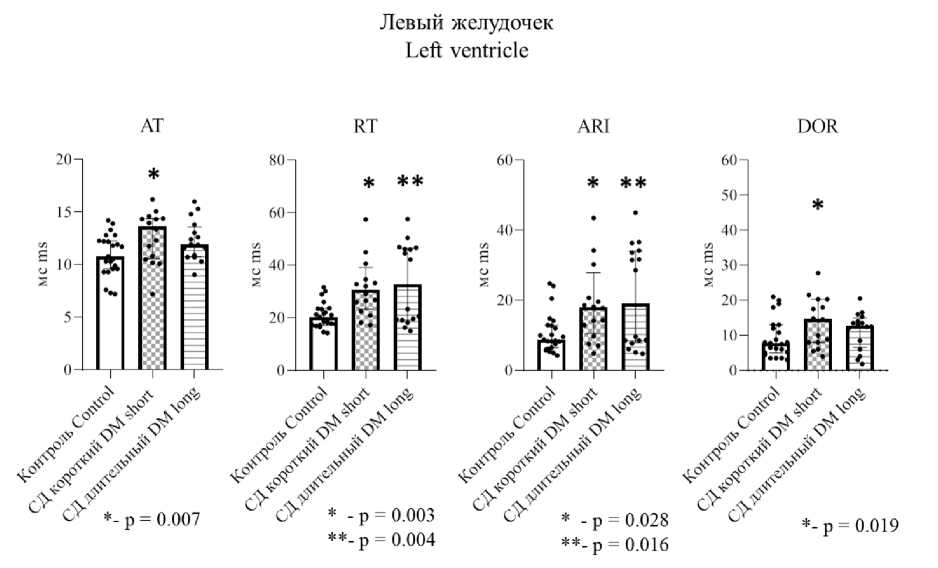
Рис. 2 . Сравнение электрофизиологических параметров верхушки левого желудочка (зона последующей ишемии/реперфузии) в группах животных (U-критерий Манна – Уитни)
Fig. 2. Comparison of electrophysiological parameters of the left ventricular apex (the zone of subsequent ischemia/reperfusion) in different animal groups (Mann – Whitney U test)
У крыс с сахарным диабетом наблюдалось значительное замедление продольной и поперечной скорости проведения как в левом, так и в правом желудочках (рис. 3).
Регистрация потенциалов действия кардиомиоцитов желудочков методом patch- clamp в режиме current-clamp показала увеличение их длительности в обеих группах с сахарным диабетом (рис. 4).
Стоит отметить, что рост продолжительности СД до 8 нед. не привел к дополнительному удлинению ПД (рис. 4).
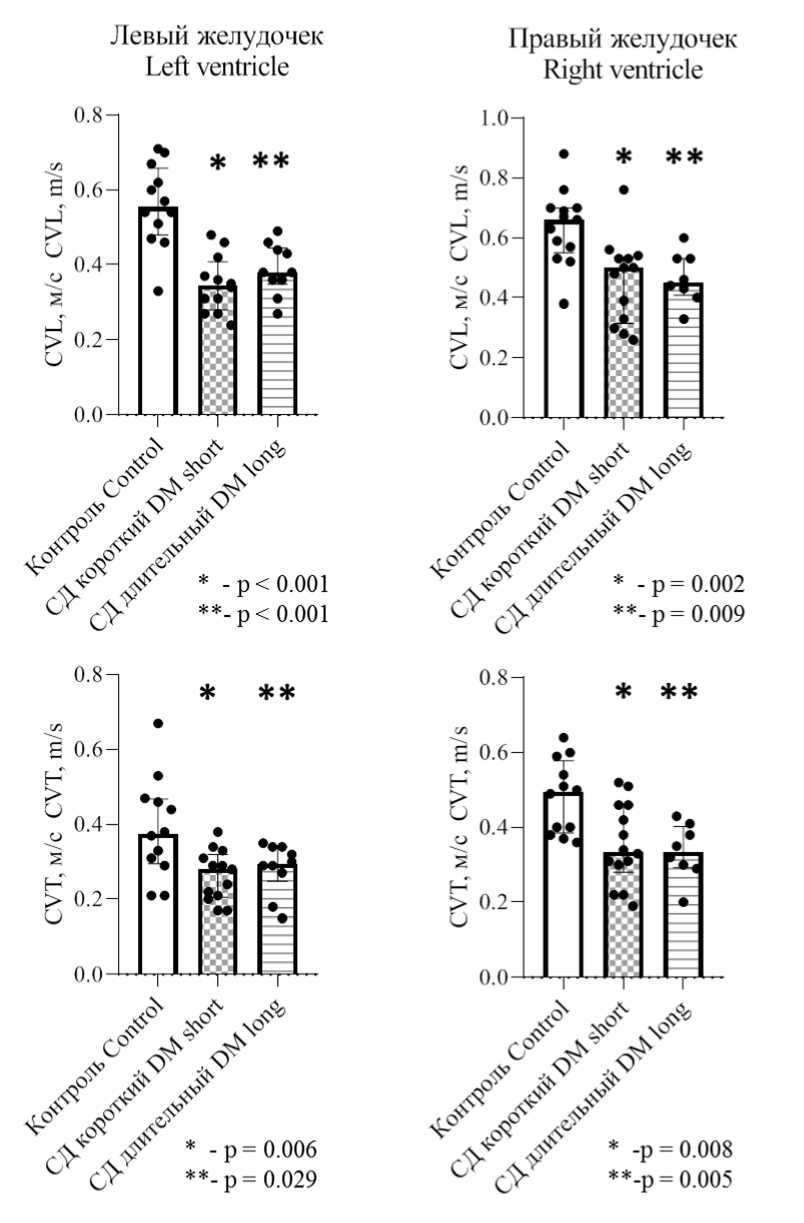
Рис. 3. Сравнение CVL и CVT в левом и правом желудочках в группах животных (U-критерий Манна – Уитни)
Fig. 3. Comparison of CVL и CVT in the left and right ventricles in different animal groups (Mann – Whitney U test)
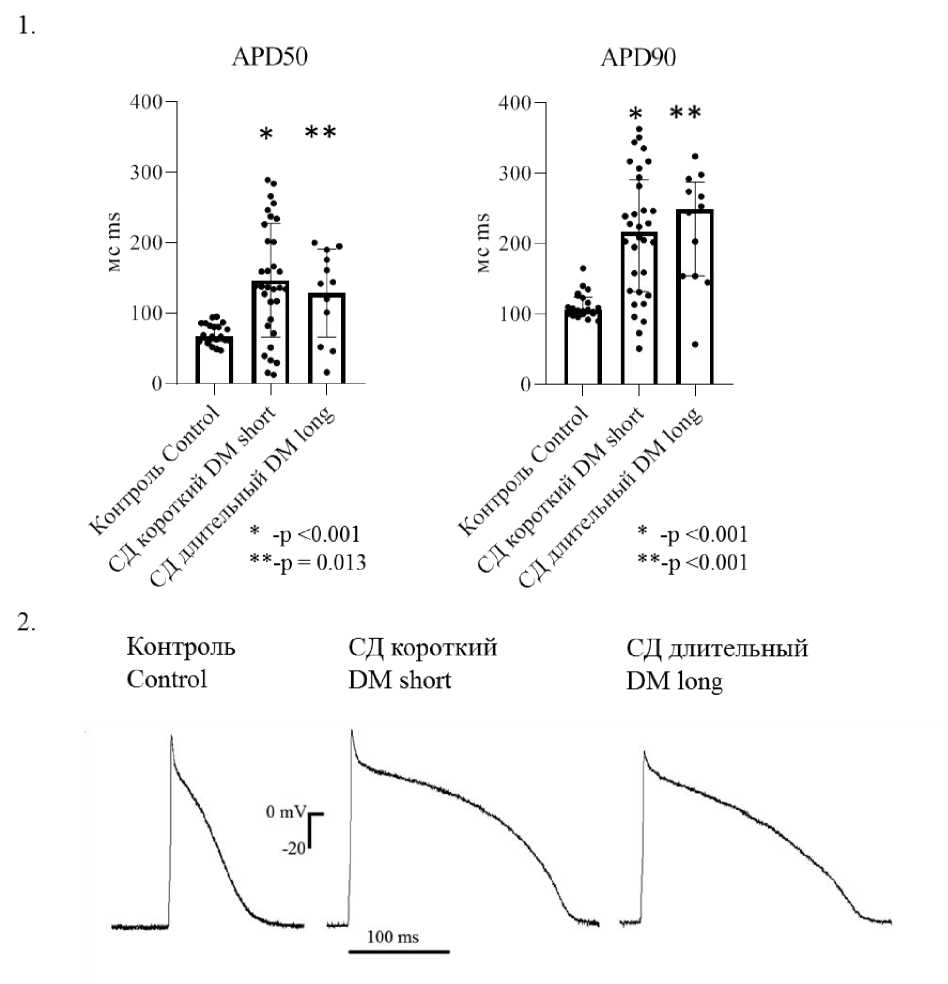
Рис. 4. Сравнение длительности потенциала действия кардиомиоцитов желудочков в группах животных на уровне 50 % и 90 % реполяризации (APD50 и APD90) (U-критерий Манна – Уитни): 1 – длительность ПД кардиомиоцитов желудочков на уровне 50 % и 90 % реполяризации (APD50 и APD90);
2 – репрезентативные записи ПД
Fig. 4. Comparison of the duration of ventricular cardiomyocytes action potential in animal groups at 50 % and 90 % repolarization (APD50 and APD90) (Mann–Whitney U-test): 1 – duration of ventricular cardiomyocyte action potential at 50 % and 90 % repolarization (APD50 and APD90); 2 – representative action potential recordings
Моделирование ишемии/реперфузии левого желудочка привело к появлению реперфузионных ЖТ/ФЖ. В исследуемых группах контроля, СД короткого и длительного стажа частота ЖТ/ФЖ составила 39,1 % (9 из 23),
50,0 % (8 из 16) и 6,3 % (1 из 16) соответственно. Частота ЖТ/ФЖ была значительно выше в группе с коротким стажем СД по сравнению с группой с длительным стажем (p=0,015).
Обсуждение. В нашем исследовании путем вариации длительности индуцированного стрептозотоцином СД у крыс нам удалось получить экспериментальную модель с высокой частотой индуцируемых ишемией/реперфу-зией желудочковых аритмий. У крыс с длительностью заболевания 4 нед. частота ЖТ/ФЖ была выше, чем у крыс с 8-недельным СД.
Электрокардиографическим выражением влияния сахарного диабета на реполяризацию желудочков было удлинение интервалов QT и Tpeak-Tend. Эти параметры ЭКГ и ранее показали себя как предикторы желудочковых аритмий и внезапной смерти при различной патологии сердца [16].
При исследовании изолированных желудочковых кардиомиоцитов крыс методом patchclamp в режиме current-clamp обнаружилось значимое увеличение длительности потенциала действия. Это может быть связано с изменениями ионных токов в кардиомиоцитах, в частности с усилением токов натрия (INa) и кальция (ICaL) [11, 17, 18] и/или ослаблением токов калия (Ito, IKr) [16, 19, 20]. Удлинение продолжительности потенциала действия за счет медленной реполяризации может привести к развитию ранних постдеполяризаций и желудочковых аритмий.
Также наблюдаются признаки замедления активации желудочков у крыс с СД любой продолжительности. Это проявляется снижением скорости проведения и увеличением АТ, что отражает медленное распространение импульса от проводящей системы к картируемой
области. Медленный охват миокарда возбуждением при СД может быть вызван его фиброзом. Конечные продукты гликирования, образующиеся при гипергликемии, действуют на специфический рецептор RAGE, активируют его и вызывают накопление активных форм О2, которые в свою очередь вызывают воспаление как в миокарде, так и в микроциркуля-торном русле. Окислительный стресс и хроническое воспаление миокарда приводят к активации фибробластов, усиленному синтезу коллагена и фиброзу [21, 22].
Дисперсия реполяризации увеличивалась только в группе со стажем СД 4 нед. Повышенная дисперсия реполяризации, предрасполагающая к однонаправленному блоку проведения возбуждения, ранее показана как проар-итмический фактор [23, 24]. Это предполагает высокую вероятность re-entry как механизма, приводящего к развитию желудочковых аритмий у животных с малым стажем экспериментального СД.
Заключение. При экспериментальном СД частота развития реперфузионной желудочковой тахикардии и/или фибрилляции желудочков была выше в группе экспериментального СД длительностью 4 нед., что, возможно, связано с большей дисперсией длительности реполяризации миокарда левого желудочка в этой группе животных. Удлинение длительности реполяризации без роста ее дисперсии или неоднородности не повышает частоту развития желудочковых аритмий при ишемии и реперфузии левого желудочка.
Работа поддержана грантом РНФ (соглашение № 23-25-00455).
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Вклад авторов
Концепция и дизайн исследования: Седякина Е.Н., Цветкова А.С., Азаров Я.Э., Овечкин А.О.
Литературный поиск, участие в исследовании, обработка материала: Седякина Е.Н., Цветкова А. С., Азаров Я. Э., Дуркина А.В., Гонотков М.А., Овечкин А. О.
Статистическая обработка данных: Седякина Е.Н., Цветкова А. С., Азаров Я.Э., Дуркина А.В., Гонотков М.А., Овечкин А. О.
Анализ и интерпретация данных: Седякина Е.Н., Цветкова А. С., Азаров Я.Э., Овечкин А.О.
Написание и редактирование текста: Седякина Е.Н., Овечкин А.О.
Список литературы Дисперсия реполяризации как предиктор жизнеугрожающих желудочковых аритмий при экспериментальном сахарном диабете малого стажа
- Rubler S., Dlugash J., Yuceoglu Y.Z., Kumral T., Branwood A.W., Grishman A. New type of cardiomyopathy associated with diabetic glomerulosclerosis. Am J Cardiol. 1972; 30 (6): 595-602. DOI: 10.1016/0002-9149(72)90595-4
- Bugger H., Abel E.D. Molecular mechanisms of diabetic cardiomyopathy. Diabetologia. 2014; 57 (4): 660-671. DOI: 10.1007/s00125-014-3171-6 EDN: NYILZL
- Zaccardi F., Khan H., Laukkanen J.A. Diabetes mellitus and risk of sudden cardiac death: a systematic review and meta-analysis. Int J Cardiol. 2014; 177 (2): 535-537. DOI: 10.1016/j.ijcard.2014.08.105
- Aune D., Schlesinger S., Norat T., Riboli E. Diabetes mellitus and the risk of sudden cardiac death: A systematic review and meta-analysis of prospective studies. Nutr Metab Cardiovasc Dis. 2018; 28 (6): 543-556. DOI: 10.1016/j.numecd.2018.02.011
- Gallego M., Casis O. Cellular Mechanism Underlying the Misfunction of Cardiac Ionic Channels in Diabetes. Diabetic Cardiomyopathy. Advances in Biochemistry in Health and Disease. 2014; 9: 189-199. DOI: 10.1007/978-1-4614-9317-4_11


