Дистанционный температурный контроль как способ дозирования воздействия при транссклеральной лазерной коагуляции сетчатки
Автор: Бойко Э.В., Суетов А.А., Измайлов А.С., Докторова Т.А., Иванов А.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 4S1 т.20, 2025 года.
Бесплатный доступ
Обоснование. Транссклеральные лазерные воздействия при ретинальной патологии имеют важные преимущества в случаях снижения прозрачности оптических сред и необходимости проведения воздействий на периферии глазного дна. Тем не менее, при таких воздействиях затруднена оценка степени формируемых ожогов, поэтому разработка методов дозирования, в том числе автоматизированных, поможет сделать транссклеральную лазерную коагуляцию эффективным и безопасным методом лазерного лечения и использовать ее в рутинной клинической практике. Цель. Изучить взаимосвязь температуры и ее изменения на поверхности склеры с интенсивностью лазерных ожогов при проведении транссклеральной лазерной коагуляции сетчатки. Материалы и методы. Экспериментальное исследование проведено на 5 кроликах (10 глаз). Транссклеральное лазерное воздействие проводили с помощью диодного лазера (Алод-01, Алком Медика, 810 нм) при мощности 0,2 Вт и диаметре пятна на поверхности склеры 300 мкм. Температуру измеряли дистанционно с помощью тепловизора (Guide MobIR Air, Китай) на поверхности склеры в точке воздействия. Интенсивность коагуляционного повреждения характеризовали как едва видимые, слабые, умеренные и интенсивные ожоги, и для каждой степени учитывали время воздействия, температуру и градиент температуры на поверхности склеры в месте воздействия, при которых формируются ожоги. Результаты. Формирование едва видимых ожогов происходит при подъеме температуры на поверхности склеры на 2,10±0,320С, слабых ожогов – на 2,44±0,270С, умеренных – на 2,87±0,310С и интенсивных – на 3,39±0,240С, при этом между градиентом температуры на поверхности склеры в зоне лазерного воздействия и временем формирования ожогов при всех учитываемых интенсивностях выявлена корреляция (r>0,45; p<0,05). Заключение. При проведении транссклеральной лазерной коагуляции сетчатки повышение температуры на поверхности склеры в точке воздействия коррелирует с временем воздействия и интенсивностью формируемого ожога на глазном дне.
Сетчатка, лазерная коагуляция, транссклеральное воздействие, температурный контроль
Короткий адрес: https://sciup.org/140312703
IDR: 140312703 | DOI: 10.25881/20728255_2025_20_4_S1_14
Remote temperature control as a method for dosing effects during transscleral laser coagulation of the retina
Background. Transscleral laser coagulation in retinal pathology have important advantages in cases of reduced transparency of optical media and the need for treatment on the periphery of the fundus. However, optical media opacities make it challenging to accurately assess the severity of the burns that occur, so the development of more precise dosing methods, including automated ones, could help to make transcleral laser coagulation a more effective and safe treatment option and allow its use in routine clinical practice. Aim. To investigate the relationship between temperature and its variations on the scleral surface and the intensity of laser burns during transscleral laser coagulation of the retina. Materials and methods. An experimental study was conducted on five rabbits (10 eyes). Transscleral laser exposure was performed using a diode laser (Alod-01, Alkom Medica, 810 nm) with a power of 0.2 W and a spot diameter of 300 microns on the surface of the sclera. The temperature was measured remotely using a thermal camera (Guide MobIRAir, China) on the surface of the sclera at the point of exposure. The severity of coagulation injury was characterized as barely visible, mild, moderate and intense burns, and for each level, the duration of exposure, temperature, and temperature difference on the surface of the sclera at the point of exposure were taken into consideration. Results. The formation of barely visible burns occurs when the temperature on the surface of the sclera rises by 2.10 ± 0.320 °C, mild burns - by 2.44 ±0.270 °C, moderate burns - by 2.87 ±0.310 °C and intense burns - by 3.39 ±0.240 °C. A correlation was found between the temperature gradient on the surface of the sclera in the laser exposure zone and the time of burn formation at all intensities considered (r>0.45, p<0.05). Conclusion. During transscleral laser coagulation of the retina, the temperature on the surface of the sclera at the point of exposure increases and correlates with the time and intensity of burns formed on the fundus.
Текст научной статьи Дистанционный температурный контроль как способ дозирования воздействия при транссклеральной лазерной коагуляции сетчатки
Актуальность
Лазерная фотокоагуляция сетчатки продолжает оставаться важным методом в лечении различной ретинальной патологии, при этом процедура проводится, как правило, транспупиллярно с использованием лазерного излучения видимого или ближнего инфракрасного диапазона, а дозирование эффектов осуществляется под офтальмоскопическом контролем [1]. В ряде клинических ситуаций, при которых вследствие заболевания развивается обширная периферическая неперфузия, например при диабетической ретинопатии или ишемических венозных окклюзиях, или при периферических разрывах сетчатки, требуется проведение лазерного воздействия на периферии глазного дна, но не всегда процедура ле-

чения технически выполнима: сниженная прозрачность оптических сред вследствие, например, катаракты, кровоизлияний в стекловидное тело, не позволяют эффективно воздействовать на периферическую сетчатку.
Транссклеральные воздействия являются альтернативой в таких случаях, при этом в клинической практике при лечении периферических разрывов и локальных отслоек сетчатки уже длительное время используются методы транссклеральной криопексии и диатермокоагуляции [2,3]. Еще одним потенциально более эффективным направлением является транссклеральное воздействие лазерным излучением ближнего ИК-диапазона вследствие его способности проникать через склеру к структурам глазного дна и вызывать фотокоагуляцион-ное повреждение, при этом такой вариант обеспечивает более щадящее воздействие на структуры глазного дна [3–5]. В ряде исследований было показано, что диод-лазерная транссклеральная коагуляция обеспечивает хороший терапевтический эффект при лечении отслоек сетчатки, ретинопатии недоношенных, серповидноклеточной ретинопатии [6–8]. Тем не менее, для повышения эффективности и безопасности любого варианта транссклерального воздействия необходим контроль получаемых коагуляционных повреждений на глазном дне и возможность дозирования процедуры, что при невозможности офтальмоскопического контроля требует разработки новых подходов, не предполагающих прямую визуализацию зоны воздействия на глазном дне.
Цель
Изучить в эксперименте взаимосвязь температуры и ее изменения на поверхности склеры с интенсивностью лазерных ожогов при проведении транссклеральной лазерной коагуляции сетчатки.
Материалы и методы
Экспериментальное исследование проведено на 5 кроликах (20 глаз) породы шиншилла (самцы массой 2,5–3 кг) с умеренной пигментацией глазного дна. Работа была выполнена в соответствии с международными правилами работы с животными (European Communities Council Directive, 86/609/EEC).
Транссклеральное лазерное воздействие проводили в условиях наркоза (ксилазин 5 мг/кг и кетамина гидрохлорид 35 мг/кг внутримышечно за 15 мин. до манипуляций), мидриаза (циклопентолат 1%) и местной анестезии (оксибупрокаина гидрохлорид 0,4%).
Источником лазерного излучения служил лазерный модуль АЛОД-01 с длиной волны 810 нм (Алком Медика, Россия), при этом для доставки лазерного излучения использовали транссклеральный зонд, наконечник которого располагали на склере на расстоянии 10–20 мм от лимба (экваториальная и постэкваториальная зона) перпендикулярно ее поверхности контактно, но без продавливания оболочек глаза. При проведении воздействия в режиме непрерывной генерации диаметр пятна пилотного лазера при трансиллюминации на глазном дне составлял 300 мкм, мощность лазерного излучения 0,2 Вт. Во всех глазах наносили по 30 лазерных ожогов различной интенсивности (едва видимые, слабые, умеренные и интенсивные ожоги), ориентируясь на градацию F.A. L’Esperance [9].
При воздействии формирование ожогов на глазном дне отслеживали при биомикроофтальмоскопии (щелевая лампа SM-2, Takagi Seiko Co LTD, Япония) с панфундус-линзой Volk SuperQuad 160 PRP (Volk Optical, США).
Температуру на поверхности склеры в точке воздействия измеряли с помощью тепловизора Guide MobIR Air (Wuhan Guide Sensmart Tech Co., Ltd., КНР), располагая его на расстоянии 0,3 м, при этом в мобильном приложении применяли опцию температурного анализа в выбранной точке. Учитывали исходную температуру, температуру, при которой формируются ожоги различной интенсивности, а также время формирования ожогов.
Статистический анализ результатов производили в пакете программ Statistica 10.0 Statistica 12.0 (StatSoft Inc., США). Результаты представлены в виде M±m, коэффициента вариации V (%). Анализ различия значений показателей с помощью t-критерия Стьюдента. Для оценки взаимосвязи показателей использовали корреляционный анализ. Статистически значимыми считали результаты с уровнем значимости p<0,05.
Результаты
При лазерном воздействии во всех случаях на глазном дне наблюдали формирование ожогов различной интенсивности (Рис. 1), при этом ни в одном из случаев не было зафиксировано термического повреждения конъюнктивы и глубжележащих тканей в зоне контакта транссклерального зонда. Важно, что фиксируемая в момент воздействия интенсивность ожогов в дальнейшем еще менялась из-за «созревания» ожогов вследствие распространения нагрева тканей с вовлечением в повреждение соседних структур.
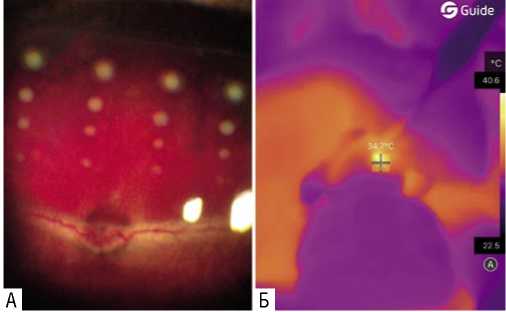
Рис. 1. Фундус-изображение с лазерными ожогами различной интенсивности (а) и пример измерения температуры на склере в зоне лазерного воздействия (б).

Время формирования ожогов, с
Температура на поверхности склеры, °С
37 •

34,5 •
Едва Слабый Умеренный Интенсивный видимый
Едва Слабый Умеренный Интенсивный видимый
Едва Слабый Умеренный Интенсивный видимый
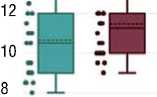
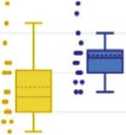
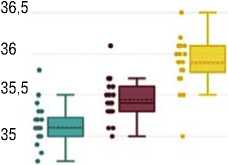
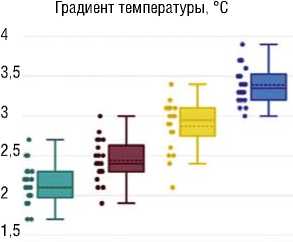
Рис. 2. Время формирования ожогов различной интенсивности и регистрируемые при этом температура и ее градиент на поверхности склеры в зоне воздействия.
При анализе времени формирования ожогов выявлено, что для едва видимых ожогов при используемых параметрах лазерного воздействия необходимая экспозиция составляет 8,88±0,58 с, для слабых ожогов 10,15±0,78 с, для умеренных 12,05±0,54 с, а для интенсивных 14,03±0,73 с, при этом значения экспозиции для каждой интенсивности ожога значимо отличаются (p<0,001; Рис. 2), а коэффициент вариации значений экспозиции находится в диапазоне от 4,5 до 7,6%.
Температура тканей на поверхности склеры до воздействия составляла 33,10±0,15 °С, при формировании едва видимых ожогов было выявлено значимое увеличение температуры до 35,11±0,28 °С, слабовыра-женных ожогов до 35,45±0,25 °С, умеренных ожогов до 35,88±0,31 °С и интенсивных до 36,4±0,27 °С (p<0,001; Рис. 2). Динамика температурного градиента при увеличении интенсивности ожогов соответствовала регистрируемой температуре: для получения едва видимых ожогов необходим был подъем температуры на 2,10±0,320С, слабых ожогов – на 2,44±0,27 °С, умеренных – на 2,87±0,31 °С и интенсивных – на 3,39±0,24 °С, при этом значения градиента значимо отличались друг от друга для разных интенсивностей ожогов (p<0,001; Рис. 2), коэффициент вариации находился в диапазоне от 7,1 до 15,3%.
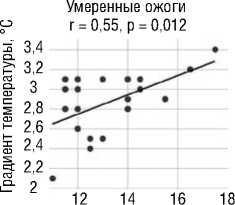
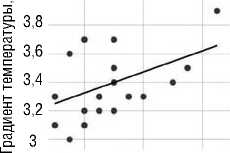
При проведении корреляционного анализа выявлено наличие значимой умеренной прямой связи между градиентом температуры на поверхности склеры в зоне лазерного воздействия и временем формирования ожогов при всех учитываемых интенсивностях (r>0,45 при p<0,05; Рис. 3).
Полученные результаты свидетельствуют о возможности дозирования воздействия при транссклеральной лазерной коагуляции сетчатки: в условиях эксперимента при используемых параметрах лазерного воздействия для получаемых ожогов различной интенсивности были определены диапазоны изменения температуры на поверхности склеры, которые значимо отличались между собой.
Выявленная корреляция между градиентом температуры на поверхности склеры и временем формирования ожогов объясняется процессом распространения тепла
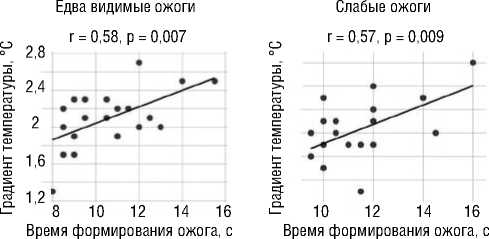
Время формирования ожога, с
Рис. 3. Зависимость между градиентом температуры на поверхности склеры и временем формирования ожогов различной интенсивности.
Интенсивные ожоги r = 0,45, p = 0,044
14 16 18
Время формирования ожога, с
из зоны воздействия, но в дальнейших исследованиях необходимо учитывать возможные особенности динамики нагрева тканей при увеличении мощности лазерного излучения с целью сокращения времени проведения процедуры.
Также важным является то, что в проведенном эксперименте длительность воздействия, необходимая для получения фотокоагуляционных эффектов, значительно превышала используемые в клинической практике значения (более 8 с для едва видимых ожогов), поэтому накопление и распространение тепла в тканях способствовало увеличению тяжести ожогового повреждения уже после завершения воздействия, меняя тем самым морфологию ожогов сетчатки. Тем не менее, эта проблема может быть решена в будущем за счет введения соответствующих поправок при расчетах температуры и времени воздействия.

Заключение
При проведении транссклеральной лазерной коагуляции сетчатки повышение температуры на поверхности склеры в точке воздействия коррелирует с временем воздействия и интенсивностью формируемого ожога на глазном дне.
Источник финансирования: исследовательская работа проведена на личные средства авторского коллектива.


