Дофаминергический дисбаланс, дизрегуляция салиенса и система вознаграждения при шизофрении (обзор материалов XXI конгресса Европейской психиатрической ассоциации)
Автор: Алфимов Павел Викторович
Журнал: Сибирский вестник психиатрии и наркологии @svpin
Рубрика: Лекции. Обзоры
Статья в выпуске: 4 (85), 2014 года.
Бесплатный доступ
Настоящая публикация представляет собой обзор симпозиума «Reward, Salience and Dopaminein Schizophrenia Patients» (Вознаграждение, салиенс и дофаминергическая передача у пациентов с шизофренией), прошедшего 8 апреля 2013 г. под председательством A. Heinz (Германия) и O. Howes (Великобритания) в рамках XXI конгресса Европейской психиатрической ассоциации (6-9 апреля 2013 г., Ницца, Франция). Приведен краткий обзор основных дефиниций и гипотез, докладов четырех независимых научноисследовательских групп из разных регионов Европы и соответствующих публикаций, посвященных дофаминергическому дисбалансу, нейровизуализационным находкам, нарушению салиенса и обработки сигналов в системе вознаграждения, имеющих место при шизофрении.
Шизофрения, салиенс, вознаграждение, дофаминергическая передача, негативные симптомы, нейровизуализация, вентральная область полосатого тела, конгресс епа (2013)
Короткий адрес: https://sciup.org/14295786
IDR: 14295786 | УДК: 616.895.8
Dopaminergic imbalance, salience dysregulation and reward system in schizophrenia: a report on symposium held at the XXIst EPA congress
This paper provides an overview of the symposium Reward, Salience and Dopamine in Schizophrenia Patients, which was held on April 8, 2013 under the chairmanship of A. Heinz (Germany), and O. Howes (UK) during the XXI st Congress of the European Psychiatric Association (6-9 April 2013, Nice, France). This paper provides a brief review of key definitions, reports of four independent research groups from different regions of Europe and relevant publications on dopaminergic imbalance, neuroimaging findings, salience disruption and signal processing in the reward system which occur in schizophrenic patients.
Текст научной статьи Дофаминергический дисбаланс, дизрегуляция салиенса и система вознаграждения при шизофрении (обзор материалов XXI конгресса Европейской психиатрической ассоциации)
Настоящая публикация представляет собой обзор симпозиума «Reward, Salience and Dopaminein Schizophrenia Patients» (Вознаграждение, салиенс и дофаминергическая передача у пациентов с шизофренией), прошедшего 8 апреля 2013 г. под председательством A. Heinz (Германия) и O. Howes (Великобритания) в рамках XXI конгресса Европейской психиатрической ассоциации (6–9 апреля 2013 г., Ницца, Франция). Приведен краткий обзор основных дефиниций и гипотез, докладов четырех независимых научноисследовательских групп из разных регионов Европы и соответствующих публикаций, посвященных дофаминергическому дисбалансу, нейровизуализационным находкам, нарушению салиенса и обработки сигналов в системе вознаграждения, имеющих место при шизофрении. Кл юче-вые сл ова : шизофрения, салиенс, вознаграждение, дофаминергическая передача, негативные симптомы, нейровизуализация, вентральная область полосатого тела, конгресс ЕПА (2013).
DOPAMINERGIC IMBALANCE, SALIENCE DYSREGULA-TION AND REWARD SYSTEM IN SCHIZOPHRENIA: a report on symposium held at the XXIst EPA Congress. Alfimov P. V. Moscow Psychiatry Research Institute of Ministry of Healthcare of Russia. Poteshnaya 3, 107076, Moscow, Russia. This paper provides an overview of the symposium Reward, Salience and Dopamine in Schizophrenia Patients, which was held on April 8, 2013 under the chairmanship of A. Heinz (Germany), and O. Howes (UK) during the XXIst Congress of the European Psychiatric Association (6—9 April 2013, Nice, France). This paper provides a brief review of key definitions, reports of four independent research groups from different regions of Europe and relevant publications on dopaminergic imbalance, neuroimaging findings, salience disruption and signal processing in the reward system which occur in schizophrenic patients. Keywords : schizophrenia, salience, reward processing, dopaminergic transmission, neuroimaging, ventral striatum, EPA Congress (2013).
Настоящая публикация представляет собой обзор симпозиума «Reward, Salience and Dopamine in Schizophrenia Patients» (Система вознаграждения, салиенс и дофаминергическая передача у пациентов с шизофренией), прошедшего 8 апреля 2013 г. под председательством A. Heinz (Германия) и O. Howes (Великобритания) в рамках XXI конгресса Европейской психиатрической ассоциации (6–9 апреля 2013 г., Ницца, Франция).
Ниже приводится краткий обзор основных дефиниций и гипотез, докладов четырех независимых научно-исследовательских групп из различных регионов Европы, соответствующих публикаций и неопубликованных данных, посвященных вопросам дофаминергического дисбаланса, нейровизуализационным находкам, нарушению салиенса и обработки сигналов в системе вознаграждения, которые имеют место при шизофрении.
Салиенс (salience) в широком смысле понимается как способность идентифицировать значимые стимулы и отделять их от фоновых, малозначимых стимулов. Этот феномен лежит в основе функции внимания и обеспечивает выживание и научение индивида, позволяя ему сфокусировать ограниченные перцептивные и когнитивные ресурсы на важных наборах данных, поступающих из различных сенсорных систем. Выделяют два механизма салиенса – восходящий (реактивный, не связанный с памятью), который отвечает за незамедлительное привлечение внимания организма к значимому стимулу, а также нисходящий (предвосхищающий, связанный с памятью) механизм.
Основным нейроанатомическим субстратом салиенса являются мезолимбические и лимбические структуры, а основным нейромедиатором, участвующим в формировании реакции на значимый стимул, является дофамин, который преобразует эмоционально нейтральный бит информации в эмоционально окрашенную (положительную или отрицательную) реакцию – т. е. в «салиентное событие». S. Kapur (2003) предположил, что гипердофаминергическое состояние лимбической системы, имеющее место при шизофрении, приводит к нарушению адекватного распределения салиентных событий в ответ на различные внешние и внутренние стимулы. Предполагается, что это нарушение обусловливает широкий спектр позитивных симптомов шизофрении (галлюцинаторнобредовые симптомы, дезорганизация мышления и др.). Некоторые биологически ориентированные психиатры небезосновательно считают нарушение салиенса стержневым феноменом при шизофрении и предлагают сгруппировать расстройства шизофренического спектра в будущих классификациях в группу «синдромов дизрегуляции салиенса» (van Os J., 2009).
В качестве возможных вариантов русского перевода этого термина предложены «синдром нарушения различения (приоритизации) стимулов», «синдром сверхвключаемости объектов восприятия» и «синдром нарушения избирательной фильтрации информации» (Мосолов С. Н., 2010).
Важным нейрофизиологическим понятием является «побудительный салиенс» (incentive salience). Этот конструкт был разработан при изучении роли дофаминергической передачи в системе вознаграждения при аддиктивных расстройствах (Berridge K. et al., 1998). Побудительный салиенс – это мотивационный атрибут «желания» (wanting), который присваивается стимулу, предвосхищающему вознаграждение. Этот атрибут «желания» шире, чем простое гедонистическое «влечение» (liking), которое возникает при контакте с привлекательным стимулом. Атрибут «желания» придает стимулу мотивационное безусловное качество – он перестает быть простым сенсорным переживанием, он привлекает внимание и стимулирует поисковое поведение.
В качестве примера можно привести отдаленный этап наркотической зависимости, когда у пациента давно утерян гедонистический компонент употребления ПАВ, однако стимулы, напоминающие об употреблении (например, плакат с изображением шприцев, игл и ампул), способны спровоцировать поиск и употребление наркотического вещества. Предполагается, что дофаминергическая система участвует в процессе принятия решений, влияя на приоритетность или уровень «желанности» стимула. Дофаминергическая передача усиливается, когда фактическое вознаграждающее событие по своей значимости превосходит ожидание, и наоборот, ослабляется, когда это событие качественно хуже ожидаемого.
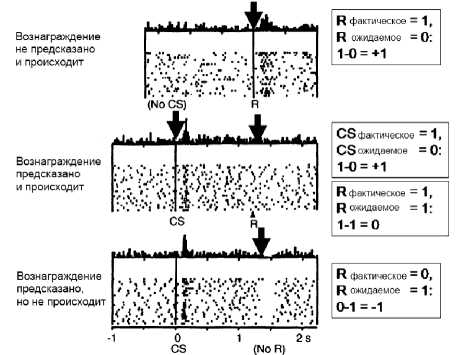
Рис. 1 . Фазное усиление высвобождения дофамина, отражающее ошибку «предсказания» вознаграждения (reward prediction error). Адаптировано из публикации W. Schultz (1997).
Примечание . Вверху: вознаграждение (R) не предсказано; разница между фактическим и ожидаемым вознаграждением положительна, что приводит к краткосрочному усилению высвобождения дофамина. Посередине: условный сигнал соответствует предсказанному вознаграждению (CS), усиления выброса дофамина не происходит. Внизу : ожидаемого вознаграждения не происходит; наблюдается фазное ослабление высвобождения дофамина.
Условные сигналы, связанные с приближающимся вознаграждением, могут приводить к короткому фазному усилению дофаминергической передачи в ситуации, когда вознаграждение «не предсказано», т. е. превосходит ожидания индивида. В ситуации, когда вознаграждение соответствует ожиданиям, соответствующий стимул не приводит к фазному усилению дофаминергической передачи (Schultz W. et al., 1997) (см. рис. 1).
T. Robinson et al. (1993) предположили, что фазное усиление высвобождения дофамина отражает т. н. ошибку предсказания и связано с атрибутом «побудительного салиенса», который присваивается условным сигналам, связанным с вознаграждением. Эта гипотеза была рассмотрена несколькими научными группами в контексте расстройств шизофренического спектра (Heinz A. et al., 2002; Kapur S., 2003). Предполагается, что хаотическое (и связанное со стрессом) усиление дофаминергической передачи в афферентных путях, идущих к полосатому телу, приводит к тому, что атрибут «побудительного салиенса» присваивается нерелевантным стимулам, что может объяснить возникновение продромальных позитивных симптомов (например, бредового настроения по C. Conrad), «полноценной» галлюцинаторнобредовой симптоматики, а также некоторых негативных симптомов (см. ниже).
В недавних исследованиях подчеркивалась важность связи между обработкой сигналов в системе вознаграждения и негативными симптомами шизофрении (Juckel G. et al., 2006a; Waltz J. et al., 2008). При шизофрении выявляется нарушение присвоения атрибута «желания», который в норме придает стимулам мотивационную окраску (Berridge K. et al., 1998). У фармакологически интактных больных шизофренией и у больных, получающих лечение антипсихотиками первого поколения (АПП), на фМРТ-картине наблюдается ослабление сигнала вентрального полосатого тела (ВПТ) при выполнении тестов с предвосхищением вознаграждения (Juckel G. et al., 2006b; Schlagenhauf F. et al., 2008). Кроме того, наблюдается отрицательная корреляция между активацией вентрального полосатого тела и общей тяжестью негативной симптоматики (Juckel G. et al., 2006a). Подробнее эта проблема рассмотрена в обзоре немецких авторов (см. далее).
В фМРТ-исследованиях, описанных ниже, для оценки психопатологической симптоматики применялись шкалы CDSS, AES, PANSS и другие распространенные психометрические инструменты (точнее, их валидизированные национальные версии) и использовался тот или иной вариант теста денежного стимулирования с задержкой (Monetary incentive delay task – Knutson B. et al., 2001; Abler B. et al., 2005).
На рисунке 2 представлены стимулы, отражающие возможные варианты вознаграждения (1 евро, 20 центов, 0 евро), а также последовательность действий теста денежного стимулирования с задержкой. Процедура теста выглядит следующим образом: сначала пациенту, находящемуся в МР-томографе, предоставляется стимул, предусматривающий то или иное вознаграждение в случае, если он примет правильное решение в ходе последующей задачи на различение (нажатие одной из двух кнопок). Оценка графических данных выполняется в периоды задержки (предвосхищения вознаграждения) и после объявления результатов, когда пациенту сообщается о том, сколько денег он «выиграл».
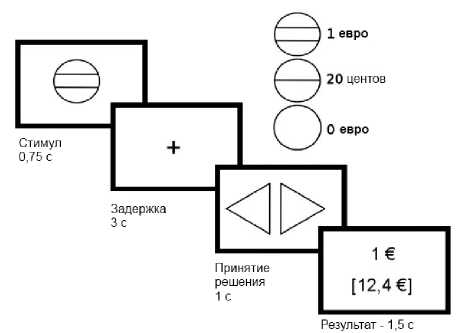
Рис. 2. Тест денежного стимулирования с задержкой по B. Abler et al. [2005]
Доклад коллектива авторов под руководством O. Howes (Институт психиатрии Лондонского Королевского колледжа, Великобритания) был посвящен раннему выявлению дофаминергической дисфункции при шизофрении, а также ее динамике при развитии психоза. Авторы подчеркивают, что время возникновения этой дисфункции неизвестно. Не менее загадочной представляется динамика этого нарушения после развития психоза. Для изучения описанной проблемы авторами было проведено лонгитудинальное исследование на небольшой когорте (n=20, средний возраст 25,0 года, СО=4,1) пациентов с «ультравысоким риском развития психоза» (Howes O. et al., 2011). Исследование включало 2 последовательных ПЭТ-сканирования с использованием 18F-DOPAс промежутком в 2 года. У 8 (36 %) пациентов к моменту второго сканирования диагностировано психотическое расстройство по критериям DSM-IV-TR (шизофрения, n=6; шизофрено-формное расстройство, n=1; эпизод психотической мании в рамках БАР I типа, n=1). У оставшихся 12 пациентов психоз не развился ни через 2 года, ни в последующие 12 месяцев ка-тамнестического наблюдения.
В качестве показателя способности к синтезу дофамина применялась константа инфлюкса ( K i или K cer i /мин), которая рассчитывалась по результатам графического анализа. Лонгитудинальное измерение K cer i проводилось для всего полосатого тела и для его функциональных подразделений (в качестве референтной области использовался мозжечок). В ходе анализа областей интереса обнаружено, что у пациентов с продромальными симптомами, у которых в дальнейшем развился психоз, отмечается значимое увеличение значения K cer i (рис. 3) в ассоциативной области полосатого тела.
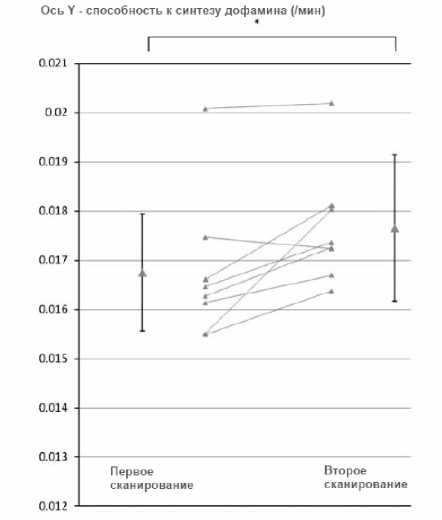
Рис. 3. Изменение способности к синтезу дофамина в сенсомоторной области полосатого тела среди пациентов, у которых развился психоз к моменту второго сканирования. Адаптировано из O. Howes et al. [2011]
Примечание . Средние значения для всей когорты показаны слева и справа для первого и второго сканирований соответственно. В качестве меры измерения способности к синтезу дофамина используется рассчитанная константа инфлюкса Kcer i /мин. «Усы» на диаграмме представляют СО. *– p<0,05.
Эта находка подтвердилась после того, как из анализа исключили 2 пациентов, получавших антипсихотическую терапию к моменту второго сканирования. Не обнаружено значимых изменений для всего полосатого тела и других его функциональных отделов (лимбического и сенсомоторного). Проведен отдельный анализ вокселов в графических данных пациентов с психозом, у которых отмечалось увеличение K cer i в правой скорлупе (сенсомоторный отдел полосатого тела – рис. 4). Что касается пациентов, чьи продромальные симптомы не привели к развитию психоза, в анализе вокселов и в анализе областей интереса не обнаружено значимых изменений.
Авторы подчеркивают необходимость проведения подобных лонгитудинальных ПЭТ-исследований с б о льшим числом пациентов и длительным периодом катамнестического наблюдения.
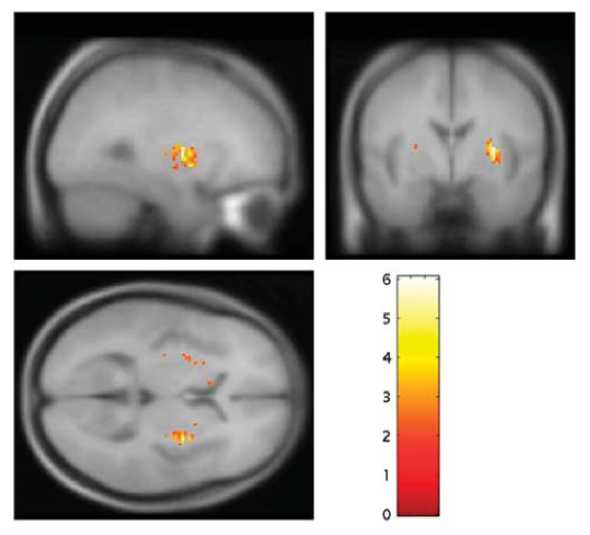
Рис. 4. ПЭТ-картина прогрессирующего усиления способности к синтезу дофамина в сенсомоторном отделе полосатого тела у пациентов с продромальными симптомами, у которых психоз развился к моменту второго сканирования. [Howes O. et al., 2011].
Примечание . Усиление способности к синтезу дофамина зарегистрировано в правой скорлупе (правом дорсолатеральном [сенсомоторном] отделе полосатого тела). Разброс кластера воксела 124. Координаты MNI пикового воксела: 30, -4, 6.
Авторами также представлены неопубликованные результаты исследования со схожим дизайном, которое было проведено в нескольких группах: двух сопоставимых когортах с высоким риском развития психоза, когорте здоровых лиц, когорте лиц, хорошо реагирующих на терапию антипсихотиками, и когорте терапевтически резистентных пациентов. Способность к синтезу дофамина была значимо повышена в двух независимых когортах пациентов с высоким риском развития психоза во всем полосатом теле, а также в ассоциативном участке полосатого тела. Этот феномен коррелировал с тяжестью позитивной симптоматики. Среди пациентов, у которых впоследствии развился психоз, отмечалось прогрессирующее увеличение способности к синтезу дофамина. Авторы делают следующие осторожные выводы. Увеличение способности к синтезу дофамина в полосатом теле: а) предвосхищает развитие психоза у лиц с продромальными симптомами (пациентов с высоким риском развития психоза); б) возрастает со временем при развитии психоза; в) коррелирует с реагированием на антипсихотическую терапию.
Пожалуй, самым важным заявлением авторов является то, что терапия антипсихотиками среди пациентов с продромальной симптоматикой способна снизить риск развития психоза за счет угнетения дофаминергической передачи в полосатом теле.
Были также доложены обнадеживающие результаты недавно опубликованного метаанализа нейровизуализационных исследований (Howes O. et al., 2012). Подчеркивается, что современные методы антипсихотической терапии, основанные, главным образом, на блокаде D 2 -рецепторов, имеют ограниченную эффективность у большей части больных шизофренией. Авторы предприняли попытку уточнения природы дофаминергической дисфункции при шизофрении – проведен метаанализ нейровизуа-лизационных (главным образом ПЭТ и ОФЭКТ) исследований in vivo, в которых количественно оценивалась дофаминергическая активность в полосатом теле.
В анализ вошло 44 исследования, опубликованных с 1960 по 2011 г., в которые в общей сложности было включено 618 больных шизофренией и 606 здоровых лиц. Оценивались пре-синаптическая функция дофаминовых нейронов, доступность транспортера дофамина, а также доступность дофаминовых рецепторов в полосатом теле. Получены следующие результаты: при шизофрении выявляется значительное ( d Коэна 0,79) и статистически достоверное (p<0,01) усиление пресинаптической дофаминергической функции (рис. 5).

Рис. 5 . Метаанализ нейровизуализационных исследований пресинаптической дофаминергической функции у больных шизофренией. Адаптировано из публикации O. Howes et al. [2012]
Примечание . На диаграмме в правой части рисунка приведены размеры эффектов и 95 % ДИ различий в размере эффекта между здоровыми лицами и пациентами с шизофренией. Суммарный размер эффекта (белый ромб внизу справа) отражает значимое усиление пресинаптиче-ской дофаминергической функции при шизофрении (d=0,79).
Не обнаружено значимых изменений в доступности транспортера дофамина; выявлено незначительное ( d Коэна 0,26) увеличение доступности D 2 - и D 3 -рецепторов, которое, однако, не наблюдалось у фармакологически интактных пациентов.
Авторы пришли к выводу, что наиболее важными при шизофрении являются пресинаптиче-ские дофаминергические аномалии – нарушение синтеза и высвобождения дофамина, а также изменение его исходной пресинаптиче-ской концентрации. Авторы утверждают, что дальнейшее изучение антипсихотических препаратов, чей механизм действия основан на связывании с D 2 - и D 3 -рецепторами, является малоперспективным. Целесообразной представляется разработка новых методов лечения, направленных на регуляцию пресинаптического синтеза и высвобождения дофамина.
Доклад коллектива под руководством S. Kaiser и J. Simon (Кафедра психиатрии Гейдельбергского университета Гейдельберга, Германия; Психиатрическая больница Цюрихского университета, Швейцария) был посвящен взаимосвязи между аномальной обработкой сигналов в системе вознаграждения и двумя доменами психопатологической симптоматики (апатией и ангедонией/депрессией). Представлены результаты одного опубликованного исследования (Simon J. et al., 2010) и одного исследования, которое готовится к публикации.
В первое исследование вошли 15 пациентов с шизофренией и 15 здоровых лиц. Все пациенты получали терапию АВП, а 5 пациентов дополнительно получали терапию антидепрессантами или нормотимиками. Все участники проходили комплексное психометрическое исследование (шкалы PANSS, CDSS, AES, шкалы Чапмана для оценки физической и социальной ангедонии – PAS и SAS), а также тест денежного вознаграждения с задержкой, совмещенного с фМРТ. При графическом анализе областей интереса не выявлено значимых межгрупповых различий в активации ВПТ в ситуациях с ожиданием и без ожидания вознаграждения, а также в ситуациях с получением и неполучением вознаграждения. Тем не менее обнаружена отрицательная корреляция между тяжестью апатии и активацией ВПТ на МР-картине (т. е. у пациентов с выраженной апатией отмечалось ослабление сигнала в ВПТ). Кроме того, выявлена отрицательная корреляция между тяжестью депрессии и изменением МР-сигнала, когда пациентам сообщали о результатах теста (у пациентов с б о льшим баллом по шкале Калгари отмечалось снижение активации ВПТ, когда им сообщали о денежном вознаграждении).
В связи с тем, что графические данные оказались малоинформативными, в настоящем обзоре не представлены полученные авторами МР-снимки. Авторы подчеркивают свои методологические недоработки: нельзя исключить, что отсутствие значимых межгрупповых различий в анализе графических данных связано с тем, что все пациенты получали адекватную терапию АВП.
Во второе исследование, пока еще не опубликованное, вошли 24 больных шизофренией и 36 здоровых добровольцев. Обнаружена отрицательная корреляция между активацией ВПТ во время ожидания вознаграждения и тяжестью апатии. Кроме того, обнаружена отрицательная корреляция между тяжестью позитивных симптомов и изменением сигнала в ситуациях получения и неполучения денежного вознаграждения.
Взяв за основу не только собственные результаты, но и работы других исследователей, авторы составили упрощенную схему, описывающую связь между основными нейроанато-мическими субстратами системы вознаграждения (ВПС и медиальной орбитофронтальной корой [мОФК]), этапами обработки сигналов в этой системе («желание» [wanting] и «влечение» [liking]), а также двумя основополагающими доменами негативной симптоматики (апатия, т. е. потеря мотивации, и ангедо-ния/депрессия) (рис. 6).
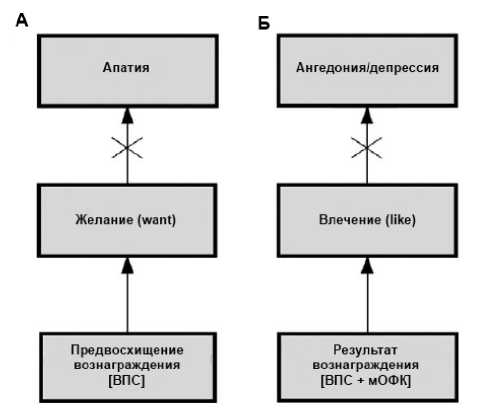
Рис. 6. Роль системы вознаграждения в возникновении «мотивационных» симптомов шизофрении. Адаптировано из J. Simon et al. [2010]
Примечание . А: дисфункциональная активация ВПС, регистрируемая во время предвосхищения ожидания, приводит к апатии (отсутствию мотивации). Б: дисфункциональная активация ВПС и (или) мОФК, регистрируемая в ходе получения вознаграждения, приводит к ангедонии и (или) депрессии.
Доклад коллектива под руководством M. Nielsen (Психиатрическая больница Копенгагенского университета, Глоструп, Дания), пожалуй, был одним из самых интересных. В нём подробно рассмотрена дисфункция системы вознаграждения у фармакологически интактных больных шизофренией и даны ценные терапевтические замечания. Приведены результаты двух последовательных лонгитудинальных нейровизуализационных исследований.
В первое исследование (Nielsen M. et al. 2012a) включен 31 фармакологически интактный больной шизофренией (в сопоставимую по полу, возрасту, социальному статусу и доминантному полушарию контрольную группу вошел 31 здоровый человек). Все участники прошли психометрическое обследование по шкалам PANSS и GAF. Использовался модифицированный авторами тест денежного вознаграждения с задержкой, совмещенный с фМРТ, который позволил условно разделить «общий са-лиенс» (побуждающие события) на «поведенческий компонент салиенса» (события, при которых получение предсказанного вознаграждения требует усилий) и «компонент предвосхищения награды».
В период предвосхищения, когда участникам представляли салиентные стимулы, у больных шизофренией отмечалось выраженное ослабление активации в вентральной покрышке, ВПТ и передней поясной извилине. Ослабление сигнала в ВПТ было связано с тяжестью позитивных симптомов и значимо коррелировало с изменением «поведенческого компонента сали-енса». Кроме того, у больных шизофренией отмечалось изменение паттерна активации правой префронтальной коры в ходе оценки ими результатов теста (количества полученных денег). Авторы предполагают, что МР-картина изменений в периоде предвосхищения отражает начало болезненного процесса. Наиболее значимые изменения наблюдались для «общего салиенса», при этом в ВПТ эти изменения четко коррелировали с тяжестью позитивной симптоматики.
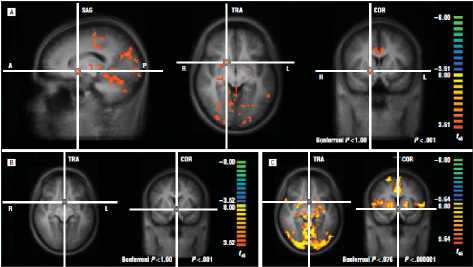
Рис. 7. МР-картина межгрупповых различий среди здоровых лиц и больных шизофренией во втором исследовании – исходный уровень (Nielsen M. et al., 2012b)
Примечание . A: полновокселное межгрупповое сравнение различий в МР-сигнале между здоровыми лицами и больными шизофренией (обнаруженные различия обусловлены ослаблением активации у больных). B: здоровые лица; C: фармакологически интактные больные шизофренией.
Во второе исследование (Nielsen M. et al., 2012b) вошли 23 пациента и 24 здоровых добровольца из первого исследования. Ранее не леченные пациенты в течение 6 недель полу- чали амисульприд в дозах до 500–600 мг/сут (доза подбиралась с учетом индивидуальной переносимости).
Схемы психометрического и инструментального обследований соответствовали таковым в первом исследовании. Через 6 недель терапии у больных шизофренией отмечалось усиление МР-сигнала, связанного с предвосхищением, – настолько, что терялись статистически значимые отличия от здоровых лиц. Это изменение было прямо пропорционально улучшению в сфере позитивной симптоматики.
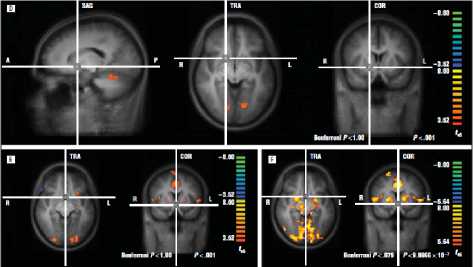
Рис. 8. МР-картина межгрупповых различий среди здоровых лиц и больных шизофренией во втором исследовании – через 6 недель терапии амисульпридом (Nielsen M. et al., 2012b)
Примечание. D: полновокселное межгрупповое сравнение различий в МР-сигнале между здоровыми лицами и больными шизофренией. E: здоровые лица. F: больные после 6 недель терапии амисульпридом (статистически значимые межгрупповые различия потеряны).
Авторы приходят к следующим выводам: курс лечения антагонистом D 2 -рецепторов может приводить к нормализации обработки сигналов в системе вознаграждения. Этот эффект наиболее выражен в случае выраженной фармакологической редукции позитивной симптоматики.
В докладе коллектива под руководством A. Heinz (докладчик F. Schlagenhauf) (Медицинский университетский центр Шарите, Берлин, Германия) были представлены краткие сведения о патологии системы вознаграждения и дофаминергической дисфункции при шизофрении, а также результаты двух любопытных нейровизуализационных исследований.
Первое исследование (Juckel G. et al., 2006a) по своему дизайну во многом было похоже на упомянутую выше работу M. Nielsen et al. (2012a). В него были включены 10 фармакологически интактных мужчин, соответствовавших диагностическим критериям МКБ-10 и DSM-IV-TR для шизофрении (средний возраст составил 26,8±7,8 года). 7 мужчин никогда не получали терапию антипсихотиками, 3 мужчин не получали ее в течение последних 2 лет. В контрольную группу вошли 10 здоровых добровольцев (с сопоставимым средним возрастом).
Все участники прошли психометрическое обследование по шкале PANSS, а также тест денежного вознаграждения с задержкой (в собственной модификации авторов), совмещенный с фМРТ.
По сравнению со здоровыми лицами у неле-ченных больных шизофренией отмечалось статистически значимое ослабление активации ВПТ при презентации стимулов, указывающих на вознаграждение. Выявлена отрицательная корреляция этого феномена с тяжестью негативной симптоматики (R Спирмана -0,66; p=0,04) и тяжестью позитивной симптоматики (значимость на уровне статистической тенденции; R Спирмана -0,61; p=0,06). По мнению авторов, усиление дофаминового обмена в полосатом теле, наблюдаемое при шизофрении, способно создавать «шум» в системе вознаграждения и вмешиваться в нейрональную обработку соответствующих салиентных сигналов (за счет фазного усиления высвобождения дофамина). Кроме того, этот нейробиологический феномен может быть связан с тяжестью негативной симптоматики, в частности с тяжестью ангедонии и апатии.
Во втором исследовании (Juckel G. et al., 2006b) отличались лишь изучаемые когорты (методы и материалы практически соответствовали таковым в первом исследовании). В исследование были включены 10 пациентов, получающих АПП (преимущественно галоперидол), 10 пациентов, получающих АВП (оланзапин или рисперидон), а также 10 здоровых добровольцев. Выявлено усиление активации ВПТ в ответ на стимулы, указывающие на вознаграждение, у здоровых лиц и пациентов, получавших АПП (но не АВП).
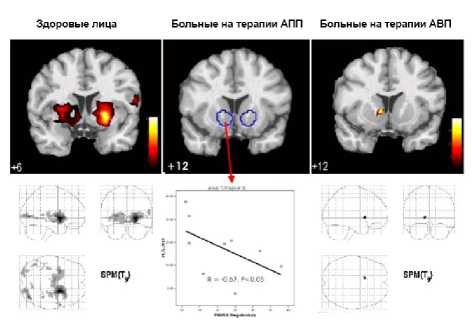
Рис. 9. МР-картина изменений в активации ВПТ у больных шизофренией, получавших АПП и АВП (Juckel G. et al., 2006b)
Примечание. На диаграмме в центре представлена корреляция между ослаблением активации ВПТ и тяжестью негативной симптоматики, которая измеряется баллом негативной подшкалы PANSS.
У пациентов, получавших АПП, ослабление активации в левом ВПТ значимо коррелировало с тяжестью негативной симптоматики (R Спир-мана -0,67; p<0,05) (рис. 9).
В последующей оживленной дискуссии прозвучало мнение о глобальном преимуществе АВП перед АПП, а также приведены дополнительные доводы в пользу «атипичности» ами-сульприда, который по своему механизму действия все же ближе к традиционным D 2 -блокаторам.
Обращают на себя внимание высокое методологическое качество и валидность результатов описанных выше исследований. Работа этих четырех независимых исследовательских групп находится на переднем крае как фундаментальной, так и прикладной нейронауки. Надеемся, что в обозримом будущем эти результаты найдут применение в практической медицине и будут использованы при разработке новых методов лечения психических расстройств.
Сокращения
18F-DOPA – 6-[18-фтор]-L-дигидроксифенилаланин
AES – шкала оценки апатии
CDSS – шкала Калгари для оценки депрессии при шизофрении
DSM-IV-TR – диагностическое и статистическое руководство по психическим расстройствам, четвертая редакция, пересмотренная
GAF – шкала глобальной оценки функционального статуса
PANSS – шкала оценки позитивных и негативных синдромов
PAS – шкала Чапмана для оценки физической ангедонии
SAS – шкала Чапмана для оценки социальной ангедонии
АВП – антипсихотики второго поколения
АПП – антипсихотики первого поколения
БАР – биполярное аффективное расстройство
ВПА – Всемирная психиатрическая ассоциация
ВПС – вентральная часть полосатого тела
ДИ – доверительный интервал
ЕПА – Европейская психиатрическая ассоциация
МКБ-10 – Международная классификация болезней десятого пересмотра мОФК – медиальная орбитофронтальная кора
ОФЭКТ – однофотонная эмиссионная компьютерная томография
ПЭТ – позитронно-эмиссионная томография
СО – стандартное отклонение фМРТ – функциональная магнитно-резонансная томография


