Двухэтапная резекция печени по методике ALPPS
Автор: Навматуля А.Ю., Цикоридзе М.Ю., Альмухаметова Ф.Р., Царегородцев А.Е., Братов О.З., Савчук С.А., Кузнецов А.И., Гельфонд В.М., Загрядских А.С., Чернобривцева В.В., Мирошников Б.И., Егоренков В.В., Моисеенко В.М., Соловьев И.А.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Оригинальные статьи
Статья в выпуске: 3 т.16, 2021 года.
Бесплатный доступ
Колоректальный рак является третьей по значимости причиной смерти от рака в России. При первичном выявлении опухоли у 30-50% пациентов выявляются синхронные метастазы в печени. Двухэтапная резекция печени зачастую является единственной возможностью радикального хирургического лечения пациентов с массивным метастатическим поражением печени за счет предотвращения пострезекционной печеночной недостаточности. Цель: оценить возможность двухэтапных резекций печени по методике ALPPS у больных с метастазами колоректального рака. Материал и методы. Расширенная гемигепатэктомия по методике ALPPS выполнена 18 больным с массивным билобарным поражением печени и планируемым объемом остающейся паренхимы
Метастатический колоректальный рак, билобарные метастазы в печени, двухэтапная резекция печени, alpps, острая печеночная недостаточность
Короткий адрес: https://sciup.org/140290433
IDR: 140290433 | DOI: 10.25881/20728255_2021_16_3_36
Two-stage liver resection ALPPS
Colorectal сancer is the third leading cause of cancer death in Russia. Upon initial detection of a tumor, synchronous liver metastases are detected in 30-50% of patients. Two-stage liver resection is often the only option for radical surgical treatment of patients with massive metastatic liver disease by preventing postresection liver failure. Objective: to assess the possibility of ALPPS liver resections in patients with colorectal cancer metastases. Material and methods. Extended hepatectomy according to the ALPPS was performed in 18 patients with massive bilobar liver lesions and with planned future liver remnants about
Текст научной статьи Двухэтапная резекция печени по методике ALPPS
Двухэтапная резекция печени по методике ALPPS (от англ. Associated Liver Partition and Portal vein ligation for Staged hepatectomy), впервые описанная Schnitzbauer A.A. в 2012 г. [1], рассматривается в качестве одного из возможных вариантов расширения радикального хирургического лечения больных с изначально недостаточным объемом остающейся части органа (FLR — future liver remnant) менее 30% с целью предупреждения развития острой печеночной недостаточности в послеоперационном периоде.
В качестве первого этапа операции ALPPS выполняется перевязка или клипирование правой ветви воротной вены и расщепление паренхимы печени вдоль серповидной связки до нижней полой вены. Как показали клинические наблюдения, развивающаяся при этом редукция портального кровотока в пораженной доле печени (за счет пересечения всех портальных сосудистых коллате-

ралей) провоцирует быструю гипертрофию остающейся паренхимы печени. По данным многих авторов минимальный показатель остаточного объема печени (FLR) в 30%, при котором значимо снижается риск развития острой печеночной недостаточности, может быть достигнут при применении данного хирургического приема уже в течение 9–14 суток, после этого допустимо основное хирургическое пособие — расширенная правосторонняя гемигепатэктомия вторым этапом [1–4].
В первых зарубежных публикациях при операциях АLPPS описывались достаточно высокие показатели частоты различных послеоперационных осложнений и летальности, достигавшие 66,7% и 28,7% соответственно [2; 5]. Однако с накоплением опыта, уточнением показаний и противопоказаний к данному хирургическому вмешательству, особенностей его технического выполнения, результаты операции претерпели значительные изменения. На сегодняшний день проведено одно рандомизированное контролируемое исследование LIGRO trial, анализирующее результаты расширенных резекций печени по методике ALPPS и по стандартной методике PVE/PVL (резекция печени после предварительной эмболизации или перевязки правой ветви воротной вены). Исследование включало в себя 100 больных (по 50 человек в каждой группе), лечившихся в 6 гепатобилиарных центрах. Результаты анализа показали, что в группе больных, оперированных по методике ALPPS, отмечено значимое увеличение степени прироста FLR (68±38% vs 36±18%), укорочение интервала между этапами операции (11±11 vs 43±15 суток), а также повышение частоты выполнения R0-резекции (72% vs 57%). Сопоставимыми оказались показатели 90-дневной летальности и частоты осложнений ≥3 уровня по Сlavien — Dindo [3].
Несмотря на свою привлекательность, расширенные двухэтапные резекции печени по методике ALPPS у больных с объемом остающейся части печени менее 30% пока не получили широкого применения. В нашей стране они представлены, главным образом, единичными наблюдениями [6-8] и только в одной работе анализируются непосредственные результаты 22 операций [4].
Цель . Оценить непосредственные и отдаленные результаты двухэтапных расширенных резекций печени по методике ALLPS у пациентов с метастазами колоректального рака и планируемым объемом остающейся паренхимы печени ≤30%.
Материал и методы
В период с 2017 по 2020 гг. в Санкт-Петербургском клиническом научно-практическом центре специализированных видов медицинской помощи (онкологический) было выполнено 316 резекций печени различного объема. Из них двухэтапная расширенная гемигепатэктомия по методике ALPPS была запланирована у 19 больных и реализована в полном объеме у 18 из них. Это составило 5,6% от общего числа пациентов, оперированных по поводу метастазов колоректального рака в печени.
Каждый больной из этой группы имел свои особенности по характеру и локализации первичной опухоли, давности и объему хирургического вмешательства. Но всех пациентов объединяло массивное метастатическое поражение правой доли печени и крайне малые размеры ее левой доли (FLR в пределах 18,7–22,7%). Реализация у них одномоментной правосторонней расширенной гемигепатэктомии имела высокий риск развития острой пострезекционной печеночной недостаточности. Разделение хирургического вмешательства в такой ситуации на два этапа, с целью предварительного достижения должного объема остающейся части печени, являлось вынужденной мерой (табл. 1).
В исследованную группу включены больные в возрасте от 39 до 73 лет (в среднем 61,7±8,4 год) с одиночными (n = 7) или множественными (n = 11) метастатическими узлами правой доли печени с распространением на IV сегмент. У 9 пациентов дополнительно имелись единичные (от 1 до 3) субкапсулярно расположенные метастазы во втором или третьем сегментах печени, позволявшие выполнить метастазэктомию без нанесения значимого ущерба объему остающейся части печени.
У 15 больных метастазы в печени были выявлены синхронно с первичной опухолью ободочной кишки, у 4 человек они диагностированы в среднем через 24 месяца (от 2 до 82 месяцев) после удаления первичной опухоли.
У 12 больных первичная опухоль была удалена до оперативного лечения метастазов в печени. У 6 пациентов решено провести симультанное оперативное вмешательство и сочетать удаление первичной опухоли кишки с первым этапом операции ALPPS. У одного из больных раком прямой кишки была избрана тактика «liver first ap-proach», и комбинированное лечение первичной опухоли запланировано после удаления метастазов в печени.
Одним из непременных условий проведения двухэтапных расширенных гемигепатэктомий по поводу метастазов колоректального рака в печени являлась эффективность предоперационной химиотерапии. В нашей группе предоперационная химиотерапия проведена 17 пациентам, из них 7 пациентам — в комбинации с таргетными препаратами (бевацизумаб, цетуксимаб, панитумумаб). В результате проведенного лечения у 12 больных отмечена стабилизация процесса, у 5 — частичный регресс (табл. 1).
Первый этап операции у 17 больных выполнялся из лапаротомического доступа по Starlz, у 2 — лапароскопическим способом. С целью исключения мелких метастазов в остающейся доле печени, не определявшихся ранее, производилось интраоперационное ультразвуковое исследование.
Операция включала в себя выделение, перевязку и пересечение правой воротной вены с расщеплением паренхимы печени (полным — у 13 пациентов, частичным — у 5 пациетов) вдоль серповидной связки при помощи биполярного коагулятора, ультразвукового
Табл. 1. Характеристика больных
|
N |
Возраст |
Пол |
Локализация первичной опухоли |
Удаление первичной опухоли |
Предшествующая химиотерпия |
Эффект химиотерапии |
Локализация метастазов (сегменты печени) |
Max диаметр метастазов (мм) |
|
1 |
54 |
ж |
Ободочная кишка |
ранее |
Folfoxiri + бевацизумаб №3 |
S |
SIV-V |
93 |
|
2 |
57 |
ж |
Сигмовидная кишка |
симультанно |
Folfoxiri №3, Folfiri + цетуксимаб №3 |
S |
SVI-VII-VIII |
57 |
|
3 |
66 |
м |
Сигмовидная кишка |
ранее |
Folfoxiri №3 |
S |
SVIII |
68 |
|
4 |
69 |
ж |
Слепая кишка |
ранее |
Капецитабин №6 |
S |
SVII, SV, SVI |
36, 46, 22 |
|
5 |
67 |
м |
Прямая кишка |
ранее |
Folfoх №3 |
S |
SV, SVI, SIV, SVII |
10, 13, 23, 47 |
|
6 |
59 |
м |
Ободочная кишка |
ранее |
Folfiri №9 |
S |
SVII-VI-VIII |
115 |
|
7 |
56 |
м |
Прямая кишка |
симультанно |
FOLFOX+бевацизумаб №9 |
PR |
SVI, SVI; SVI; SV; SV; SIVа; SVIII; SVIII; SVIII |
|
|
8 |
64 |
ж |
Сигмовидная кишка |
ранее |
FOLFOX + бевацизумаб №3 |
PR |
SVII-VI-V |
70 |
|
9 |
69 |
ж |
Ободочная кишка |
ранее |
Folfox + бевацизумаб №6 |
PR |
SVII; SII, SIII; SIII |
69, 32, 30, 10 |
|
10 |
61 |
м |
Сигмовидная кишка |
ранее |
FOLFOX №3 |
S |
SVIII-VI-V |
80 |
|
11 |
39 |
ж |
Сигмовидная кишка |
симультанно |
FOLFOXIRI №3 |
S |
SV-VI-VIII; SII |
23, 7 |
|
12 |
64 |
м |
Сигмовидная кишка |
ранее |
FOLFOX №4, капецитабин №5 |
S |
SVIII — SIVa |
48 |
|
13 |
58 |
ж |
Прямая кишка |
ранее |
FOLFOX №5 |
S |
SVI-VII-VIII |
98 |
|
14 |
57 |
м |
Сигмовидная кишка |
симультанно |
Folfox №3, Folfox + Эрбиткус №3 |
S |
SVIII, SIVa, SVII, SII |
37,5; 23; 20; 22 |
|
15 |
68 |
м |
Прямая кишка |
liver first approach * |
FOLFIRI/6 |
S |
SVI, SIII, SIV |
67, 10, 13 |
|
16 |
73 |
ж |
Ободочная кишка |
ранее |
FOLFOX+Бевацизумаб №3 |
PR |
SV-VI-VII, SIII |
14, 8 |
|
17 |
52 |
ж |
Сигмовидная кишка |
симультанно |
FOLFOX+панитумумаб №3, mFOLFOXIRI №3+ панитумумаб №5 |
PR |
SV-VI-VII-VIII с переходом на SIV, SII, SIII |
98х102 |
|
18 |
61 |
м |
Прямая кишка |
ранее |
– |
– |
SV-VI-VII-VIII |
128х105 |
Примечание : S — стабилизация, PR — частичный регресс, * liver first approach — удаление метастазов колоректального рака в печени до хирургического лечения первичной опухоли.
диссектора и методики crash clamp (раздавливание паренхимы печени зажимом) с параллельной перевязкой и пересечением трубчатых структур. Связочный аппарат печени не разрушался.
У 9 больных параллельно были удалены субкапсулярные метастазы из остающейся части печени: у 8 пациентов выполнена атипичная резекция S2 или S3, а у одного — лапароскопически-ассистированная микроволновая абляция метастатического очага. В завершении операции по линии транссекции паренхимы печени укладывалась гемостатическая губка Surgicel, в подпеченочное пространство устанавливалась дренажная трубка.
Шести пациентам одновременно была удалена первичная опухоль с формированием кишечного анастомоза: у 4 — резекция сигмовидной кишки, у 1 — передняя резекция прямой кишки, у 1 — правосторонняя гемиколэктомия, при этом лапароскопический доступ использовался у 2 пациентов.
Второй этап операции выполнялся по достижению остающейся частью печени не менее 30% от общего ее объема по данным КТ-волюмометрии, нормализации биохимических показателей функции печени (трансаминазы, билирубин, белок, коагулограмма) и при отсутствии прогрессирования заболевания. Это оказалось возможным у 18 из 19 больных. У 1 пациента констатировано прогрессирование основного заболевания (появление новых метастазов в остающейся паренхиме печени), и от второго этапа операции решено было воздержаться.
Второй этап операции в объеме расширенной правосторонней гемигепатэктомии в сочетании со стандартной лимфодиссекцией выполнялся посредством лапаротом-ного доступа по Starlz. Отличительные особенности этого этапа операции заключались в следующем. Практически у всех больных имелся выраженный спаечный процесс вокруг печени и непосредственно в зоне транссекции паренхимы печени, нередко с наличием осумкованного жидкостного скопления в этой области. Это затрудняло доступ к гепатодуоденальной связке, нижней полой вене, окончательному разобщению удаляемой и остающейся частей печени. Сложности операции особенно возрастали при частично выполненном расщеплении паренхимы печени на первом этапе операции. В условиях развившегося спаечного процесса окончательное завершение этого этапа операции сопровождалось значительной кровопотерей. Кроме того, гипертрофия левой доли печени влекла за собой уменьшение размеров операционного поля, что затрудняло выделение и перевязку коротких вен печени. Вследствие этого у отдельных больных лигирование данных сосудов приходилось проводить не по стандартной методике, а через зону транссекции паренхимы печени. Кроме того, за счет гипертрофии левой доли печень ротировалась относительно нижней полой вены, что влекло за собой поворот по оси гепатодуоденальной связки с
изменением типичной синтопии ее элементов. Это также затрудняло выделение правого желчного протока и одноименной печеночной артерии. У одного из пациентов это повлекло за собой нарушение пассажа желчи в двенадцатиперстную кишку с развитием желтухи.
Послеоперационные осложнения оценивались по шкале Clavien-Dindo, печеночная недостаточность и формирование желчной фистулы — согласно рекомендациям International Study Group of liver Surgery (ISGS).
Результаты и обсуждение
Длительность первого этапа операции составила 166±55,8 мин. при лапаротомическом доступе и 130±14,1 мин. — при лапароскопическом; при симультанных операциях продолжительность вмешательства составила 215±8,6 мин. Средняя кровопотеря — 170,9±87,8 мл. Показатели АЛТ и АСТ на следующий день после операции составляли, соответственно, 422,6±260,9 Ед/л и 476,3±267,3 Ед/л, на 6 сутки после первого этапа операции — 194,7±219,5 и 129,0±170,3 Ед/л. Нормализация биохимических показателей в среднем происходила в течение 10,9 суток (от 6 до 16 суток). Послеоперационные осложнения развились у 2 больных: формирование наружного желчного свища со «скудным» отделяемым, не потребовавшего хирургического вмешательства (grade B по критериям ISGLS) и несостоятельность кишечного анастомоза после симультанной операции (передняя резекция прямой кишки), по поводу чего сформирована илеостома (табл. 2).
Гипертрофия остающейся части печени до минимального показателя 30% по отношению к общему объему печени, по литературным данным, наступает в течение 9–11 суток после первого этапа операции. По мнению многих авторов по истечение данного периода допустим второй этап операции [1; 3; 4].
Наше отношение к раннему выполнению второго этапа операции было весьма сдержанным и объяснялось отсутствием опыта таких вмешательств и достоверных
Табл. 2. Структура осложнений у пациентов после ALPPS резекции (n = 18)
|
Степень осложнения по Clavien–Dindo |
Характер осложнения |
Число осложнений |
|
|
На первом этапе |
На втором этапе |
||
|
I |
Желчная фистула |
1 |
3 |
|
II |
– |
– |
– |
|
III a III b |
Стриктура холедоха |
– |
1 |
|
Несостоятельность кишечного анастомоза |
1 |
– |
|
|
Кровотечение из края резекции печени |
– |
1 |
|
|
IV |
ОППН |
– |
1 |
|
V |
ОППН |
– |
1 |
|
Всего |
2 |
7 |
|
Примечание : ОППН — острая пострезекционная печеночная недостаточность.
критериев функционального статуса остающейся части печени, стремлением к максимальному снижению степени риска развития печеночной недостаточности в послеоперационном периоде. Поэтому к решению вопроса о возможности второго основного этапа операции мы подходили не ранее 3–4 недель после первого этапа. В среднем расширенная правосторонняя гемигепатэк-томия выполнялась нами через 58,2±26,7 суток после первого этапа (от 28 до 120 суток). Средняя величина гипертрофии остающейся ткани печени к этому сроку составила 85,2±8,5%, а отношение остающегося объема печени (FLR — future liver remnant) к ее общему объему печени (TLV — total liver volume) по данным КТ-волюмо-метрии увеличилось в среднем с 21,06±2,4% до 33,1±2,8% (табл. 3, Рис. 1).
При этом одним из факторов, влиявшим на скорость гипертрофии остающейся паренхимы, являлась полнота выполнения транссекции печени. Так, при неполном способе расщепления печеночной ткани интервал между двумя этапами операции увеличивался примерно вдвое по сравнению с полной транссекцией (90,6 vs 45 суток соответственно). У 1 больного при неполном расщеплении печени процесс гипертрофии оставшейся части печени и вовсе отсутствовал. По истечении 30, 45 и 60 суток отношение FLR к TLV продолжало оставаться в пределах 20,5%. В этом случае была предпринята дополнительная эмболизация шунтирующих вен. Однако желаемого эффекта по истечении 20 суток также не было достигнуто (FLR2/TLV = 24,0%). Тогда решено было выполнить
Табл. 3. Оценка прироста остающейся ткани печени, объема гипертрофии и интервала между этапами ALPPS резекции
|
№ |
FLR1 (мл) |
FLR1/ TLV, % |
FLR2 (мл) |
FLR2/ TLV, % |
Гипертрофия, % |
Интервал между этапами (сутки) |
|
1 |
299 |
19 |
530 |
30,6 |
77 |
78 |
|
2 |
247 |
22 |
470 |
35,5 |
90 |
45 |
|
3 |
238 |
19,6 |
462 |
32,2 |
94 |
57 |
|
4 |
343 |
20,5 |
617 |
31,7 |
80 |
84 |
|
5 |
273 |
21 |
508 |
33 |
86 |
76 |
|
6 |
211 |
20 |
399 |
32,2 |
89 |
28 |
|
7 |
236 |
20,5 |
412 |
31 |
74 |
120 |
|
8 |
327 |
19,2 |
624 |
31,2 |
91 |
69 |
|
9 |
290 |
18,7 |
490 |
28 |
67 |
95 |
|
10 |
243 |
22 |
417 |
32,7 |
71 |
39 |
|
11 |
273 |
22,7 |
510 |
35,5 |
87 |
28 |
|
12 |
239 |
22,7 |
415 |
33,8 |
73 |
30 |
|
13 |
255 |
21 |
457 |
32,6 |
79 |
37 |
|
14 |
269 |
18,5 |
533 |
31 |
98 |
69 |
|
15 |
262 |
19,4 |
487 |
30,9 |
86 |
68 |
|
16 |
269 |
19,2 |
532 |
32 |
98 |
65 |
|
17 |
315 |
27,3 |
560 |
40 |
78 |
32 |
|
18 |
252 |
25,7 |
473 |
39,4 |
88 |
28 |
Примечание : FLR1 — исходный объем остающейся ткани печени, FLR2 — объем остающейся ткани печени после первого этапа ALPPS, TLV — общий объем печени, TLV1 — общий исходный объем печени.

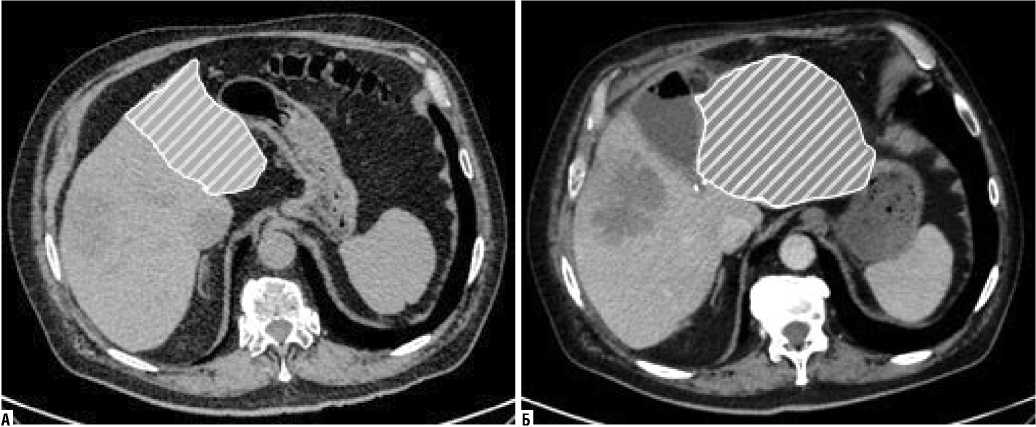
Рис. 1. Иллюстрация снимка компьютерной томографии печени до и после первого этапа ALPPS резекции. А — исходный размер остающейся части печени (заштриховано); Б — Размер остающейся части печени через 28 дней после первого этапа ALPPS (заштриховано).
повторное расщепление паренхимы печени, но теперь уже в полном объеме, до ретропеченочного сегмента нижней полой вены. При контрольном исследовании на 28 сутки после операции по данным КТ-волюмометрии зарегистрировано увеличение объема оставшейся ткани печени до 35% по отношению к общему объему печени. У этого больного интервал между этапами операций составил 120 суток.
Продолжительность второго этапа операции в среднем составила 213,2±90,2 мин. Средняя величина кровопотери составила 546,4±207,7 мл. Более высокая степень кровопотери (около 1000 мл) наблюдалась среди больных, у которых на первом этапе было выполнено частичное расщепление паренхимы печени между ее частями (у 3 из 5 человек). Окончательное разделение печеночной ткани в условиях развившегося спаечного процесса сопровождалось более высокой кровопотерей. У 2 больных она составила 1700 и 3000 мл и была связана, в одном случае, с нарушением целостности нижней полой вены при мобилизации коротких вен печени, а в другом — с краевой резекцией нижней полой вены из-за инвазии опухолевого узла в устье правой печеночной вены. Всем больным выполнена R0 резекция.
Показатели АЛТ и АСТ по истечении первых суток составляли 280,4±153,6 и 246,9±106,9 Ед/л, соответственно, на 6 сутки — 76,7±49,5 и 49,9±35,3 Ед/л, соответственно. Полная нормализация биохимических показателей печени колебалась в пределах 4–13 суток (в среднем 8 суток).
Послеоперационные осложнения второго этапа развились у 7 больных (39,0%). При этом осложнения ≥3а степени по Clavien-Dindo — у четырех из них (23,5%). Прежде всего, не удалось избежать острой печеночной недостаточности и она последовала у двух оперированных (grade С по критериям ISGLS). У 1 пациента наблюдалось кровотечение из зоны расщепления печени (релапаротомия, остановка кровотечения электрокоагуляцией, гемостатическими губками). У 3 больных сформировались желчные фистулы со cкудным отделяемым (grade B по критериям ISGLS), не повлиявших на исход лечения. В одном случае наблюдался перекрут печеночнодвенадцатиперстной связки с нарушением пассажа желчи в двенадцатиперстную кишку (наружное дренирование общего желчного протока) (табл. 2).
Умерла 1 больная (5,5%) на вторые сутки после расширенной правосторонней гемигепатэктомии от острой пострезекционной печеночной недостаточности. Нам представляется, что причиной ее развития явилось преждевременное выполнение второго этапа операции. Несмотря на то, что прошло 95 суток после первого этапа и биохимические показатели крови нормализовались, объем остающейся паренхимы печени составлял 28%, а степень гипертрофии составила 67%, что ниже средних показателей по этой группе больных (33,1±2,8% и 82,8%, соответственно).
Прогрессирование заболевания в виде появления метастазов в оставшейся ткани печени и/или в легких в течение первого года после операции отмечено у 10 из 17 больных (58,8%), при этом общая выживаемость в течение года составила 66,6%.
Обсуждение
Собственный опыт первых операций по методике ALPPS свидетельствует о том, что расщепление паренхимы печени по междолевой борозде с пересечением внутрипеченочных венозных коллатералей и перевязкой ветви воротной вены пораженной доли приводит к усилению регенеративных способностей остающейся паренхимы печени и более быстрой ее гипертрофии. При этом на начальном этапе накопления клинического

опыта мы практиковали частичную транссекцию ткани печени. Однако в дальнейшем мы убедились, что частичная транссекция, с одной стороны, часто не приводила к должной гипертрофии остающейся части органа, а с другой стороны — создавала повышенные трудности при выполнение второго этапа операции ввиду последующего развития спаечного процесса, что нередко влекло за собой излишнюю кровопотерю. Учитывая эти обстоятельства, мы в последующем полностью отказались от частичного расщепления печеночной ткани между долями печени в пользу полной транссекции до ретропеченочного сегмента нижней полой вены.
Эффективная гипертрофия FLR способствует расширению возможностей выполнения радикальных резекций у пациентов с изначально нерезектабельными или условно резектабельными метастазами в печени. Доля таких больных среди прооперированных нами пациентов с метастазами колоректального рака в печени составила 5,62%. При этом частота послеоперационных осложнений и летальности сопоставима со стандартными двухэтапными резекциями печени [9–11]. Это дает основание рассматривать методику ALPPS в качестве перспективного направления в лечебном алгоритме предупреждения острой пострезекционной печеночной недостаточности у больных с изначально недостаточным FLR (менее 30%).
Дальнейший прогресс во внедрении этой методики мы связываем с разработкой четких критериев оценки функции остающейся ткани печени для точного расчёта безопасных сроков выполнения второго, основного этапа операции у конкретного пациента. Определение оптимального интервала между этапами операции только на основании объемных характеристик остающейся паренхимы печени является недостаточным и небезопасным. Оценка функционального статуса ткани печени также позволит сократить интервал между этапами операции, при этом ожидаемы меньшая выраженность рубцовоспаечного процесса и, соответственно, снижение длительности этапа мобилизации печени и выделения структур гепато-дуоденальной связки на основном этапе [4].
Первостепенной задачей остается также разработка критериев отбора пациентов для данного хирургического вмешательства с целью минимизации риска прогрессирования заболевания в раннем послеоперационном периоде. По данным большинства авторов, безрецидивная выживаемость в течение 1 года у этих больных не превышает 50% [9]. В нашей группе оперированных пациентов этот показатель составил 38,6%.
Заключение
В настоящее время операция ALPPS, бесспорно, продолжает оставаться «вынужденным» вмешательством, но для ряда пациентов оно может стать единственным способом выполнения радикальной операции при нере-зектабельных или погранично резектабельных метастазах колоректального рака в печени.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Двухэтапная резекция печени по методике ALPPS
- Schnitzbauer AA, Lang SA, Goessmann H, et al. Right portal vein ligation combined with in situ splitting induces rapid left lateral liver lobe hypertrophy enabling 2-staged extended right hepatic resection in small-for-size settings. Ann Surg. 2012; 255(3): 405-414. doi: 10.1097/SLA.0b013e31824856f5.
- Nadalin S, Capobianco I, Li J, et al. Indications and Limits for Associating Liver Partition and Portal Vein Ligation for Staged Hepatectomy (ALPPS). Lessons Learned from 15 Cases at a Single Centre. Zeitschrift Für Gastroenterologie. 2014; 52(01): 35-42. doi: 10.1055/s-0033-1356364.
- Per Sandström, Bärd I R0sok, Ernesto Sparrelid, et al. ALPPS Improves Resectability Compared With Conventional Two-stage Hepatectomy in Patients With Advanced Colorectal Liver Metastasis Results From a Scandinavian Multicenter Randomized Controlled Trial (LIGRO Trial). Ann Surg. 2018; 267(5): 833-840. doi: 10.1097/SLA.0000000000002511.
- Восканян С.Э., Чучуев Е.С., Артемьев А.И. и др. Associating Liver Partition and Portal vein Ligation for Staged hepatectomy (ALPPS) в лечении очаговых образований печени // Хирургия. Журнал им. Н.И. Пирогова. —2018. — №2. — С.39-44. [Voskanyan SE, Chuchuyev ES, Artemiyev AI. et al. Associating Liver Partition and Portal vein Ligation for Staged hepatectomy (ALPPS) in focal liver diseases management. Pirogov Russian Journal of Surgery. 2018; 2: 39-44. (In Russ).] doi: 10.17116/hirurgia2018239-44.
- Dokmak S, Belghiti J. Which Limits to the «ALPPS» Approach. Ann Surg. 2012; 256(3): e6. doi: 10.1097/sla.0b013e318265fd64.
- Чайченко Д.В., Надвигова Е.А., Важенин А.В. и др. Непосредственные результаты применения ALPPS-процедуры у пациентов с обширным метастатическим поражением печени // Российский онкологический журнал. — 2014. — 19(4). — С.51-52. [Chaychenko DV, Nadvigova EA, Vazhenin AV, Privalov AV. Immediate results of the ALPPS procedure in patients with extensive metastatic liver disease. Russian Journal of oncology. 2014; 19(4): 51-52. (In Russ).]
- Скипенко О.Г., Чардаров Н.К., Багмет Н.Н. и др. ALPPS — новая возможность двухэтапного хирургического лечения больных с метастазами рака толстой кишки // Хирургия. — 2014. — №9. — С. 23-29. [Ski-penko OG, Chardarov NK, Bagmet NN, et al. Associated liver partition and portal vein ligation for staged hepatectomy (ALPPS) — new opportunity in two-stage liver resection in patients with colorectal cancer metastases. Khirurgiia. 2014; 9: 23-29. (In Russ).]
- Козырин И.А., Ермаков Н.А., Лядов В.К., Коваленко З.А. Опыт двух-этапной резекции печени (ALPPS) // Хирургия. Журнал им. Н.И. Пирогова. — 2014. — №12. — С.24-28. [Kozyrin IA, Ermakov NA, Lyadov VK, Kovalenko ZA. Experience of two-staged liver resection (ALPPS). Pirogov Russian Journal of Surgery. 2014; 12: 24-28. (In Russ).]
- Dimitri A. Raptis, Michael Linecker, Patryk Kambakamba, et al. Defining Benchmark Outcomes for ALPPS. Ann Surg. 2019; 270(5): 835-841. doi: 10.1097/SLA.0000000000003539.
- Liu Y, Yang Y, Gu S, Tang K. A systematic review and meta-analysis of associating liver partition and portal vein ligation for staged hepatectomy (ALPPS) versus traditional staged hepatectomy. Medicine. 2019; 98(15): e15229. doi: 10.1097/MD.0000000000015229.
- Pim B. Olthof, Andreas A. Schnitzbauer, Erik Schadde. The HPB controversy of the decade: 2007-2017 — Ten years of ALPPS. Eur J Surg Oncol. 2018; 44(10): 1624-1627. doi: 10.1016/j.ejso.2018.06.005.


