Факторы риска геморрагической трансформации инфаркта головного мозга
Автор: Батищева Е.И., Кузнецов Алексей Николаевич
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Статья в выпуске: 1 т.4, 2009 года.
Бесплатный доступ
Обследованы 239 пациентов с ишемическим инсультом. Проанализированы возможные факторы риска цереброваскулярной патологии.
Инфаркт головного мозга, геморрагическая трансформация, факторы риска
Короткий адрес: https://sciup.org/140187723
IDR: 140187723 | УДК: 616-005.8:612.116.2(063)
Текст научной статьи Факторы риска геморрагической трансформации инфаркта головного мозга
Геморрагическая трансформация (ГТ) инфаркта головного мозга на протяжении последних 100 лет изучалась в основном зарубежными исследователями. Fisher and Adams в 50-х годах XX века предложили свою широко известную гипотезу о реканализации артерии при церебральной кардиоэмболии, которая устанавливала взаимосвязь между самостоятельным разрушением эмбола и последующей ГТ области инфаркта [8]. Несколько позднее Globus, Epstein and Faris оспорили данную теорию и указали, что интраишемическое кровоизлияние наиболее возможно при сочетании стойкой закупорки сосуда и сохраненном коллатеральном потоке внутрь зоны, пораженной ишемией, особенно если пациент пережил короткий период повышенного артериального давления (АД) [7, 9]. На сегодняшний день доказано, что артериальная реканализация не является обязательным условием для возникновения ГТ инфаркта мозга [19].
Достаточно широко представлены в литературе публикации, посвященные изучению влияния кардиоэмболического инсульта на развитие последующей геморрагической конверсии [1, 2, 3, 6, 7, 19]. В качестве факторов риска ГТ также указывались возраст, сахарный диабет в анамнезе, наличие ранних ишемических изменении во время нейровизуализации, обширность области инфаркта, отек мозговой паренхимы, тяжесть инсульта, лейкоареоз и другие [4, 6, 10, 13, 16, 17, 20].
В настоящее время в связи с активным внедрением в клиническую практику тромболитического лечения инсульта и довольно высокой частотой развития в процессе такого лечения клинически значимых интраишемических кровотечений интерес к факторам риска ГТ инфаркта переживает свое второе рождение. Наиболее хорошо изученные возможные причины возникновения ГТ легли в основу официально утвержденных противопоказаний к использованию тромболизиса [4]. Вне тромболитического лечения ГТ области ишемии возникает довольно часто. По данным КТ интраишемическое кровотечение сопровождает инфаркт в 43–50% случаев [6, 19, 22]. А по результатам МРТ в случае кардиоэмболического инсульта в каротидном бассейне ГТ обнаруживаются у 70% больных [12].
Пациенты и методы исследования
Проведено обследование 239 пациентов с ишемическим инсультом (ИИ) головного мозга в остром периоде, находившихся на лечении с 2004 по 2007 годы. Все обследованные больные (n=239) были разделены на две группы: пациенты с ИИ головного мозга – Группа А (n=164); пациенты, перенесшие ИИ с геморрагической трансформацией ишемического очага – Группа Б (n=75). Нейровизуализацию (КТ и/или МРТ) выполняли на 1-ый, 2-ой и 21-ый дни заболевания, а при ухудшении состояния – внепланово. КТ проводили на аппаратуре Somatom Sensation (Siemens), Hi Speed NX/ I (General Electric). Для МР-исследования пользовались оборудованием Giroscan INTERA NOVA (Toshiba), Signa Infinity (General Electric) с напряжением магнитного поля 1,5 и 1 Тесла, соответственно.
Проанализированы возможные факторы риска цереброваскулярной патологии. Для этого использовали данные амбулаторной медицинской документации и расширенной стационарной программы клинико-инструментального обследования. Особое внимание уделяли мониторированию систолического и диастолического АД в течение первых двух суток от дебюта инсульта. Для этого пациентам измеряли АД 5 раз в день. Максимальное систолическое и диастолическое АД, зафиксированное в 1-е и 2-е сутки заболевания, было включено в анализ.
Сосудистую визуализацию осуществляли посредством ультразвукового триплексного сканирования экстра- и интракраниальных артерий, КТ-ангиографии и/или МР-ангиографии, в ряде случаев – инвазивной церебральной ангиографии с оценкой степени стено-ок-клюзирующего поражения церебральных артерий, структуры атеросклеротической бляшки. При необходимости сопровождали вышеописанное исследование эмболоде-текцией. Для выявления кардиальной патологии наряду с традиционной ЭКГ выполняли трансторакальную и/или трансэзофагеальную ЭхоКГ, позволявшую детектировать наличие потенциальных источников эмболии клапанного и неклапанного происхождения.
Среди лабораторных исследований обращали внимание на состояние системы свертывания крови, липидный спектр, отдельные показатели биохимического анализа крови (глюкоза, мочевина, креатинин).
Установление подтипа ИИ проводили согласно критериям TOAST с делением на кардиоэмболический инсульт (КЭ), инсульт вследствие атеросклероза крупных артерий (АТ), инсульт вследствие окклюзии артерий мелкого калибра (лакунарный инсульт, ЛА), инсульт другой известной этиологии (вследствие патологии крови, васкулита, диссекции артерии и т.д., ДЭ) и инсульт неясного генеза (НЭ).
В определении размеров ИИ пользовались классификацией Научного центра неврологии РАМН, в соответствии с которой выделяли: обширные инфаркты, распространяющиеся на весь бассейн одной из магистральных артерий головы; большие – распространяющиеся на весь бассейн одной из церебральных артерий или бассейн крупных ветвей позвоночных или базилярной артерии; средние – возникающие в пределах бассейна отдельных ветвей этих артерий; лакунарные – небольшие очаги размером 5–15 мм в диаметре.
Результаты
Произведено сопоставление размеров ишемической области в обследованных группах. (Рис. 1).
Установлено, что обширные и большие инсульты достоверно чаще сопровождались геморрагической трансформацией и были зарегистрированы соответственно в 33,3% и 53,4% случаев среди пациентов с ГТ инфаркта и только у 6,7% и 20,7% пациентов группы А (p<0,0001 и
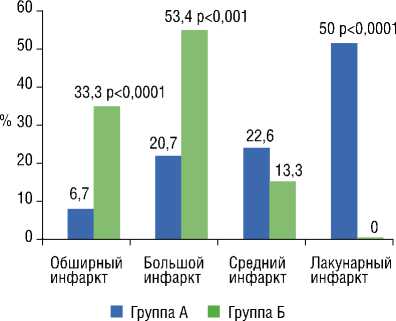
Рис. 1. Частота встречаемости инфарктов головного мозга различных размеров среди пациентов группы А и группы Б p<0,001). Инсульты среднего размера незначительно преобладали в группе с ИИ без геморрагии. ЛА обнаружены исключительно у больных группы А (50% против 0%; p<0,0001).
Так как, помимо обширности ишемического поражения, весомое значение для развития интраишеми-ческого внутричерепного кровотечения может иметь тяжесть инсульта в дебюте заболевания, нами сопоставлен функциональный и неврологический статус в дебюте заболевания у пациентов с наличием и отсутствием ГТ. Результаты данной оценки приведены в таблице 1.
Пациенты с развившейся впоследствии ГТ инфаркта головного мозга имели в дебюте заболевания более выраженный неврологический дефицит по Шкале NIHSS (11,5 ± 6,0 против 7,9 ± 4,1; p<0,0001), более глубокий уровень угнетения сознания (13,7 ±2 ,2 против 14,4 ± 1,6; p<0,0001) и худший функциональный статус (3,8 ± 1,1 против 3,1 ± 0,8; p<0,0001).
Достаточно наглядный результат дает сопоставление частоты встречаемости в 1-е сутки инсульта легко выраженных, умеренных и выраженных изменений неврологического статуса и уровня угнетения сознания в изучаемых группах пациентов. ГТ развивались достоверно чаще при первоначальном уровне неврологического дефицита более 15 баллов по Шкале NIHSS (p<0,001) и угнетении уровня сознания до степени оглушения (p<0,0001) и комы (p<0,01).
В результате исследования предрасположенности того или иного подтипа ИИ к последующей ГТ установлено, что наиболее подверженным геморрагической конверсии является кардиоэмболический инфаркт, частота встречаемости которого с высокой достоверностью (p<0,0001) превалировала среди больных с ГТ. Напротив, лакунарный подтип наблюдался исключительно в группе А (p<0,00001), где составил почти третью часть. Атеро-тромботический инсульт одинаково часто встречался среди обеих групп и составил 18,3% и 18,7%, соответственно. Неуточненным характер инсульта оставался достоверно чаще среди пациентов без ГТ (19,5% против 10,6%; p<0,001), а инсульт ДЭ был зафиксирован в единичных случаях в обеих группах (1,8% и 5,5%) (Рис. 2).
Табл. 1. Неврологический и функциональный статус пациентов в 1-е сутки заболевания
|
Признак |
Группа А Больные, перенесшие ишемический инсульт (n=164) (M±m) |
Группа Б Больные, перенесшие ишемический инсульт с ГТ (n=75) (M±m) |
|
Клиническое состояние и функциональный статус пациента в 1-е сутки заболевания: |
||
|
Шкала NIHSS |
7.9±4.1 |
11.5±6,0**** |
|
Шкала Глазго |
14.4±1.6 |
13.7±2.2**** |
|
Шкала Ранкина |
3.1±0.8 |
3.8±1.1**** |
***** p<0,00001;
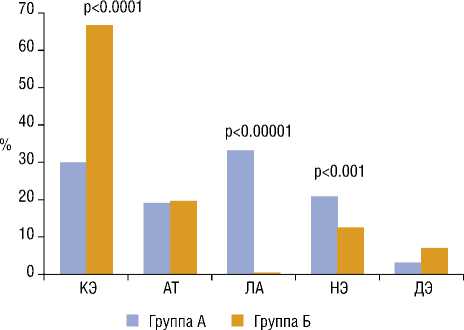
Рис. 2. Частота различных подтипов ИИ среди пациентов с ИИ без вторичной геморрагии (Группа А) и среди пациентов с ГТ ИИ (Группа Б)
Учитывая большую представленность кардиоэмболии как причинного фактора данного ишемического события была проведена оценка частоты встречаемости тех или иных имеющихся потенциальных источников эмболии среди больных групп А и Б и возможное их участие в развитии последующей геморрагии (Табл. 2).
Установлено, что группы достоверно не различались по частоте диагностирования пароксизмальной формы мерцательной аритмии, инфаркта миокарда, патологии клапанного аппарата сердца, других источников кар-диоцеребральной эмболии. Только постоянная форма мерцательной аритмии обнаружила достоверно большую представленность среди больных с ГТ ишемического инфаркта головного мозга. Она диагностировалась почти у каждого третьего пациента группы с ГТ ишемического очага – 23 (30,7%), и намного реже наблюдалась среди больных группы А – 22 (13,4%; p<0,01). Кроме того, обращает на себя внимание тот факт, что имеющиеся кардиогенные источники с потенциальным образованием
Табл. 2. Частота встречаемости различных потенциальных источников кардиоцеребральной эмболии среди обследованного контингента
Интересной оказалась взаимозависимость мерцательной аритмии и последующего формирования более обширной геморрагии. Так, у больных с постоянной формой мерцательной аритмии частота возникновения паренхимальных гематом почти в два раза превышала частоту возникновения геморрагических инфарктов (p<0,05).
Результаты оценки других факторов риска цереброваскулярной патологии продемонстрировали отсутствие достоверных различий в анамнезе среди пациентов с ИИ и пациентами с ГТ в частоте диагностирования гипертонической болезни, болезней крови. Сахарный диабет незначительно превалировал среди больных группы А, однако различия между группами были недостоверны (p>0,05) (Табл. 3).
Установлена обратная корреляционная связь между гиперхолестеринемией в анамнезе и будущим развитием ГТ (57,9% против 37,3%; p<0,01). Кроме того, гиперхолестеринемия диагностирована у 22 (43,1%) больных с геморрагическим инфарктом и у 6 (25%) пациентов с паренхимальной гематомой. Также ГТ развивались чаще у пациентов, имеющих церебральные сосудистые события в анамнезе (p<0,01). Зафиксированный нами уровень систолического и диастолического АД в 1-е и 2-е сутки инсульта был существенно выше у пациентов с развившимся впоследствии интраишемическим кровотечением (Табл. 3). Уровень диастолического АД также оказался значимым в развитии паренхимальной гематомы (107,1 мм рт.ст. против 98,3 мм рт.ст; p<0,05).
С помощью модели logit-регрессии произведено выделение наиболее значимых предикторов ГТ. В качестве зависимой переменной мы рассматривали вероятность возникновения ГТ, а в качестве независимых переменных следующие факторы риска.
-
1. Подтип ИИ (бинарная) (х1). За подтип ИИ «1» принимали кардиоэмболический инфаркт; за подтип ИИ «0» – принимали атеротромботический, лакунарный, инсульт другой уточненной причины либо недифференцированный инсульт.
-
2. Наличие ИИ, ТИА в анамнезе (бинарная) (х2). За «1» принимали наличие ИИ, ТИА в анамнезе, за «0» – их отсутствие.
-
3. Размер зоны ИИ (бинарная) (х3). За «1» принимали обширный размер инфарктной зоны у пациента, за «0» – меньшие размеры инфарктов.
-
4. NIHSS (х4) – цифровое выражение тяжести неврологического дефицита, измеренное по шкале NIHSS.
-
5. Наличие сахарного диабета в анамнезе (бинарная) (х5). За «1» принимали наличие сахарного диабета в анамнезе, за «0» – его отсутствие.
Полученная в результате logit-регрессии математическая модель (Рис. 3) позволяет в 92,1% случаев правильно
Табл. 3. Частота встречаемости факторов риска цереброваскулярной патологии
|
Признак |
Группа А Больные, перенесшие ишемический инсульт (n=164) |
Группа Б Больные, перенесшие ишемический инсульт с ГТ (n=75) |
|
Гипертоническая болезнь в анамнезе |
137 (83.5%) |
63 (84%) |
|
Болезни крови в анамнезе |
4 (2.4%) |
2 (2.6%) |
|
Сахарный диабет в анамнезе |
39 (23.8%) |
12 (16%) |
|
Гиперхолестеринемия |
95 (57,9%)** |
28 (37,3%) |
|
Ранее перенесенные церебральные сосудистые события (ТИА, инсульты) |
19,5% |
37,3%** |
|
АД систолическое максимальное в 1-е и 2-е сутки |
144,6 ± 29,1 |
180,9 ± 37,6**** |
|
АД диастолическое максимальное в 1-е и 2-е сутки |
96,6 ± 12,8 |
100,9 ± 20,1* |
*p<0,05; ** p<0,01; *** p<0,001; **** p<0,0001;
предсказать развитие ИИ головного мозга без последующей ГТ, и в 32,8% случаев верно установить последующее развитие интраишемической геморрагии.
По итогам статистического анализа можно сделать вывод, что наличие кардиоэмболического подтипа инсульта увеличивает риск развития ГТ. Причем наибольшая реализация данного фактора происходит в случае инсультов незначительной и умеренной тяжести, где риск возрастает почти вдвое. В случае выраженной тяжести инсульта вероятность геморрагической конверсии при других подтипах инсульта почти сравнивается с кардиоэмболическим.
Обсуждение
Обширность ишемической зоны – это первый потенциальный предиктор развития ГТ, изученный нами и показавший свою значимость. Убедительное превалирование обширных и больших инсультов среди пациентов
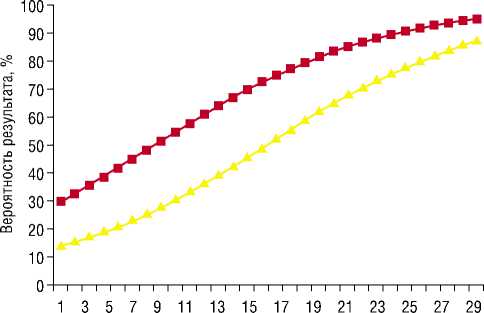
NIHS
-■- Подтип ИИ=1 Подтип ИИ=0
Рис. 3. Графическое выражение модели logit-регрессии с развившейся ГТ закономерно. Большой размер ишемической зоны увеличивает вероятность возникновения патологически повышенной проницаемости стенок сосудов и степень ишемической васкулопатии, в том числе с некрозом сосудистой стенки, что индуцирует развитие интраишемического кровотечения [6, 7, 12, 17, 20, 23].
В корреляции с обширностью области ишемии находится тяжесть неврологического дефицита. Khatry P. et al. называют первоначальную тяжесть инсульта главным предвестником клинически значимой ГТ [17]. По мнению зарубежных исследователей ГТ преимущественно сопровождают инсульты умеренной и выраженной тяжести (со значением шкалы NIHSS >15) [15]. Нами получены аналогичные результаты.
Установленный в результате проведенного исследования весомый вклад кардиоэмболии в последующее развитие ГТ еще раз указывает на значимость данного фактора в геморрагической конверсии. Наличие ГТ инфаркта мозга много ранее описывалось исследователями как паттерн КЭ [8, 11]. Сопоставимая частота встречаемости атеротромботического подтипа инсульта в группе пациентов с ИИ и в группе с ГТ согласуется с мнением Hart и Easton, что при артерио-артериальной эмболии и гемодинамических инфарктах «водораздела», развивающихся при наличии гемодинамически значимых стенозов церебральных артерий, степень ишемии недостаточна для такого нарушения проницаемости сосудистой стенки, которое приводит к ГТ [11].
Обращает на себя внимание состав потенциальных источников кардиогенной церебральной эмболии при развитии ГТ. Отмечается заметное преобладание источников с потенциальным образованием красных тромбов в полостях сердца – это постоянная и пароксизмальная формы мерцательной аритмии, инфаркт миокарда, в совокупности составившие более 60%. В основе образования красных тромбов лежит стагнация крови в полостях сердца с последующей активацией каскадов коагуляции [1, 2, 3]. Образование красных тромбов, а также активация собственной тромболитической системы организма, вероятно, являются причиной раннего спонтанного лизиса эмболического субстрата или дистальной миграции фрагментов эмбола с последующей реканализацией артерии и развитием геморрагического инфаркта. Частота спонтанной реканализации при кардиоэмболическом инсульте довольно значительна и составляет 61,8% [21]. В случае развития некроза артериальной стенки, высокая вероятность которого существует при тяжелой ишемии и обширном инфаркте с возможным участием гемодинамических, гемореологических и биохимических процессов, ГТ может протекать по типу паренхимальной гематомы.
Роль ГБ в развитии ГТ изучалась многими исследователями [5, 6, 7, 9, 19]. Однако, как правило, подобная взаимосвязь отрицалась [16]. Мы также не получили подтверждения влияния ГБ в анамнезе на развитие ин-траишемического кровотечения. Однако максимальный уровень систолического и диастолического АД, зафиксированный нами в 1-е и 2-е сутки заболевания, оказался заметно выше у пациентов с геморрагической конверсией инфаркта головного мозга. А у больных с последующей паренхимальной гематомой – только уровень диастолического АД. Это позволило предположить, что не хроническое повышение АД, а только систолическая и/или диастолическая артериальная гипертензия, сохраняющаяся в первые 24-48 часов от дебюта инсульта, то есть в период наиболее высокого риска развития спонтанных и посттромболитических ГТ, имеет значение для последующего развития интраишемической геморрагии и определяет ее объем. Однако, остается неясным, является ли острое повышение давления тем критическим фактором, который, взаимодействуя с интенсивной реперфузионной циркуляцией крови, приводит к возникновению кровоизлияния. Этот вопрос является практически важным, поскольку выраженное снижение АД в остром периоде инсульта также может являться неблагоприятным фактором в отношении клинического течения инсульта [7, 9, 19, 23]. Все это указывает на важность тщательного мониторинга АД в течение первых-вторых суток инсульта независимо от проводимой терапии.
В своей работе мы еще раз подтвердили мнение многих исследователей об ангиопротективных свойствах холестерина [3, 16], получив достоверное преобладание пациентов с гиперхолестеринемией в анамнезе среди больных без геморрагии.
Использование метода logit-регрессии позволило подтвердить значимость установленных нами факторов риска и выделить наиболее важные из них. Мы не стали использовать в качестве одной из независимых переменных уровень АД, зафиксированный в 1-е и 2-е сутки заболевания, несмотря на его установленную значимость потому, что только 30% ГТ были обнаружены нами в первые 48 часов заболевания. Оставшиеся 70% вторичных геморрагий, зафиксированные на протяжении последующих 3-х недель, по всей видимости, имеют незначительную связь с первоначальным гемодинамическим статусом. Этот факт подтверждается многими исследователями [6, 14, 15]. Результаты logit-регрессии еще раз подтвердили важную роль в развитии интраишемического кровотечения кардиоэмболического подтипа инсульта, а также тяжести инсульта в дебюте. При инсультах незначительной и умеренной тяжести кардиоэмболический механизм их развития играет особенно важную роль, а тяжелые инсульты имеют повышенную предрасположенность к геморрагической конверсии, независимо от подтипа инсульта. Подобные предположительные выводы по данным аутопсии делались Lodder J. et al. в 1986 году [18].
Таким образом, ГТ инфаркта головного мозга характерна для инсультов умеренной или выраженной степени тяжести с большими или обширными размерами зоны ишемического повреждения. КЭ имеет особое, но не эксклюзивное предрасположение к ГТ инфаркта. Мерцательная аритмия является не только наиболее частым потенциальным источником кардиогенной церебральной эмболии, но и предиктором интраишемического кровотечения большего размера, особенно – паренхимальной гематомы. Повышенный уровень АД в первые несколько суток инсульта является фактором риска ГТ инфаркта головного мозга.
Список литературы Факторы риска геморрагической трансформации инфаркта головного мозга
- Ворлоу Ч.П., Денис М.С., Гейн Ж.В. и др. Инсульт/Практическое руководство для ведения больных. -СПб: Политехника, 1998. -629 с.
- Шевченко Ю.Л., Одинак М.М., Михайленко А.А., Кузнецов А.Н. Кардиоэмболический инсульт. -СПб., 1997. -66 с.
- Шевченко Ю.Л., Одинак M.M, Кузнецов А.Н., Ерофеев А.А. Кардиогенный и ангиогенный церебральный эмболический инсульт. -М.: ГЭОТАР-Медиа. -2006. -270 с.
- Adams H.P., Brott T.C., Furlan A.L. et al. Guidelines for trombolytic therapy for acute stroke//Stroke. -1996. -Vol. 27. -P. 1711-1718.
- Adams R.D., Van der Ecken H.M. Vascular diseases of the brain//Ann. Rev. Med. -1953. -Vol. 4. -P. 213-252.
- Alexandrov A.V., Black S.E., Ehrlich L.E. et al. Predictors of hemorrhagic transformation occurring spontaneously and on anticoagulants in patients with acute ischemic stroke//Stroke. -1997. -Vol. 28. -P. 1198-1202.
- Faris A.A. Hardin C.A., Poser C.M. Pathogenesis of hemorrhagic infarction of the brain//Arch. Neurol. -1963 -Vol. 9. -P. 468-472.
- Fisher C.M., Adams R.D. Observations on brain embolism with special reference to the mechanism of hemorrhagic infarction//J. Neuropathol. Exp. Neurol. -1951. -Vol. 10. -P. 92-93.
- Globus J.H., Epstein J.A. Massive cerebral hemorrhage: spontaneous and experimentally induced//J. Neuropathol. Exp. Neurol. -1953. -Vol.12. -P. 107-131.
- Hardin C., Hendren T.H., Faris A.A. et al. Pathogenesis of hemorrhagic infarction of the brain//Arch. Neurol. -1963. -Vol.9. -P. 473-476.
- Hart R.G., Easton J.D. Hemorrhagic infarcts//Stroke. -1986. -Vol. 17. -P. 586-589.
- Hornig C.R. Rick evaluation of anticoagulant therapy in cardioembolic stroke/Stroke prevention/Eds W. Dorndorf, P.Marx. -Basel, 1994. -P. 165-179.
- Horowitz S.H., Zito J.L., Donnarumma R. et al. Computed tomographic-angiographic findings within the first five hours of cerebral infarction//Stroke. -1991. -Vol.22. -P. 1245-1253.
- International Stroke Trial Collaborative Group. The International Stroke Trial//Lancet. -1997. -Vol. 349. -P. 1569-1581.
- Kase C.S., Furlan A.J., Wechsler L.R. at al. Cerebral hemorrhage after intra-arterial thrombolysis for ischemic stroke//Neurology. -2001. -Vol. 57. -P. 1603-1610.
- Kerenyi L., Kardos L., Sza´sz J. et al. Factors influencing hemorrhagic ransformation in ischemic stroke//Europ. J. of Neurol. -2006. -Vol. 13. -P. 1251-1255.
- Khatri P., Wechsler L.R., Broderick J.P. Intracranial Hemorrhage Associated With Revascularization Therapies//Stroke. -2007. -Vol. 38. -P. 431-440.
- Lodder J., Krijne-Kubat B., Broekman j. Cerebral hemorrhagic infarction at autopsy//Stroke. -1986. -Vol. 17. -P. 626-629.
- Lyden P.D., Zivin J.A. Hemorrhagic transformation after cerebral ischemia//Cerebrovasc. Brain Met. Rev. -1993. -Vol. 5. -P. 1-16.
- Olsen T.S., Skriver E.B., Herning M. Cause of cerebral infarction in the carotid territory//Stroke. -1985. -Vol. 16. -P. 459-466.
- Rha J., Saver J.L. The Impact of Recanalization on Ischemic Stroke Outcome//Stroke. -2007. -Vol. 38. -P. 967-973.
- Toni D., Fiorelli M., Bastianello S. et al. Hemorrhagic transformation of brain infarct//Neurology. -1996. -Vol. 46. -P. 341-345.
- Torvik A. The pathogenesis of watershed infarcts in the brain//Stroke. -1984. -Vol. 15. -P. 221-223.


