Фармакологические исследования и фармацевтический анализ детских суппозиториев с цетиризина дигидрохлоридом
Автор: Арчинова Татьяна Юрьевна, Манджиголадзе Татьяна Юрьевна, Романцова Наталья Александровна, Макарова Лариса Михайловна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Коррекция экологического неблагополучия
Статья в выпуске: 5-2 т.17, 2015 года.
Бесплатный доступ
Изучена антигистаминная активность детских суппозиториев с цетиризина дигидрохлоридом в опытах на белых крысах на модели создания острого воспалительного отека. Разработаны методики идентификации цетиризина дигидрохлорида в детских суппозиториях с использованием реакций соле-, комплексообразования, осаждения, нитрования, а также с помощью электронного спектра поглощения по расположению максимумов и минимумов. Разработана методика количественного спектрофотометрического определения цетиризина дигидрохлорида в детских суппозиториях и проведена ее валидационная оценка.
Суппозитории, цетиризина дигидрохлорид, антигистаминная активность, спектрофотометрический метод, валидационная оценка методики
Короткий адрес: https://sciup.org/148204097
IDR: 148204097 | УДК: 615.218.2454.2:543.422.3
Pharmacological researches and pharmaceutical analysis of cetirizine dihydrochloride child suppositories
Studied children antihistamine activity of cetirizine dihydrochloride suppositories in experiments on white rats on a model of acute inflammatory edema creation. Developed a technique of identification of cetirizine dihydrochloride in children suppositories using reactions salt, chelation, precipitation, nitration, and using the electronic absorption spectrum for the location of maximum and minimum. The technique of quantitative spectrophotometric determination of cetirizine dihydrochloride in children suppositories and held her validation assessment.
Текст научной статьи Фармакологические исследования и фармацевтический анализ детских суппозиториев с цетиризина дигидрохлоридом
Цель исследования: изучить антигистаминную активность ЦДХ в суппозиториях, а также разработать оптимальные методики их анализа.
Противогистаминную активность суппозиториев с ЦДХ изучали путем создания модели острого воспалительного отека в опытах на белых крысах-самцах массой 200-210 г. [1, 4]. Отек вызывали субплантарным введением в заднюю лапку крысы 0,25мл 0,01% раствора гистамина. Объем лапок (см3) измеряли онкометром до начала опыта и через 1 час после моделирования отека. Динамику воспалительного отека оценивали через 15 и 60 минут после введения гистамина.
В эксперименте использовали 6 групп животных по 4 крысы в каждой группе. В качестве препарата сравнения выбран раствор ЦДХ. Контрольной группе животных перорально вводили воду очищенную. Второй группе животных вводили водный раствор ЦДХ в дозе 10 мг/кг. Третья группа животных получала суппозиторную основу – плацебо (per rectum) в объеме 0,1 мл/100 г. Четвертой группе животных вводили суппозитории с ЦДХ в дозе 0,02 мг/кг. Пятой группе животных вводили суппозитории с ЦДХ в дозе 0,005 мг/кг, а шестой группе – 0,1 мг/кг. Объем вводимых жидкостей в опытной и контрольной группах животных были эквивалентны. Для выбора доз ЦДХ при приеме per os руководствовались средней терапевтической дозой препарата для ребенка в пересчете на крысу (К=5,9). Так как целью исследований явилось изучение возможности применения ЦДХ в виде суппозиториев, то в суппозиториях содержалась та же доза ЦДХ, что и при приеме per os. Критерием оценки противо-отечного действия ЦДХ являлся объем жидкости (мл), вытесняемый при погружении в нее конечности животного. Статистически обработанные результаты опытов представлены в табл. 1.
Таблица 1. Влияние ЦДХ на выраженность гистаминного отека (n=6)
|
Условия опыта |
Исходный объем лапок, мл3 |
Изменение объема лапок после введения гистамина, %* ) |
|
|
15 минут |
60 минут |
||
|
рer os |
|||
|
контроль (вода очищенная) |
1,48±0,06 |
52,3±6,4 |
46,0±3,7 |
|
раствор ЦДХ |
1,56±0,01 |
44,8±2,5 |
28,1±3,2 |
|
рer rectum |
|||
|
контроль (суппозиторная основа-плацебо) |
1,76±0,05 |
28,3±4,5 |
16,2±1,9 |
|
суппозиторий с ЦДХ |
1,81±0,02 |
37,9±4,2 |
10,5±1,9 |
Примечание: * результаты с достоверной вероятностью 95% относительно контрольной группы
Установлено, что: при пероральном применении ЦЛХ происходит угнетение гистаминного отека в 1,52 раза относительно животных контрольной группы; ректальное введение ЦДХ приводит к подавлению гистаминного отека в 1,8 раза. Таким образом, разработанные нами суппозитории с ЦДХ в дозе 0,005г можно рекомендовать к использованию для лечения детских аллергических заболеваний.
Далее в задачу наших исследований входила разработка оптимальных методик качественного и количественного анализа ЦДХ в суппозиториях. Для этого учитывали связь структуры исследуемого вещества с его физическими, физико-химическими и химическими свойствами [6]. Цетиризина дигидрохлорид – (RS)-2-{2-[4-[(4-Хлорфенил) фенилметил]-пиперазин-1-ил] этокси}- уксусной кислоты дигидрохлорид представляет собой соль слабого основания и сильной кислоты, поэтому легко растворим в воде и растворим в 95% спирте этиловом. Является производным пиперазина, содержит два третичных амина, два фенильных радикала, органически связанный хлор, простую спиртовую группу и карбоксильную группу. Для идентификации ЦДХ в суппозиториях использовали химические реакции на функциональные группы, а также спектрофотометрический метод. Так как ЦДХ легко растворим в воде, он способен легко высвобождаться из суппозиториев при нагревании.
Исследуемое вещество извлекали из 5 суппозиториев 20-25 мл воды очищенной при нагревании на водяной бане. Извлечение фильтровали. Фильтрат делили на 5 частей и проводили реакции идентификации. Наличие третичной аминогруппы подтверждали реакцией комплексообразования с реактивом Драгендорфа. Простую эфирную группу обнаруживали по образованию ониевого катиона. По появлению светлоголубого осадка (реактив – 5% раствор меди (II) сульфата) судили о наличии карбоксильной группы. При наслаивании кислоты азотной концентрированной появлялось кольцо желтого цвета (фенильные радикалы). Кроме того, для более объективной идентификации цетиризина дигид- рохлорида в суппозиториях использовали электронный спектр поглощения.
Исследуемый раствор готовили следующим образом. ЦДХ извлекали из 1 суппозитория 25мл воды очищенной при нагревании. Извлечение охлаждали, фильтровали в мерную колбу вместимостью 100 мл. Фильтрат доводили водой очищенной до метки и перемешивали. 10 мл полученного раствора помещали в мерную колбу вместимостью 50 мл, доводили водой очищенной до метки и перемешивали. Спектр поглощения полученного раствора измеряли в диапазоне длин волн от 200 до 300 нм. В спектре наблюдалась полоса поглощения с максимумом в области 230±2 нм и минимумом 220±2 нм. Полученный электронный спектр поглощения полностью совпадал со спектром поглощения 0,001% водного раствора стандартного образца ЦДХ. Полученные результаты позволили использовать спектрофотометрический метод и для количественного определения ЦДХ в суппозиториях.
Предварительные исследования показали, что оптимальным растворителем с точки зрения получения стабильных и воспроизводимых результатов, является 0,1М раствор кислоты хлористоводородной. В спектре поглощения 0,001% раствора ЦДХ в 0,1М растворе кислоты хлористоводородной наблюдается полоса поглощения с одним максимумом в области 231±2 нм и минимумом в области 219±2нм. Подчинение солянокислых растворов закону Бугера-Ламберта-Бера соблюдается в диапазоне концентраций от 0,0005 до 0,0035% (рис. 1).
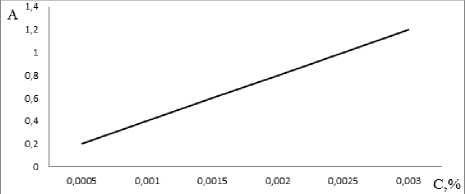
Рис. 1. Градуировочный график ЦДХ в 0,1М растворе кислоты хлористоводородной
Для подтверждения линейной зависимости нами расчитано уравнение градуировачного графика, а так же коэффициент корреляции (r). Данные представленны в табл. 2.
Согласно требованиям ОФС 42-0111-09 угловой и свободный коэффициенты линейной зависимости рассчитывали по формулам:
т£А1 С^—ЕС^ХА^ b=
SAi-bSq a= ,
т
,
где b - угловой коэффициент линейной зависимости; a – свободный коэффициент линейной зависимости.
Таблица 2. Исходные данные для расчета градуировочного графика (m=6)
|
№ п/п |
Концентрация раствора цетиризина дигидрохлорида ( C i ), % |
Оптическая плотность ( A i ) |
A i 2 |
C2 |
А·С |
|
1 |
0,0005 |
0,175 |
0,030625 |
0,00000025 |
0,0000875 |
|
2 |
0,0010 |
0,360 |
0,129600 |
0,00000100 |
0,0003600 |
|
3 |
0,0015 |
0,545 |
0,297025 |
0,00000225 |
0,0008175 |
|
4 |
0,0020 |
0,725 |
0,525625 |
0,00000400 |
0,0014500 |
|
5 |
0,0025 |
0,910 |
0,828100 |
0,00000625 |
0,0022750 |
|
6 |
0,0030 |
1,095 |
1,199025 |
0,00000900 |
0,0032850 |
|
2 |
0,0105 |
3,810 |
3,010000 |
0,00002275 |
0,0082750 |
Уравнение градуировочного графика принимает следующий вид:
А=367,43с – 0,008, (3)
где А – оптическая плотность; 367,43 – угловой коэффициент линейной зависимости; -0,008 – свободный коэффициент линейной зависимости.
Нами была разработана методика количественного спектрофотометрического определения ЦДХ в детских суппозиториях, которая заключается в следующем: 1 суппозиторий помещают в коническую колбу вместимостью 200 мл, прибавляют 30-40 мл 0,1М раствора кислоты хлористоводородной и ставят на кипящую водяную баню до полного расплавления суппозитория при постоянном перемешивании в течение 20 минут. Затем содержимое охлаждают и фильтруют через двойной фильтр в мерную колбу вместимостью 100 мл. Аналогичную операцию повторяют дважды, фильтраты объединяют, объем раствора доводят 0,1М раствором кислоты хлористоводородной до метки и перемешивают (раствор А). 25 мл раствора А помещают в мерную колбу вместимостью 100 мл, доводят объем раствора до метки и перемешивают. Оптическую плотность полученного раствора измеряли в кварцевых кюветах относительно растворителя на спектрофотометре при λmax = 231нм. Содержание ЦДХ в одном суппозитории (x) в граммах рассчитывали по уравнению градуировочного графика по формуле:
(Aj-ayw^
x (г) = , (4)
где ( А i – a )/ b – концентрация ( C i ) ЦДХ, %; W 1 , W 2 – объемы мерных колб, мл; v – аликвота, мл.
Статистически обработанные результаты 7 параллельных определений представлены в табл. 3.
Таблица 3. Результаты количественного спектрофотометрического определения ЦДХ в одном суппозитории
|
№ п/п |
Оптическая плотность A i |
Найдено ( X i ), г |
Метрологические характеристики |
|
1 |
0,452 |
0,00501 |
=0,00493; S2 =6,76 SD =2,6; RSD=±2,61 =0,98; Δ x =2,4 = ±2,4% |
|
2 |
0,455 |
0,00504 |
|
|
3 |
0,440 |
0,00488 |
|
|
4 |
0,458 |
0,00508 |
|
|
5 |
0,437 |
0,00484 |
|
|
6 |
0,443 |
0,00492 |
|
|
7 |
0,428 |
0,00476 |
Относительная погрешность определения не превышает ±2,4%.
Валидность предложенной методики устанавливали по критериям «Правильность», «Линейность» и «Прецизионность». «Линейность» методики устанавливали на основании коэффициента корреляции (r) градуировочного графика, рассчитанного по формуле, приведенной в ОФС 42-0111-09. Правильность методики определяли по двум критериям: «Открывае-мость» и рассчитанному коэффициенту Стьюдента. Открываемость устанавливали по трем уровням концентраций растворов, приготовленных из исходного раствора А, полученного из искусственной смеси, сос-тоящей их 0,0500 г ЦДХ и 10,0 г основы. В качестве растворителя служил
0,1 М раствор кислоты хлористоводородной. Были приготовлены три серии растворов по три раствора в каждой. Их оптическую плотность измеряли на спектрофотометре при длине волны λ max = 231нм.
Количественное содержание ЦДХ рассчитывали по уравнению градуировочного графика (см. выше). «Открываемость» (R) рассчитывали по формуле:
найдено аналита (г) взято аналита (г)
-100%
Результаты приведены в табл. 4.
Таблица 4. Результаты установления точности методики с использованием «открываемости»
|
№ п/п |
Уровень |
Концентрация (%) |
Взято цетиризина дигидрохлорида (г) |
Оптическая плотность ( А , +0,008) |
Найдено цетиризина дигидрохлорида (г) |
Откры-вае-мость R (%) |
Метроло гические характеристики |
|
1 |
1 |
0,000625 |
0,0500 |
0,226 |
0,0492 |
98,4 |
R ср =99,6% |
|
2 |
1 |
0,000625 |
-//- |
0,228 |
0,0496 |
99,2 |
|
|
3 |
1 |
0,000625 |
-//- |
0,231 |
0,0503 |
100,6 |
|
|
4 |
2 |
0,001250 |
-//- |
0,451 |
0,0491 |
98,2 |
|
|
5 |
2 |
0,001250 |
-//- |
0,456 |
0,0496 |
99,2 |
SD=0,9% |
|
6 |
2 |
0,001250 |
-//- |
0,462 |
0,0504 |
100,8 |
t=1,33 |
|
7 |
3 |
0,001875 |
-//- |
0,692 |
0,0501 |
100,2 |
t таб =3,37 |
|
8 |
3 |
0,001875 |
-//- |
0,690 |
0,0500 |
100,0 |
|
|
9 |
3 |
0,001875 |
-//- |
0,688 |
0,0499 |
99,8 |
Так как расчетный коэффициент Стьюдента меньше табличного, методика не отягощена систематической ошибкой и поэтому может считаться правильной.
«Прецизионность» методики устанавливали по результатам девяти параллельных определений. Исходный раствор (раствор А) готовили аналогично раствору А (см. раздел «Правильность»). Затем в девять мерных колб вместимость. 100 мл помещали по 2,5 мл раствора А, доводили объем растворов 0,1М кислоты хлористоводородной до метки и перемешивали. Оптическую плотность полученных растворов измеряли в кварцевых кюветах с толщиной слоя 1см при λmax=231 нм относительно растворителя (табл. 5).
Результаты проведенной валидацион-ной оценки методики приведены в табл. 6. Полученные данные свидетельствуют о пригодности методики для аналитических целей.
Таблица 5. Результаты установления «Прецизионности»
|
№ п/п |
Взято вещества (г) |
Оптическая плотность ( А , +0,008) |
Найдено (г) |
Метрологические характеристики |
|
1 |
0,0500 |
0,456 |
0,0496 |
Х ср =0,00498 SD=0,72 |
|
2 |
-//- |
0,454 |
0,0494 |
|
|
3 |
-//- |
0,461 |
0,0502 |
|
|
4 |
-//- |
0,458 |
0,0498 |
|
|
5 |
-//- |
0,459 |
0,0499 |
|
|
6 |
-//- |
0,462 |
0,0503 |
|
|
7 |
-//- |
0,455 |
0,0495 |
|
|
8 |
-//- |
0,457 |
0,0497 |
|
|
9 |
-//- |
0,460 |
0,0500 |
Таблица 6. Результаты валидационной оценки методики количественного спектрофотометрического определения ЦДХ в суппозиториях
|
№ п/п |
Определяемый критерий |
Результат |
Требования НД |
|
1 |
открываемость (R ср ) |
99,60% |
99-101% |
|
2 |
правильность (коэффициент Стьюдента t) |
1,33 |
3,37 |
|
3 |
уравнение градуировочного графика |
А=367,4с – 0,008 |
- |
|
4 |
линейность (коэффициент корреляции r) |
0,997 |
~1,0 |
|
5 |
прецизионность (SD) |
0,72 |
не более 3,0 |
Выводы:
-
1. Фармакологическими исследованиями доказана антигистаминная активность разработанных нами ранее детских суппозиториев с ЦДХ, которые подавляли выраженность гистаминового отека в 1,8 раза по сравнению с пероральным применением.
-
2. Разработаны методики качественного и количественного определения ЦДХ с использованием химических и оптических методов.
-
3. Проведена валидационная оценка методики количественного спектрофотометрического определения ЦДХ в суппозиториях.
Список литературы Фармакологические исследования и фармацевтический анализ детских суппозиториев с цетиризина дигидрохлоридом
- Бадальян, З.В. Сравнительное фармакологическое изучение ферментированного сока подорожника/З.В. Бадальян, Л.М. Макарова, В.Е. Погорелый и др.//Научные ведомости Белгородского гос. университета. Серия: Медицина. Фармация. 2012. Т. 18, №10-3 (129). С. 121-123.
- Верткин, А.Л. Острые аллергические заболевания: социальные последствия эпидемии/А.Л. Верткин, А.В. Дадыкина, К.Н. Турлубеков//Ремедиум. 2004. №7-8. С. 26.
- Викторов, А.П. Побочные действия современных противогистаминных лекарственных средств//Doctor. 2006. №2. С. 22-24.
- Киселева, Г.С. Приборы и методы оценки фармацевтической доступности лекарственных форм/Г.С. Киселева, А.И. Тенцова//Фармация. 1993. Т. 42, №4. С. 58-62.
- Манджиголадзе, Т.Ю. Детские суппозитории с цетиризина дигидрохлоридом для профилактики и лечения аллергических заболеваний/Т.Ю. Манджиголадзе, Т.Ю. Арчинова, Н.А. Романцова//Известия Самарского научного центра Российской академии наук. 2013. Т. 15, №3(6). С. 1860-1863.
- Маринина, Т.Ф. Разработка технологии и анализа двухслойных суппозиториев кровоостанавливающего действия/Т.Ф. Маринина, Л.Н. Савченко, А.Ю. Саенко, И.Я. Куль//Научные ведомости Белгородского гос. университета. Серия: Медицина. Фармация. 2011. №22 (117). Вып. 16. С. 235-238.


