Фазовая диаграмма системы Na-Na2O
Автор: Зайцева Ольга Владимировна, Трофимов Евгений Алексеевич, Самойлова Ольга Владимировна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Металловедение и термическая обработка
Статья в выпуске: 2 т.18, 2018 года.
Бесплатный доступ
Фазовые равновесия в системе Na-O представляют интерес в связи с тем, что металлический натрий широко используется в ядерных реакторах в качестве теплоносителя. Целью работы стало термодинамическое моделирование системы Na-O в области Na-Na2O и построение фазовой диаграммы этой системы. В ходе работы проанализированы имеющиеся экспериментальные данные о растворимости кислорода в жидком натрии. Используя литературные данные, в ходе нашей работы осуществлено моделирование фазовых равновесий и расчёт координат фазовой диаграммы области Na-Na2O. В процессе проведённой работы для расчётов использованы возможности программного комплекса FactSage. Использованы данные базы SGPS (SGTE pure substances database) о стандартных энтальпиях образования, стандартных энтропиях и параметрах фазовых переходов, а также температурных зависимостях молярных теплоёмкостей для твёрдых и жидких веществ, образующих систему твёрдого и жидкого Na, кристаллических модификаций Na2O и его расплава. Моделирование расплава Na-Na2O выполнено посредством двухподрешёточной модели ионной жидкости. Параметр взаимодействия для этой модели, температурная и концентрационная зависимость которого выражена посредством полинома Редлиха - Кистера, определён в ходе работы. Согласно результатам моделирования система Na-O в области Na-Na2O характеризуется наличием области расслаивания на две жидких фазы. Координаты критической точки: температура 2457 К, содержание кислорода ~26 ат. %. Крайняя левая точка кривой расслаивания на две жидкие фазы характеризуется следующими координатами: температура 1405 К, содержание кислорода ~4,8 ат. %.
Натрий, кислород, фазовая диаграмма, термодинамическое моделирование
Короткий адрес: https://sciup.org/147157133
IDR: 147157133 | УДК: 669.017.11 | DOI: 10.14529/met180205
Phase diagram of the Na-Na2O system
Phase equilibria in the Na-O system are interesting because metallic sodium is widely used as a coolant in nuclear reactors. The aim of this work was the thermodynamic modeling of the Na-O system in the Na-Na2O region, as well as the calculation of the phase diagram of this system. In the course of the study, the available experimental data on the solubility of oxygen in liquid sodium are analyzed. Using literature data, in the course of the study, the phase equilibria were simulated and the coordinates of the phase diagram of the Na-Na2O region were calculated. In the process of the study, the “FactSage” software was used for calculations. The data of the SGPS (SGTE pure substances database) base are used, such as standard enthalpies of formation, standard entropies, and phase transition parameters, as well as temperature dependences of molar heat capacities for solid and liquid substances forming the system (solid and liquid Na; crystalline modifications of Na2O and its melt). Modeling of the Na-Na2O melt is performed by means of the two-sublattice model of ionic liquid. The interaction parameters for this model are determined in the process of the work. Temperature and concentration dependences are expressed by means of the Redlich-Kister polynomial.
Текст научной статьи Фазовая диаграмма системы Na-Na2O
Фазовые равновесия в системе Na–O представляют интерес, поскольку металлический натрий широко используется в ядерных реакторах в качестве теплоносителя. В процессе эксплуатации натрий может вступать (прежде всего в аварийных ситуациях) во взаимодействие как с газообразным кислородом, так и с различными оксидными фазами. В ходе изучения такого взаимодействия важное место занимает исследование условий сосуществования металлической фазы с оксидными фазами в этой системе.
Целью настоящей работы стало термодинамическое моделирование системы Na–O в области Na–Na 2 O и построение фазовой диаграммы этой системы.
Изучению системы Na–O посвящено множество работ. Подробный обзор, сделанный H.A. Wriedt [1], показывает, однако, что область Na–Na2O исследована недостаточно и только в части растворимости кислорода в жидком натрии при температурах ниже 900 К. Очевидно, это связано с серьёзными трудностями экспериментального изучения этой системы, особенно возрастающими при повышении температуры. Вместе с тем та область, которая стала объектом внимания исследователей, изучена достаточно хорошо. В литературе [2–9] представлена информация о сотнях экспериментально определённых значениях растворимости кислорода в натрии. В работе [2] приводятся 17 литературных зависимостей растворимости (в мас. %) кислорода в натрии от температуры, полученных для различных интервалов температур от 110 до 555 °С, а также результаты обобщения собственных экспериментальных данных.
Обобщение результатов экспериментальных работ (107 экспериментальных точек из литературы) позволило автору работы [3] ре-
комендовать следующую зависимость
lg X O =
- 2447
T
+ 0,396.
Автор работы [4], анализируя результаты 268 измерений различных авторов, рекомен-
дует следующую зависимость
-2444 5
lg X о + 0,4145-
Автор [5] в ходе анализа собственных и литературных данных получил следующую
зависимость
lg X о =
- 2372
T
+ 0,32
Надо сказать, что результаты большей части проведённых исследований хорошо соотносятся между собой, о чём, в частности, позволяет судить рис. 1, на котором показаны результаты расчёта по трём приведённым зависимостям для интервала температур 400–833 К,
а также в виде точек представлена некоторая часть экспериментальных данных о растворимости кислорода в натрии в зависимости от температуры.
Представленная в обзоре [1] фазовая диаграмма для области Na–Na 2 O носит схематический характер и в значительной степени опирается на предположения. Используя зависимость из работы [4], а также предположения о виде фазовой диаграммы анализируемой системы, приводимые автором работы [1], в ходе нашей работы осуществлено моделирование фазовых равновесий и расчёт координат фазовой диаграммы этой системы для области Na–Na 2 O (рис. 2). Отметим, что расчёт проведён без учёта фазовых равновесий с участием газовой фазы, т. е. для условий, когда давление в системе обеспечивает существование только конденсированных фаз и при этом не влияет на положение границ между конденсированными фазами.
В процессе проведённой работы для расчётов использован программный комплекс FactSage [10–12] версия 7.0. Расчёт фазовой диаграммы проводился посредством модуля «Phase Diagram», формирование базы индивидуальных веществ – с помощью модуля «Compound», а формирование базы термодинамических параметров для описания фаз
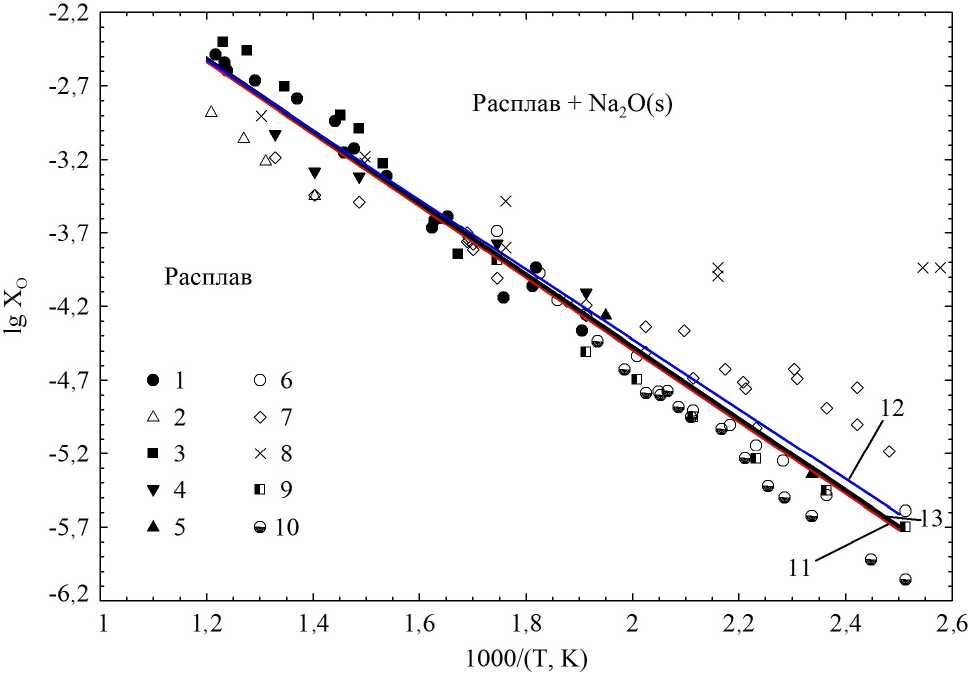
Рис. 1. Растворимость кислорода в натрии для интервала температур 400–833 K: 1 – S.L. Walters (1950) согласно [3]; 2 – A.D. Bogard и D.D. Williams (1951) согласно [3]; 3 – J.D. Noden и K.Q. Bagley (1954) согласно [3]; 4 – S. Dorner (1966) согласно [3]; 5 – K.S. Bergstresser и др. (1965) согласно [3]; 6 – V.J. Rutkauskas и G.E. Meadows (1967) согласно [3]; 7 – [6]; 8 – [7]; 9 – [8]; 10 – [9]; 11 – расчёт по зависимости из [3]; 12 – расчёт по зависимости из [5]; 13 – расчёт по зависимости из [4], результаты которого практически совпадают с результатами моделирования, проведённого в ходе настоящей работы
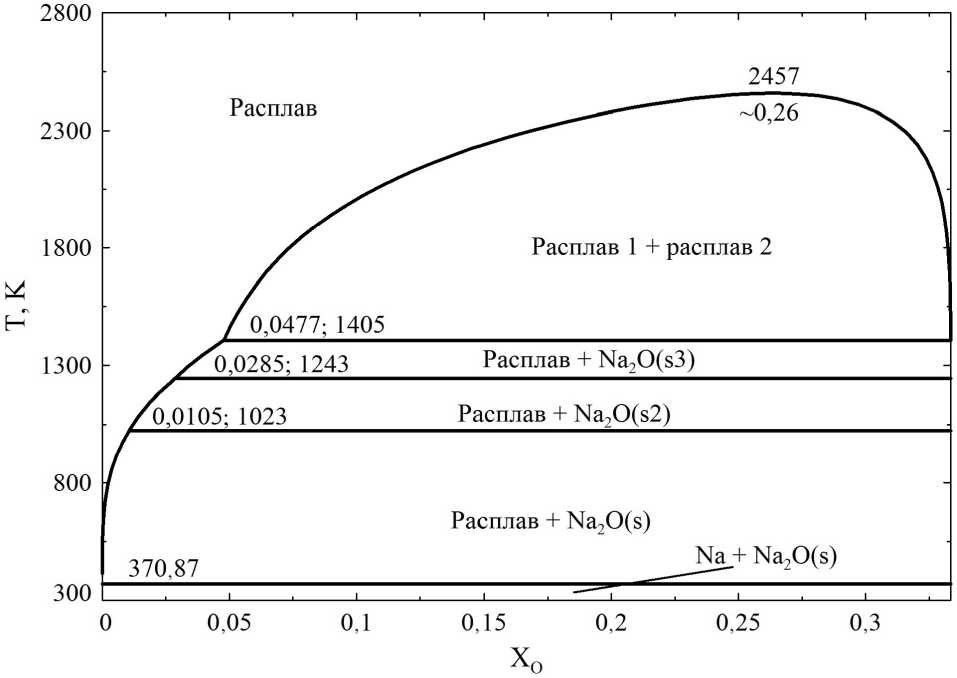
Рис. 2. Фазовая диаграмма системы Na–Na 2 O. Результаты расчёта для конденсированных фаз
переменного состава – с помощью модуля «Solution».
Данные для расчёта энергий Гиббса твёрдых и жидких веществ, образующих систему твёрдого и жидкого Na, кристаллических модификаций Na 2 O (α, β и γ формы с кристаллами кубической сингонии) и его расплава заимствованы из базы данных SGPS [13]. К заимствованным данным относятся стандартная энтальпия образования, стандартная энтропия и параметры фазовых переходов, а также температурные зависимости молярных теплоёмкостей этих веществ при условии постоянства давления.
Для моделирования расплава Na–Na 2 O использовалась двухподрешёточная модель ионной жидкости, описанная в работах [14, 15]. Формула ионной жидкости для данного расплава приняла следующий вид:
(Na+) p (O–2, Va– q ) q ; (1)
q = У Na + = 1; (2)
p = 2 У O - 2 + qy Va = 2 У O - 2 + y Va . (3) Здесь Va – вакансия; y s – доля компонента s в катионной или анионной подрешётке. Избыточная энергия Гиббса согласно используемой модели рассчитывается по формуле
G m У Na + У O - 2 У Va L Na + :O - 2,Va
= У O - 2 У Va L Na + :O - 2 ,Va , (4) где L – параметр взаимодействия, температурная и концентрационная зависимость которого выражены посредством полинома Ред-лиха – Кистера. В настоящей работе эта зависимость определена следующим образом:
L Na + :O 2 - ,Va - = 92699 " 21,33 T +
+ ( 107912 - 60,71 T + 3-KT6 T 3 )( У O 2 - - У Va - ) . (5)
В процессе расчёта фазовых диаграмм предусматривалась возможность одновременного сосуществования двух жидких фаз.
О качестве проведённого моделирования позволяет судить рассчитанная линия растворимости кислорода в натрии, представленная на рис. 1.
Крайняя левая точка кривой расслаивания на две жидкие фазы на рассчитанной нами диаграмме (см. рис. 2) характеризуется более высоким содержанием кислорода в системе, нежели показано на диаграмме в работе [1] (~ 4,8 ат. % против 4,7 ат. %). Поскольку экспериментальные данные для условий гипотетического монотектического равновесия отсутствуют, а значение 4,7 ат. % получено экстраполяцией экспериментальных значений, полученных в интервале температур от 114 до 555 °С на область температур порядка 1130 °С, указанное расхождение вряд ли можно считать существенным недостатком проведённого моделирования.
Заключение
В ходе исследования, опираясь на представленные в литературе экспериментальные данные, осуществлено термодинамическое моделирование фазовых равновесий в системе Na–Na 2 O. Получен набор модельных параметров. Рассчитана фазовая диаграмма исследованной системы.
Исследование выполнено при финансовой поддержке РФФИ в рамках научного проекта № 16-38-60144 мол_а_дк.
Список литературы Фазовая диаграмма системы Na-Na2O
- Wriedt H.A. The Na-O (Sodium-Oxygen) System//Bulletin of Alloy Phase Diagrams, 1987, vol. 8, no. 3, pp. 234-246 DOI: 10.1007/BF02874915
- Alcock C.B. and Stavropoulos G.P. Galvanic Cell Measurements on the Sodium-Oxygen System//Can. Metall. Q., 1971, vol. 10, no. 4, pp. 257-265 DOI: 10.1179/cmq.1971.10.4.257
- Eichelberger R.L. Solubility of Oxygen in Liquid Sodium. U.S. At. Energy Comm. Rep. AI-AEC-12685, 1968 DOI: 10.2172/4808140
- Noden J.D. General Equation for the Solubility of Oxygen in Liquid Sodium. Addendum//J. Br. Nucl. Energy Soc., 1973, vol. 12, no. 3, pp. 329-331.
- Claxton K.T. Solubility of Oxygen in Liquid Sodium and the Interpretation of Predictions for the Corrosion Rate of Stainless Steels in Liquid Sodium. Junta Energ. Nucl. (Spain), Rep. JEN-446, 1979. (in Spanish)
- Beisswenger H., Dorner S. Solubility of Oxygen in Liquid Sodium//J. Nucl. Mater., 1968, vol. 28, no. 3, pp. 297-302 DOI: 10.1016/0022-3115(68)90196-7
- Salmon N. and Cashman T.J. The Solubility of Sodium Monoxide in Liquid Sodium, KAPL-1653, 1956.
- De la Torre Cabezas M. Behavior of Oxygen in Liquid Sodium. Junta Energ. Nucl. (Spain), Rep. JEN-310, 1975. (in Spanish)
- Smith D.L. and Lee R.H. Characterization of the Vanadium-Wire Equilibration Method for Measurement of Oxygen Activity in Liquid Sodium. Argonne Natl. Lab Rep. ANL-7891 Argonne, IL, 1972.
- Bale C.W., Chartrand P., Degterov S.A., Eriksson G., Hack K., Ben Mahfoud R., Melançon J., Pelton A.D., Petersen S. FactSage Thermochemical Software and Databases//Calphad, 2002, vol. 26, no. 2, pp. 189-228 DOI: 10.1016/S0364-5916(02)00035-4
- Bale C.W., Bélisle E., Chartrand P., Decterov S.A., Eriksson G., Hack K., Jung I.-H., Kang Y.-B., Melançon J., Pelton A.D., Robelin C., Petersen S. FactSage Thermochemical Software and Databases -Recent Developments//Calphad, 2009, vol. 33, no. 2, pp. 295-311 DOI: 10.1016/j.calphad.2008.09.009
- Bale C.W., Bélisle E., Chartrand P., Decterov S.A., Eriksson G., Gheribi A.E., Hack K., Jung I.-H., Kang Y.-B., Melançon J., Pelton A.D., Petersen S., Robelin C., Sangster J., Spencer P., Van Ende M.-A. FactSage thermochemical software and databases, 2010-2016//Calphad, 2016, vol. 54, no. 1, pp. 35-53 DOI: 10.1016/j.calphad.2016.05.002
- SGPS database (SGTE pure substances database), FactSage 7.0.
- Hillert M., Jansson B., Sundman B., Agren J. A Two-Sublattice Model for Molten Solutions with Different Tendency for Ionization//Met. Trans. A, 1985, vol. 16A, pp. 261-266 DOI: 10.1007/BF02816052
- Sundman B. Modification of the Two-Sublattice Model for Liquids//Calphad, 1991, vol. 15, no. 2, pp. 109-119 DOI: 10.1016/0364-5916(91)90010-H


