Фазовые равновесия при взаимодействии бария с компонентами жидкой стали
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Статья в выпуске: 2 т.14, 2014 года.
Бесплатный доступ
Выполнен термодинамический анализ процессов финишного раскисления стали барием, магнием и алюминием. Установлено, что образующиеся включения даже при малых концентрациях бария, алюминия и магния являются, скорее всего, тугоплавкими и мелкими, что может привести к модифицированию жидкой стали, блокированию роста первичного литого зерна, снижению анизотропии и повышению технологической пластичности. Эффект модифицирования может быть усилен за счет снижения добавками бария межфазного натяжения при протекании в стали гетерогенных реакций.
Барий, магний, модификатор, сталь, диаграммы состояния, поверхности растворимости
Короткий адрес: https://sciup.org/147156869
IDR: 147156869 | УДК: 669.18.054:669.893
Phase equilibria in barium and molten steel component interaction
Thermodynamic analysis of the processes of final deoxidation of steel with barium, magnesium and aluminium is carried out. It is established that even at low concentrations of barium, aluminium and magnesium the most likely formed inclusions are high-melting and fine. This may lead to the modification of the liquid steel, to the blocking of primary cast grain growth, to the decrease of anisotropy and to the increase of technological plasticity. Modification effect may be intensified by the decrease of interphase surface tension with barium additions when heterogeneous reactions occur in steel.
Текст научной статьи Фазовые равновесия при взаимодействии бария с компонентами жидкой стали
Современные методы плавки стали позволяют в настоящее время за счет развития внепечных технологий стабильно получать металл с предельно низким содержанием кислорода, порядка 4–5 ppm, и серы ~20–40 ppm. В этих условиях может существенно изменяться химия раскисления стали и состав неметаллических включений. При этом необходимо учитывать, что растворимость бария в железе вряд ли превысит 0,001 мас. %. Точнее растворимость бария в жидком металле не установлена. Растворимость кальция составляет при открытой плавке 0,015–0,020 мас. %. При столь глубоком раскислении металла в сталь может восстанавливаться магний из шлака и футеровки и достигать концентрации порядка 0,001 мас. %. Тогда встает вопрос: какие фазы образуются в металле при столь малых концентрациях магния, бария, алюминия и кислорода? Для прояснения проблемы необходимо построить поверхность растворимости компонентов в металле (ПРКМ) и выделить облас- ти фазовых равновесий при малых концентрациях примесей.
Построение ПРКМ всегда связано с определением оксидных фаз, сопряженных с областью существования жидкого металла. Так в равновесии с металлом, содержащим в качестве примесей барий, магний и кислород, будут фазы, определяемые на диаграмме состояния BaO–MgO. На рис. 1 в верхнем левом углу приведен вид такой оксидной диаграммы [1], здесь же представлен расчет основных элементов данной диаграммы с использованием теории субрегулярных ионных растворов [2]. Как видно из рис. 1, диаграмма состояния BaO–MgO является диаграммой с простой эвтектикой. Температура эвтектического превращения составила 1526 °С, точка эвтектического превращения задана при x BaO = 0,62. На рис. 1 нанесены литературные экспериментальные данные ▲ и + [3], а также точка эвтектики • [1]. Диаграмма состояний FeO–BaO (рис. 2) также представляет
Рис. 1. Расчетная диаграмма состояния системы BaO–MgO: • – [1]; ▲ – [3]; + – [3]
Рис. 2. Расчетная диаграмма состояния системы FeO–BaO
диаграмму с простой двойной эвтектикой. Диаграмма FeO–MgO (рис. 3) говорит о неограниченной растворимости компонентов в твердом и жидком состоянии. Линии ликвидус этих диаграмм состояния хорошо описываются в рамках теории субрегулярных растворов. На рис. 4 представлена диаграмма состояний системы FeO–BaO–MgO. В литературе такая диаграмма состояний не построена, но по данным двойных диаграмм системы удалось подобрать параметры теории субрегулярных ионных растворов для тройной системы. Параметры теории представлены в табл. 1.
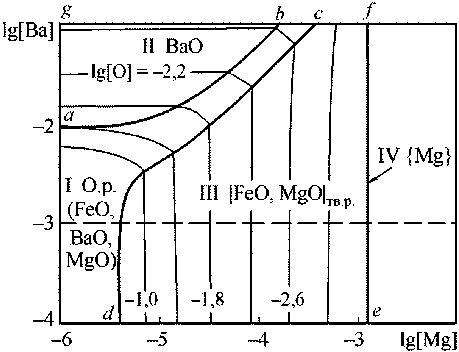
Были выполнены расчеты координат ПРКМ для условий раскисления стали магнием и барием (рис. 5) по методике, изложенной в работе [2].
В металле всегда остается какое-то количество остаточного алюминия, который вступает во взаимодействие с остаточным кислородом и другими компонентами расплава, образуя шпинельные и алюминатные фазы. В этом случает необходимо иметь сведения о диаграмме состояний BaO–MgO–Al2O3. При раскислении и модифици- ровании стали необходимо учесть также и наличие в стали углерода.
В табл. 2 приведены сведения об основных соединениях, которые образуются при раскислении стали барием, магнием, алюминием и углеродом и приведены температурные зависимости констант равновесия для реакций образования этих соединений из компонентов жидкого металла. Коэффициенты активности компонентов жидкого металла рассчитывались с помощью параметров взаимодействия e i j , приведенных в табл. 3.
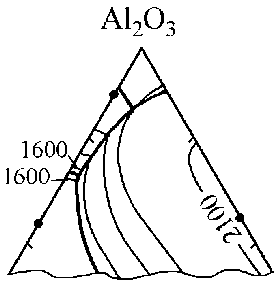
На рис. 6 построен расчетный вариант диаграммы состояний BaO–MgO–Al 2 O 3 . Диаграмму удалось построить, опираясь на термодинамические данные диаграмм состояний BaO–MgO, BaO–Al 2 O 3 и MgO–Al 2 O 3 . Из внешнего вида этой диаграммы состояний следует, что поля кристаллизации оксидных твердых фаз из шлаков крайне невелики. При взаимодействии магния, бария и алюминия с кислородом в стали жидкоподвижные включения выпадать не будут. Все образующиеся
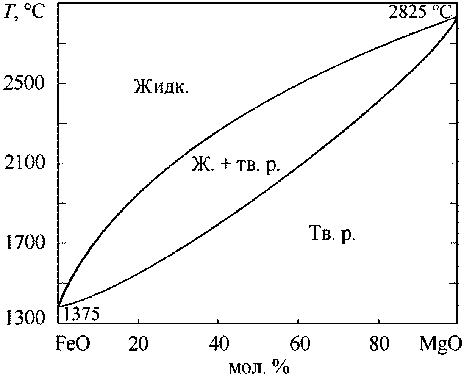
Рис. 3. Расчетная диаграмма состояния системы FeO–MgO
MgO
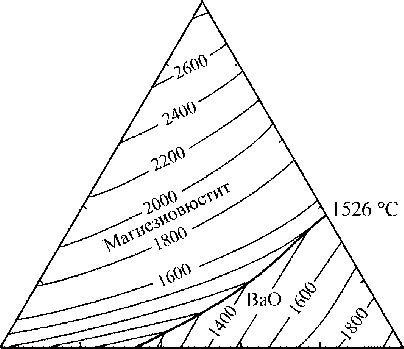
FeO 20 1066 40 60 80 BaO
мол. %
Рис. 4. Расчетная диаграмма состояния системы FeO–MgO–BaO
Таблица 1
Энергетические параметры теории субрегулярных ионных растворов для оксидных расплавов FeO–BaO–MgO–Al 2 O 3
|
Система |
Параметры теории Qijkl , кал/моль |
||
|
FeO–BaO |
–5000 |
–10 000 |
–5000 |
|
FeO–MgO |
–2500 |
–5000 |
–2500 |
|
FeO–Al 2 O 3 |
661 |
–16 329 |
–4917 |
|
BaO–MgO |
–10 000 |
–10 000 |
–20 000 |
|
BaO–Al 2 O 3 |
–21 194 |
–10 073 |
–32 395 |
|
MgO–Al 2 O 3 |
–14 517 |
2876 |
–1539 |
|
FeO–BaO–MgO |
–25 000 |
–35 000 |
–20 000 |
|
FeO–BaO–Al 2 O 3 |
–10 000 |
–20 000 |
–30 000 |
|
FeO–MgO–Al 2 O 3 |
–16 000 |
–23 000 |
–16 000 |
|
BaO– MgO–Al 2 O 3 |
–50 000 |
–90 000 |
–30 000 |
Таблица 2
Зависимость констант равновесия от температуры
|
№ |
Реакция |
Константа равновесия, K ; a – активность, мас. % |
lg K = – A / T + B |
|
|
A |
B |
|||
|
1 |
(FeO) = [Fe] + [O] |
K = [Fe] a [O]/ a ( FeO ) |
6320 |
4,734 |
|
2 |
(BaO) = [Ba] + [O] |
K = a [Ba] a [O] (a ( BaO ) |
20 384 |
7,36 |
|
3 |
(MgO) = [Ca] + [O] |
K = a [Mg] a [O]/ a ( MgO ) |
22 457 |
6,54 |
|
4 |
(Al 2 O 3 ) = 2[Al] + 3[O] |
K = a 2Ai] a 30] ] a ( A1 2 O 3 ) |
58 320 |
18,02 |
|
5 |
|BaO| = [Ba] + [O] |
K = a [Ba] a [O] |
23 400 |
8,73 |
|
6 |
|FeO| = [Fe] + [O] |
K = [Fe] a [O]/ a FeO |
8069 |
5,8 |
|
7 |
|MgO| = [Ca] + [O] |
K = a [Mg] a [O]/ a |MgO| |
26 500 |
7,85 |
|
8 |
|Al 2 O 3 | = 2[Al] + 3[O] |
23 K = a [Al] a [O] |
64 000 |
20,48 |
а)
Рис. 5. ПРКМ системы Fe–Ba–Mg–O–C, Т = 1600 °C, P общ = 1 атм: а) [C] = 0; б) [C] = 0,1 мас. %
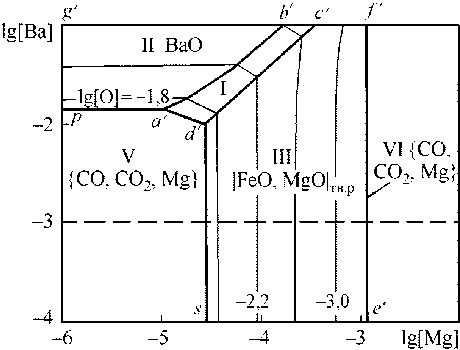
б)
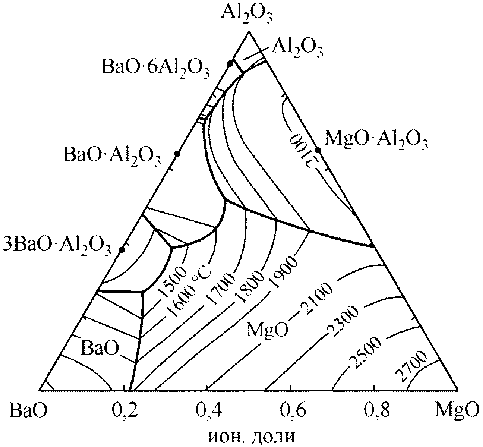
Рис. 6. Расчетный вариант диаграммы состояний BaO–MgO–Al 2 O 3
Окончание табл. 2
|
9 |
I ВаО^А1 2 О з | = [Ba] + 2[Al] + 4[O] |
24 K = a \ Ba ] a [A1] a [O] |
84 000 |
25,76 |
|
10 |
I BaO^6A№ | = [Ba] + 12[Al] + 19[O] |
12 19 K = a [ Ba ] a [A1] a [O] |
402 350 |
125,99 |
|
11 |
{CO} = [C] + [O] |
K = a [C] a [O]/ p {CO} |
1168 |
–2,07 |
|
12 |
{CO 2 } = [C] + 2[O] |
K = a [C] a[O]] p {CO2} |
9616 |
2,51 |
|
13 |
{Mg} = [Mg] |
K = P { Ca } / a [ Ca ] |
6670 |
–6,48 |
Таблица 3
Параметры взаимодействия компонентов ei j в жидком металле при T = 1873 К
|
Элемент i |
Элемент j |
||||
|
Al |
O |
С |
Ba |
Mg |
|
|
Al |
0,045 |
–1,62 |
0,0966 |
–0,064 |
–0,000998 |
|
O |
–0,96 |
–0,2 |
–0,45 |
–0,95 |
–1,98 |
|
С |
0,043 |
–0,34 |
0,14 |
–0,006 |
0,007 |
|
Ba |
–0,325 |
–8,155 |
–0,068 |
0 |
–0,12838 |
|
Mg |
–0,0089 |
–3,008 |
0,14 |
–0,0195 |
–0,0085 |
а)
б)
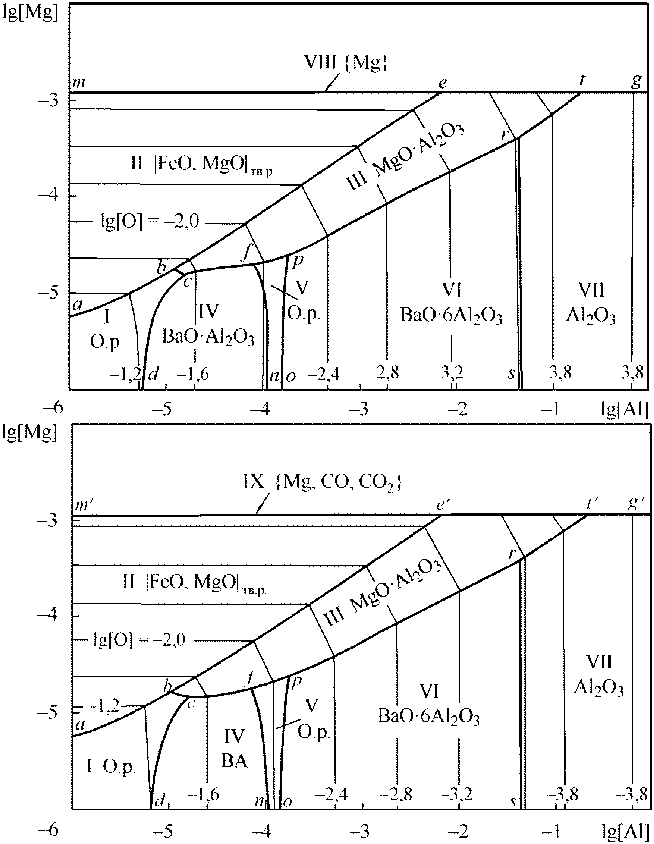
Рис. 7. ПРКМ системы Fe–0,001 % Ba–Mg–Al–O–C, Т = 1600 °C, P общ = 1 атм: а) [C] = 0; б) [C] = 0,1 мас. %
в системе Fe–Mg–Bа–Al–O включения – тугоплавкие.
На рис. 7, а приведена ПРКМ системы Fe–Mg–Bа–Al–O при [Ba] = 0,001 мас. %. Из вида этой диаграммы следует: при предельной концентрации бария и содержании магния порядка 0,001 мас. % в равновесии с металлом в зависимости от концентрации алюминия могут находиться оксид магния MgO и магнезиальная шпинель. И только при очень низкой концентрации магния, порядка 10–5 мас. %, возможно образование алюминатов бария. Естественно, что по механизму эндогенного раскисления образования неметаллических включений образования включений с барием не происходит.
На рис. 7, б приведена поверхность растворимости компонентов системы Fe–Mg–0,0001 % Bа– Al–O–С при 1873 К и [C] = 0,1 мас. %. Можно здесь отметить, что присутствие углерода фактически не сказалось на распределении образующихся фаз по концентрационным полям диаграммы ПРКМ. Только в области IX в равновесии с металлом образуется газовая фаза, содержащая также некоторое количество CO и CO 2 .
Из рассмотренных диаграмм ПРКМ при низких концентрациях магния, бария, алюминия и кислорода следует, что образующиеся включения периклаза, шпинелей, алюминатов бария – это мелкие тугоплавкие частицы, образование которых может модифицировать структуру кристалли- зующегося металла, измельчить первичное литое зерно стали, снизить анизотропию и повысить технологическую пластичность.
Выводы
При низких концентрациях бария, магния и алюминия в металле возможно образование тугоплавких микрофазных образований, в результате которых при кристаллизации стали может реализоваться модифицирующий эффект.
Модифицирующий эффект микросодержаний магния, бария и алюминия может усилиться за счет влияния бария на межфазное натяжение при протекании гетерогенных реакций образования неметаллических включений.
Список литературы Фазовые равновесия при взаимодействии бария с компонентами жидкой стали
- Levin, E.M. Phase Diagrams for Ceramists/E.M. Levin, C.R. Robbins, H.F. McMurdie. -Columbus, Ohio, The American Ceramic Society. -1964. -Vol. 1. -265 p.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов -М.: Издат. Дом МИСИС. -2009. -519 с.
- Wartenberg, H.V. Schmelzdiagramme höchstfeuerfester Oxyde. V. Systeme mit MgO/H.V. Wartenberg, E. Prophet//Zeitschrift für anorganische und allgemeine Chemie. -1932. -Vol. 208, no. 4. -P. 369-379 DOI: 10.1002/zaac.19322080405