Фазовые равновесия в жидких железоуглеродистых сплавах, легированных иттрием и хромом
Автор: Михайлов Геннадий Георгиевич, Макровец Лариса Александровна
Журнал: Вестник Южно-Уральского государственного университета. Серия: Металлургия @vestnik-susu-metallurgy
Рубрика: Физическая химия и физика металлургических систем
Статья в выпуске: 3 т.17, 2017 года.
Бесплатный доступ
В рамках термодинамического моделирования рассматривается взаимодействие между компонентами металлического расплава и кислородом применительно к анализу процессов раскисления и легирования низкоуглеродистых низколегированных сталей, содержащих хром и иттрий. В данной работе использован метод построения поверхностей растворимости компонентов в жидком металле термодинамической системы Fe-Y-Cr-O-С. В рамках реализации этого метода детально исследована система Y2O3-Cr2O3, определены энтальпия и энтропия образования соединения Y2O3•Cr2O3, уточнены координаты точек эвтектического преобразования в системе Y2O3-Cr2O3. На основании уточненных координат линий ликвидус для оксидных двойных систем FeO-Cr2O3, FeO-Y2O3, и Y2O3-Cr2O3 определены энергетические параметры Qijkl в уравнениях зависимости активностей компонентов оксидного расплава FeO-Cr2O3-Y2O3 от состава в модели субрегулярных ионных растворов и рассчитаны координаты поверхности ликвидус оксидной системы FeO-Cr2O3-Y2O3. Так как углерод не растворим в оксидной системе, сопряженной с областью существования жидкого металла, установлено, что в качестве конденсированных неметаллических фаз после легирования металла хромом и модифицирования иттрием образуются оксиды Y2O3 и Cr2O3, соединение Y2O3•Cr2O3, оксидный расплав (FeO, Cr2O3, Y2O3) и газовая фаза {CO, CO2}. Дополнительные термодинамические расчеты показали возможность наличия в оксидном расплаве до 2 % двухвалентного хрома (Cr2+). Разработанная схема фазовых равновесий позволила установить константы равновесия образования оксидов, соединения оксидов, оксидных компонентов расплава и газовых фаз. Рассчитаны также по методу Вагнера активности компонентов металлических расплавов. Совокупность установленных термодинамических параметров позволила построить диаграмму поверхности растворимости компонентов в жидком металле (ПРКМ) и таким образом связать составы жидкой металлической фазы с составом сопряженных оксидных фаз.
Фазовые равновесия, иттрий, хром, диаграммы состояний, термодинамика, раскисление
Короткий адрес: https://sciup.org/147157102
IDR: 147157102 | УДК: 669.017 | DOI: 10.14529/met170301
Phase equilibrium in liquid iron-carbon alloys doped with yttrium and chromium
In the framework of thermodynamic modeling, the interaction between the metallic melt components and oxygen is considered, as applied to the analysis of deoxidation and alloying processes in the low-carbon low-alloy steels containing chromium and yttrium. In this paper a plotting method solubility surfaces of components in a liquid metal of the Fe-Y-Cr-O-C thermodynamic system was used. Within the scope of implementing that method, the Y2O3-Cr2O3 system has been studied in detail, the enthalpy and entropy values of Y2O3•Cr2O3 have been determined, and the coordinates of eutectic points in the Y2O3-Cr2O3 system have been adjusted. Based on the adjusted coordinates of the liquidus curves for oxide binary FeO-Cr2O3, FeO-Y2O3, and Y2O3-Cr2O3 systems, the energy parameters of Qijkl in the FeO-Cr2O3-Y2O3 oxide melt component activity coefficient-composition equations for the sub-regular ionic solutions model have been determined and the coordinates of the liquidus surface of the FeO-Cr2O3-Y2O3 system have been calculated. Since carbon is not soluble in an oxide system conjugated with a field of liquid metal, it has been found that oxides Y2O3 and Cr2O3, Y2O3•Cr2O3, the oxide melt (FeO, Cr2O3, Y2O3) and the gas phase of {CO, CO2} form as the condensed non-metallic phases after chrome alloying and yttrium modification of the metal. Additional thermodynamic calculations suggested the possibility of the oxide melt containing up to 2 % of bivalent chrome (Cr2+). The system of phase equilibria developed during the study allowed to establish the formation constants for oxides, oxide compounds, oxide melt components, and gas phases. Activity coefficients for the metal melts components have also been calculated using Wagner’s method. The set of thermodynamic parameters established made it possible to plot the solubility surface of liquid metal components and link the liquid metal phase compositions to the conjugated oxide phase composition.
Текст научной статьи Фазовые равновесия в жидких железоуглеродистых сплавах, легированных иттрием и хромом
В современном сталеплавильном процессе при выплавке углеродистых малолегированных конструкционных марок сталей повышение механических и эксплуатационных свойств стали добиваются введением в глубо-кораскисленный и провакуумированный металл сплавов, содержащих редкоземельные элементы [1, 2]. Введение РЗМ существенно измельчает литое зерно стали [3, 4], глобуля-ризирует неметаллические включения в стали [4]. Иттрий вводится в металл с целью повышения поверхностной жаростойкости стали. Значительная часть публикаций по этим проблемам отмечает суммарное действие многокомпонентных по РЗМ сплавов [5].
Приводятся также данные по использованию сплавов РЗМ цериевой группы [6], иттриевой группы [7], мишметалла [8]. Но зачастую в табличных данных приводятся просто цифры суммарного содержания редкоземельных элементов – Ce, La, Pr, Nd под общим обозначением РЗМ. Несмотря на в целом схожие химические свойства, в неметаллических включениях присутствуют РЗМ и в виде оксидных, и в виде сульфидных фаз в разных кристаллических образованиях [1]. Это связано и с разным химическим составом используемых сплавов, и с разным сродством редкоземельных металлов к кислороду. Для того чтобы появилась возможность дифференци- рования участия редкоземельных металлов в процессе раскисления, необходимо рассмотреть частные жидкометаллические системы, содержащие отдельные редкоземельные элементы. Вообще говоря, иттрий не относится формально к редкоземельным элементам, но по своим химическим свойствам он близок к редкоземельным металлам. Кроме того, оксиды иттрия входят в состав редкоземельных сырьевых материалов. В настоящей работе предлагается подробно рассмотреть термодинамику процессов раскисления стали иттрием. В методику расчетов входит выполнение ряда операций [9]. В частности, необходимо установить значения констант равновесия для реакций раскисления стали иттрием с образованием оксидов, комплексных оксидных соединений, значения констант равновесия для реакций образования жидких и газообразных фаз [9]. Далее, необходимо построить диаграммы состояний равновесных с металлом оксидных диаграмм состояний и на основании этих данных разработать метод построения поверхностей растворимости компонентов
(иттрия, хрома, кислорода и углерода) в жидком металле (ПРКМ) [10]. На таких диаграммах устанавливаются составы металла, находящегося в равновесии с соответствующими оксидными фазами.
На рис. 1 приведены результаты расчета координаты линий ликвидус, точек эвтектических превращений, а так же определены температуры и теплоты плавления оксидов Y 2 O 3 , Сr 2 O 3 и соединения Y 2 O 3 ·Cr 2 O 3 . Штриховой линией обозначены литературные данные [11], сплошной линией приведены данные, полученные расчетным путем в данной работе. Температуры плавления оксидов и соединения, используемые в расчете, взяты из справочника [11]. Некоторые расхождения с литературными данными наблюдаются в химическом составе эвтектик. Эти данные приведены в табл. 1. При получении расчетных табличных данных использовалась теория субрегулярных растворов. Расчетные формулы активностей в соответствии с этой теорией получены в приближении квадратичной зависимости координационного числа катионов в
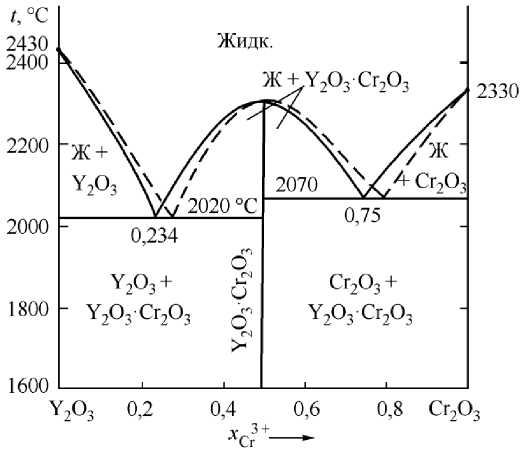
Рис. 1. Диаграмма состояний системы Y 2 O 3 –Сr 2 O 3 : сплошная линия, пунктир – литературная [11]
Таблица 1
Координаты инвариантных точек для системы Y 2 O 3 –Cr 2 O 3
Для оксидных расплавов системы Y2O3– Cr2O3 активности оксидов можно представить следующими выражениями:
In a 1 = 2ln x 1 + 21^3 x 1 x 2 Q 1 1 12 +
+ x 1 x 2 ( 2 - 3 x 1 ) Q 1122 + x 2 ( 1 - 3 x 1 ) Q 1222 ]/ ( RT ) ;
ln a 2 = 2ln x 2 + 2 1^ x 3 ( 1 - 3 x 2 ) Q 1112 +
+ x 1 x 2 ( 2 - 3 x 2 ) Q 1122 + 3 x 1 x 2 Q 1222 J/ ( RT ) , где Y2O3 – 1-й компонент, Cr2O3 – 2-й компонент.
По характерным экспериментальным координатам диаграммы состояний Y 2 O 3 –Cr 2 O 3 (см. рис. 1) установлены величины энергий смешения:
Q 1112 = –7075,
Q 1122 = –23 192,
Q 1222 = –5395 кал/моль, а так же рассчитаны термодинамические данные для образования соединения Y 2 O 3 ·Cr 2 O 3 (энтальпия и энтропия) из компонентов оксидного расплава:
A m H ° o = 63 340 кал/моль, T m
A mSL = 15,64 кал/(моль-К).
T m
В табл. 2 приведены константы реакций плавления, используемые для расчета диаграммы состояний системы Y 2 O 3 –Cr 2 O 3 (реакции (2)–(4)).
При введении в сталь иттрия и хрома состав продуктов раскисления определяется на диаграмме состояний FeO–Y 2 O 3 –Cr 2 O 3 . В литературе отсутствуют какие-либо надежные сведения о диаграмме состояний FeO–Y 2 O 3 –Cr 2 O 3 . Поэтому по данным уже исследованных двойных диаграмм состояний FeO–Y 2 O 3 [13], FeO–Cr 2 O 3 [14] и изученной в данной работе системы Y2O3–Cr2O3 были установлены энергетические параметры теории субрегулярных растворов для тройных систем [9]. Эти сведения представлены в табл. 3.
На рис. 2 представлен расчетный (смоделированный) вариант диаграммы состояний FeO–Y 2 O 3 –Cr 2 O 3 . Были выполнены также расчеты координат (состав и температура) инвариантных равновесий для данной диаграммы (табл. 4).
Из вида тройной оксидной диаграммы следует, что в легированной хромом и модифицированной иттрием стали, в зависимости от температуры и состава металла, возможно образование твердых оксидов |Cr 2 O 3 | и |Y 2 O 3 |, соединений |FeO·Cr 2 O 3 | и |Y 2 O 3 ·Cr 2 O 3 | и оксидного расплава (FeO, Y 2 O 3 , Cr 2 O 3 ). Но оксидный расплав может включать в себя еще и оксид хрома (II). Его активность была приравнена к ионной доле. Активности остальных компонентов оксидного расплава FeO, Y 2 O 3 , Cr 2 O 3 рассчитывали по теории субрегулярных ионных растворов с использованием параметров, приведенных в табл. 3.
Таблица 2
Термодинамические данные для реакций фазовых превращений, K – константа плавления оксидов и их соединений
|
№ |
Реакция |
lg K = – A / T + B |
|
|
A |
B |
||
|
1 |
|FeO| = (FeO) |
1749 |
1,061 |
|
2 |
|Y 2 O 3 | = (Y 2 O 3 ) |
4372 |
1,617 |
|
3 |
|Cr 2 O 3 | = (Cr 2 O 3 ) |
6557 |
2,519 |
|
4 |
|Y 2 O 3 ·Cr 2 O 3 | = (Y 2 O 3 ) + (Cr 2 O 3 ) |
13 845 |
3,419 |
|
5 |
|FeO·Cr 2 O 3 | = (FeO) + (Cr 2 O 3 ) |
12 093 |
4,894 |
Таблица 3
Параметры теории субрегулярных ионных растворов FeO–Y 2 O 3 –Cr 2 O 3
|
Система |
Энергетические параметры, кал/моль |
Источник |
||
|
FeO–Y 2 O 3 |
0 |
0 |
0 |
[13] |
|
FeO–Cr 2 O 3 |
1042 |
6382 |
1283 |
[14] |
|
Y 2 O 3 –Cr 2 O 3 |
–7075 |
–23 l92 |
–5395 |
Данная работа |
|
FeO–Y 2 O 3 –Cr 2 O 3 |
–9000 |
–18 000 |
–17 000 |
Данная работа |
Таблица 4
Инвариантные точки системы FeO–Y 2 O 3 –Cr 2 O 3
|
№ точки |
Равновесие |
Состав, ион. доли |
Т , °С |
||
|
x Fe2 + |
x Y 3 + |
x Cr3 + |
|||
|
1 |
FeO + Y 2 O 3 ·Cr 2 O 3 + Y 2 O 3 + жидкость |
0,77 |
0,22 |
0,01 |
1216 |
|
2 |
FeO·Cr 2 O 3 + FeO + Y 2 O 3 ·Cr 2 O 3 + жидкость |
0,90 |
0,06 |
0,04 |
1314 |
|
3 |
FeO·Cr 2 O 3 + Cr 2 O 3 + Y 2 O 3 ·Cr 2 O 3 + жидкость |
0,37 |
0,15 |
0,48 |
1789 |
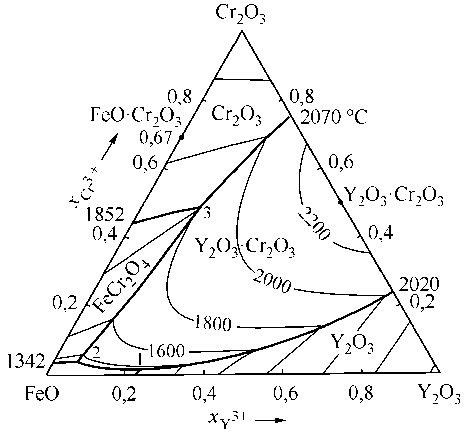
Рис. 2. Расчетные координаты поверхности ликвидус системы FeO–Y 2 O 3 –Cr 2 O 3 для температур выше 1400 °С
В табл. 5 приведены все возможные реакции, протекающие в хромсодержащем железе, раскисленном иттрием.
Активность компонентов в металлическом расплаве рассчитывалась с помощью параметров взаимодействия (по теории Вагнера), их численные значения приведены в табл. 6. Параметр eCYr в литературе не приво- дится. Но известны параметры взаимодействия хрома с сильными раскислителями [16]:
eCLra = 0,0108, eCCre = 0,00642, eCZrr = 0,013, eCMrg = 0,01213, eCCra= 0,016, eCArl = 0,00255.
Видно, что параметр взаимодействия хрома e C Y r в этом случае может быть порядка 0,01. Были проведены расчеты ПРКМ Fe–Y–Cr–O–C
Таблица 5
Зависимости констант равновесия реакций раскисления от температуры
|
№ |
Реакция |
lg K = – A / T + B |
|
|
A |
B |
||
|
1 |
(FeO) = [Fe] + [O] |
6320 |
4,734 |
|
2 |
(Y 2 O 3 ) = 2[Y] + 3[O] |
67 028 |
20,19 |
|
3 |
(Cr 2 O 3 ) = 2[Cr] + 3[O] |
33 460 |
14,85 |
|
4 |
(CrO) = 2[Cr] + [O] |
8203 |
4,51 |
|
5 |
|Y 2 O 3 | = 2[Y] + 3[O] |
71 400 |
21,81 |
|
6 |
|Cr 2 O 3 | = 2[Cr] + 3[O] |
40 014 |
17,37 |
|
7 |
|FeO·Cr 2 O 3 | = [Fe] + 2[Cr] + 4[O] |
51 870 |
24,48 |
|
8 |
|Y 2 O 3 ·Cr 2 O 3 | = 2[Y] + 2[Cr] + 6[O] |
114 333 |
38,459 |
|
9 |
{CO} = [C] + [O] |
1168 |
–2,07 |
|
10 |
{CO 2 } = [C] + 2[O] |
9616 |
2,51 |
Таблица 6
Параметры взаимодействия e i j в жидком железе, T = 1600 °С [15–17]
|
Элемент i |
Элемент j |
|||
|
Cr |
Y |
O |
С |
|
|
Cr |
–0,0003 |
0 |
–0,133 |
–0,104 |
|
Y |
0 |
0,030 |
–4,41 |
–1,21 |
|
O |
–0,041 |
–0,79 |
–0,2 |
–0,45 |
|
С |
–0,024 |
–0,16 |
–0,34 |
0,14 |
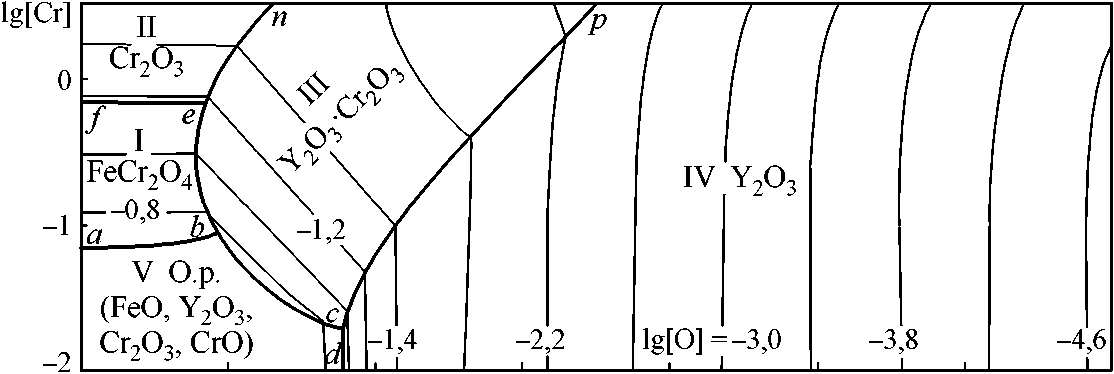
8 -7 -6 -5 -4 -3 -2 lg[Y]
а)
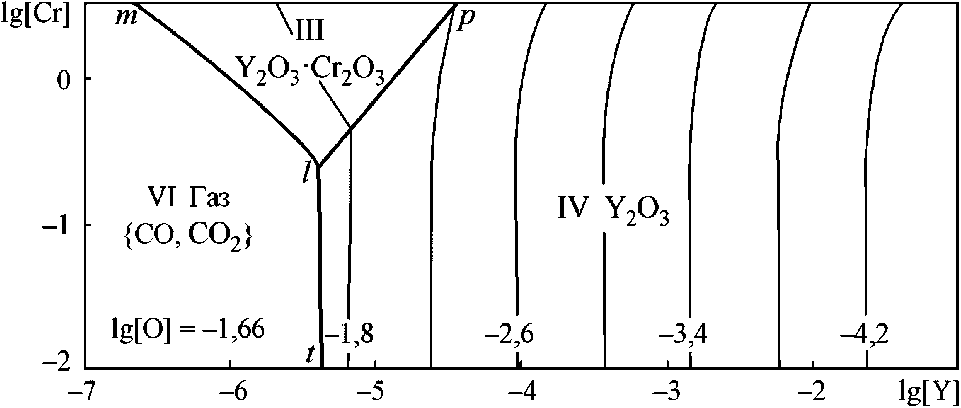
б)
Рис. 3. ПРКМ системы Fe–Y–Cr–O–С, 1600 °C, P общ = 1 атм: а) [C] = 0; б) [C] = 0,1 мас. %
для условий e C Y r = 0 и e C Y r = 0,01. Незначительная разница в результатах расчета начинает проявляться только при [Y] > 10–4 мас. % и [Cr] > 1 мас. %. Поэтому при более низких концентрациях Cr и Y можно считать величину e C Y r ≈ 0, что и было принято в расчетах.
Для расчета координат поверхности растворимости необходимо так же определить константы равновесия для основных реакций раскисления. Эти данные представлены в табл. 5.
На рис. 3, а представлены ПРКМ системы Fe–Y–Cr–O при 1600 °С. На полях рисунка заданы составы металла, равновесного с указанными на этих полях оксидными фазами.
На контрастных линиях заданы составы металла, равновесного с двумя соседними оксидными фазами, в узлах пересечений определены составы металла, равновесного с тремя оксидными фазами. Тонкими линиями обозначены изокислородные сечения ПРКМ. На рис. 3, б представлена ПРКМ системы Fe–Y–Cr–O–С при [C] = 0,1 мас. %. В области VI заданы составы жидкого металла, равновесного с газовой фазой (CO, CO 2 ) на основе CO.
Заключение
-
1. Рассмотрены термодинамические закономерности процессов раскисления иттрием хромсодержащей конструкционной стали. Впервые в приближении теории субрегуляр-
- ных ионных растворов построены диаграммы состояний оксидных систем Y2O3–Cr2O3 и FeO–Y2O3–Cr2O3. В результате расчетов диаграммы Y2O3–Cr2O3 подобраны термодинамические данные для образования соединения У-Оз^Сг-Оз (A mH ° =63 340 кал/моль, A mS° =
-
2. Установлены оксидные фазы, образующиеся после введения иттрия в хромсодержащую малоуглеродистую сталь. Показано, что в зависимости от температуры и исходного состава стали в качестве неметаллических включений могут образовываться твердые Y 2 O 3 , Cr 2 O 3 , FeO·Cr 2 O 3 , Y 2 O 3 ·Cr 2 O 3 , жидкие оксиды (FeO, Cr 2 O 3 , Y 2 O 3 , CrO) и газовая фаза {CO, CO 2 }.
-
3. Разработана методика расчета построения поверхностей растворимости компонентов (ПРКМ) в жидком металле системы Fe–Y–Cr–O–С. Установлена возможность образования в качестве неметаллических включений твердого Y 2 O 3 и соединения Y 2 O 3 ·Cr 2 O 3 .
T m T m
= 15,64 кал/(моль·К)) из компонентов оксидного расплава.
Статья выполнена при поддержке Правительства РФ (Постановление № 211 от 16.03.2013 г.), соглашение № 02.A03.21.0011.
Список литературы Фазовые равновесия в жидких железоуглеродистых сплавах, легированных иттрием и хромом
- Голубцов, В.А. Модифицирование стали для отливок/В.А. Голубцов, В.В. Лунев. -Челябинск; Запорожье: ЗНТУ, 2009. -356 с.
- Рябчиков, И.В. Модификаторы и технологии внепечной обработки железоуглеродистых сплавов/И.В. Рябчиков -М.: ЭКОМЕТ, 2008. -400 с.
- Лунев, В.В. Применение комплексных лигатур с РЗМ и ЩЗМ для улучшения свойств литых и деформированных сталей/В.В. Лунев, Ю.В. Шульте//Влияние комплексного раскисления на свойства сталей: темат. отраслевой сб. МЧМ СССР. -М.: Металлургия, 1982. -С. 33-50.
- Применение редкоземельных металлов в металлургии. -http://www.urm.ru/ru/75-journal124-article64.
- Аверин, В.В. Применение РЗМ в металлургии стали/В.В. Аверин//Металлургические методы повышения качества стали: сб. -М., 1979. -С. 33-40.
- Куликов, И.С. Раскисление металлов/И.С. Куликов. -М.: Металлургия, 1975. -504 с.
- Лопато, Л.М. Фазовые отношения в системах окись магния -окислы РЗЭ цериевой группы/Л.М. Лопато, Л.И. Лугин, А.В. Шевченко//Журнал неорганической химии. -1971. -Т. 16, № 1. -С. 131-133.
- Keune, H. Chimica -ein Wissensspeicher. Wiley-VCH Verlag GmbH & Co, KGaA, Weinheim, 1959 DOI: 10.1002/bbpc.19840880624
- Михайлов, Г.Г. Термодинамика раскисления стали/Г.Г. Михайлов, Д.Я. Поволоцкий. -М.: Металлургия, 1993. -144 с.
- Михайлов, Г.Г. Термодинамика металлургических процессов и систем/Г.Г. Михайлов, Б.И. Леонович, Ю.С. Кузнецов. -М.: Издат. Дом МИСИС. -2009. -519 с.
- Диаграммы состояния силикатных систем. Справочник. Выпуск первый. Двойные системы/Н.А. Торопов, В.П. Барзаковский, В.В. Лапин, Н.Н. Курцева. -Л.: Наука, Ленингр. отд-ние, 1969. -822 с.
- Preliminary data on subsolidus phase equilibria in the La2O3-Сr2O3-Y2O3 and La2O3-Сr2O3-ZrO2 systems/M. Hrovat, S. Bernik, J. Holc et al.//Journal of Materials Science Letters. -1995. -No. 14. -P. 1684-1687 DOI: 10.1007/BF00422675
- Михайлов, Г.Г. Термодинамическое моделирование фазовых равновесий с оксидными системами, содержащими РЗМ. Сообщение 2. Диаграммы состояния оксидных систем с Y2O3/Г.Г. Михайлов, Л.А. Макровец//Вестник ЮУрГУ. Серия «Металлургия». -2014. -Т. 14, № 4. -С. 5-10 DOI: 10.14529/met150401
- Михайлов, Г.Г. Термодинамический анализ процессов раскисления корозионностойкой стали Х18Н10Т кальцием и барием/Г.Г. Михайлов, Л.А. Чернова//Известия вузов. Черная металлургия. -1991, № 12. -С. 37-40.
- Bůžek, Z. Vliv přechodných kovú na aktivitu a rozpustnost kysliku v železe při 1600 °C/Z. Bůžek, M. Macoszek, J. Szlauer//Hutnické listy. -1972. -vol. 27, no 8. -P. 547-557.
- Параметры взаимодействия первого порядка. -http://steelcast.ru/first-order_ interaction_coefficients.
- Балковой, Ю.В. Параметры взаимодействия первого порядка в расплавах на основе железа: Обзор. информ./Ю.В. Балковой, Р.А. Алеев, В.К. Баканов. -М.: Ин-т «Черметинформация», 1987. -42 с.


