Фенольные соединения листьев какалии копьевидной (Cacalia hastata L.)
Автор: Оленников Д.Н., Мазур Л.В., Танхаева Л.М., Ботоева Е.А.
Журнал: Вестник Восточно-Сибирского государственного университета технологий и управления @vestnik-esstu
Статья в выпуске: 4 (31), 2010 года.
Бесплатный доступ
Исследован состав фенольных соединений листьев Cacalia hastata. В результате хроматографического разделения было выделено 11 соединений, идентифицированных с кемпферолом, кверцетином, гиперозидом, рутином, (+)-катехином, умбеллифероном, скополетином, эскулетином, галловой, кофейной и хлорогеновой кислотами, причем флавоноиды и катехин обнаружены в данном растительном виде впервые. Методом ВЭЖХ установлено количественное содержание указанных соединений в листьях Cacalia hastata.
Флавоноиды, кумарины, фенилпропаноиды, вэжх
Короткий адрес: https://sciup.org/142142226
IDR: 142142226 | УДК: 581.198
Phenolic compounds of Cacalia hastata L. Leaves
The composition of phenolic compounds of Cacalia hastata leaves was investigated. As a result of chromatographic separation 11 compounds were isolated and identified as kaempferol, quercetin, hyperoside, rutin, (+)-catechin, umbelliferone, scopoletin, esculetine, gallic, caffeic and chlorogenic acids. Flavonoids and catechin are found in this plant at the first time. Using HPLC quantitative content of these compounds in Cacalia hastata leaves was determined.
Текст научной статьи Фенольные соединения листьев какалии копьевидной (Cacalia hastata L.)
Какалия копьевидная Cacalia hastata L. семейство Астровые Asteraceae Dumort. – лекарственное растение, которое издавна применяется в народной и тибетской медицине как ранозаживляющее и кровоостанавливающее средство, при лечении простудных заболеваний и болезней печени [1].
Cacalia hastata – многолетнее корневищное травянистое растение высотой до 190 см, широко распространено в России; за рубежом встречается на севере Монголии, северо-востоке Китая, Корее, Японии, Северной Америке. C. hastata встречается в разреженных хвойных или мелколиственных лесах, изредка в борах; по опушкам смешанных лесов, в березняках и зарослях ольховника и кедрового стланика. На Дальнем Востоке - также в дубовых лесах, по приречным долинам, в кустарниковых зарослях, на лесных и приречных лугах, в горах по речным долинам в лесном поясе, местами поднимается до нижней части альпийского пояса [2].
Химический состав C. hastata разнообразен и представлен различными группами биологически активных веществ. Из листьев C. hastata были выделены алкалоиды [3], сесквитерпены [4-7], тритерпены [8], каротиноиды [9]. В составе свободных углеводов листьев C. hastata установлено наличие фруктозы, глюкозы и галактозы. Из комплекса водорастворимых полисахаридов выделены глюкоарабиногалактан (какалан А) и два арабиногалактана (какаланы В и С). Пектиновые вещества листьев C. hastata относятся к классу высокоэтерифицированных пектинов, а гемицеллюлозные производные группы А являются ксилоглюкофруктанами, группы Б – ксиланами [10].
Для листьев C. hastata характерно высокое содержание компонентов цикла ди- и трикарбоновых кислот – до 7.2% [11]. Фенольные соединения листьев C. hastata представлены кумаринами и дубильными веществами [12]. Также в C. hastata обнаружены фотосинтетические пигменты [9], аскорбиновая кислота [13], тиамин (2.34±0.14 мг%) и рибофлавин (3.19±0.20 мг%) [12].
Целью настоящей работы является детальное исследование состава фенольных соединений листьев C. hastata .
Экспериментальная часть
Растительное сырье – листья C. hastata были собраны в Мухоршибирском районе (с. Мухорши-бирь) в июле 2008 г. Видовая принадлежность определена д. фарм. н. Асеевой Т.А. (ИОЭБ СО РАН). Образец сырья хранится в гербарии Отдела биологически активных соединений ИОЭБ СО РАН (№ At/f-51/4-07/0807).
Колоночную хроматографию проводили на силикагеле L 100/400 (Chemapol) и полиамиде (Woelm), гель-хроматографию – на Сефадексе LH-20 (Pharmacia), препаративную ТСХ – на пластинах с силикагелем Сорбфил ПТСХ-П-А (Имид Ltd.), ВЭТСХ – на пластинах с силикагелем Сорбфил ПТСХ-АФ-В (Имид Ltd.). Спектрофотометрические исследования проводили на спектрофотометре UV-Vis-mini (Shimadzu). Оптическое вращение определяли на поляриметре СМ-3 (Загорский оптикомеханический завод). ИК-спектры регистрировали на ИК-Фурье спектрометре Spectrum 100 (Perkin-Elmer) в пленке на пластинах КРС-5 в интервале 4000-650 см-1. ГХ/МС анализ проводили на хромато-масс-спектрометре 5973 N (Agilent Technologies) с масс-селективным детектором 6890N (Agilent Technologies) с диффузным насосом с применением капиллярной колонки PH-Innowax (30 м/250 мкм/0.50 мкм). Спектры 13С-ЯМР регистрировали на ЯМР-спектрометре VXR 500S (Varian) с рабочей частотой 125.7 МГц для 1% растворов веществ в ДМСО-d6. ВЭЖХ проводили на микроколоночном жидкостном хроматографе Милихром А-02 (Эконова), колонка Nucleosil 100-5 C18 (5 μм, 75×2 мм), градиентный режим элюирования (А – 0.05 М КН2РО4/МеCN 95:5, В – МеОН), v = 0.15 мл/мин, Т = 35°С, УФ-детектор при λ = 202, 224, 270, 278 нм. В ходе анализа определялись хроматографическая подвижность, спектр в остановленном потоке растворителя, спектральные соотношения, а также проводились опыты с добавками стандартных соединений.
Высушенное измельченное сырье (520 г) экстрагировали пятикратно 80%-ным этанолом (модуль 1:25) при 80°С. Объединенное спиртовое извлечение концентрировали до водного остатка, который подвергали жидкофазной экстракции гексаном, хлороформом, этилацетатом и н -бутанолом что привело к получению следующих фракций: гексановой (22.31 г; 4.29% от массы возд.-сух. сырья), хлороформной (33.80 г; 6.50%), этилацетатной (4.58 г; 0.88%), бутанольной (40.14 г; 7.72%) и водного остатка (107.17 г; 20.61%). Общий выход экстрактивных веществ составил 40% от массы воздушно-сухого сырья.
Для разделения хлороформной фракции (20 г) применяли колоночную хроматографию на силикагеле (3×50 см) в системах гексан-хлороформ (100:0→70:30) и хлороформ-метанол (100:0→50:50) с последующей рехроматографией в условиях гель-хроматографии на LH-20 (2×40 см) в градиентной системе хлороформ-метанол (100:0→0:100), препаративной ТСХ (система толуол-этилацетат-муравьиная кислота 3:3:1) и ВЭТСХ (система петролейный эфир-диэтиловый эфир-муравьиная кислота 9:4:1). В результате выделено пять соединений: 1 (11 мг), 2 (9 мг), 3 (25 мг), 4 (14 мг) и 5 (5 мг).
Этилацетатное (4.2 г) извлечение (7 г) хроматографировали на SiO 2 -колонке (2×30 см) в системах хлороформ-ацетон (100:0→70:30), ацетон-этанол (100:0→50:50), этанол-вода (95:5→40:60). Субфракции разделяли на колонках с полиамидом (2×20 см; элюент этанол-вода 0:100→95:5, ацетон) с последующей препаративной ТСХ (системы толуол-этилацетат-муравьиная кислота 5:4:1, этилацетат-метанол-вода 9.6:1.9:1). Хроматографическое разделение этилацетатной фракции привело к выделению шести соединений: 6 (22 мг), 7 (28 мг), 8 (7 мг), 9 (16 мг), 10 (18 мг) и 11 (84 мг). Выделенные вещества были идентифицированы по данным физико-химического анализа (температура плавления, оптическое вращение), а также УФ-, ИК-, 13С-ЯМР-спектроскопии и МС.
|
R 1 |
R 2 |
|
|
( 3 ) |
OH |
OH |
|
( 4 ) |
OH |
OCH |
|
( 5 ) |
ОН |
Н |
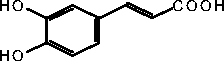
( 6 ) ( 7 )
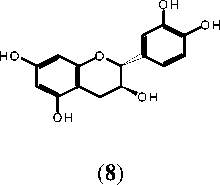
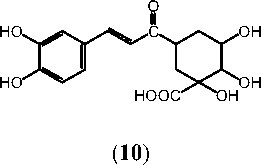
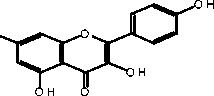
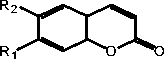
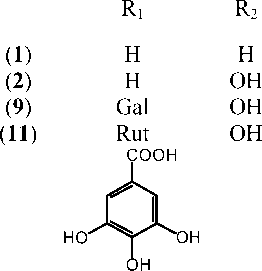
Рис. Структурные формулы соединений, выделенных из листьев C. hastata. Gal – галактоза, Rut – рутиноза
Обсуждение результатов
В результате фракционирования экстрактивных веществ листьев C. hastata был получен ряд узких фракций. Хроматографическое разделение хлороформной и этилацетатной фракций с применением колоночной хроматографии на силикагеле, полиамиде, Сефадексе LH-20, а также препаративной ТСХ и ВЭТСХ, позволило выделить 11 соединений, идентификацию которых проводили с использованием данных физико-химического анализа, УФ-, ИК- 13С-ЯМР-спектроскопии и масс-спектрометрического анализа.
Выделенные соединения относятся к классам флавоноидов – кемпферол ( 1 ; 3,5,7,4'-тетрагидроксифлавон), кверцетин ( 2 ; 3,5,7,3',4'-пентагидроксифлавон), гиперозид ( 9 ; 3,5,7,3',4'-пентагидроксифлавона 3- О -β-галактозид), рутин ( 11 ; 3,5,7,3',4'-пентагидроксифлавона 3- О -рутинозид); катехинов – (+)-катехин ( 8 ; 3,5,7,3',4'-пентагидроксифлаван); кумаринов – умбеллиферон ( 3 ; 6,7-дигидроксикумарин), скополетин ( 4 ; 6-метокси-7-гидроксикумарин), эскулетин ( 5 ; 7-гидроксикумарин); фенольных кислот – галловая ( 6 ; 3,4,5-тригидроксибензойная кислота); фенилпропаноидов – кофейная ( 7 ; 3,4-дигидроксикоричная кислота), хлорогеновая кислоты ( 10 ; 3-кофеил-хинная кислота) (рис.). Соединения 3 - 7 , 10 были ранее выделены из C. hastata [7, 14], а 1 , 2 , 8 , 9 , 11 – обнаружены в данном растительном виде впервые. Доминирующим соединением фенольного комплекса листьев C. hastata является хлорогеновая кислота ( 10 ); в составе флавоноидов преобладает рутин ( 11 ).С применением метода ВЭЖХ проведен количественный анализ состава спиртового экстракта (70% этанол) из листьев C. has-tata (табл.). Установлено, что содержание хлорогеновой кислоты ( 10 ) и рутина ( 11 ) – 18.72 и 9.94 мг/г, соответственно; в пересчете на сырье эти показатели составляют 7.84 и 4.32 мг/г от массы воздушносухого сырья.
Полученные результаты расширяют сведения о химическом составе C. hastata и позволяют определить данный растительный вид в качестве перспективного для дальнейшего химического и фармакологического исследований.
Таблица
Содержание фенольных соединений в спиртовом извлечении и сырье C. Hastate
|
Соединение |
Содержание, мг/г |
|
|
в спиртовом экстракте |
в сырье |
|
|
( 1 ) |
2.04±0.06 |
0.86±0.03 |
|
( 2 ) |
1.14±0.03 |
0.67±0.02 |
|
( 3 ) |
0.42±0.01 |
0.183±0.005 |
|
( 4 ) |
0.64±0.02 |
0.282±0.008 |
|
( 5 ) |
0.052±0.002 |
0.027±0.001 |
|
( 6 ) |
8.63±0.26 |
3.77±0.11 |
|
( 7 ) |
12.84±0.36 |
5.21±0.16 |
|
( 8 ) |
2.33±0.07 |
0.97±0.03 |
|
( 9 ) |
2.88±0.09 |
1.15±0.04 |
|
( 10 ) |
18.72±0.56 |
7.84±0.24 |
|
( 11 ) |
9.94±0.30 |
4.32±0.12 |
Заключение
В результате химического исследования из листьев C. hastatа выделено 11 соединений фенольной природы, 5 из которых обнаружены в данном растительном виде впервые (кемпферол, кверцетин, гипе-розид, (+)-катехин, рутин).


