Феохромоцитома надпочечников в рамках синдрома множественных эндокринных неоплазий 2А типа
Автор: Грицкевич А.А., Байтман Т.П., Чевина А.А., Борукаев А.Ю., Карельская Н.А., Оганян В.А., Грицкевич Е.Ю., Петросян К.А., Животов В.А., Поддубный Е.И.
Журнал: Вестник Национального медико-хирургического центра им. Н.И. Пирогова @vestnik-pirogov-center
Рубрика: Клинические наблюдения
Статья в выпуске: 4-1 т.17, 2022 года.
Бесплатный доступ
Представлено клиническое наблюдение пациента 30 лет с синдромом множественных эндокринных неоплазий 2А типа (МЭН 2А). Клинически заболевание манифестировало артериальной гипертензией. На момент начала обследования артериальное давление (АД), периодически повышавшееся в течение 15 лет, достигало 230/100 мм рт. ст. При мультиспиральной компьютерной томографии (МСКТ) обнаружено объемное образование правого надпочечника диаметром 92 мм, с кистозной трансформацией, несколько образований левого надпочечника, диаметром 6-20 мм. Результаты лабораторных исследований подтвердили гормональную активность новообразования. По данным УЗИ щитовидной железы, в левой доле выявлено узловое образование 44 мм (EU-TIRADS 5). При тонкоигольной аспирационной биопсии (ТАБ) очагового образования щитовидной железы получена цитологическая картина, подозрительная в отношении злокачественной опухоли (Bethesda V), также выявлено повышение уровня кальцитонина более 2000 пг/мл в смыве из узлового образования левой доли. Кальцитонин крови 1920 пг/мл, паратиреоидный гормон - 204,9 пг/мл, кальций общий - 3,02 ммоль/л. В октябре 2021 г., после консервативной предоперационной подготовки селективным блокатором постсинаптических а1 -адренорецепторов доксазозином и стабилизации АД, выполнена правосторонняя адреналэктомия. В послеоперацизивную терапию. Послеоперационный период протекал без осложнений. В апреле 2022 г. выполнена тиреоидэктомия с центральной лимфаденэктомией, субтотальная паратиреоидэктомия (удаление трех околощитовидных желез) по поводу МЭН 2А, медуллярного рака щитовидной железы, первичного гиперпаратиреоза, продолжено динамическое наблюдение объемных образований левого надпочечника. Клинический случай демонстрирует важность тщательного сбора анамнеза, лабораторного и инструментального обследования пациентов с объемными образованиями надпочечников. Своевременная и полноценная диагностика синдрома МЭН 2А позволяет верно определить тактику лечения, избежать характерных пери- и интраоперационных осложнений, значимо улучшить качество жизни и прогноз лечения пациента.
Синдром множественных эндокринных неоплазий, феохромоцитома, медуллярный рак щитовидной железы, мутация ret-протоонкогена, клинический случай
Короткий адрес: https://sciup.org/140296600
IDR: 140296600 | DOI: 10.25881/20728255_2022_17_4_2_156
Adrenal pheochromocytoma within the multiple endocrine neoplasia type 2A syndrome
A clinical case of a 30-year-old patient with type 2A multiple endocrine neoplasia syndrome (MEN 2A) manifesting with arterial hypertension is considered. At the beginning of the survey, blood pressure (BP), which had been periodically rising for 15 years, reached 230; 100 mm Hg. Computed tomography (MSCT) revealed a tumour of the right adrenal gland with a diameter of 92 mm, with cystic transformation, several tumours of the left adrenal gland, with a diameter of 6-20 mm. The results of laboratory studies confirmed the hormonal activity of the neoplasm. The mother and the sister of the patient’s mother have tumors of the thyroid gland. According to the ultrasound of the patient’s thyroid gland, echographic signs of multinodular goiter (EU-TIRADS 5). Fine-needle aspiration biopsy of a focal thyroid tumour revealed an increase in the level of calcitonin by more than 2000 pg/ml in a wash from a needle. The right-sided adrenalectomy was performed in October 2021, after conservative preoperative preparation with a selective blocker of postsynaptic a1-adrenergic receptors doxazosin and stabilization of BP. The normalization of the BP was noted in the postoperative period, which made it possible to cancel the antihypertensive therapy. The postoperative period proceeded without any complications. Thyroidectomy with central lymphadenectomy, total parathyroidectomy for medullary thyroid cancer, primary hyperparathyroidism was performed in April 2022, and dynamic monitoring of the left adrenal gland is continuing. The clinical case demonstrates the importance of careful history taking, laboratory and instrumental examination of patients with adrenal masses. Timely and complete diagnosis of the MEN 2A syndrome allows to determine the tactics of treatment, to avoid typical peri- and intraoperative complications, and significantly improves the quality of life and prognosis of the patient.
Текст научной статьи Феохромоцитома надпочечников в рамках синдрома множественных эндокринных неоплазий 2А типа
Актуальность
МЭН относят к нейроэндокринным опухолям (НЭО), обширной группе новообразований, исходящих из нейроэндокринных клеток эмбриональной кишки, которым присуща биологическая активность [1]. Большинство НЭО носят спорадический характер, их факторы риска недостаточно изучены на данный момент
-
[2] . НЭО встречаются во всех органах, происходящих из нейроэктодермы. В период эмбриогенеза часть клеток нейроэктодермы располагается по обе стороны от нервной трубки и образует нервный гребень (ганглиозную пластинку), из которой развиваются спинномозговые узлы. Другая часть мигрирует в поверхностный слой дермы (меланоциты) или
- во внутренние органы (ганглии вегетативной системы, мозговое вещество надпочечников, хромаффинная ткань). Часть эктодермы формирует прехордальную пластинку, будущий эпителий полости рта, глотки, пищевода, трахеи, бронхов и легких. Данная особенность эмбриогенеза приводит к развитию опухолей в органах, выполняющих различные функции.

История изучения НЭО началась в 1907 г., когда немецкий патологоанатом Зигфрид Оберндорфер (S. Obern-dorfer) описал своеобразные опухоли тонкой кишки, назвав их «карциноиды» [3]. Первоначально эти опухоли расценивались как доброкачественные, хотя гистологическая характеристика соответствовала злокачественным опухолям, что стало основанием для выделения их в особую группу «карциномоподобных» опухолей.
Современные представления о НЭО начали формироваться в конце 1960-х гг., когда английский патологоанатом A.G. Pearse открыл так называемую APUD-систему (Amine Precursor Uptake and Decarboxylation) — диффузно разбросанные в различных тканях и органах клетки, которые обладали сходными свойствами поглощать предшественники аминов (L-дигидроксифенилаланин и 5-гидрокситриптофан) и декарбоксилировать их с образованием аминов, необходимых для синтеза регуляторных пептидов. Клетки, которые описывал A.G. Pearse, обладали свойствами как нервных, так и эндокринных клеток, что обусловило появление термина «нейроэндокринные опухоли» [4]. Другой английский патологоанатом, К. Lengli, в 1994 г. выделил следующие основные характеристики нейроэндокринных клеток: продукцию нейротрансмиттеров, нейромодуляторов или нейропептидных гормонов; наличие секреторных гранул с плотным ядром, из которых высвобождаются гормоны посредством экзоцитоза в ответ на внешний стимул; отсутствие аксонов и синапсов [5]. Всеми этими свойствами обладают и опухолевые нейроэндокринные клетки.
К группе НЭО относятся карциноиды, мелкоклеточный рак легкого, феохромоцитома (ФХЦ), параганглиома, эндокринные опухоли поджелудочной железы (гастринома, инсулинома, глюкагонома, соматостатинома), адренокортикальный рак, медуллярный рак щитовидной железы, опухоли аденогипофиза). НЭО могут развиваться в различных органах и тканях и обладают свойствами, отличающими их от классических опухолевых образований. Это продукция специфических веществ, экспрессия их в ткани. Данные свойства НЭО активно используются в современной диагностике — определение опухолевых маркеров в крови и тканях. В последние десятилетия в мире отмечается рост заболеваемости НЭО [6]. Подходы к терапии НЭО различны и зависят от степени дифференцировки опухоли.
Синдромы МЭН классифицируют по основным клиническим проявлениям, обусловленным нарушениями секреции гормонов в зависимости от локализации гиперплазии или опухоли эндокринных желез. Эти формы отличаются друг от друга также распространенностью, возрастом манифестации заболевания, типом мутации, ассоциацией с другими заболеваниями и прогнозом. Заболеваемость МЭН 2 в мире составляет 1 на 35 000 населения [7]. Синдром МЭН 2A наиболее распространен (90% пациентов с МЭН 2), тогда как синдром МЭН 2B (5–10% всех случаев) — более редкий и агрессивный вариант заболевания [8].
МЭН 2А включает медуллярный рак щитовидной железы (мРЩЖ), ФХЦ и гиперплазию околощитовидных желез. Чаще (в 97% случаев) синдром МЭН 2А диагностируется при обследовании по поводу мРЩЖ, но в 3% случаев первым проявлением заболевания является ФХЦ [9]. ФХЦ, как правило двусторонняя и/или многофокусная, имеет место у 40–50% пациентов с MEN2 [10].
МЭН 2А входит в группу синдромов, обусловленных эмбриональными мутациями гена RET (rearranged during transfection), включающего 21 экзон, размещенного на хромосоме 10q11.2 [11]. RET — протоонкоген, который может активироваться при генетической рекомбинации, был открыт в 1985 году [12]. Его продуктом является тирозинкиназа рецепторного типа, отвечающая за рост, дифференцировку и выживание клетки. Мутация гена RET в эмбриональных клетках приводит к экспрессии патологически модифицированного сверхактивного RET-протеина в ней роэндокринных тканях, что влечет за собой бесконтрольную клеточную пролиферацию [13]. Заболевание диагностируется редко, поражает оба пола с одинаковой частотой. В настоящее время описано более 1000 семейных линий МЭН 2, а спорадические варианты практически не встречаются. Почти в 50% случаев первопричиной синдрома является герминативная мутация RET, которая возникает только в отцовском аллеле [14].
Критерии установления диагноза:
-
1) данные анамнеза;
-
2) данные лабораторных и инструментальных исследований;
-
3) результаты патолого-анатомического исследования биопсийного (операционного) материала.
ФХЦ встречаются относительно редко, ежегодно выявляется 2–9 новых случаев на 1 млн. населения [15–17]. ФХЦ, в том числе вне синдрома МЭН 2, составляют до 30% среди всех новообразований надпочечников [18]. Как правило, это заболевание диагностируется в 30–50 лет, с одинаковой частотой у мужчин и женщин [17; 19].
Одним из наиболее значимых клинических маркеров ФХЦ в рамках МЭН 2А является артериальная гипертензия, которая характеризуется кризовым течением и является пароксизмальной. У пациентов могут отмечаться приступы сердцебиения, тревожного состояния, головной боли или потливости, но во многих случаях симптомы отсутствуют. Терапия классическими антигипертензивными препаратами в данном случае малоэффективна. Перечисленные критерии отграничивают иные факторы и состояния, являющиеся причиной вторичной артериальной гипертензии.
Таким образом, актуальность синдрома МЭН 2 и, в частности, ФХЦ обусловлена тяжелым течением, поражением преимущественно пациентов трудоспособного возраста, а также редкостью, затрудняющей своевременное распознавание и формирование единых рекомендаций по диагностике и лечению данного синдрома.
Описание набдюдения
Пациент: Н., 29 лет, обратился с жалобами на повышение систолического артериального давления до 230 мм рт. ст. Из анамнеза: с 14 лет отмечает эпизоды повышения артериального давления до 150 мм рт. ст. С июля-августа 2021 г. артериальное давление повышается до 230 мм рт. ст., начато обследование. В связи с вышеуказанными жалобами пациент обратился в ФГБУ «Национальный медицинский исследовательский центр хирургии им. А.В. Вишневского» Минздрава РФ для определения дальнейшей тактики лечения.
В сентябре 2021 г. пациенту была выполнена МСКТ с внутривенным контрастным усилением. Выявлено объемное образование правого надпочечника 92 мм, с частичной кистозной трансформацией, несколько более мелких образований левого надпочечника размером 6–20 мм (Рис. 1, 2). В правом надпочечнике образование 92 мм, с четкими контурами, гетерогенное, преимущественно солидного строения, с частичной кистозной трансформацией. В солидном компоненте визуализируются крупнокалиберные сосуды, градиент накопления контрастного вещества (КВ) 90 HU, максимальное накопление КВ солидным
компонентом в венозную фазу контрастного усиления. В структуре солидного компонента одиночные мелкие аморфные кальцинаты. Плотность кистозного компонента 13 HU. В левом надпочечнике образование 20 мм, с четкими контурами, гетерогенного, преимущественно солидного строения, с точечными кистозными включениями. Градиент накопления КВ солидным компонентом 95 HU, максимальное накопление КВ солидным компонентом в венозную фазу контрастного усиления. В структуре солидного компонента кальцинаты не выявлены. Также в теле и медиальной ножке надпочечника два аналогичных образования, 6 мм и 10 мм. Нет признаков распространения образования правого надпочечника на паренхиму правой почки, правой доли печени. Метастазы в паренхиматозных органах, лимфатических узлах не выявлены. По данным МРТ, образование в правом надпочечнике окружено тонкой псевдокапсулой, солидный компонент выраженно ограничивает диффузию, кистозный компонент с высоким содержанием белка, седиментацией содержимого (Рис. 3).
Проведено лабораторное исследование, представленное в Табл. 1.
По данным семейного анамнеза у матери и её сестры — новообразования щитовидной железы. Проведено молекулярно-генетическое исследование: массовое параллельное секвенирование. В гене RET (NM 020975.6) в 10 экзоне обнаружен ранее описанный в литературе вариант (HG38, chr10:43113622G>C, c.1826G>C) в гетерозиготном состоянии, приводящий к аминокислотной замене p.Cys609Ser с глубиной покрытия 388х (rs77939446), патогенный. По данным УЗИ щитовидной железы, в левой доле
Табл. 1. Лабораторные показатели пациента Н. до оперативного лечения
|
Показатель |
Значение |
Референсный интервал |
|
Метанефрин сут. мочи (мкг/сут) |
9764,0 |
44,0–261,0 |
|
Норметанефрин сут. мочи (мкг/сут) |
3808,0 |
128,0–484,0 |
|
АКТГ утр., пг/мл |
22,0 |
<60,0 |
|
Кортизол утр. в ходе ночного дексаметазонового теста, нмоль/л |
40,0 |
<50,0 |
|
Ренин, мкМЕ/мл |
360,6 |
4,4–46,1 |
|
Альдостерон, пг/мл |
136,0 |
22,1–353,0 |
|
ТТГ, мЕд/л |
2,0 |
0,4–4,0 |
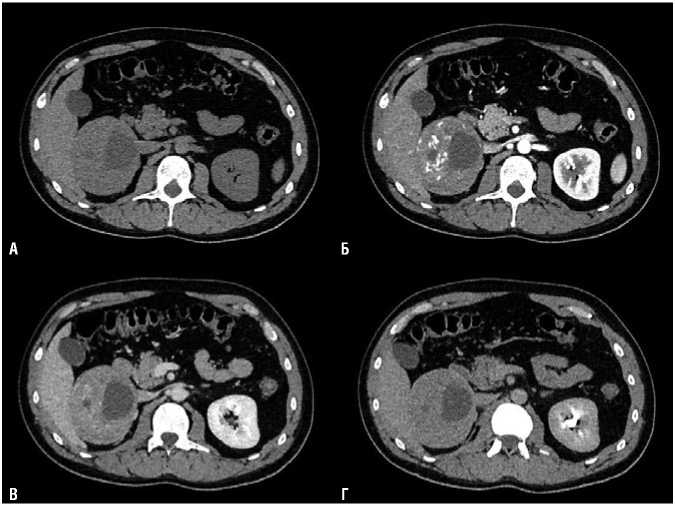
Рис. 1. Данные КТ с внутривенным контрастным усилением (A — нативная, Б — артериальная, В — венозная, Г — отсроченная фаза). В правом надпочечнике образование 92 мм, гетерогенного, преимущественно солидного строения, с частичной кистозной трансформацией. В солидном компоненте визуализируются крупнокалиберные сосуды, градиент накопления КВ 90 HU, максимальное накопление КВ солидным компонентом в венозную фазу контрастного усиления. В структуре солидного компонента одиночные мелкие аморфные кальцинаты. Плотность кистозного компонента 13 HU.
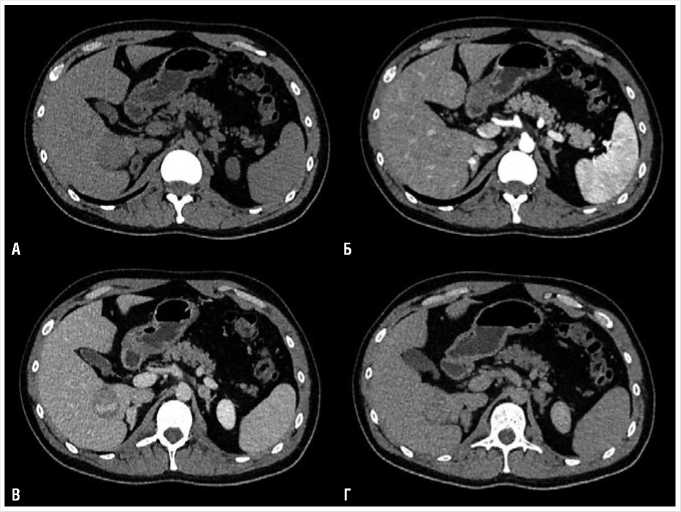
Рис. 2. А — нативная, Б — артериальная, В — венозная, Г — отсроченная фаза. Данные КТ с внутривенным контрастным усилением. В левом надпочечнике образование 20 мм, гетерогенного, преимущественно солидного строения, с точечными кистозными включениями. Градиент накопления КВ солидным компонентом 95 HU, максимальное накопление КВ солидным компонентом в венозную фазу контрастного усиления. В структуре солидного компонента кальцинаты не выявлены.

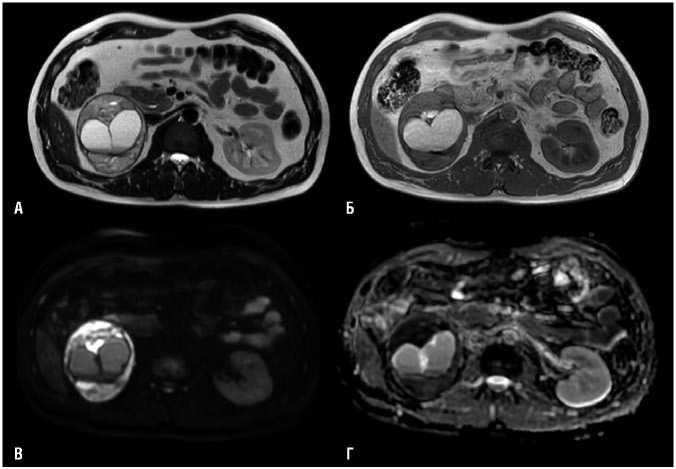
Рис. 3. Данные МРТ. А — Т2, Б — Т1, В — ДВИ, Г — ИКД. В правом надпочечнике образование 92 мм, гетерогенного, преимущественно солидного строения, окружено тонкой псевдокапсулой, солидный компонент выраженно ограничивает диффузию. Кистозный компонент с высоким содержанием белка, седиментацией содержимого.
выявлено узловое образование пониженной эхогенности с множественными кальцинатами, с неровными контурами размерами 27 x 2,5 x 2,5 см (EU-TIRADS 5), визуализируются паратрахеальные лимфоузлы размерами 1,7 x 0,8 см неоднородной структуры. При тонкоигольной аспирационной биопсии (ТАБ) очагового образования щитовидной железы получена цитологическая картина, подозрительная в отношении злокачественной опухоли (Bethesda V), также выявлено повышение уровня кальцитонина более 2000 пг/мл в смыве из узлового образования левой доли. Кальцитонин крови 1920 пг/мл, паратиреоидный гормон — 204,9 пг/мл, кальций общий — 3,02 ммоль/л.
В связи с наличием характерной клинической картины, отягощенного семейного анамнеза по материнской линии, данных инструментальной и лабораторной диагностики был уставлен диагноз: синдром множественной эндокринной неоплазии 2А типа (герминальная мутация в гене RET c.1826G>C p.Cys609Ser). ФХЦ правого надпочечника с преобладающим метанефриновым типом секреции. Вторичная артериальная гипертензия. Медуллярный рак щитовидной железы cT3N1aMx. Первичный гиперпаратиреоз, бессимптомная форма. Гиперплазия околощитовидных желез справа.
В октябре 2021 г. была выполнена правосторонняя адреналэктомия. Продолжительность операции состави- ла 170 мин, кровопотеря — 300 мл. Во время операции не отмечено эпизодов неконтролируемой нестабильной гемодинамики.
Гистологическое исследование: с учетом результатов иммуногистохимического исследования морфологическая картина соответствует ФХЦ правого надпочечника, размером 9,5 x 10 x 7 см. Узел ограничен собственной псевдокапсулой, без врастания в нее. В подпаянном фрагменте печени без элементов опухоли. Узел удален целиком. рТ2 сNх сМ0; М8120/3; Рn0; L0; V0; R0 (AJCC, TNM 8th ed).
Сразу после удаления новообразования отмечено значительное снижение АД. Послеоперационный период протекал без осложнений. Проводилась заместительная гормональная терапия, инфузионная, гастропротекторная, анальгетическая терапия, антитромботическая и антибактериальная профилактика. Данные контрольных обследований представлены в табл. 2.
Достигнуты стабильные целевые показатели АД (110–115/70–80 мм рт. ст.), электролитного обмена. На втором этапе в 2022 г. пациенту выполнены тиреоидэктомия, центральная лимфаденэктомия, субтотальная паратиреоидэктомия (удаление трех околощитовидных желез).
Гистологическое исследование: медуллярный рак щитовидной железы с депозитами амилоида в строме, без признаков инвазивного роста в капсулу
Табл. 2. Лабораторные показатели пациента Н. после оперативного лечения
|
Показатель |
Значение |
Референсный интервал |
|
Метанефрин сут. мочи (мкг/сут) |
133, 6 |
44,0–261,0 |
|
Норметанефрин сут. мочи (мкг/сут) |
334,8 |
128,0–484,0 |
|
Холестерин, ммоль/л |
5,4 |
|
|
Белок общий, г/л |
53,0 |
60,0–85,0 |
|
K+, ммоль/л |
3,50 |
3,5–5,2 |
доли, 1 из 5 лимфатический узел с признаками метастатического поражения pT2(m)pN1apMх Рn0; LV0; R0 (AJCC, TNM 8th ed). Аденомы двух околощитовидных желез.
Послеоперационный период без осложнений. Пациент получает заместительную терапию гормонами щитовидной железы. Через 14 дней после операции пациент приступил к работе.
В настоящее время АД стабильно и не превышает целевые показатели. По данным контрольных анализов от июня 2022 г., также нет отклонений от референсных значений. Продолжено динамическое наблюдение объемных образований левого надпочечника.
Обсуждение
За последние десятилетия отмечено повышение частоты встречаемости ФХЦ в рамках синдрома МЭН 2, что, возможно, объясняется совершенствованием методов лучевой и лабораторной диагностики, а также более детальным изучением причин артериальной гипертензии у пациентов [20].
Синдром артериальной гипертензии считается ведущим проявлением ФХЦ [21]. Клиническая картина ФХЦ очень многогранна — от классических симпато-адреналовых кризов с вегетососудистыми реакциями до бессимптомных форм, когда опухоль диагностирует во время или после операции [22]. Характерной чертой гипертонического криза при ФХЦ является его непродолжительность и купирование без приема гипотензивных препаратов [23]. Другой маркер ФХЦ — наличие факторов, провоцирующих гипертонический криз (смена положения тела, физическая нагрузка, пальпация опухоли, прием β-адрено-блокаторов, прием пищи или голодание, наркоз) [24].
У пациентов с ФХЦ, помимо артериальной гипертензии, часто отмечаются тахикардия, нарушения ритма сердца, ди-
латационная кардиомиопатия, гипокалиемия, полиурия. В связи с этим пациенты данной категории имеют высокий риск кардиальных осложнений в периоперационной периоде. Перед оперативным вмешательством рекомендуется выполнить эхокардиографию, холтеровское мониторирование. При регистрации нарушений ритма сердца в медикаментозную терапию включаются бета-адреноблокаторы, блокаторы кальциевых каналов.
Анестезиологическое пособие при хирургическом лечении ФХЦ является сложной задачей. При отсутствии противопоказаний чаще используется сочетание комбинированной общей и эпидуральной анестезии. Обязательно применение инвазивного мониторинга артериального давления, при выраженных и плохо контролируемых колебаниях гемодинамики измеряется давление заклинивания легочной артерии (ДЗЛА) при помощи катетера Сван-Ганца для оценки преднагрузки [25]. С целью коррекции гемодинамики применяются урапидил, норадреналин, адреналин, заместительная гормональная терапия гидрокортизоном или метилпреднизолоном.
В настоящее время хирургическое вмешательство является единственным доступным методом лечения, но несет в себе потенциальные риски, включая гипертонические и гипотензивные кризы, нарушения ритма сердца, инфаркт миокарда, острые нарушения мозгового кровообращения из-за высвобождения катехоламинов из опухоли во время индукции в наркоз и манипуляций с опухолью [26].
На сегодняшний день не достигнуто единого мнения относительно «идеальной» предоперационной стратегии, отчасти из-за недостатка данных высококачественных научно обоснованных исследований, сравнивающих различные схемы лечения.
В представленном клиническом случае у пациента с генетически подтвержденным диагнозом синдрома МЭН 2А имеются два классических компонента синдрома: очаговое образование щитовидной железы, секретирующее кальцитонин, медуллярный рак щитовидной железы, первичный гиперпаратиреоз двусторонняя ФХЦ с преобладающим мета-нефриновым типом секреции. Примечательно, что, несмотря на данные многочисленных источников о том, что МЭН 2А манифестирует с проявлений МРЩЖ, в случае нашего пациента заболевание стартовало с проявлений симптоматики ФХЦ, а именно вторичной артериальной гипертензии, длительно текущей и плохо контролируемой. Данный аспект демонстрирует важность проведения тщательной дифференциальной диагностики синдрома артериальной гипертензии у пациентов на ранних этапах. Своевременное определение причины артериальной гипертензии и вовремя начатое лечение во многом влияют на благоприятный исход заболевания. В случае нашего пациента гипертензию надпочечникового происхождения можно было предположить, исходя из данных анамнеза: артериальная гипертензия с подросткового возраста, которая имела кризовое течение с быстрым повышением артериального давления, сопровождалась классической триадой катехоламинового криза: тахикардия, профузное потоотделение, головная боль; также ввиду отсутствия определенных критериев исключались иные причины вторичной АГ. Но необходимо учесть тот факт, что для ФХЦ артериальная гипертензия не всегда является обязательным компонентом.
Поставить точный клинический диагноз МЭН 2А, основываясь лишь на данных анамнеза, затруднительно, так как его частота в популяции не так высока, а клинические симптомы нерепрезентативны. В данном вопросе необходимы настороженность и своевременность в диагностике и лечебной тактике, в сомнительных случаях следует проводить молекулярно-генетическое исследование как можно раньше, во избежание ошибочного диагноза. В завершение данного клинического примера стоит добавить, что выявление артериальной гипертензии в молодом возрасте при тщательно собранном анамнезе должно явиться поводом для исключения ее надпочеч-никого генеза.
Заключение
Проблемы комплексной диагностики, лечения и, в частности, особенностей периоперационного ведения и анестезиологического пособия при ФХЦ сохраняют свою значимость, несмотря на большие достижения за последние годы. Данный клинический случай демонстрирует важность тщательного сбора анамнеза заболевания и семейного анамнеза, своевременной диагностики множественных неоплазий с целью подбора адекватной тактики лечения пациента. При отсутствии своевременного выявления и лечения ФХЦ в рамках множественных неоплазий повышается риск летальных осложнений. Пациенты с синдромом МЭН 2А на протяжении всей жизни должны находиться под наблюдением, вследствие того что медуллярный рак щитовидной железы и ФХЦ часто рецидивируют. Необходимо также помнить о генетическом обследовании, исследовании ближайших родственников для выявления мутации и принятия решения о дальнейшей тактике ведения.
Согласие пациента . Пациент добровольно подписал информированное согласие на публикацию персональной медицинской информации в обезличенной форме.
Авторы заявляют об отсутствии конфликта интересов (The authors declare no conflict of interest).
Список литературы Феохромоцитома надпочечников в рамках синдрома множественных эндокринных неоплазий 2А типа
- Клинические рекомендации по ней роэндокринным опухолям / Общероссийский национальный союз «Ассоциация онкологов России»; Общероссийская общественная организация «Российское общество клинической онкологии»; Общественная организация «Российская ассоциация эндокринологов», 2020. — 52 с.
- Eriksson B, Klöppel G, Krenning E, et al. Consensus guidelines for the management of patients with digestive neuroendocrine tumors — welldifferentiated jejuna-ileal tumor/carcinoma. Neuroendocrinology. 2008; 87: 8-19.
- Oberndorfer S. Uber die „kleinen Dunndarm Carcinome“. Verh Dtsch Ges Pathol. 1907; 11: 113-116.
- Pearse A.G. The cytochemistry and ultrastructure of polypeptide hormone-producing cells of the APUD series and the embryologic, physiologic and pathologic implications of the concept. J Histochem Cytochem. 1969; 17(5): 303-313. doi: 10.1177/17.5.303.
- Langley K. The neuroendocrine concept today. Ann N Y Acad Sci. 1994; 733: 1-17. doi: 10.1111/j.1749-6632.1994.tb17251.x.
- Алекберзаде А.В., Крылов Н.Н., Гарманова Т.Н., Шахбазов Р., Азари Ф., Зуйкова К.С., Литовченко Е.Д. Нейроэндокринные опухоли двенадцатиперстной кишки // Хирургия. Журнал им. Н.И. Пирогова. — 2019. — №7. — С.87-95. doi: 10.17116/hirurgia2019071.
- Znaczko A, Donnelly DE, Morrison PJ. Epidemiology, clinical features, and genetics of multiple endocrine neoplasia type 2B in a complete population. Oncologist. 2014; 19(12): 1284-1286. doi:10.1634/theoncologist.2014-0277.
- Юкина М.Ю., Гончаров Н.П., Бельцевич Д.Г., Трошина Е.А. Множественная эндокринная неоплазия 2-го типа // Проблемы эндокринологии. — 2011. — Т.57 — №6. — С.21-22. doi.org/10.14341/probl201157621-26.
- Brandi ML, Gagel RF, Angeli A. Guidelines for diagnosis and therapy of MEN type 1 and type 2. J Clin Endocrinol Metab. 2001; 86(12): 5658–5671.
- Thosani S, Ayala-Ramirez M, Palmer L, Hu MI, Rich T, Gagel RF, Cote G, Waguespack SG, Habra MA, Jimenez C. The characterization of pheochromocytoma and its impact on overall survival in multiple endocrine neoplasia type 2. J Clin Endocrinol Metab. 2013; 98(11): E1813-1819. doi: 10.1210/jc.2013-1653.
- RET fusions in solid tumors. A.Y. Li, et al. Cancer Treatment Reviews. 2019; 81: 101911. doi: 10.1016/j.ctrv.2019.101911.
- Takahashi M, Ritz J, Cooper G.M. Activation of a novel human transforming gene, ret, by DNA rearrangement. Cell. 1985; 42(2): 581-588. doi: 10.1016/0092-8674(85)90115-1.
- Raue F, Frank-Raue K. Multiple endocrine neoplasia type 2. Horm Res. 2007; 68: 101-104. doi: 10.1159/000110589.
- Kaufman FR, Roe TF, Isaacs HJr, Weitzman JJ. Metastatic medullary thyroid carcinoma in young children with mucosal neuroma syndrome. Pediatrics. 1982; 70: 263-267.
- Farrugia FA, Martikos G, Tzanetis P, Zavras N, Charalampopoulos A, Sotiropoulos D, Koliakos N, Paspala A, Kephalidi Er, Machairas A. Adrenal incidentaloma or epinephroma and review of the literature. Differential diagnosis of adrenal incidentaloma. Khirurgiia. 2016; 82: 120-128.
- Andrade MO, Cunha VSD, Oliveira DC, Moraes OL, Lofrano-Porto A. What determines mortality in malignant pheochromocytoma? — Report of a case with eighteen-year survival and review of the literature. Arch Endocrinol Metab. 2018; 62: 264269. doi: 10.20945/2359-3997000000033.
- Farrugia FA, Charalampopoulos A. Pheochromocytoma. Endocr Regul. 2019; 53(3): 191212. doi: 10.2478/enr-2019-0020.
- Бельцевич Д.Г., Мельниченко Г.А., Кузнецов Н.С. Трошина Е.А., Платонова Н.М., Ванушко В.Э., Юкина М.Ю., Молашенко Н.В. Клинические рекомендации Российской ассоциации эндокринологов по дифференциальной диагностике инциденталом надпочечников // Эндокринная хирургия. — 2016. — Т.10. — №4. — С.31-42. doi: 10.14341/serg2016431-42.
- Rossitti HM, Soderkvist P, Gimm O. Extent of surgery for phaeochromocytomas in the genomic era. Br J Surg. 2018; 105: e84–e98. doi: 10.1002/bjs.10744.
- Кузнецов Н.С., Бельцевич Д.Г., Ванушко В.Э., Солдатова Т.В., Ремизов О.В., Кац Л.Е., Лысенко М.А. Дифференциальная диагностика инциденталом надпочечников // Эндокринная хирургия. — 2011. — Т. 5. — №1. — С.5-16. doi.org/10.14341/2306-3513-2011-1-5-16.
- Джериева И.С. Антоненко М.И., Оруджов С.О., Омельченко К.А. Болезни современных технологий или «эпидемия» инциденталом надпочечников // Здоровье и образование в XXI веке. — 2014. — Т.16. — №2. — С.29-30.
- Заривчацкий М.Ф., Колеватов А.П., Шевчук Е.В., Косяк А.А. и др. Случай успешного лечения пациента с недиагностированной («немой») феохромоцитомой // Современные аспекты хирургической эндокринологии: материалы XIX российского симпозиума с международным участием. 15–17 сентября 2010 года. Челябинск. — Челябинск, 2010. — С.126-127.
- Дедов И.И., Бельцевич Д.Г., Кузнецов Н.С. и др. Феохромоцитома. — Москва: Практическая медицина, 2005. — 230 с.
- Котельникова Л.П., Федачук А.Н., Мокина Г.Ю. Клинико-морфологические особенности хромаффинных опухолей // Медицинский альманах. — 2014. — №5(35). — С.142-145.
- Li N, Kong H, Li SL, Zhu SN, Wang DX. Combined epidural-general anesthesia was associated with lower risk of postoperative complications in patients undergoing open abdominal surgery for pheochromocytoma: A retrospective cohort study. PLoS One. 2018 Feb 21; 13(2): e0192924. doi: 10.1371/journal.pone.0192924.
- Challis BG, Casey RT, Simpson HL, Gurnell M. Is there an optimal preoperative management strategy phaeochromocytoma/paraganglioma? Clin Endocrinol (Oxf). 2017; 86(2): 163-167. doi: 10.1111/cen.13252.


