Ферментативная активность различных органов и тканей дальневосточного трепанга как система индикаторов созревания и качества продукции
Автор: Пивненко Татьяна Николаевна, Позднякова Юлия Михайловна, Ковалев Николай Николаевич, Михеев Евгений Валерьевич, Есипенко Роман Владимирович
Журнал: Вестник Мурманского государственного технического университета @vestnik-mstu
Рубрика: Биотехнология пищевых продуктов и биологически активных веществ
Статья в выпуске: 3 т.21, 2018 года.
Бесплатный доступ
Рассмотрены активность, субстратно-ингибиторная специфичность, температурная и рН зависимости, сезонные изменения протеолитических и нуклеолитических ферментных систем пищеварительного тракта, мышечной и репродуктивной тканей трепанга. Показана разнонаправленная изменчивость активности ферментов на разных стадиях развития. На стадии роста протеолитические ферменты кишечного тракта имеют наибольшую активность, которая значительно снижается в период нереста. В мышечной ткани наблюдаются противоположные процессы, связанные с изменением прочности. Проведено разделение протеаз пищеварительного тракта трепанга методом ионообменной хроматографии. Обнаружено два белковых пика, проявляющих активность трипсина, соответствующих обладающим отрицательным зарядом изоформам этого фермента. Молекулярная масса соответствующих пиков, определенная методом электрофореза, составила 26 и 28 кДа. Полученные данные аналогичны установленным ранее для других видов голотурий. Определение активности протеаз мышечной ткани трепанга в разные сезоны показало невысокий уровень протеолитической активности в период роста...
Голотурии, протеазы, нуклеазы, стадии развития, сезонные изменения
Короткий адрес: https://sciup.org/142217116
IDR: 142217116 | УДК: 664.951.7:639.4 | DOI: 10.21443/1560-9278-2018-21-3-402-411
The enzymatic activity of various organs and tissues of Far-Eastern trepang as a system of indicators of maturation and quality of products
The activity, substrate-inhibitory specificity, temperature and pH dependence, seasonal changes in proteolytic and nucleolytic enzyme systems of the digestive tract, muscle and reproductive trepangs tissues have been considered. The different-rule variability of enzyme activity at different stages of development has been shown. At the stage of growth proteolytic enzymes of the intestinal tract have the greatest activity, which is significantly reduced during spawning. In muscle tissue, there are opposite processes associated with changes in the strength. Separation of proteases of the trepang digestive tract by ion exchange chromatography has been carried out. Two peaks of proteins showing trypsin activity corresponding to the isoforms of this enzyme possessing a negative charge have been detected. The molecular weight of the corresponding peaks determined by the electrophoresis method is 26 and 28 kDa. The data obtained are similar to those established earlier for other types of holothurians...
Текст научной статьи Ферментативная активность различных органов и тканей дальневосточного трепанга как система индикаторов созревания и качества продукции
Активность эндогенных ферментов морских биоресурсов непосредственно влияет на состав их тканей, питательную ценность, срок хранения и пищевые характеристики продукции. Внутривидовое разнообразие факторов (биологический возраст, питание, качество воды, температура среды) влияет на такие показатели, как консистенция или текстура, цвет, запах, посмертные превращения тканей. Знание направленности действия ферментных систем позволяет разрабатывать маркеры качества, способы регулирования действия ферментов путем изменения условий окружающей среды, условий переработки и хранения, а также использования регуляторов активности, таких как ингибиторы и активаторы.
Также активность ферментов морских биоресурсов может быть использована как индикатор качественных изменений сырья, полуфабрикатов и готовой продукции, так как большинство используемых показателей определяется изменением активности эндогенных ферментов (т. е. присутствующих в самом организме).
Голотурии или морские огурцы являются морскими беспозвоночными типа Echinodermata , класс Holothuroidea . Трепанг Apostichopus japonicus ( Selenka ) уже давно используется как важный экономический ресурс в Китае, Японии, России, Северной и Южной Корее. Это одна из наиболее экономически значимых голотурий в аквакультуре Китая. В 2009 г. производство трепанга в этой стране составило более 100 000 т [1–2].
A. japonicus – это откармливающийся вид, питающийся донными осадками, с простым, трубчатым пищеварительным трактом, который пропускает большое количество осадка через кишечник и ассимилирует доступные органические материалы. Состоят органические материалы в основном из бактерий, диатомей, детрита макроводорослей и простейших [3–4]. Ввиду низкой питательности субстрата этот вид животных, вероятно, использует бактерий, присутствующих в его кишечнике и поставляющих более 70 % потребностей в энергии путем переваривания и усвоения пищевых компонентов [5–6]. Протеолитическая активность также связана с механизмами регенерации кишечного тракта после эвисцерации (выбрасывания внутренностей) в качестве защиты от хищников, хотя эта способность также может быть инициирована экологическими и механическими факторами, такими как высокие температуры, низкий уровень кислорода и переработка [7].
Продолжительность жизни дальневосточного трепанга составляет около четырех лет. За этот период трепанг испытывает широкий диапазон изменений условий окружающей среды и пищевого рациона.
Сезонные изменения температуры воды и структуры пищи являются важными факторами, влияющими на биохимический состав морских организмов. Предполагается, что активность ферментных систем различных тканей голотурий оказывает существенное влияние на качество получаемых пищевых продуктов [8–9].
Активность протеолитических ферментов пищеварительного тракта является основным фактором, определяющим рост и развитие этого организма. Субстратная специфичность и сезонные изменения активности ферментов определяют возможности использования искусственных кормов путем регулирования их состава. Основная проблема, связанная с потерей требуемого качества продукции из голотурий, связана с тем, что после вылова мышечная ткань вследствие посмертных изменений теряет свои упруго-эластичные свойства и очень быстро наступает состояние автолиза, сопровождающееся значительным размягчением мышечной оболочки [10–11]. Процессы роста и полового созревания способны оказывать существенное влияние на состав и активность ферментов мышечной ткани трепанга, в этом случае будут полезны рекомендации по способам вылова и переработки данного объекта промысла. Ферментативные системы (нуклеолитического и протеолитического действия) репродуктивной ткани (гонад) голотурий также связаны с процессами роста и развития этого организма и могут служить биомаркерами полового созревания.
Цель работы – анализ активности основных гидролитических ферментов пищеварительного тракта трепанга, а также мышечной и репродуктивной тканей, что связано с их воздействием на жизнеспособность на разных стадиях развития, способность усвоения кормов (что особенно важно при искусственном разведении), а также сохранностью тканей при последующей технологической переработке.
Материалы и методы
Объектом исследования служил дальневосточный трепанг, выловленный в бухте Северная (залив Славянский) Японского моря с апреля по сентябрь 2017 г. Средняя масса одного экземпляра составляла 36 ± 4 г. Образцы для анализа готовили путем составления общей пробы из органов от 3–5 экземпляров. Соматический индекс определяли как соотношение массы (г) тела к его длине (см).
Протеолитическую активность ферментных препаратов определяли по методу Каверзневой, в качестве субстратов использовали казеин и гемоглобин. Нуклеолитическую активность определяли по методу, описанному Гафуровым [12].
Для определения эстеразной активности трипсина и химотрипсина использовали метод Шверта и Такенака в модификации Хаммеля. В качестве субстратов использовали ТАМЭ (N-тозил-l-аргинин метиловый эфир) и БТЭЭ (бензоил-l-аргинин этиловый эфир).
Содержание ДНК определяли по методу Дише [13].
Для разделения белков методом ионообменной хроматографии в качестве носителей были использованы ДЭАЭ- и КМ-сефадексы G-75, хроматографические колонки размером 1,5 × 50 см, рабочий буфер 0,05 М трис-HCl, рН 7,8–8,0. Для элюции применяли линейный градиент NaCl от 0 до 1,0 М.
Измерения предельного напряжения сдвига мышечной ткани голотурий проводили на коническом пластометре КП-3. Перед измерением помещали образцы в льдо-солевую смесь на 15 мин. Величину показателя ( Q o , Па) рассчитывали по уравнению Ребиндера
Qo = К · m/h2, где К – константа используемого индентора (2,13 Н/кг); m – рабочая масса подвижной части прибора (0,1 кг); h – максимальная глубина погружения индентора в продукт (м) при заданной массе (m), при достижении равновесия сил тяжести и сопротивления измеряемого образца.
Результаты и обсуждение
Ферменты кишечного тракта. Основными питательными компонентами голотурий являются макро-и/или микроводоросли. Ферменты, участвующие в переваривании пищи, вырабатываются секретирующими клетками слизистой оболочки кишечной трубки. Нормальная величина pH в кишечнике голотурий около 6,1 [14]. Такие условия оптимальны для действия амилаз, пектиназ и некоторых протеаз. Известно, что после эвисцерации, когда выбрасывается центральная часть пищеварительной трубки, функции пищеварения переходят к передним (глотки и пищевода) и задним (клоаки) областям кишки, а у некоторых видов также и к щупальцам. Регенерация занимает 3–4 недели, в течение которых метаболизм значительно замедляется.
Влияние рН. Протеолитическая активность обнаружена в органах пищеварительной системы многих видов иглокожих. При этом спектр активности в широком диапазоне рН характерен для большинства видов голотурий, обитающих как в холодных, так и тропических водах [14]. На рис. 1 представлена зависимость активности протеолитических ферментов внутренних органов трепанга в диапазоне рН от 2,5 до 9,0 во время двух сезонных стадий развития: май – период интенсивного роста, июль – период нереста. В оба исследованных периода сохраняется общая тенденция изменения активности протеолитических ферментов. Пиковые значения соответствуют кислой зоне рН в диапазоне 3,5–6,0, что характерно для аспартильных и цистеиновых протеаз. В щелочной зоне рН, оптимальной для работы сериновых и металлопротеиназ, активность значительно ниже. Такие сезонные изменения соответствуют физиологическим процессам, происходящим в организме голотурий, интенсивный рост которых соответствует интенсивному пищеварению, в период нереста наблюдается снижение активности потребления пищи.
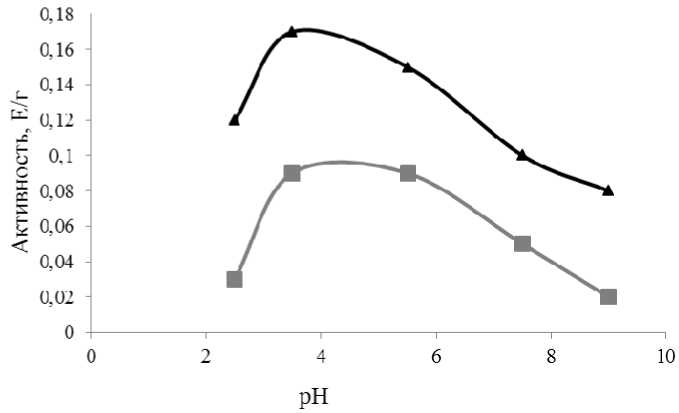
Рис. 1. рН-зависимость протеолитической активности пищеварительного тракта трепанга: ▲ – период роста (май), ■ – период нереста (июль)
Fig. 1. pH-dependence of proteolytic activity of the trepang digestive tract:
▲ – growth period (May), ■ – spawning period (July)
Влияние температуры. Кажущаяся оптимальной температура активности протеаз кишечного тракта Apostichopus japonicus (рис. 2) была аналогична данным, полученным другими авторами [14], которые наблюдали пик активности для цистеиновых протеаз голотурий при 46–50 °C.
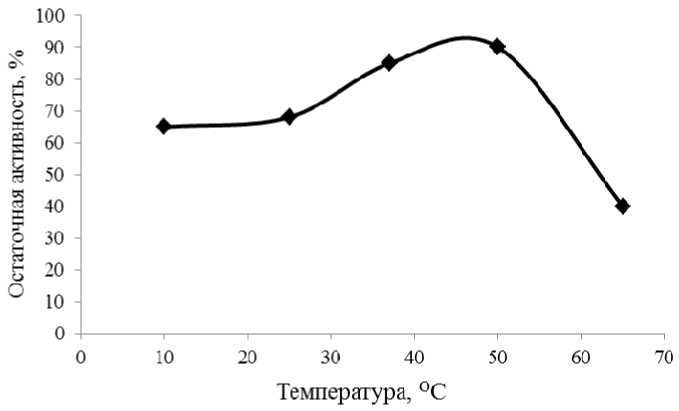
Рис. 2. Температурная зависимость протеолитической активности пищеварительного тракта трепанга при рН 6,5
Fig. 2. Temperature dependence of proteolytic activity of the trepang digestive tract at pH 6.5
Оптимальный температурный диапазон действия пищеварительных ферментов зависит от условий среды обитания животных. Температура окружающей среды, в которой живет S. japonicus , составляет от 3–4 до 24–26 °C. Известно, что ферменты водных организмов обладают значительно большей активностью при низких температурах, чем аналогичные ферменты у теплокровных наземных животных [15]. Температурный оптимум при 46–50 °C соответствует общим законам термодинамики, но при таких высоких температурах стабильность ферментов быстро снижается. Они могут так интенсивно работать в течение около 30 мин, после чего происходит их постепенная инактивация.
Активность индивидуальных сериновых протеаз пищеварительного тракта трепанга определяли по эфирным субстратам: для ТАМЭ, соответствующего специфичности трипсина, она составила 0,2 Е/г, для БТМЭ, соответствующего специфичности химотрипсина, активность не была зарегистрирована. Методом ионообменной хроматографии обнаружено два белковых пика, проявляющих активность трипсина, вероятно, соответствующих изоформам этого фермента, обладающих отрицательным зарядом (анионные формы). Молекулярная масса соответствующих пиков, определенная методом электрофореза, составила 26 и 28 кДа. Полученные данные аналогичны установленным ранее для других видов голотурий. Известно, что основным отличием сериновых протеаз трипсинового и химотрипсинового типов высших позвоночных от аналогов у беспозвоночных и рыб является наличие у последних множественных анионных форм. Это свойство определяет устойчивость сериновых протеаз к автолизу и быструю инактивацию в кислой среде [16].
При определении субстратной специфичности ферментов кишечника трепанга по отношению к различным белковым субстратам (табл. 1) установлено, что наиболее быстро протеолизу подвергаются гемоглобин и казеин. Это соответствует как структуре самих субстратов, так и возможностям большинства протеаз. Коллагенолитическая активность в кишечнике трепанга достаточно высока, так, например для пилорических придатков рыб подобная величина не превышает 1–1,5 % для нативного коллагена и 3–5 % для денатурированного [16].
Таблица 1. Субстратная специфичность протеолитических ферментов кишечника трепанга по отношению к различным белковым субстратам (рН 6,0)
Table 1. Substrate specificity of proteolytic enzymes of trepang intestine in relation to various protein substrates (pH 6.0)
|
Субстрат |
Остаточная активность, % |
|
Гемоглобин |
100 |
|
Казеин |
94,7 |
|
Протамин |
30,2 |
|
Фибрин |
9,9 |
|
Коллаген 1 типа |
2,5 |
|
Денатурированный коллаген |
6,7 |
Исследовано воздействие таких необратимых ингибиторов, как тозиллизил-хлорметилкетон (TЛХК) – необратимый ингибитор трипсина, этилендиаминтетрауксусная кислота (ЭДТА) – ингибитор металлопротеиназ, соевый ингибитор трипсина (СТИ) – белковый ингибитор широкого спектра, тормозящий активность многих сериновых протеиназ. При этом остаточная активность протеаз кишечника трепанга по отношению к контрольному образцу (без ингибиторов) составила 57, 69 и 74 % соответственно. Полученные результаты свидетельствуют о присутствии сериновых протеиназ, в частности, трипсинового типа и металлопротеиназ.
Таким образом, экстракты внутренностей трепанга А. japonicas показали преобладание активных в низкотемпературных условиях кислых и нейтральных протеаз, нестабильных при высоких температурах. Субстратно-ингибиторный анализ позволяет с наибольшей вероятностью отнести их к группе цистеиновых металлопротеаз. Показано присутствие ферментов трипсинового типа при нулевой активности химотрипсина.
Ферменты мышечной ткани. Для анализа протеолитической активности ферментов мускульного мешка голотурий был выбран тот же диапазон рН и использованы образцы, взятые в два периода – нагула и нереста (рис. 3).
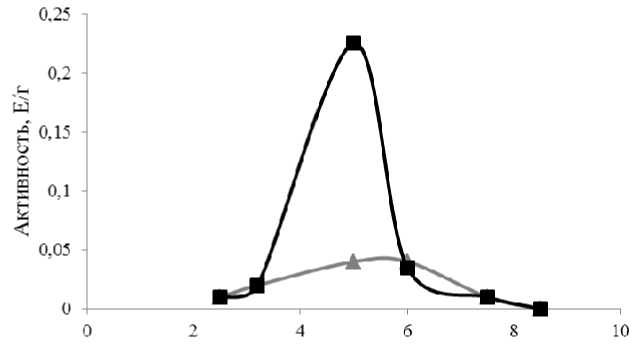
pH
Рис. 3. рН зависимость протеолитической активности мышечной ткани трепанга: ▲ – период роста (май), ■ – период нереста (июль)
Fig. 3. pH dependence of trepang muscle tissue proteolytic activity:
▲ – growth period (May), ■ – spawning period (July)
Период роста характеризуется невысоким уровнем протеолитической активности, что соответствует преобладанию анаболитических процессов. При этом величины активности кислых и нейтральных протеаз близки между собой. Активность щелочных протеаз весьма мала. В период нереста в мышечной ткани значительно повышается активность кислых протеаз, в нейтральной и щелочной зоне протеолиз остается на прежнем уровне. Сопоставление с литературными данными позволяет говорить о присутствии и важной роли катепсинов, в частности катепсина L, в метаболизме мышечной ткани трепанга [17]. Катепсин L – эндогенная термостойкая протеаза, обеспечивающая процессы автолиза. Изменения активности протеолитических ферментов в кишечнике и мышечной ткани трепанга имеют противоположную сезонную направленность, соответствующую направленности метаболитических процессов.
При сравнении уровня активности протеолитических ферментов в мышечной ткани трепанга, ее прочностных характеристик и интенсивности роста была показана их корреляция (табл. 2). Для этого использовали следующие показатели: предельное напряжение сдвига как условная характеристика прочности, соответствующая действию касательной составляющей приложенной силы, и соматический индекс (СИ) как соотношение массы особи к ее длине.
Таблица 2. Соотношение активности протеаз мышечной ткани трепанга (рН 3,0), ее прочности и интенсивности роста
Table 2. The ratio of proteases activity of trepang muscle tissue (pH 3.0), its strength and growth rate
|
Протеолитическая активность, Е/г ткани |
Предельное напряжение сдвига, Па × сек |
Соматический индекс, г/см |
|
Май (период роста) |
||
|
0,025 1 |
350 1 |
6,5 |
|
Июль (период нереста) |
||
|
0,22 1 |
220 1 |
8,2 |
СИ трепанга достигает максимальной величины к периоду нереста, при этом одновременно происходит увеличение активности протеаз и снижение прочностных характеристик его мышечной ткани.
Преобладающим белком мышечной ткани голотурий является коллаген (около 70 % от общего белка) [18], он же определяет ее биомеханические свойства, изменения которых могут быть связаны с активацией интерстециальных коллагенолитических ферментов, относящихся к группе металлозависимых протеаз, активных в диапазоне рН 4,5–5,5.
Недавно установлено [19], что коллаген иглокожих имеет непостоянную структуру с быстро изменяющимися механическими свойствами, что обеспечивает комплексную локомоцию, поддержание положения, защиту и репродуктивные стратегии. Блок-фибриллы соединительной ткани иглокожих постоянно растягиваются, скользят и переориентируются относительно друг друга. Голотурии достигают этого необычного свойства, изменяя жесткость сцепления матрицы между отдельными фибриллами, а не свойства самих фибрилл. В этих процессах, несомненно, важно значение ферментативных воздействий. Известно, что нормальная вязкость стенки тела Stichopus japonicus может варьироваться от 80 до 350 Па × сек. Значение величины вязкости зависит от района вылова трепанга и состава среды [10] и, как показано в нашей работе, стадии развития организма.
Таким образом, активация нейтральных и кислых протеаз в период нереста определяет биохимические и структурно-механические изменения мышечной ткани дальневосточного трепанга. Протекающие процессы могут быть объяснены как действием металлозависимых протеаз, обеспечивающих необходимую лабильность соединительнотканного матрикса, так и действием цистеиновых протеаз, включающихся в процессы автолиза и ускоряющих их после вылова данного объекта на данной стадии развития. Полученные результаты важны для организации способов переработки трепанга на разных стадиях развития.
Ферментативная активность репродуктивной ткани голотурий непосредственно связана с созреванием половых продуктов и готовности гонад к вымету. Основную роль в этих процессах играют ферменты нуклеолитического (дезоксирибинуклеазы – ДНКазы) действия.
Известно, что в метаболизме репродуктивной ткани важную роль играют щелочные Ca, Mg-зависимые ДНКазы и кислые ДНКазы, которые принимают участие в деградации ДНК на первых стадиях ее преобразований в слабокислой или нейтральной области рН [12]. В гонадах различных видов гидробионтов, в том числе иглокожих, преобладает активность кислых ДНКаз. Высокое содержание ДНК в гонадах обычно соответствует высокой активности ферментов [20]. Это также оказалось справедливым для гонад голотурий.
Опосредованное участие протеаз в процессах преобразования ДНК в репродуктивной ткани объясняется тем, что они расщепляют белки, связанные с ДНК, защищающие ее от действия нуклеаз. Протеазы могут таким образом создавать условия для прямого контакта ДНК с эндогенными нуклеазами, что способствует ее последующей деградации. Кроме того известно, что эндонуклеазы, содержащиеся в различных органах, образуются из высокомолекулярного предшественника и активируются под действием протеиназ [20].
Для установления специфичности протеаз была определена эстеразная активность в ткани молок горбуши по субстратам, специфическим для трипсина и химотрипсина – ТАМЭ и БТЭЭ соответственно. Полученные результаты показали, что содержащиеся в молоках ферменты не относятся к сериновым протеазам трипсинового и химотрипсинового типа.
Дальневосточный трепанг нерестится 1 раз в год, в его репродуктивном цикле выделяют: стадию быстрого роста весной, сопровождающуюся достижением гонады преднерестового состояния, в середине лета наступает стадия нереста, далее идут восстановительная стадия и стадия медленного роста в зимние и первые весенние месяцы. О готовности гонад к нересту судят по количеству половых клеток, их размеру и расположению в гонадах [21]. Однако существует годовая изменчивость в сроках наступления нереста не только в различных акваториях, но и в отдельных бухтах, что зависит от температуры воды. Для уточнения сроков нереста может быть использован биохимический подход, основанный на определении в гонадах количества ДНК, активности Ca 2+ , Мд 2+ -зависимых ДНКаз и протеаз. Наибольшее количество ДНК и максимальная активность ферментов наблюдаются в период роста, что свидетельствует об интенсивно протекающих биосинтетических процессах в репродуктивной ткани (табл. 2).
Таблица 3. Активность гидролитических ферментов и содержание ДНК в гонадах трепанга, период роста Table 3. Activity of hydrolytic enzymes and DNA content in trepang gonads, growth period
|
Щелочные ДНКазы, Е/г, рН 7,8 |
Кислые ДНКазы, Е/г, рН 5,0 |
Протеазы, Е/г, рН 7,8 |
ДНК, % от массы гонад |
|
Период роста |
|||
|
134,2 |
1420 |
0,80 |
4,40 |
|
Период нереста |
|||
|
55,1 |
440 |
0,12 |
1,54 |
Во время нереста все исследованные показатели резко снижаются, что вероятно, связано с частичным выметом половых продуктов. В посленерестовом периоде они имеют нулевые значения. Таким образом, биохимические показатели могут быть использованы как маркеры полового цикла голотурий, что следует учитывать при организации рационального лова.
Заключение
Полученные результаты позволяют сделать заключение о том, что на различных стадиях развития дальневосточного трепанга в его пищеварительной системе, мышечной и репродуктивной тканях происходят разнонаправленные процессы, позволяющие судить об интенсивности анаболических и катаболических процессов. Так, стадия роста сопровождается увеличением активности пищеварительных ферментов и низким уровнем активности мышечных протеаз, где в этот период происходят процессы синтеза. Во время нереста меняется пищевое поведение и снижается выработка пищеварительных ферментов в кишечнике, в мышечной ткани в это же время наблюдается изменение (ослабление) прочности мускульного мешка, определяемое лабильностью коллагена, способного изменять связи между отдельными фибриллами. В этом процессе безусловное значение имеют ферментативные процессы, интенсивность которых значительно возрастает. Период роста также сопровождается активными ферментативными процессами в репродуктивной ткани. Особенно высока активность кислых ДНКаз, которая существенно уменьшается в нерестовый период и практически полностью исчезает после нереста.
Эти данные могут быть использованы как маркеры полового цикла и рекомендованы к учету при организации рационального лова. Исследования субстратно-ингибиторной специфичности ферментов показывают, что во всех тканях преобладают кислые и нейтральные протеазы. Подтверждено наличие сериновых и металлопротеаз, активных при низких температурах. Полученные данные возможно применять при разработке способов переработки трепанга с использованием регуляции активности ферментов.
Список литературы Ферментативная активность различных органов и тканей дальневосточного трепанга как система индикаторов созревания и качества продукции
- Bordbar S., Anwar F., Saari N. High-value components and bioactives from sea cucumbers for functional foods: a Review//Marine Drugs. 2011. V. 9, Iss. 10. P. 1761-1805. md9101761 DOI: https://doi.org/10.3390/
- Purcell S. W., Samyn Y., Conand C. Commercially important sea cucumbers of the world//FAO Species Catalogue for Fishery Purposes. 2012. N 6. 150 р.
- Hauksson E. Feeding biology of Stichopus tremulus, a deposit feeding holothurian//Sarsia. 1979. V. 64, Iss. 3. P. 155-160.
- Zhang Z., Wang S., Cao Y. DGGE technique and its application in study on microbial diversity in marine environment//Marine Environmental Science. 2008. N 3. P. 297-300.
- Amaro T., Luna G. M., Danovaro R., Billett D. S. M., Cunha M. R. High prokaryotic biodiversity associated with gut contents of the holothurian Molpadia musculus from the Nazaré Canyon (NE Atlantic)//Deep-Sea Research Part I: Oceanographic Research Papers. 2012. V. 63. Р. 82-90. j.dsr.2012.01.007 DOI: https://doi.org/10.1016/
- Ray A. K., Ghosh K., Ringø E. Enzyme-producing bacteria isolated from fish gut: a Review//Aquaculture Nutrition. 2012. V. 18, Iss. 5. Р. 465-492. DOI: https://doi.org/10.1111/j.1365-2095.2012.00943.x.
- Sun L. M., Zhu B. W., Wu H. T., Yu L., Zhou D. Y. . Purification and characterization of cathepsin B from the gut of the sea cucumber (Stichopus japonicas)//Food Science and Biotechnology. 2011. V. 20, Iss. 4. Р. 919-925. DOI: https://doi.org/10.1007/s10068-011-0127-1.
- Gao F., Xu Q., Yang H. Seasonal biochemical changes in composition of body wall tissues of sea cucumber Apostichopus japonicus//Chinese Journal of Oceanology and Limnology. 2011. V. 29, Iss. 2. P. 252-260. DOI: https://doi.org/10.1007/s00343-011-0041-7.
- Dunstan G. A., Olley J., Ratkowsky D. A. Major environmental and biological factors influencing the fatty acid composition of seafood from Indo-Pacific to Antarctic waters//Recent research developments in lipids research. 1999. V. 3. P. 63-86.
- Motokawa T. The viscosity change of the body-wall dermis of the sea cucumber Stichopus japonicus caused by mechanical and chemical stimulation//Comparative Biochemistry and Physiology. Part A: Physiology. 1984. V. 77, Iss. 3. P. 419-423. DOI: https://doi.org/10.1016/0300-9629(84)90206-8.
- Kariya Y., Watabe S., Ochiai Y., Murata K., Hashimoto K. Glycosaminoglycan involved in the cation-induced change of body wall structure of sea cucumber Stichopus Japonicus//Connective Tissue Research. 1990. V. 25, Iss. 2. Р. 149-159. DOI: https://doi.org/10.3109/03008209009006989.
- Гафуров Ю. М. Дезоксирибонуклеазы. Методы исследования и свойства. Владивосток: Дальнаука, 1999. 230 с.
- Карклиня В. А., Бирска И. А., Лимаренко Ю. А. Количественное определение нуклеиновых кислот в молоках лососевых различными методами//Химия природных соединений. 1989. № 1. С. 122-126.
- Hernández-Sámano A. C., Guzmán-García X., García-Barrientos R., Ascencio-Valle F., Sierra-Beltrán A. . Characterization of protease activity from the digestive tract and tentacles of Isostichopus fuscus sea cucumber//Invertebrate Survival Journal (ISJ). 2017. V. 14. Р. 282-294.
- Seafood enzymes: utilization and influence on postharvest seafood quality/eds. N. F. Haard, B. K. Simpson. New York -Basel: Marcel Dekker, Inc, 2000. 689 р.
- Пивненко Т. Н. Панкреатические сериновые протеиназы рыб и морских беспозвоночных. Свойства, методы очистки и практическое применение = Pancreatic serine proteinases from sea fishes and invertebrates. Properties. Methods of purification. Practical application: . Владивосток: ТИНРО-Центр, 2008. 286 с.
- Zhou D. Y., Chang X. N., Bao S. S., Song L., Zhu B. W. . Purification and partial characterisation of a cathepsin L-like proteinase from sea cucumber (Stichopus japonicus) and its tissue distribution in body wall//Food Chemistry. 2014. V. 158. P. 192-199. DOI: https://doi.org/10.1016/j.foodchem.2014.02.105.
- Слуцкая Т. Н. Исследования по химии и технологии трепанга и кукумарии: дис.. канд. техн. наук: 05.18.04. Владивосток, 1974. 118 с.
- Mo J., Prévost S. F., Blowes L. M., Egertová M., Terrill N. J. Interfibrillar stiffening of echinoderm mutable collagenous tissue demonstrated at the nanoscale//Proceedings of the National Academy of Sciences of the USA (PNAS). 2016. V. 113 (42). Р. E6362-E6371 DOI: https://doi.org/10.1073/pnas.1609341113
- Позднякова Ю. М., Пивненко Т. Н., Касьяненко Ю. И. Влияние эндогенных ферментов на состав олигонуклеотидов при их выделении из гонад гидробионтов//Прикладная биохимия и микробиология. 2003. Т. 39, № 5. С. 524-529.
- Евдокимов В. В., Матросова И. В. Сезонная характеристика гаметогенеза некоторых промысловых гидробионтов//Цитология. 2009. Т. 51, № 10. С. 861-865.


