Филогенетическое разнообразие бактерий в каменной соли Верхнекамского месторождения (Пермский край)
Автор: Пьянкова А.А., Белоглазова Ю.А., Корсакова Е.С., Бачурин Б.А., Плотникова Е.Г.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2021 года.
Бесплатный доступ
С использованием молекулярно-генетических методов получены новые данные о филогенетическом разнообразии бактерий в галогенных отложениях Верхнекамского месторождения солей (Пермский край). Анализ генов 16S рРНК, обнаруженных в тотальной ДНК образца каменной соли (глубина отбора 239.7-239.8 м), позволил установить присутствие бактерий, принадлежащих классам Actinobacteria (близкородственных родам Rhodococcus, Demequina), Gammaproteobacteria (родам Pseudomonas, Serratia, Shigella), Betaproteobacteria (роду Ralstonia) и Alphaproteobacteria (роду Phyllobacterium). Кроме того, выявлены два филотипа класса Alphaproteobacteria (клон 66ВА (GenBank MH410136) и клон 12ВА (GenBank MH410128), проявляющие низкий уровень сходства по генам 16S рРНК (98.46%) с ближайшими типовыми штаммами рода Mesorhizobium ( M. alhagi CCNWXJ12-2T) и рода Chelativorans ( C. multitrophicus DSM9103T), которые могут представлять новые таксономические единицы.
Верхнекамское месторождение солей, некультивируемые бактерии, клонирование, секвенирование, ген 16s ррнк
Короткий адрес: https://sciup.org/147236785
IDR: 147236785 | УДК: 579.26 | DOI: 10.17072/1994-9952-2021-4-256-262
Phylogenetic diversity of bacteria in rock salt of the Verkhnekamskoe deposit (Perm krai)
New data on the phylogenetic diversity of bacteria in the salt of the Verkhnekamskoe deposit (Perm Krai) have been obtained using molecular genetic methods. Analysis of the 16S rRNA genes of total DNA from the rock salt sample (depth intervals of 239.7-239 m) evinces the presence of bacteria belonging to the classes: Actinobacteria (closely related to the genera Rhodococcus, Demequina), Gammaproteobacteria (the genera Pseudomonas, Serratia, Shigella ), Betaproteobacteria (the genus Ralstonia ) and Alphaproteobacteria (the genus Phyllobacterium ). In addition, we identified two phylotypes of the Alphaproteobacteria (clone 66BA (GenBank MH410136) and clone 12BA (GenBank MH410128) that show lower similarity in 16S rRNA genes (98.46%) with the closest type strains of the genus Mesorhizobium ( M. alhagi CCNWXJ12-2T) and the genus Chelativorans ( C. multitrophicus DSM9103T). The identified phylotypes may represent new taxonomic units.
Текст научной статьи Филогенетическое разнообразие бактерий в каменной соли Верхнекамского месторождения (Пермский край)
Верхнекамское месторождение солей (ВКМС) является одним из крупнейших по запасам калийно-магниевой руды в мире. Месторождение расположено на северо-востоке Пермского края и занимает площадь порядка 4 000 км2. Наиболее распространенными породами пермской галогенной толщи ВКМС являются каменная соль, сильвинитовые и карналлитовые породы. Каменная соль представляет собой почти мономинеральную породу, сложенную на 90–98% галитом (NaCl) с включениями глинистого и органического вещества, гипса, KCl, MgCl 2 и др. [Кудряшов 2001; Барях, Асанов, Паньков, 2008]. Анализ геологической среды ВКМС предполагает возможность выживания в таких экстремальных условиях уникальных галофильных и галотолерантных микроорганизмов. Интерес к данной группе микроорганизмов обусловлен их высоким биотехнологическим потенциалом, поскольку они могут быть использованы для получения осмопротекторных соединений, биополимеров и ферментов, активных при высокой осмолярности среды. Галофильные и галотолерантные микроорганизмы могут применяться в сельскохозяйственной и пищевой промышленности, природоохранных технологиях [Margesin, Schinner, 2001].
Месторождения солей распространены по всему миру. Микробные изоляты и нуклеотидные последовательности 16S рРНК были извлечены из галитовых отложений в Северной и Южной Америке, Европе и Восточной Азии. Жизнеспособные археи и бактерии были выделены из галита возрастом до 280 млн лет. Тем не менее, микробные сообщества глубинных подземных экосистем, в том числе соляных пород, изучены крайне недостаточно [Jaakkola et al., 2016].
В настоящее время для более глубокого изучения разнообразия микроорганизмов все чаще используются культурально-независимые подходы, поскольку предполагается, что менее 1% микроорганизмов, которые представлены в природных местообитаниях, подлежат культивированию [Alain, Querellou, 2009; Равин и др. 2015].
Цель исследования – оценка филогенетического разнообразия бактерий в галите (каменной соли) ВКМС культурально-независимыми методами.
Материалы и методы исследования
Образец для исследований . В качестве материала для исследований был использован образец каменной соли с глубины 239.7–239.8 м скважины № 704/1 Половодовского участка, расположенной в северной части ВКМС (N 56°57ʹ21.60ʺ, E 59°44ʹ24ʺ). Образец соли предоставлен сотрудниками Горного института УрО РАН (Пермь, Россия). Общая минерализация образца каменной соли определялась согласно протоколу [Практикум …, 2001]. Содержание ионов Na+, K+, Ca2+ определяли методом водной вытяжки (приготовленной согласно ГОСТу 26423-85) с последующей детекцией на атомноабсорбционном спектрофотометре АА-6300 («Shimadzu», Япония), как описано [Корсакова и др., 2013].
Рассеянное органическое вещество экстрагировали из образца каменной соли хлороформом [Бачурин, Одинцова, Хохрякова, 2016]. Фракции углеводородов и гетеросоединений в экстрактах хлороформа (хлороформный битум, ХБ) количественно определяли с помощью газового хроматографа-масс-спектрометра Agilent Technologies 6890N MSD 5975 («Agilent», США) путем сопоставления спектров с библиотекой масс-спектров NIST98.
Поверхностную стерилизацию образца каменной соли проводили путем полного погружения в 10M раствор NaOH, а затем в 70%-ный раствор этанола и выдерживали под ультрафиолетовым излучением в ламинарном шкафу в течение 30 мин.
Накопительное культивирование. При получении накопительной культуры (НК) из образца каменной соли была использована среда ATCC 213 «Halobacterium medium» ( ATCCAdvancedCatalogSearch), содержание хлорида натрия в среде составляло 200 г/л. Один грамм образца соли (из толщи керна, отобранный в стерильных условиях) помещали в 100 мл среды и инкубировали в течение 4 недель при температуре 28°С.
Выделение ДНК, ПЦР-амплификация и клонирование генов 16S рРНК . Выделение ДНК из полученной НК проводили с применением набора реактивов Fast DNA spin kit for soil («MP Biomedicals», Франция). Концентрацию выделенной ДНК измеряли с использованием прибора Qubit® Fluorometer 257
(«Invitrogen», США) и набора реактивов Quant-iT™ dsDNA BR Assay Kit («Invitrogen», США). Амплификацию фрагментов бактериальных генов 16S рРНК проводили при использовании универсальных бактериальных праймеров 27F/1492R [Lane, 1991] на приборе C1000 TouchTM Thermal Cycler («Bio-Rad Laboratories», США). Продукты реакции разделяли методом электрофореза в 1%-ном агарозном геле при напряжении 10 В/см, окрашивали раствором бромистого этидия (5 мкг/мл) и фотографировали в УФ-свете с использованием системы гель-документирования Gel DocTM XR («Bio-Rad Laboratories», США).
Для получения библиотек клонов бактериальных генов 16S рРНК полученные ПЦР-фрагменты клонировали в клетках Е . сoli JM109 в составе вектора pTZ57R/T. Для трансформации компетентных клеток Е . сoli JM109 использовали набор реактивов Thermo Scientific InsTAclone PCR Cloning Kit («Thermo Scientific», Литва). Последующий отбор рекомбинантных клонов осуществляли на основании «белоголубого» теста, высевая трансформанты на среду Luria-Bertrani (LB) [Short protocols in molecular biology, 1995], содержащую 50 мкг/мл ампициллина, 100 мМ IPTG, 20 мкг/мл X-gal («Fermentas», Литва). С ДНК-матрицы отобранных рекомбинантных клонов проводили амплификацию фрагментов бактериальных 16S рРНК генов с праймерами 27F/1492R [Lane, 1991]. Анализ полиморфизма длин рестрикционных фрагментов 16S рРНК генов (ПДРФ-анализ) осуществляли с использованием эндонуклеазы рестрикции Hha I («Fermentas», Литва). Для подготовки к секвенированию клонированных в составе вектора pTZ57R/T фрагментов ДНК проводили амплификацию вставки с использованием стандартных праймеров M13 (М13F 5’-GTTTTCCCAGTCACGAC-3’ и М13R 5’-CAGGAAACAGCTATGAC-3’), для которых имеются сайты связывания в векторе pTZ57R по обеим сторонам от полилинкера.
Секвенирование и анализ генов 16S рРНК. Определение нуклеотидных последовательностей проводили с применением набора реактивов Big Dye Terminator Cycle Sequencing Kit v. 3.1 («Applied Biosystems», США) на автоматическом секвенаторе Genetic Analyser 3500XL («Applied Biosystems», США) в Пермском государственном национальном исследовательском университете (кафедра ботаники и генетики растений) согласно рекомендациям производителя. Поиск гомологов генов 16S рРНК осуществляли по международным базам данных GenBank (http:/ и EzBioCloud . Анализ нуклеотидных последовательностей выполняли с использованием алгоритма BLAST (http:/. Множественное выравнивание нуклеотидных последовательностей и построение филогенетического дерева проводили с использованием программы MEGA 7.0 . При построении филогенетического дерева применяли кластерный метод «neighbor-joining». Оценку статистической достоверности ветвления («bootstrap»-анализ) осуществляли на основе 1000 альтернативных деревьев.
Данные о нуклеотидных последовательностях фрагментов генов 16S рРНК исследованных бактериальных клонов депонированы в международной базе данных GenBank под номерами MH399229, MH410126-45.
Результаты и их обсуждение
Химический анализ водной вытяжки исследованного образца каменной соли показал, что ее общая минерализация составила 3.96%; концентрация ионов Na+, K+, Ca2+ – 4.13 г/л, 5.2 г/л, 20.95 г/л, соответственно.
Содержание хлороформного битума (ХБ) в образце составило 68.65 мг/кг. Газохроматический и масс-спектрометрический анализ хлороформных экстрактов показал присутствие углеводородной фракции (3.02%), представленной только алифатическими соединениями. Гетеросоединения (96.98%) являются доминирующими в ХБ и представлены кислородсодержащими структурами (41.07%), в основном – окисями, спиртами, эфирами (38.68%), а также кислотами и их производными (10.09%).
Из образца каменной соли путем прямого высева на агаризованную среду ATCC 213 «Halobacterium medium» не удалось выделить чистые культуры микроорганизмов, поэтому дальнейшие исследования проводились с использованием молекулярно-генетических методов.
Из накопительной культуры, полученной при культивировании образца каменной соли в жидкой среде ATCC 213 «Halobacterium medium», была выделена тотальная ДНК. Концентрация выделенной ДНК составляла 7.12 мкг/мл. При амплификации генов 16S рРНК бактерий с матрицы тотальной ДНК получен ПЦР-продукт искомого размера (около 1400 п.н.). В результате клонирования была создана библиотека генов 16S рРНК, состоящая из 120 бактериальных клонов с покрытием 87.2%, что указывает на то, что большая часть оцененного микробного разнообразия была взята в анализ.
На основе анализа полиморфизма длин рестрикционных фрагментов (ПДРФ-анализ) полученных ампликонов с использованием рестриктазы Hha I, исследуемые клоны были подразделены на 24 группы. На рисунке 1 представлена электрофореграмма рестрикционных фрагментов клонированных генов 16S рРНК восемнадцати произвольно выбранных клонов.
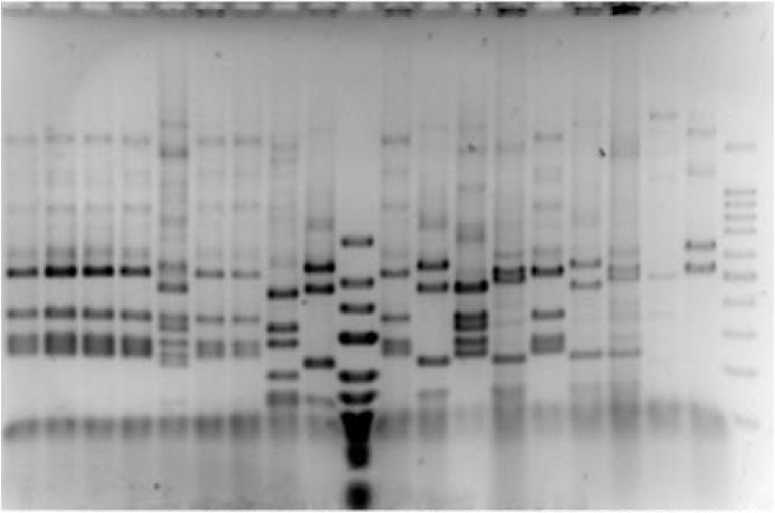
1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20
Рис. 1 . Электрофореграмма рестрикционных фрагментов клонированных генов 16S рРНК после обработки эндонуклеазаой HhaI :
10 – маркер длин ДНК GeneRulerTM Low Range DNA Ladder («Thermo Scientific», США); 20 – маркер длин ДНК 100+ bp DNA Ladder («Евроген», Россия); 1–9 и 11–19 – рекомбинантные клоны
[Electrophoregram of restriction fragments of cloned 16S rRNA genes after treatment with HhaI endonuclease:
10 - DNA length marker GeneRulerTM Low Range DNA Ladder (Thermo Scientific, USA); 20 - DNA length marker 100+ bp DNA Ladder (Eurogen, Russia); 1-9 and 11-19 - recombinant clones]
Далее, у представителей каждой рестрикционной группы были определены нуклеотидные последовательности фрагментов генов 16S рРНК. По результатам проведенного биоинформационного анализа, последовательности клонированных 16S рДНК были подразделены на 9 групп (операционных таксономических единиц, OTЕ). Индекс Симпсона (D) составлял 0.14, индекс разнообразия Шеннона (H) – 1.42.
Девять ОТЕ на филогенетическом дереве (рис. 2) формировали кластеры, соответствующие двум фи-лумам: « Proteobacteria » и « Actinobacteria ». Филум « Proteobacteria » включал 7 филотипов, относящихся к классам Alpha - Beta - и Gammaproteobacteria . Большая часть клонов (61.74% от всех бактериальных клонов) была отнесена к роду Pseudomonas (класс Gammaproteobacteria ). Наибольший процент сходства (99.73%) клоны имели с типовым штаммом вида Pseudomonas edaphica , изолированного из ризосферы многолетнего кустарника Cistus ladanifer L. (Испания) [Ramirez-Bahena et al., 2019].
Также были выявлены клоны, близкородственные (уровень сходства по генам 16S рРНК составлял 99.34–100%) представителям родов Serratia и Shigella (семейство Enterobacteriaceae , класс Gammaproteobacteria ) и некультивируемым бактериальным клонам генов 16S рРНК, обнаруженных в различных природных источниках, в том числе в арктических донных осадках (FJ849472) [Larouche et al., 2012], в микробиоме северного калифорнийского морского льва (JQ207675), заболоченной почве в Китае (KR148991) (рис. 2).
В исследованном образце каменной соли были обнаружены гены 16S рРНК (филотипы), проявляющие наибольшее сходство с представителями почвенных (ризосферных) бактерий рода Ralstonia (класс Betaproteobacteria ) и рода Phyllobacterium (класс Alphaproteobacteria ) (рис. 2). Кроме того, выявлены два филотипа класса Alphaproteobacteria (клон 66ВА и клон 12ВА), проявляющие низкий уровень сходства по генам 16S рРНК (98.46%) с типовыми штаммами узаконенных видов родов Mesorhizobium ( Mesorhizo-bium alhagi CCNWXJ12-2T) и Chelativorans ( Chelativoran smultitrophicus DSM9103T) [Zhou et al., 2012; Doronina et al., 2010], и которые, вероятно, представляют новые таксономические единицы.
В пределах филума « Actinobacteria » встречались только представители класса Actinobacteria . Около 20% бактериальных клонов от общего их числа включают последовательности генов 16S рРНК с уровнем сходства 99.72% с Rhodococcus qingshengii JCM15477T. Другая группа клонов (0.87% клонов) принадлежит минорному филотипу и содержит последовательность, близкую таковой типового штамма вида
Demequina aestuarii (уровень сходства 99.55%), который был изолирован из донных морских отложений в Корее [Hamada et al., 2015] (рис. 2).
я
<1
IM
|&ттдИа;^м11й1:аБК2(КЯ035070) '
KiKHSedNCB15(FJ849472)
Кпеи92ВА(МН410140)
Клон 77ВА (МН4К130> Клеи ЗОВА (МН4К130> Клеи 119ВА(МН4К14<
ти
---- Клеи 53ВА (MH4K135> Клеи КОВА (МН4К141)
SfogeIIas™si СЕСТ4887’ (FR870445 ™ S6igftt2sp. CH-42 (KR148991) KudhSItlRc 02 0SL4aFA(JQ207675)
Клеи ИВА (МН4К127)
Клеи 121ВА (MH4K145JL Кши 7В А (МН4К126)
Psexdomoxa^ A7ap6i:aKD25’ (LC272923)
Gammaproteobacferia
Psesdraaxm oart^enmns OLsAul(MF598585) Клин S1-037 (KF182781) -Клеи87ВА(МН410139)
-Клеи 1KB A (MH4KU43X Knot 6 В A (МН3992Э)
- №гаа;И АТС C 27511’ (10VLO1000020)
Клои39ВА(МН4К131)
JWsiasia sp. IWLA2 (MN515074)
JMs}asiasp.MI16(LC385700)
-Кп$иК5ВА(МН4К142)
Клон8У71112-1 (KM269680)
<7
Ki™10UB(K¥968992)
Ki™JR42(KC207921) «liWtii™ И 8658’ (KC577468)
Клои71ВА(МН410137)
е СЬе&Штогаа! жибйгирМст DSM9103T (EF457243) СЬеЬЩ-югш» xiiiititrc^!ii:iis LPM-410(FJ167675)
Кп<«12ВА(™410128)
Aiphaproteobacieria
' pKmHSIHA746N9D0 168 В (LN568107)
J |—Клои66ВА(МН4К136)
^7 tesrbizsii™ al&igi CCNWKJ12-2’ (АНАМ) 1000052)
ii
iifcssrtozsMim sp. L CD31 (MH59602) К1юн№игб™#шм sp.T15 (LC070335)
РЫосмта: sp.Toyi4Cthlll (MT626151)
Phsdococcus degra^ixs CsDWL-128 (MT415127)
Phsdococcus qixgsiexgii JCM 15477’(LKRJO1000016)
Клеи 25В А (MH410129X Клеи SOBA (MH4K132> Клеи 52BA (MH4K134)
I---КлоноЫТО! (EFO34304)
TuTil К™™ 51В А (МН410133)
SwItw^aiaaa^jaaniNBRC 106260’ (BBRD01000001) L Demeqxilia sp. ЕЫ 80499 (КТ734858)
Aitmobacts™
ijiji
Рис. 2 . Филогенетическое дерево, построенное с использованием метода neighbor-joining, показывающее положение исследуемых бактериальных клонов, основанное на сравнении нуклеотидных последовательностей гена 16S рРНК. Эволюционные расстояния рассчитаны по методу Jukes-Cantor. Масштаб соответствует 2 нуклеотидным заменам на каждые 100 нуклеотидов. Номера в базе данных GenBank указаны в скобках. Клоны с идентичными генами 16S рРНК перечислены через запятую
[A phylogenetic tree constructed using the neighbor-joining method, showing the position of the studied bacterial clones, based on a comparison of the nucleotide sequences of the 16S rRNA gene. The evolutionary distances are calculated using the Jukes-Cantor method. The scale corresponds to 2 nucleotide substitutions for every 100 nucleotides. The numbers in the GenBank database are shown in parentheses. Clones with identical 16S rRNA genes are comma-separated]
Заключение
В результате проведенных исследований получены новые данные о разнообразии бактерий солей ВКМС. Установлено, что в образце каменной соли, отобранном с глубины 239 м, присутствуют некуль-тивируемые бактерии различных таксонов: молекулярными методами было выявлено девять ОТЕ, принадлежащих классам Actinobacteria, Alpha -, Beta - и Gammaproteobacteria . Выявлены филотипы, проявляющие низкий уровень сходства по генам 16S рРНК с типовыми штаммами узаконенных видов, которые могут представлять новые таксономические единицы.
Список литературы Филогенетическое разнообразие бактерий в каменной соли Верхнекамского месторождения (Пермский край)
- Барях А.А., Асанов В.А., Паньков И.Л. Физико-механические свойства соляных пород Верхнекамского калийного месторождения: учеб. пособие. Пермь, 2008. 199 с.
- Бачурин Б.А., Одинцова Т.А., Хохрякова Е.С. Углеводородные маркеры органического вещества солей Верхнекамского месторождения // Проблемы минералогии, петрографии и металлогении. Научные чтения памяти П.Н. Чирвинского. 2016. № 19. С. 315-323.
- Корсакова Е.С. и др. Разнообразие бактерий семейства Halomonadaceae района разработок Верхнекамского месторождения солей // Микробиология. 2013. Т. 82, № 2. С. 247-250.
- Кудряшов А.И. Верхнекамское месторождение солей. Пермь, 2001. 429 с.
- Практикум по агрохимии: учеб. пособие / под ред. В.Г. Минеева и др. М.: Изд-во МГУ, 2001. 689 с.
- Равин Н.В. и др. Метагеномика как инструмент изучения «некультивируемых» микроорганизмов // Генетика. 2015. Т. 51, № 5. С. 519-528.
- Alain K., Querellou J. Cultivating the uncultured: limits, advances and future challenges // Extremophiles: Life Under Extreme Conditions. 2009. Vol. 13, № 4. P. 583-594.
- Ausbel F.M. et al. Short protocols in molecular biology. Third edition. N.Y.: John Wiley and Sons, 1995. 450 p.
- Doronina N.V. et al. Chelativorans multitrophicus gen. nov., sp. nov. and Chelativorans oligotrophicus sp. nov., aerobic EDTA-degrading bacteria // Int. J. Syst. Evol. Microbiol. 2010. Vol. 60 (Pt 5). P. 1044-1051.
- Fierer N. et al. Assessment of soil microbial community structure by use of taxon-specific quantitative PCR assays // Applied and Environmental Microbiology. 2005. Vol. 71, № 7. P. 4117-4120.
- Hamada M. et al. Draft genome sequences of eight type strains of the genus Demequina // Genome An-nounc. 2015. Vol. 3, № 2. P. e00281-15.
- Jaakkola S.T. et al. Buried alive: microbes from ancient halite // Trends Microbiol. 2016. Vol. 24, № 2. P. 148-160.
- Lane D.J. 16S/23S rRNA sequencing. In: Nucleic acid techniques in bacterial systematics / Eds. E. Stackebrandt, M. Goodfellow. N.Y.: John Wiley and Sons, 1991. P. 115-175.
- Larouche J.R. et al. Microbial biogeography of arctic streams: exploring influences of lithology and habitat // Front Microbiol. 2012. Vol. 3. P. 309.
- Margesin R., Schinner F. Potential of halotolerant and halophilic microorganisms for biotechnology // Extremophiles. 2001. Vol. 5, № 2. P. 73-83.
- Ramirez-Bahena M.H. et al. Pseudomonas edaphica sp. nov., isolated from rhizospheric soil of Cistus ladanifer L. in Spain // Int. J. Syst. Evol. Microbiol. 2019. Vol. 69. P. 3141-3147.
- Zhou M. et al. Draft genome sequence of Mesorhizobium alhagi CCNWXJ12-2T, a novel salt-resistant species isolated from the desert of northwestern China // J. Bacteriol. 2012. Vol. 194, № 5. P. 1261-1262.


