Физико-химическая и биохимическая характеристика смешанной слюны на различных сроках после дентальной имплантации
Автор: Зекий Ангелина Олеговна
Журнал: Природные системы и ресурсы @ns-jvolsu
Рубрика: Биология и биотехнология
Статья в выпуске: 4 (14), 2015 года.
Бесплатный доступ
В исследовании проведено сравнение физико-химических (pH, буферная емкость, вязкость) и биохимических (концентрации альбумина, кальция, фосфатов, активность a - амилазы и щелочной фосфатазы) показателей в смешанной слюне (ротовой жидкости, РЖ) лиц спустя 2-4 месяца и 5-11 месяцев после установки дентальных имплантатов и лиц с санированной полостью рта и удовлетворительным состоянием гигиены. Значение pH РЖ практически не различалось у лиц группы сравнения, а также на разных сроках после имплантации и при разном числе имплантатов. Буферная емкость РЖ в различные сроки после установки единичных имплантатов варьировала в пределах, характерных для группы сравнения. В сроки 2-4 месяца после установки трех и более имплантатов отмечалось уменьшение буферной емкости РЖ в 2,4 раза, в последующем это снижение восстанавливалось не полностью. Установка единичных имплантатов не сопровождалась изменением вязкости РЖ, в то время как при множественной дентальной имплантации на сроках 2-4 месяца вязкость была в 2,1 раза меньше, чем в группе сравнения. Показано, что изменения ряда биохимических показателей в РЖ, вызванные присутствием дентальных имплантатов в организме, зависят от их числа и сроков с момента начала нагрузки на установленные конструкции. Таким образом, наиболее значимые изменения заключаются в снижении буферной емкости и вязкости РЖ, концентрации ионов кальция, а также активности a - амилазы и сохраняются на сроках 5-11 месяцев с момента имплантации. Эти изменения сопоставлены с возможными функциональными свойствами РЖ, которые могут влиять на адаптацию зубо-челюстной системы к новым условиям функционирования, связанным с установкой дентальных имплантатов.
Дентальная имплантация, слюна, ротовая жидкость, буферная емкость, электролиты, амилаза, щелочная фосфатаза
Короткий адрес: https://sciup.org/14967481
IDR: 14967481 | УДК: 616.314-0 | DOI: 10.15688/jvolsu11.2015.4.3
Physico-chemical and biochemical characteristics of mixed saliva in patients at various time after dental implantation
The study deals with comparison of physico-chemical (pH, buffer capacity, viscosity) and biochemical (concentration of albumin, calcium, phosphate, the activity of a-amylase and alkaline phosphatase) variables in the mixed saliva (oral fluid, OF) in persons with dental implants depending on its number (1-2 or 3 and more) and time after installation (2-4 and 5-11 months), and those with satisfactory state of oral health and without implants. The pH value in OF was almost similar in patients of group comparison and at different times after implantation and at different number of implants. The OF buffer capacity in different periods after the installation of single implants varied, been typical for the comparison group. A 2.4-fold decrease of buffer capacity was character at 2-4 months after installation of three or more implants, later this decline has not recovered fully. The installation of a single implant was not accompanied by changes in the OF viscosity, while multiple dental implant installation let to increase of viscosity 2.1 times less than in the comparison group at 2-4 months terms. The alterations of some biochemical properties of OF after dental implantation were shown to depend on the number and timing since the load on the installed constructions. Thus, more significant changes in oral fluid are to reduce the buffer capacity and viscosity of oral fluid, the concentration of calcium ions and the activity of a-amylase, they may be stored at the time of 5-11 months after implantation. These changes are associated with possible functional properties of oral fluid, which may affect the adaptation of dental system to new functional conditions connected to dental implant installation.
Текст научной статьи Физико-химическая и биохимическая характеристика смешанной слюны на различных сроках после дентальной имплантации
Успехи ортопедической стоматологии, обусловленные появлением новых диагностических и лечебных технологий, привели к тому,
что дентальная имплантация претендует на роль «золотого стандарта» в восстановлении утраченных зубов. Число операций в крупных стоматологических клиниках исчисляется тысячами в год с эффективностью свыше 95 %, а в отдельных возрастных группах городского населения развитых стран доля людей с дентальными имплантатами приближается к 20 % [1; 12; 13; 24].
На настоящий момент наиболее часто для внутрикостной имплантации используются винтовые внутрикостные титановые имплантаты, прочность их прикрепления к кости (остеоинтеграция) обеспечивается за счет химической и биологической связи оксида титана непосредственно с костным матриксом [6; 17]. Именно с частичной утратой этой связи, бактериальным заселением образовавшихся зазоров и развитием воспаления окружающих тканей связывают основные причины неудач дентальной имплантации [3; 7; 14].
Полноценное функционирование имплантата и установленной на него ортопедической конструкции начинается спустя несколько месяцев с момента имплантации, когда область остеоинтеграции уже полностью закрыта твердыми и мягкими тканями, а между десной и шейкой имплантата сформирован аналог десневой борозды – периимплантаци-онная борозда (peri-implant sulcus), заполненная собственным секретом [8; 10; 15].
Смешанная слюна (РЖ) в настоящее время широко используется в качестве биоматериала для неинвазивного определения различных состояний, как в полости рта, так и в организме в целом [4; 21]. Поскольку наличие дополнительных секретирующих тканей в области имплантации может оказывать влияние на состав и свойства РЖ, нам представилось целесообразным исследовать ее на этот предмет у пациентов с различной длительностью функционирования дентальных имплантатов.
Цель работы
Выявить особенности физико-химических свойств и биохимического состава ротовой жидкости лиц, имеющих функционирующие дентальные имплантаты, в зависимости от их количества и сроков функционирования.
Материал и методы исследования
Основную группу составили 102 пациента (40 мужчин и 62 женщины) в возрасте от 21 до 74 лет, которым были установлены винтовые титановые имплантаты: Touareg (ADIN Dental implant systems Ltd, Израиль) – 21 пациенту (41 имплантат); SPI (Alpha-Bio. Tec. Ltd, Израиль) – 81 пациенту (183 имплантата). Единичные (один-два) имплантаты были установлены 68 пациентам, множественные (три и более) – 34 пациентам. Исследование РЖ у этих лиц проведено в сроки от 2 до 11 месяцев с момента установления абатментов: у 53 пациентов (21 мужчина и 32 женщины) в сроки от двух до четырех месяцев, у 49 (19 мужчин и 30 женщин) – в сроки 5–11 месяцев. В качестве группы сравнения были обследованы образцы РЖ у 37 человек (15 мужчин и 22 женщины возраста 28–63 лет), обратившихся в планово-профилактическом порядке к стоматологу и не имеющих на момент обследования заболеваний твердых тканей и/ или пародонта, состояние гигиены полости рта у которых было удовлетворительным. Половозрастной состав двух клинических групп был достаточно сходным (см. табл. 1).
В качестве биологического материала использовали смешанную слюну, или РЖ. Сбор материала проводили натощак, в состоянии покоя, строго с 8.00 до 9.00, учитывая циркадианные особенности биохимического
Таблица 1
Половозрастная характеристика обследованнных групп
Определение pH проводили сразу после получения РЖ при помощи прибора «Acorn pH5 series pH/oC Meter» (Oakton, США). Перед каждым последующим определением электрод промывался в физиологическом растворе и дважды – в дистиллированной воде. Отдельно 1 мл слюны смешивали с 1мл 0,01н раствора соляной кислоты, после чего также определяли pH. Эффективную буферную емкость при закислении (BA, мг-экв./л) рассчитывали по формуле:
BA = 10 / (pH0– рНA), где 10 – коэффициент пересчета на 1,0 л слюны; pH0– значение pH исходной РЖ; рНA– значение pH при добавлении кислоты.
Вязкость РЖ определяли на ротационном вискозиметре DV-II+ (Brookfield, США) с использованием специального адаптера для образцов малого объема. Значения показателя выражали в Па х с.
Биохимические исследования РЖ проводили на автоматическом анализаторе «SINOWA B-300», с помощью коммерческих наборов реактивов фирмы «DiaSys» (Германия). Определяли концентрации альбумина (г/л), ионов кальция (ммоль/л), фосфатов (ммоль/л), активности a -амилазы (мкКат/л) и щелочной фосфатазы (мкКат/л) в соответствии с инструкциями производителя.
Статистический анализ проводили с помощью программного пакета Statistica 8.0 (StatSoft Inc., США). На основании критериев Колмогорова–Смирнова и Шапиро–Уилка было не подтверждено нормальное распределение в выборке, в связи с чем были использованы непараметрические критерии: распределение в выборках выражали в виде медианы и интервала между первым и третьим квартилем (Ме [Q1 + Q3]), при сравнении выборок использовали критерий Манна–Уитни ( p < 0,01) [2].
Результаты исследования
Данные о величинах отдельных физикохимических показателей в РЖ у лиц исследуемых групп приведены в таблице 2.
Значение pH РЖ оказалось весьма консервативным показателем, и при данных способах получения биоматериала величина показателя практически не различалась у лиц группы сравнения, а также на разных сроках после имплантации и при разном числе имплантатов.
Буферная емкость РЖ в различные сроки после установки единичных имплантатов также варьировала в пределах, характерных для группы сравнения. В то же время в сроки 2–4 месяца после установки трех и более имплантатов отмечалось уменьшение буферной емкости в 2,4 раза ( p < 0,01), на сроке 5–11 месяцев после имплантации это снижение восстанавливалось не полностью. Исследование вязкости РЖ также показало, что установка единичных имплантатов не сопровождается изменением ее значения в РЖ, тогда как при множественной дентальной имплантации на сроках 2–4 месяца регистрируется низкая ве-
Таблица 2
Физико-химическая характеристика РЖ пациентов в различные сроки после дентальной имплантации и лиц группы сравнения (Ме [Q1 ÷ Q3])
|
Показатель |
Группа сравнения ( n = 37) |
Основная группа |
||
|
Количество имплантатов |
2–4 месяца ( n = 53) |
5–11 месяцев ( n = 49) |
||
|
pH |
6,80 [6,63 ÷ 7,01] |
1–2 |
6,69 [6,56 ÷ 6,92] |
6,65 [6,47 ÷ 6,97] |
|
> 2 |
6,55 [6,42 ÷ 6,80] |
6,61 [6,39 ÷ 7,00] |
||
|
B A , мг-экв./л |
7,9 [7,3 ÷ 8,4] |
1–2 |
7,1 [6,6 ÷ 7,8] |
7,6 [6,9 ÷ 8,3] |
|
> 2 |
3,3 [2,9 ÷ 4,7] * |
5,2 [3,7 ÷ 6,8] |
||
|
Вязкость, Па × ?с |
0,15 [0,12 ÷ 0,19] |
1–2 |
0,12 [0,06 ÷ 0,17] |
0,20 [0,11 ÷ 0,27] |
|
> 2 |
0,07 [0,04 ÷ 0,11] * |
0,17 [0,09 ÷ 0,25] |
||
Примечание . «*» – p < 0,01 с группой сравнения по критерию Манна – Уитни.
личина вязкости РЖ – в 2,1 раза меньше, чем в группе сравнения ( p < 0,01).
Данные о динамике отдельных биохимических показателей в РЖ у лиц исследуемых групп приведены в таблице 3.
Концентрация альбуминов в РЖ варьировала в группе сравнения от 0,47 до 0,68 г/л, в подгруппах основной группы – от 0,36 до 0,72 г/л, для периода 2–4 месяца в подгруппе с множественной имплантацией было характерно низкое значение показателя – в 1,4 раза меньше, чем в группе сравнения ( p < 0,01).
Концентрация ионов кальция в РЖ у пациентов основной группы через 2–4 месяца с момента нагрузки на имплантаты была ниже, чем у пациентов группы сравнения, в 1,7– 2,2 раза (p < 0,01), и тем ниже, чем больше имплантатов было установлено. Это снижение нормализовалось на сроках 5–11 месяцев у пациентов с единичными имплантатами, но сохранялось сниженным при множественной дентальной имплантации.
Содержание фосфатов в РЖ снижалось в гораздо меньшей степени, достоверные изменения зарегистрированы лишь в подгруппе с множественной дентальной имплантацией на сроках 2–4 месяца. Активность a -амилазы у большинства пациентов основной группы была значительно ниже, чем у пациентов группы сравнения, достоверные различия выявлялись во всех подгруппах. В противовес этому существенных отклонений от показателей в группе сравнения в отношении активности щелочной фосфатазы не было выявлено.
Анализируя полученные результаты, прежде всего остановимся на происхождении исследованных компонентов РЖ и опосредуемых ими свойств (см. рисунок).
Таблица 3
Отдельные биохимические характеристики РЖ пациентов в различные сроки после дентальной имплантации и лиц группы сравнения (Ме [Q1 ÷ Q3])
|
Показатель |
Группа сравнения ( n = 37) |
Основная группа |
||
|
Количество имплантатов |
2–4 месяца ( n = 53) |
5–11 месяцев ( n = 49) |
||
|
Альбумин, г/л |
0,56 [0,47 ÷ 0,68] |
1–2 |
0,51 [0,42 ÷ 0,64] |
0,59 [0,44 ÷ 0,72] |
|
> 2 |
0,40 [0,30 ÷ 0,48] * |
0,52 [0,39 ÷ 0,68] |
||
|
Кальций, ммоль/л |
1,60 [1,24 ÷ 1,88] |
1–2 |
0,94 [0,62 ÷ 1,03] * |
1,40 [1,17 ÷ 1,72] |
|
> 2 |
0,74 [0,47 ÷ 0,81] * |
1,22 [0,92 ÷ 1,53] * |
||
|
Фосфаты, ммоль/л |
5,85 [4,22 ÷ 7,07] |
1–2 |
4,95 [4,54 ÷ 4,48] |
5,59 [4,77 ÷ 6,14] |
|
> 2 |
4,25 [3,87 ÷ 4,69] * |
5,43 [4,60 ÷ 5,97] |
||
|
α-Амилаза, мкКат/л |
4,82 [4,05 ÷ 5,62] |
1–2 |
2,17 [1,48 ÷ 3,03] * |
2,35 [1,50 ÷ 3,18] * |
|
> 2 |
2,33 [1,57 ÷ 3,24] * |
2,29 [1,39 ÷ 2,95] * |
||
|
Щелочная фосфатаза, мкКат/л |
1,58 [1,14 ÷ 1,85] |
1–2 |
1,42 [0,96 ÷ 1,86] |
1,60 [1,08 ÷ 2,29] |
|
> 2 |
1,75 [1,23 ÷ 2,44] |
1,84 [1,15 ÷ 2,42] |
||
Примечание. «*» – p < 0,01 с группой сравнения по критерию Манна – Уитни.
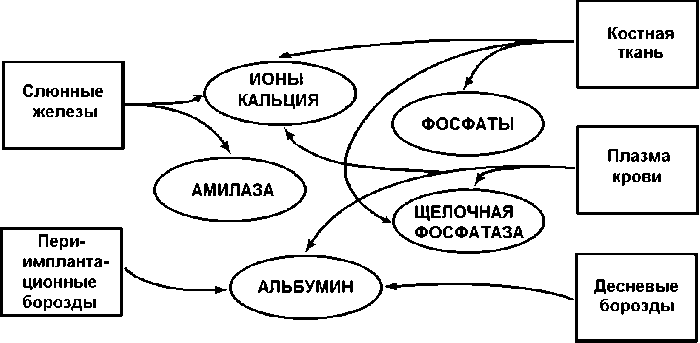
Основные источники изучаемых компонентов ротовой жидкости
Альбумин РЖ имеет комплексное происхождение, поступая в эту жидкость как в составе слюнного секрета, так и в составе большинства других секретов мягких тканей ротовой полости. Считается, что основным источником альбуминов в РЖ являются жидкость десневых борозд и, при их наличии, десневых карманов [19; 23]. Снижение альбуминов может быть результатом активного поглощения микрофлорой [14]. Именно нарушение микробного баланса полости рта после дентальных имплантаций может быть основной причиной уменьшения альбуминов в РЖ, выявленное нами у пациентов основной группы в ранние сроки после множественной дентальной имплантации.
Амилаза РЖ попадает туда практически полностью из слюнных желез, из плазмы крови может вторично поступать только при массивных деструкциях поджелудочной железы [19]. Обнаруженное уменьшение амилолитической активности РЖ у пациентов с дентальными имплантатами имеет практическое значение в плане оценки изменений пищеварительной функции в полости рта у этих лиц. Как минимум эта интересная находка требует дальнейшего изучения. Щелочная фосфатаза в саливодиагностике рассматривается как маркер повышенной остеорезорбции и воспалительных заболеваний пародонта и периимплантитов [9; 11; 22]. В нашем исследовании подтверждено, что в подавляющем числе случаев после проведенной дентальной имплантации эти процессы не активируются, что свидетельствует об успешном течении периода адаптации к новым конструкциям в полости рта.
Что касается ионов кальция и фосфатов, то интерес к их соджержанию в РЖ обусловлен участием в минерализации твердых тканей зубов, а уменьшения трактуются как фактор риска патологии этих тканей. Выявленные снижения содержания кальция в РЖ пациентов спустя 5–11 месяцев после начала нагрузок на имплантаты следует трактовать именно с этих позиций. Механизм снижения требует дальнейшего изучения и объяснения, но, по всей видимости, он косвенно связан с потреблением кальция на процессы остеоинтеграции и ремоделирования кости, окружающей дентальные имплантаты.
Безусловно, взаимоотношения отдельных компонентов зубочелюстной системы в процессе адаптации к дентальным имплантатам могут быть конкретизированы при изучении секреции в РЖ специфических маркеров межклеточных сигнализации, таких как цитокины и факторы роста, а также ферментативных систем, участвующих в остеоинтеграции и ремоделировании кости [20; 22]. Вероятно, более информативными при этом являются исследования материала, максимально приближенного к имплантатам, такого как жидкость периимплантационной борозды, но эти исследования только начинаются [16; 18].
Список литературы Физико-химическая и биохимическая характеристика смешанной слюны на различных сроках после дентальной имплантации
- К вопросу об остеоинтеграции дентальных имплантатов и способах ее стимуляции/С. В. Поройский //Вестник Волгогр. гос. мед. ун-та. -2015. -№ 3 (55). -С. 6-9.
- Новиков, Д. А. Статистические методы в медико-биологическом эксперименте (типовые случаи) /Д.А. Новиков, В.В. Новочадов. -Волгоград: Изд-во ВолгГМУ, 2005. -84 с.
- Оценка изменения качества жизни пациентов с дефектами зубных рядов и заболеваниями пародонта до и после проведения протезирования и имплантации зубов/Е. В. Турусова //Сарат. н.-мед. журн. -2011. -Т. 7, № 3. -С. 689-692.
- Постнова, М. В. Ротовая жидкость как объект оценки функционального состояния организма человека/М. В. Постнова, Ю. А. Мулик, В. В. Новочадов//Вестник Волгоградского государственного университета. Серия 3, Экономика, экология. -2011. -№ 1. -С. 246-253.
- Циркадианная организация физико-химических свойств ротовой жидкости практически здоровых людей / В.И. Шемонаев и др. //Научные ведомости Белгородского государственного университета. Серия: Медицина. Фармация. -2012. -Т. 17, № 4. -С. 243-249.
- A retrospective study on r elated factors affecting the survival rate of dental implants/H. W. Jang //J. Adv. Prosthodont. -2011. -Vol. 3, № 4. -P. 204-215.
- A review of dental implants and infection/A. D. Pye //J. Hosp. Infect. -2009. -Vol. 72, № 2. -P. 104-110.
- Bhardwaj, S. K. Comparative volumetric and clinical evaluation of peri-implant sulcular fluid and gingival crevicular fluid/S. K. Bhardwaj, M. L Prabhuji//J. Periodontal Implant Sci. -2013. -Vol. 43, № 5. -P. 233-242.
- Biofilm and saliva affect the biomechanical behavior of dental implants/D. Bordin //J. Biomechanics. -2015. -Vol. 48, Iss. 6. -P. 997-1002.
- Clinical outcomes measures for assessment of longevity in the dental implant literature: ORONet approach/F. Bassi //Int. J. Prosthodont. -2013. -Vol. 26, № 4. -P. 323-330.
- Current developments in salivary diagnostics/C. S. Miller //Biomark. Med. -2010. -Vol. 4, № 1. -P. 171-189.
- Harford, J. Population ageing and dental care/J. Harford//Com. Dent. Oral Epidemiol. -2009. -Vol. 37, № 2. -P. 97-103.
- Implant-supported mandibular overdentures in very old adults: a randomized controlled trial/F. Muller //J. Dent. Res. -2013. -Vol. 92, Suppl. 2. -P. 154S-160S.
- Early microbial succession in re-developing dental biofilms in periodontal health and disease/F. R. Teles //J. Periodontal. Res. -2012. -Vol. 47, № 1. -P. 95-104.
- Escoe, R. Saliva and dentures/R. Escoe//J. Am. Dent.Assoc. -2008. -Vol. 139, № 8. -P. 1028-1029.
- Gupta, G. Gingival crevicular fluid as a periodontal diagnostic indicator-I: Host derived enzymes and tissue breakdown products/G. Gupta//J. Med. Life. -2012. -Vol. 5, № 4. -P. 390-397.
- Interaction of titanium, zirconia and lithium disilicate with peri-implant soft tissue: study protocol for a randomized controlled trial/K. Kuhn //Trials. -2015. -Vol. 16. -P. 467.
- Kajale, A. M. Interleukin-1b level in peri-implant crevicular fluid and its correlation with the clinical and radiographic parameters/A. M. Kajale, D. S. Mehta//J. Indian Soc. Periodontol. -2014. -Vol. 18, № 2. -P. 220-225.
- Malamud, D. Saliva as a diagnostic fluid/D. Malamud, I. R. Rodriguez-Chavez//Dent. Clin. North Am. -2011. -Vol. 55, № 1. -P. 159-178.
- Release of bone markers in immediately loaded and nonloaded dental implants: a randomized clinical trial/A. J. Prati //J. Dent. Res. -2013. -Vol. 92 (12 Suppl.). -P. 161S-167S.
- Salivary biomarkers associated with gingivitis and response to therapy/B. Syndergaard //J. Periodontol. -2014. -Vol. 85, № 8. -Р. 295-303.
- Spielmann, N. Saliva: diagnostics and therapeutic perspectives/N. Spielmann, D. T. Wong//Oral Dis. -2011. -Vol. 17, № 4. -P. 345-354.
- Targeted salivar y biomarker s for discrimination of periodontal health and disease(s)/J. L.Ebersole //Front. Cell Infect. Microbiol. -2015. -Vol. 5. -P. 62.
- Tomasi, C. Longevity of teeth and implants: a systematic review/C. Tomasi, J. L. Wennström, T. J. Berglundh//Oral Rehabil. -2008. -Vol. 35, Suppl. 1. -P. 23-32.


