Физико-химические закономерности создания новых гибридных эпоксиполимерных нанокомпозитов с повышенными прочностными характеристиками
Автор: Ситников П.А., Рябков Ю.И., Белых А.Г., Васенева И.Н., Кучин А.В.
Журнал: Известия Коми научного центра УрО РАН @izvestia-komisc
Рубрика: Химические науки
Статья в выпуске: 1 (25), 2016 года.
Бесплатный доступ
Методом рК-спектроскопии исследованы кислотно-основные свойства поверхности оксидов алюминия, железа, кремния. Изучены физико-химические закономерности реакций между эпоксидными олигомерами и модифицирующими наполнителями. Отмечена наивысшая реакционная способность γ-Al2O3 и γ-AlO(OH) за счет наличия наиболее активных поверхностных групп с рК1≈4. Дано обоснование повышения прочностных характеристик гибридных эпоксиполимерных нанокомпозитов.
Кислотно-основные свойства, оксиды алюминия, железа, кремния, наномодификаторы, эпоксидные полимеры, композиты
Короткий адрес: https://sciup.org/14992803
IDR: 14992803 | УДК: 547.912.4.678
Physical and chemical regularities of creating new hybrid epoxy polymer nanocomposites with increased strength characteristics
By the method of pK-spectroscopy the acid-base properties of the surface of oxides of aluminium, iron, silicon are investigated. Physical and chemical regularities of the reactions between epoxy oligomers and modified fillers are studied. Higher reactivity of γ-Al2O3 and γ-AlO(OH) is observed due to the presence of the most active surface groups with pK1≈ 4. Substantiation for increasing the strength characteristics of hybrid epoxy polymer nanocomposites is given.
Текст научной статьи Физико-химические закономерности создания новых гибридных эпоксиполимерных нанокомпозитов с повышенными прочностными характеристиками
В настоящий момент для новых инфраструктурных проектов, например, морских объектов в Арктике, требуются новые материалы и технологии производства изделий. Эксплуатация ледовых платформ, конструкционных элементов трубопроводов и других изделий в экстремальных природно-климатических условиях, жесткие требования по безопасности и необходимость выдерживать максимальные ледовые нагрузки остро ставят вопрос о постоянном совершенствовании применяемых при их изготовлении и эксплуатации материалов. Композиты на основе эпоксидных олигомеров успешно используются на ледостойких платформах в качестве защитных оболочек металлических конструкций, а также при изготовлении райзерных узлов и компонентов трубопроводов из стеклопластика [1].
На основе эпоксидов активные наполнители способны существенно менять эксплуатационные характеристики полимерных материалов (механическую прочность, тепло- и термостойкость, электропроводность) за счет образования межфазного адсорбционного слоя на границе раздела полимер– наполнитель [2–6]. К сожалению, единого подхода, который позволял бы оценивать взаимодействия на межфазной границе, прогнозировать и регулировать такие взаимодействия, а значит, направленно совершенствовать качество материалов и эффективность технологий производства изделий, до сих пор не разработано.
Анализ литературных данных позволяет утверждать, что систематические исследования по изучению влияния поверхностных реакционных центров (гидроксильные группы, координационноненасыщенные центры и пр.) дисперсных частиц модифицирующего наполнителя на адгезионную способность, физико-механические характеристики полимерной матрицы до настоящего времени не осуществлены, несмотря на то, что даже незначительное варьирование химического состава поверхности вызывает значительное изменение адсорбционной способности [7]. Поэтому предметом исследования авторов является разработка мето- дов направленной модификации поверхности наполнителей с использованием современных методов их синтеза, эффективных способов контроля параметров межфазного взаимодействия, выявление физико-химических закономерностей при получении полимерного композиционного материала. Оксиды металлов нашли широкое применение в качестве наполнителей термо- и реактопластов. В представленной работе изучены оксид кремния (аэросил), а также различные модификации оксидов алюминия (γ-AlO(OH), γ-Al2O3, α-Al2O3) и железа (γ-FeO(OH), γ-Fe2O3, α-Fe2O3), химия поверхности которых хорошо изучена [8–10]. Непосредственной целью работы является исследование влияния кислотно-основных свойств поверхности оксидов на физико-химические процессы, протекающие при их введении в эпоксидные соединения.
Методика исследования
В работе использовался оксид алюминия, полученный методом осаждения из насыщенного раствора нитрата алюминия (ЧДА) водным раствором гидроксида аммония (ω=23 %, ХЧ). Добавление осадителя проводили до рН 7,5. Для получения различных полиморфных модификаций оксида алюминия синтезированный гидроксид алюминия прокаливали при температурах 300 (γ-AlO(OH)), 650 (γ-Al 2 O 3 ), 1200°C (α-Al 2 O 3 ) в течение 1 час, со скоростью нагрева 60°С/час.
Производные гидроксида железа ситезиро-вали золь-гель способом из хлорида железа (III) (ХЧ). Полученные дисперсные системы были охарактеризованы по ряду параметров, таких как: значение pH (1,42 ± 0,02), средний размер частиц (9,3 ± 0,3 нм), содержание дисперсной фазы (0,52 ± 0,05 %), электрокинетический потенциал (+27,3 ± 2,17 мВ). Оксид кремния получен разложением паров хлорида кремния (ХЧ) в атмосфере водяного пара при температуре 1000 °С.
Кислотно-основные свойства оксидов изучали методом рК-спектроскопии. Для анализа проводился отбор образцов суспензий с размером частиц 1–2 мкм. Перед титрованием аликвот суспензий рН доводили до 2–3, и в этих условиях выдерживались в течение 1 сут. Ионную силу в процессе титрования поддерживали равной 0.1 моль/л. Титрование осуществлялось в термостатируемых (±0.2°С) полипропиленовых стаканах в токе аргона. Обычно проводили два параллельных титрования, на основании которых рассчитывали погрешность кривой титрования, учитываемую в дальнейшем при расчете рК-спектров.
Кислотно-основные свойства изучаемого материала удобно охарактеризовать с помощью метода рК-спектроскопии [11, 12]. По оси ординат pK-спектра откладывается доля кислотно-основных центров с соответствующим pK (либо удельное содержание таких центров q, ммоль/г), в зависимости от pK. Расчет рК-спектров проводится по кривым титрования:
0 cc HA V 0 - c B0 H V - [H + ] . (V о + V ) 1 H (PH) = n b ( PH ) + n H = ---------------------------- + n H
m
В этой формуле: n H — количество ионов водорода (ммоль/г), адсорбированных на частицах суспензии в начальной точке титрования pH 0 , n b (pH) – количество ионов водорода (ммоль/г), адсорбированных на частицах суспензии в ходе титрования до текущей величины pH , V 0 - объем суспензии, C HA -концентрация одноосновной сильной кислоты в ней, V – объем добавленной щелочи с концентрацией CBOH , m - масса твердой фазы суспензии в образце.
Кислотно-основные свойства оксидных материалов были интерпретированы на основе 2рК-модели [13]. Исследование процессов, протекающих при термическом воздействии на исследуемые системы, осуществлялось с помощью дифференциального сканирующего калориметра Shimadzu DSC-60 (скорость подъема температуры 2 °С/мин в воздушной атмосфере). ИК-спектры модельных систем на основе фенилглицидилового эфира и оксидов снимали после их предварительной изотермической выдержки при 90 °С в течение 1 ч при помощи спектрометра IR Prestige 21, в тонком слое, между окошками KBr.
В качестве модельного эпоксисодержащего соединения выбран фенилглицидиловый эфир (ТУ 6-08-3321-73, содержание эпоксидных групп 26%). Наличие в его структуре единственного типа функциональных групп упрощает исследование взаимодействия поверхности наполнителя с эпоксидным олигомером.
Результаты и обсуждение
Типичные зависимости n b (pH) , рассчитанные из кривых прямого и обратного потенциометрического титрования суспензии (на примере γ-Al 2 O 3 ), показаны на рис. 1. Из него видно, что последовательно выполненные прямые и обратные титрования дают идентичные результаты, значит, процессы, протекающие при титровании, обратимы.
♦ 1 -е титрование, прямое
■ 2-е титрование, прямое
А 1 -е титрование, обратное
• 2-е титрование, обратное
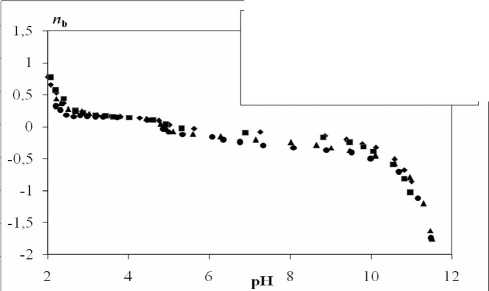
Рис.1. Адсорбция ионов водорода на поверхности Al 2 O 3 как функция рН.
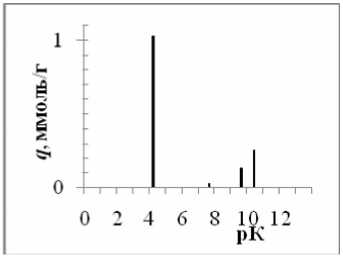
На рис. 2 представлены рК-спектры модификаций оксида алюминия. В соответствии моделью 2рК [10] пики спектров можно отнести к следующим равновесиям:
–Al–OH2+ eS –Al–OH + H+ (рК1 ≈ 4)
–Al–OH Я –Al–O- + H+ (рК 2 ≈ 10-12)
–Al–OH 2 + Cl- ^ –Al–OH+H++ Сl- (рК 3 ≈ 7-8)
–Al–OH + Na+<=* –Al–O-Na++ H+ (рК 4 ≈ 8-10) .
а)
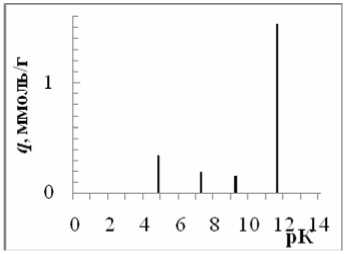
б)
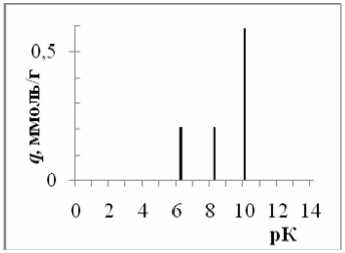
в)
Рис. 2 рК-спектры γ -AlO(ОН) ( а ), γ -Al 2 O 3 ( б ), α -Al 2 O 3 ( в ).
Величина рК 1 в ряду γ-AlO(ОН) – γ-Al 2 O 3 – α-Al 2 O 3 заметно уменьшается вплоть до полного ее исчезновения у корунда, а равновесие, соответствующее рК 2 , практически не зависит от модификации оксида алюминия.
В случае с производными гидроксида железа (III), с увеличением температуры прокаливания происходит удаление воды с образованием в конечном счете поверхностных кислотно-основных центров, поведение которых описывается уравнением: –Fe–OH Ei –Fe–O- + H+ (рК 2 ≈ 11).
При анализе кислотно-основных свойств SiO 2 обычно принимается, что заряд его поверхности изменяется за счет диссоциации поверхностных силанольных групп в соответствии с реакциями:
–Si–OH 2+ # –Si–OH + H+ (рК 1 ≈ 6)
–Si–OH S –Si–O- + H+ (рК 2 ≈ 10).
Известно, что ионы фонового электролита образуют с поверхностными гидроксильными группами оксида кремния комплексы. Весьма вероятно, что между этими слабо сорбирующимися ионами и поверхностью расположен, как минимум, один слой молекул воды, который отделяет эти ионы от атомов кислорода или кремния на поверхности, т.е. они образуют ионные пары или внешнесферные комплексы [14]. Поэтому для описания протолитических свойств оксида кремния, кроме реакции диссоциации, необходимо учитывать реакцию образования внеш-несферных комплексов с катионами электролита:
–Si–OH + Na+ Ei –Si–O-Na++ H+ (рК 4 ≈ 9-10).
Методом дифференциальной сканирующей калориметрии (ДСК) исследованы физико-химические процессы, протекающие при добавлении к фе-нилглицидиловому эфиру (ФГЭ) порошков оксидов. На основании данных ДСК представлены параметры взаимодействия в модельных системах Al 2 O 3 – ФГЭ (см. таблицу).
Температурные параметры и тепловой эффект процесса взаимодействия в модельных системах
ФГЭ – γ -AlO(ОН) и ФГЭ – γ -Al 2 O 3
|
Т start , °C |
T max , °С |
T end , °C |
Q , Дж/г |
|
|
γ-AlO(ОН) |
80 |
105 |
125 |
8.6 |
|
γ-Al 2 O 3 |
76 |
105 |
125 |
6.2 |
В случае γ-AlO(ОН) и γ-Al 2 O 3 имеется экзотермический пик химического взаимодействия эпоксидных групп с поверхностными кислотноосновными центрами, а у α-Al 2 O 3 такого пика не наблюдается. Для оксидов железа и кремния на кривых ДСК, как и в случае α-Al 2 O 3 , процессы химического взаимодействия эпоксидных групп с активными центрами поверхности наполнителя не обнаруживаются.
Так как константы равновесия K 1 и K 2 характеризуют силу кислотно-основных центров, наличие на рК-спектре линии с рК 1 около 4 для γ-AlO(ОН) и γ-Al 2 O 3 свидетельствует о более высокой их реакционной способности по сравнению с остальными изученными оксидами.
Это подтверждается также данными ИК-спектроскопии (IR Prestige 21). При нагревании смеси ФГЭ–γ-AlO(OH) (90°C, 1 час) интенсивность полос поглощения, соответствующих колебаниям эпоксидных групп (750–950 см-1), заметно снижается, что свидетельствует об исчезновении эпоксидных циклов и полимеризации фенилглицидилового эфира на поверхности оксида алюминия.
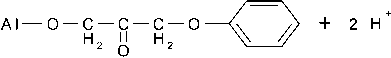
Появление полосы поглощения в области 1650–1600 см-1, отвечающей валентному колебанию связи С=О, сопряженной с атомом кислорода, позволяет предположить, что раскрытие эпоксидного цикла происходит по схеме:
H
Al OH + H 2 C C C O O H2
где Al – атом алюминия на поверхности наполнителя.
При нагревании системы ФГЭ–γ-Al 2 O 3 заметно уменьшается интенсивность полос поглощения эпоксидных групп. Кроме того, в интервале 1150–1060 см-1 появляются полосы поглощения, отвечающие алифатическим простым эфирным связям –С–О–С–. Эти изменения спектров указывают на то, что при нагревании системы происходит гомополимеризация фенилглицидилового эфира с образованием простого полиэфира, а активные центры на поверхности оксида алюминия выступают как инициаторы полимеризации:
OO
O Al O + H 2 C CH R H 2 C CH R
O Al O
Кроме указанных взаимодействий, в ИК-спек-трах проявляются поверхностные гидроксильные группы, аналогично имеющимся в γ-AlO(OH) (слабый пик в области 1640–1630 см-1). Появление гидроксильных групп связано с гидролизом [7]:
–Al–O–Al– + H 2 O 2–Al–OH.
При нагревании смесей ФГЭ с другими оксидами заметных изменений в ИК-спектрах не наблюдается.
Заключение
Таким образом, в настоящей работе показано, что из изученных модификаций оксидов алюминия, железа и кремния лишь в γ-Al 2 O 3 и γ-AlO(OH) имеются кислотно-основные центры, поведение которых описывается уравнением –Al–OH 2 + –Al– OH + H+ с рК 1 ≈ 4. Эти модификации за счет наличия активных поверхностных групп являются наиболее реакционноспособными наполнителями эпоксидных олигомеров, вступая с ними в химические реакции. При этом происходит как химическое взаимодействие эпоксида с гидроксильными группами на поверхности оксида алюминия, так и гомополимеризация фенилглицидилового эфира, инициированная поверхностно активными центрами наполнителя. Менее активные оксиды железа, кремния и корунд в непосредственное химическое взаимодействие с эпоксидными соединениями не вступают. Модифицирующее действие этих наполнителей может быть связано с образованием водородных связей между эпоксидными группами и поверхностными кислотно-основными центрами оксидов.
Результаты изучения физико-химических закономерностей процессов полимеризации матрицы композиционных материалов, модифицированной субмикро- (оксид алюминия) и нанодисперсными минеральными компонентами (наночастицы и нановолокна оксидов алюминия, железа, кремния), процессов, идущих с участием активных поверхностных групп нанооксидов, использованы для направленного получения образцов композиционных
материалов с повышенной теплостойкостью (до 160 °С), прочностными характеристиками (σ изг = 120 МПа, σ разр = 260 МПа), относительным удлинением для клеевых составов, увеличенным со 100 до 700 %.
Работа выполнена при поддержке программ фундаментальных исследований РФФИ (проект 13-03-00132), УрО РАН (проекты № 12-33-004-АРКТИКА, 12-И-3-2005).
Работа выполнена с использованием оборудования Центра Коллективного Пользования (ЦКП) «Химия» Института химии Коми НЦ УрО РАН.
Список литературы Физико-химические закономерности создания новых гибридных эпоксиполимерных нанокомпозитов с повышенными прочностными характеристиками
- Ягубов Э.З. Композиционно-волокнистые трубы в нефтегазовом комплексе. М.: Изд-во Центр ЛитНефтеГаз, 2008. 271 с.
- Хозин В.Г. Усиление эпоксидных полимеров. Казань: Изд-во ПИК «Дом печати», 2004. 446 с.
- Novak B.M. Hybrid nanocomposite Materials -Between Inorganic Glasses and Organic Polymers//Adv.Mater. Vol.5. 1993. №6. P. 422-433.
- Дебердеев Т.Р., Гарипов Р.М., Гарипова Л.Р. Моделирование процесса отверждения эпоксиаминных композиций, содержащих активные модификаторы//Структура и динамика молекулярных систем. 2003. Вып. X. Ч. 1. С. 59-61.
- Baller J., Thomassey M., Ziehmer M. et al. The catalytic influence of alumina nanoparticles on epoxy curing//Thermochimica Acta. 2011. Vol. 517. № 1-2. P. 34-39.
- Pestov A.V., Kuznetsov V.A., Mekhaev A.V. et al. Designing new adhesive materials based on epoxy oligomers filled with organic compounds//Polymer Science, Series D. Glues and Sealing Materials, 2015. Vol. 8. No. 2. P. 149-152.
- Bekir S., Özkanat Ö., Mol J. et al. Role of Surface Oxide Properties on the Aluminum/Epoxy Interfacial Bonding//J. Phys. Chem. 2013. Vol. 117. P. 4480-4487.
- Yates D. E., Levine S., and Healy T. W. Sitebinding Model of the Electrical Double Layer at the Oxide/Water Interface. J. Chem. Soc. Faraday Trans. 1974. Vol. 70. P. 1807-1818.
- Химия привитых поверхностных соединений/Под ред. Г.В. Лисичкина. М.: Физматлит, 2003. 592 с.
- Hiemstra T., Wit J.C.M.D., Riemsdijk W.H.V. Multisite proton adsorption modeling at the solid/solution interface of (hydr)oxides: A new approach II. Applications to various important (hydr)oxides. J. Colloid. Interface Sci. 1989. Vol. 133. P. 105-117.
- Рязанов М.А. Кислотно-основные свойства поверхности оксидных материалов//Известия Коми научного центра УрО РАН. 2011.Вып. 2(6). С. 25-29.
- Рязанов М.А., Дудкин Б.Н. Использование pК-спектроскопии для изучения кислотноосновных свойств золей гидратированного оксида алюминия//Коллоидный журнал. 2004. Т. 66. № 6. С. 807-810.
- Davis J.A., James R. and Leckie J.O. Surface Ionization and Complexation at the Oxide/Water Interface. I Computation of Electrical Double Layer Properties in Simple Electrolytes. J. Colloid Interf. Sci. 1978. Vol. 63. P. 480-499.
- Власова Н.Н. Сравнение моделей комплексообразования на поверхности для количественного описания кислотных свойств высокодисперсного кремнезема//Химия, физика и технология поверхности. 2008. Вып. 14. С. 6-15.


