Физиологические основы лечения синдрома диабетической стопы, осложнённой дистальной артериальной ишемией нижних конечностей, с помощью ингаляций подогретой кислородно–гелиевой смеси (обзор литературы)
Автор: Маслов В.О., Мануйлов В.М., Щербюк А.Н., Немсцверидзе Я.Э., Андрущенко А.А.
Журнал: Вестник медицинского института "РЕАВИЗ": реабилитация, врач и здоровье @vestnik-reaviz
Рубрика: Клиническая медицина
Статья в выпуске: 3 т.15, 2025 года.
Бесплатный доступ
Актуальность. В настоящее время вопросы лечения сахарного диабета первого и второго типа стоят наряду с серьёзными патологиями сердечно-сосудистой системы, бронхо-лёгочными заболеваниями и являются большой медико-социальной проблемой. По данным Эндокринологического научного центра на 1 января 2023 года, сахарный диабет второго типа занимает лидирующее место по заболеваемости в России. На его долю приходится 92,33% от общей численности пациентов с сахарным диабетом в РФ, состоящих на диспансерном учёте (4,58 млн человек). Общая численность пациентов с сахарным диабетом РФ, состоящих на диспансерном учёте, на 01.01.2023 г., по данным Федерального регистра сахарного диабета, составила 4 962 762 (3,31% населения РФ) и их численность неуклонно и стремительно растёт. Диабетическая стопа представляет собой серьёзную проблему, требующую междисциплинарного подхода в лечении и профилактике. В XXI веке важно понимать, что лечение диабетической стопы требует не только контроля уровня глюкозы в крови, но и применения современных методов диагностики и терапии, вплоть до хирургического вмешательства. Целью исследования является улучшение клинических результатов лечения пациентов с синдромом диабетической стопы путём разработки новой методики комбинированного лечения, основанной на результатах физиологического ответа организма человека на ингаляции подогретой кислородно-гелиевой смесью. Исследовать физиологические свойства подогретой кислородно-гелиевой смеси в части её влияния на центральную и перефирическую гемодинамику в различные фазы раневого процесса. Сравнить эффективность проводимой терапии у пациентов с использованием национальных клинических рекомендаций и терапии с использованием кислородногелиевой смеси. Разработать оптимальный план лечения пациентов с синдромом диабетической стопы, осложнённой диабетической ангиопатией как на госпитальном этапе, так и в амбулаторно-поликлиническом звене. Материалы и методы. Авторами произведён подробный анализ отечественной и зарубежной литературы. Литературный обзор посвящён физиологическим и патофизиологическим аспектам влияния подогретой кислородно-гелиевой смеси на лечение осложнений сахарного диабета, особенно язвенных поражений нижних конечностей. Вывод. Из полученных данных проведённого исследования можно сделать вывод, что выявление клинически важного свойства разогретой кислородно-гелиевой смеси помогает повысить эффективность комбинированного лечения, качество жизни пациентов. Применение разогретых кислородно-гелиевых смесей в клинической практике способствует сокращению стационарного койко-дня и амбулаторных сроков проводимой терапии, а также уменьшению инвалидизации пациентов от калечащих оперативных вмешательств.
Синдром диабетической стопы, диабетическая ангиопатия, дистальная ишемия, артериальная недостаточность, заболевания периферических артерий, кислородная терапия, гелий, кислородно-гелиевая смесь
Короткий адрес: https://sciup.org/143184575
IDR: 143184575 | УДК: 616.411-089 | DOI: 10.20340/vmi-rvz.2025.3.CLIN.5
Physiological basis for treatment of diabetic foot syndrome complicated by distal arterial ischemia of the lower extremities using inhalation of a heated oxygen-helium mixture (literature review)
Relevance. Currently, the issues of treatment of type 1 and type 2 diabetes mellitus are along with serious pathologies of the cardiovascular system, bronchopulmonary diseases and are a major medical and social problem. According to the Endocrinological Research Center, as of January 1, 2023, type 2 diabetes mellitus occupies a leading place in terms of morbidity in Russia. It accounts for 92.33% of the total number of patients with diabetes in the Russian Federation registered at the dispensary (4.58 million people). The total number of patients with diabetes in the Russian Federation registered at the dispensary as of 01.01.2023, according to the Federal Register of Diabetes Mellitus, amounted to 4,962,762 (3.31% of the population of the Russian Federation) and their number is steadily increasing in rapid progression. Diabetic foot is a serious problem that requires an interdisciplinary approach in treatment and prevention. In the XXI century, it is important to understand that the treatment of diabetic foot requires not only blood glucose control, but also the use of modern diagnostic and therapeutic methods, including surgery. The purpose of the study. The purpose of this scientific study is to improve the clinical results of treatment of patients with diabetic foot syndrome by developing a new method of complex (combined) surgical treatment based on the results of the physiological response of the human body to inhalation of a heated helium-oxygen mixture. To investigate the physiological properties of a heated oxygen-helium mixture in terms of its effect on central and peripheral hemodynamics in various phases of the wound process. To compare the effectiveness of therapy in patients using national clinical guidelines and therapy using an oxygen-helium mixture. To develop an optimal treatment plan for patients with diabetic foot syndrome complicated by diabetic angiopathy, both at the hospital stage and in the outpatient clinic. Materials and methods. The authors have made a detailed analysis of Russian and foreign literature. The literature review is devoted to the physiological and pathophysiological aspects of the effect of a heated oxygen-helium mixture on the treatment of complications of diabetes mellitus, especially ulcerative lesions of the lower extremities. Conclusion. From the data obtained from the study, it can be concluded that the identification of a clinically important property of a heated oxygen–helium mixture will help improve the effectiveness of combined treatment and the quality of life of patients. To open up new opportunities for the use of heated oxygen-helium mixtures in clinical practice, as a result, to reduce the inpatient bedday and outpatient duration of therapy, to reduce the disability of patients from crippling surgical interventions.
Текст научной статьи Физиологические основы лечения синдрома диабетической стопы, осложнённой дистальной артериальной ишемией нижних конечностей, с помощью ингаляций подогретой кислородно–гелиевой смеси (обзор литературы)
Гелий, занимающий вторую позицию в периодической системе химических элементов Д.И. Менделеева, является одним из наиболее распространённых веществ во Вселенной. Его открытие связано с исследованиями солнечного излучения, проведёнными в XIX веке. 18 августа 1868 года, находясь в индийском штате Андхра-Прадеш, городе Гунтур, французский учёный Пьер Жюль Сезар Жансен наблюдал солнечное затмение. Используя взаимодействие электромагнитного излучения с веществами, то есть метод спектроскопии, он анализировал свет, излучаемый хромосферой Солнца. В ходе эксперимента Жансен зафиксировал неизвестную ранее спектральную линию ярко-жёлтого цвета, которая не соответствовала характеристикам ни одного из известных на тот момент элементов. Позднее, 20 октября 1868 года, английский астроном Джозеф Норман Локьер, независимо от Жансена, который первоначально не придал должного значения своему открытию, воспроизвёл идентич-
Doctor and Health. 2025;15(3):94–108. ное наблюдение. Он также обнаружил ярко-жёлтую линию в спектре солнечного света, которая была близка по длине волны к линиям натрия D1 и D2, но не совпадала с ними. Локьер установил, что данная линия, обозначенная им как D3, не имеет ничего общего с ранее выявленными и известными миру элементами. В 1870 году, совместно с химиком Эдуардом Франклендом, он предложил название для нового элемента — «гелий», происходящее от древнегреческого слова «солнце», что подчёркивало его связь с солнечным спектром. Таким образом, открытие гелия стало результатом совместных усилий учёных, применявших спектроскопические методы для изучения космических явлений. Это событие не только расширило представления о химическом составе Вселенной, но и подтвердило важность междисциплинарного подхода в науке [1–4].
Благодаря своим уникальным физическим свойствам гелий представляет собой важный элемент в области медицины и спортивной реабилитации. Его инертность позволяет безопасно использовать га- зовые смеси, содержащие гелий и кислород, для оптимизации доставки кислорода к тканям организма.
Уникальность гелия проявляется в том, что он не угнетает активность центральной нервной системы и не вызывает негативных последствий для сердечно-сосудистой и дыхательной систем. Эти свойства делают кислородно-гелиевую смесь безопасной для использования, так как она не вызывает токсических реакций и не приводит к долгосрочным изменениям в организме.
В судебно-медицинской практике крайне редко фиксируются летальные исходы, обусловленные ингаляцией инертных газов, таких как гелий. Как показывает практика, вероятность летального исхода в подобных ситуациях принято ассоциировать с техногенными инцидентами или с нарушениями регламента безопасности при осуществлении технологических операций и процессов, предполагающих утилизацию газа. Согласно регламенту безопасности при манипуляциях с гелием, существует риск травматизации слизистой оболочки органов зрения, обморожения кожных покровов, а также получения механических повреждений при падении крупногабаритного газового баллона. Кислородная недостаточность и асфиксия могут быть спровоцированы чрезвычайно высокими концентрациями гелия в воздушной среде [5].
Пациентам с зафиксированными показателями артериального давления (АД) гипертонической болезни 3 степени, при соответствующем давлении выше или равным 180 систолического и 110 диастолического мм рт. ст. соответственно; риск манифестации и/или прогрессирования сердечнососудистых осложнений высокой степени; тяжёлой степенью бронхообструкции (ОФВ1 менее 50% от должного); выраженной одышкой с ключевыми показателями равным или более 2 баллов по шкале «The Modified Medical Research Council Dyspnea Scale(сокращенно: mMRC)», наличие избыточно воздуха в лёгких, нарушающего их анатомическую структуру, то есть эмфиземы, при наличии одного или более симптомов назначение кислородно-гелиевой смеси не показано [6].
Кислородно-гелиевая смесь особенно актуальна для лечения состояний, связанных с гипоксией, когда происходит недостаток кислорода в тканях. Кислород, доставляемый в сочетании с гелием, улучшает оксигенацию, снижая сопротивление дыхательных путей. Это важно не только для спортивной медицины, но и для терапии пациентов с различными патологическими состояниями, связанными с синдромом диабетической стопы.
Перспективный метод профилактики декомпрессионной (кессонной) болезни, возникающей при длительном нахождении в условиях высокого дав- ления при глубоководных погружениях, был впервые апробирован специалистами медицинского подразделения военно-морского флота США. Данный метод заключается в ингаляционном применение газовой смеси, которая состоит из гелия и кислорода, получившей название «Гелиокс». Благодаря низкой растворимости в тканях организма, гелий способствует вытеснению азота из кровотока, что, в свою очередь, предотвращает развитие патологических состояний, ассоциированных с быстрой декомпрессией при подъёме с глубоководного пространства. Интеграция данной методики позволяет значительно повысить уровень безопасности при осуществлении погружений на глубину и увеличить допустимую продолжительность пребывания человека в условиях высокого гидростатического давления. Данный факт стал основанием для дальнейшего изучения и применения смеси в лечебных и профилактических целях.
В настоящее время гелий и кислород в виде подогретой газовой смеси открывают новые перспективы во всех частях медицины, позволяя не только предотвратить развитие гипоксии, но и улучшить физическое состояние организма без риска побочных эффектов.
Регуляция физиологических функций организма осуществляется посредством иерархически организованной системы, отличающейся высокой степенью сложности и многоуровневой структурой. Первый уровень регуляторных механизмов ограничен относительно самостоятельными локальными системами, представленными отдельными клеточными единицами. Клетка, находясь под контролем веществ, посредством которых осуществляется передача электрохимического импульса от нервной клетки через синаптическое пространство между нейронами (то есть нейромедиаторами), модифицирует собственные метаболические процессы в ответ на воздействие различных стимулов, что позволяет ей реагировать на внешние раздражители. После прекращения воздействия раздражающего фактора клетка обладает способностью к восстановлению исходных физиологических параметров. В случае невозможности коррекции клеточного гомеостаза на первом уровне регуляции происходит активация второго уровня регуляторной системы, характеризующегося более сложными механизмами поддержания постоянства внутренней среды организма.
Вегетативные нервные центры локализованы в спинном мозге и стволовых структурах. На данном уровне регуляции в пределах соответствующей физиологической системы реализуются простейшие рефлекторные ответы, обеспечивающие быструю адаптацию к изменениям внутренней и внешней среды. Эти реакции характеризуются локальностью и ограниченностью зоны своего влияния, что позволяет осуществлять высокоточную настройку функционирования отдельных органов и тканей без вовлечения всего организма в процесс приспособления к новым условиям.
На третьем уровне стратификации регуляторной системы осуществляется генерация оценочных параметров, позволяющих анализировать состояние как эндогенных, так и экзогенных факторов, воздействующих на организм. Параллельно происходит коррекция и адаптация функциональных режимов, характерных для нижестоящих уровней регуляции, а именно первого и второго, что обеспечивает поддержание гомеостатического баланса.
Данный процесс обеспечивается деятельностью высших отделов центральной нервной системы, включающих гипоталамус, лимбическую систему и кору больших полушарий головного мозга. Селективная временная интеграция различных органов и систем, а также механизмов их регуляции, реализуемая на третьем уровне, способствует достижению организмом состояния адаптации к изменяющимся условиям внешней и внутренней среды. Эта интеграция позволяет координировать функционирование отдельных физиологических систем и обеспечивать их слаженную работу для поддержания гомеостаза и оптимального приспособления организма к воздействию различных факторов.
Принципы обратной связи, функционирующие в совокупности с трёхуровневой архитектурой регуляторных процессов, занимают центральное положение в обеспечении гомеостатического равновесия. Указанные принципы основываются на способности к межклеточной коммуникации внутри тканевых структур, что создаёт основу для обмена сигнальными данными. Благодаря этим процессам становится возможным оперативное устранение дисбаланса между актуальным и целевым состоянием физиологических функций, обеспечивая их адаптацию к изменяющимся условиям. Таким образом, наличие механизмов обратной связи, основанных на внутритканевой межклеточной коммуникации, в совокупности с трёхуровневой регуляторной системой является фундаментальным условием для поддержания гомеостатического равновесия организма.
Восприятие клеткой раздражителя посредством рецепторов является фундаментальным принципом механизмов, ответственных за оксигенацию тканей. При воздействие эндогенных и экзогенных факторов в клеточных метаболических процессах активируются адаптационные изменения, целью которых является минимизация, предотвращение или компенсация вызванных отклонений от непосредственной физиологической нормы. Модуляция метаболизма в соответствии с энергетическими и пластическими потребностями клетки обеспечивается двумя антагонистическими системами: катехоламины – янтарная кислота – цАМФ – АТФ и ацетилхолин – кетоглутарат – цГМФ – ГТФ. Интенсивность метаболических процессов коррелирует с динамикой потребления кислорода. Уровень насыщения тканей кислородом обусловлен совокупностью факторов, таких как сократительная активность миокарда, парциальное давление кислорода в газовой смеси, которая используется при ингаляции, эффективность газообмена в лёгочной системе, особенности перфузии кровеносного русла в пределах конкретных тканевых структур, а также концентрация гемоглобина в системном кровотоке и его способность к связыванию молекулярного кислорода. При этом два последних параметра играют доминирующую роль в механизмах компенсации при развитии гипоксических состояний. Ключевая роль в транспорте кислорода принадлежит эритроцитам, которые выступают основным звеном в обеспечении тканей необходимым количеством кислорода.
Адекватное насыщение клеточных структур кислородом, непосредственно оксигенация, определяется уровнем его парциального давления в капиллярной сети, которое должно достигать значений, обеспечивающих эффективную диффузию в окружающие ткани. В артериальной крови парциальное давление кислорода остаётся относительно постоянным в тканях определённой морфологической структуры, тогда как в венозной крови его концентрация варьирует в зависимости от степени утилизации кислорода конкретной тканью. При снижении интенсивности метаболических процессов потребность в увеличении доставки кислорода отсутствует. Однако при активации метаболизма ускоренное потребление кислорода клеткой превышает скорость его поступления, что приводит к развитию нарушения способности клеток поглощать кислород как при нормальной доставке к клетке, так и в связи с уменьшением эффективности окисления в результате разобщения окислительного процесса и фосфорилирования, то есть тканевой гипоксии, при которой механизмы клеточной адаптации становятся недостаточными. Продукты анаэробного метаболизма стимулируют хеморецепторы каротидных и аортальных телец, что рефлекторно активирует дыхательный и вазомоторный центры.
Инициализация функциональной возможности аппарата внешнего дыхания, то есть респираторного резерва и резерва кровотока, является фактором для включения второго уровня системы регуляции. Адекватное соотношение электролитов плазмы прямо пропорционально реагирует на органы кроветворения, периферической крови и органов кро-веразрушения, таких как красный костный мозг, сосудах, селезёнке и печени и соответственно на отклонения в функционировании перечисленных органов. Концентрация эритроцитов в системном кровотоке определяется сбалансированностью процессов эритропоэза и деструкции клеток эритрона. В физиологических условиях между этими процессами устанавливается динамическое равновесие, что обеспечивает поддержание стабильного уровня эритроцитов в циркулирующей крови. Соотношение между обеспечением тканей кислородом и их метаболическими запросами выступает в качестве основного регуляторного механизма, определяющего интенсивность процессов эритропоэза. На данном уровне регуляции функциональная адаптация дыхательной и сердечно-сосудистой систем позволяет компенсировать прогрессирование необходимой потребности клеточных структур в кислороде. Данный факт свидетельствует о том, что увеличение количества эритроцитов, принимающих участие в циркуляции крови, не представляется существенно необходимым для надежного функционирования организма. Кратковременное и умеренное гипоксическое воздействие стимулирует активацию систем, ответственных за синтез эритропоэтина (ЭПО) в почечной ткани, что сопровождается секрецией незначительного количества гормона. Почечные структуры выполняют функцию сенсора кислородного баланса благодаря наличию высокоорганизованной системы кровоснабжения и уникальной конфигурации микроциркуляторного русла [7–9].
Один из важных механизмов в физиологии человека является эффект Бора. Данный эффект заключается в следующем: при снижении уровня СО 2 в крови происходит смещение кривой диссоциации оксигемоглобина влево. Насыщение гемоглобина кислородом становится выше, сродство увеличивается. Кислород и СО 2 конкурируют за связь с гемоглобином. Чем меньше СО 2 , тем больше шанс связаться О 2 с гемоглобином. Также это происходдит при алкалозе, повышении рН, понижении температуры [10].
Также в исследовании группы специалистов МО-НИИАГ было выявлено, что происходит снижение сосудистого сопротивления, увеличение объёмного кровотока головного мозга в среднемозговой артерии.
Циркуляция крови, являясь одной из наиболее значимых физиологических функций организма, обеспечивает транспортировку кислорода от лёгочной системы к клеткам тканей, а также элиминацию углекислого газа в противоположном направлении. Необходимо отметить, что утилизация кислорода тканевыми структурами может варьировать в широком диапазоне, что обусловлено переходом от состояния релаксации к физическим нагрузкам и наоборот. Для увеличения потенциала крови в аспекте переноса кислорода и углекислого газа между лёгкими и тканями, гемоциркуляторная система должна обладать существенными резервными возможностями. Данный факт объясняется значительными колебаниями в потреблении кислорода клетками в зависимости от функционального состояния организма [11].
Транспорт кислорода. При температуре 37 °С растворимость О 2 в жидкости составляет 0,225 мл·л–1·кПа–1 (0,03 мл/л/мм рт. ст.). В условиях нормального парциального давления кислорода в альвеолярном воздухе, т.е. 13,3 кПа или 100 мм рт. ст., 1 л плазмы крови может переносить только 3 мл О 2 , что недостаточно для жизнедеятельности организма в целом.
Молекулы гемоглобина, локализованные в эритроцитах, осуществляют транспортировку кислорода от лёгочной системы к тканевым структурам организма. В процессе эволюции биологических систем проблема обеспечения эффективного транспорта кислорода была разрешена посредством возникновения специализированных клеток — эритроцитов, содержащих гемоглобин, обладающий способностью к обратимой связи с молекулами кислорода. Этот адаптационный механизм позволил достичь оптимального уровня насыщения тканей и органов кислородом, что стало ключевым фактором поддержания жизненных функций и обеспечения адаптации к динамическим изменениям окружающей среды. В процессе филогенетического развития живых организмов сформировалась высокоэффективная система транспорта кислорода, ключевыми элементами которой выступают эритроциты — высокоспециализированные клеточные структуры крови, и гемоглобин, обладающий уникальной способностью к обратимой связи с молекулами кислорода. Данный механизм, основанный на химическом связывании кислорода, демонстрирует значительно более высокую эффективность по сравнению с транспортом кислорода в физически растворённом состоянии, что обеспечивает оптимальное функционирование метаболических процессов в тканях. Человеческий организм в состоянии покоя потребляет в среднем в минуту примерно 250 мл кислорода. Для обеспечения тканей 250 мл кислорода в минуту сердечной мышце пришлось бы перекачивать колоссальные объёмы крови за отведённый промежуток времени, даже если бы кислород транспортировался исключительно в физически растворённой форме.
Кислород, поступающий из части выдыхаемого воздуха, который достиг полости перфузируемых альвеол, и вырабатываемый лёгочный сурфактант, отвечающий за регулирование поверхности натяжения во время дыхания, то есть альвеолярного воздуха, связывается с молекулой гемоглобина, образуя соединение под названием оксигемоглобин. Число молекул гемоглобина и присущая им ограниченность количества связываемого кислорода, находящихся в эритроцитах, является характерной особенностью взаимодействия кислорода с гемоглобином. В тканевых структурах происходит высвобождение необходимого количества кислорода из данного соединения. Кривая, отражающая зависимость между парциальным давлением кислорода и количеством кислорода, переносимого кровью, известна как кривая насыщения или диссоциации оксигемоглобина. Данная S-образная форма зависимости является результатом взаимодействия четырёх активных центров, присутствующих в каждой молекуле гемоглобина и обладающих способностью связывать молекулы кислорода. Таким образом, наличие четырёх активных центров в структуре гемоглобина обуславливает формирование характерной нелинейной зависимости между парциальным давлением кислорода и объёмом кислорода, транспортируемого кровью, что находит свое отражение в виде S-образной кривой насыщения оксигемоглобина [12-15].
При парциальном давлении кислорода 10 мм рт. ст. насыщение гемоглобина кислородом составляет примерно 10%, а при 30 мм рт. ст. — 50—60%. При дальнейшем увеличении парциального давления кислорода от 40 до 60 мм рт. ст. происходит уменьшение крутизны кривой диссоциации оксигемоглобина, и процент его насыщения кислородом возрастает в диапазоне от 70—75% до 90% соответственно. Затем кривая диссоциации оксигемоглобина начинает занимать практически горизонтальное положение, поскольку увеличение парциального давления кислорода с 60 до 80 мм рт. ст. вызывает прирост насыщения гемоглобина кислородом на 6%. В диапазоне от 80 до 100 мм рт. ст. процент образования оксигемоглобина составляет порядка 2. Степень насыщения гемоглобина кислородом происходит непосредственно под влиянием напряжения кислорода в артериальной крови, то есть парциального давления кислорода (PO2), и характеризует молекулярное сродство имеющегося соединения к кислороду. Анализируя зависимость насыщения гемоглобина кислородом от парциального давления кислорода, можно констатировать, что в диапазоне PO2 от 80 до 100 мм рт. ст. наблюдается незначительное увеличение процентного содержания оксигемоглобина [16]. Данная физиологическая особенность человеческого организма обуславливает возможность его пребывания на высотах, не превышающих 2000 метров над уровнем моря, без существенного риска снижения показателя насыщения артериальной крови кислородом, именуемого оксигенацией. Значительная крутизна кривой насыщения гемоглобина кислородом в диапазоне PO2 от 20 до 40 мм рт. ст. способствует эффективной диффузии существенного количества кислорода из крови в ткани организма при наличии градиента парци- ального давления кислорода между кровью и клетками тканей, который должен составлять не менее 20 мм рт. ст. Дальнейшее увеличение PO2 приводит к трансформации кривой диссоциации оксигемоглобина в горизонтальную линию, что соответствует достижению предельного значения насыщения гемоглобина кислородом, составляющего 100% [17-20].
Кривая диссоциации оксигемоглобина. Пределы колебания кривой при РСО 2 = 40 мм рт. ст. (артериальная кровь) и РСО 2 = 46 мм рт. ст. (венозная кровь) показывают изменение сродства гемоглобина к кислороду. Данное состояние именуется эффектом Холдена - снижение сродства гемоглобина к кислороду и стимуляция к более интенсивному освобождению его из эритроцитов в ткани. Суммарное содержание кислорода в организме определяется его количеством, пребывающим в форме комплексных соединений с ионами двухвалентного железа (Fe2+), входящими в состав гемсодержащих белков - гемоглобина, локализованного в эритроцитах, и миоглобина, присутствующего в клетках мышечной ткани. Таким образом, общие запасы кислорода в организме зависят от его концентрации в связанном состоянии с данными органическими молекулами. Один грамм гемоглобина связывает 1,34 мл О 2 . Поэтому в норме при концентрации гемоглобина 150 г/л каждые 100 мл крови могут переносить 20,0 мл О 2 . Кислородной ёмкостью гемоглобина называется максимальное количество кислорода, которое способно связаться с гемоглобином эритроцитов крови при условии полного насыщения указанного белка. Другим важным показателем, отражающим дыхательную функцию крови, является кислородная ёмкость крови, представляющая собой суммарное содержание кислорода, как связанного с гемоглобином, так и находящегося в физически растворённом состоянии в плазме крови. Таким образом, кислородная ёмкость крови характеризует реальное количество кислорода, транспортируемое кровью. В физиологических условиях насыщение артериальной крови кислородом достигает 97%, что соответствует содержанию приблизительно 19,4 мл кислорода в 100 мл артериальной крови [21-25].
Сахарный диабет (СД) идентифицирован как неинфекционная эпидемия глобального масштаба, имеющая высокую социальную значимость и находящаяся под мониторингом национальных систем здравоохранения по всему миру, а также Организации Объединенных Наций (ООН) [26]. Сахарный диабет представляет собой одну из наиболее значимых проблем современного здравоохранения, требующую применения междисциплинарного подхода и международного сотрудничества с целью осуществления эффективных мер контроля и профилактики данного заболевания [27-29]. Характери- зуясь неуклонным ростом распространённости, СД относится к группе патологий, представляющих серьёзную угрозу для общественного здоровья ввиду высокой частоты развития инвалидизации в раннем периоде течения заболевания и значительной смертности, обусловленной сосудистыми осложнениями. Согласно данным Международной Федерации Диабета (International Diabetes
Federation, IDF), количество пациентов с СД в возрасте 20–79 лет в мире достигло 537 млн (IDF atlas 2021), что опередило ранее прогнозируемые темпы прироста на 10–12 лет, а к 2045 г. ожидается практически двукратное увеличение – до 783 млн человек (на 46%). В Российской Федерации (РФ), так же как и в других странах мира, продолжается рост распространённости СД — с 2000 г. численность пациентов с СД увеличилась более чем в 2 раза. По последним данным Росстата [30], количество пациентов с СД в РФ на период окончания 2021 г. составило 5 млн 168,8 тыс. человек (табл. 1, рис. 1–5).
Таблица 1. Общая численность пациентов с сахарным диабетом в Российской Федерации на 01.01.2023 г.
Table 1. Total number of patients with diabetes mellitus in the Russian Federation as of 01.01.2023
|
Категория |
СД1 |
СД2 |
Другие типы |
|
Дети |
35 019 |
1 049 |
651 |
|
Подростки |
13 012 |
246 |
214 |
|
Взрослые |
229 061 |
4 580 695 |
102 815 |
|
Всего |
277 092 |
4 581 990 |
103 680 |
|
Всего на 01.01.2023 г. |
1 962 762 |
Одно из осложнений сахарного диабета – синдром диабетической стопы (СДС) представляет собой серьёзную проблему для пациентов с сахарным диабетом, так как он может привести к значительным физическим и социальным ограничениям, а также к снижению качества жизни. Лечение СДС часто оказывается сложным и требует мультидисци-плинарного подхода, включающего как консервативные, так и хирургические методы [31].
Согласно данным, многие пациенты, страдающие диабетической стопой, лишаются конечности, и это событие значительно влияет на их продолжительность жизни и общее состояние здоровья. Высокий уровень летальности в первые пять лет после ампутации подчеркивает необходимость более раннего вмешательства и применения эффективных методов лечения. Так как основной причиной развития СДС является неврологическая и сосудистая патология, важно фокусироваться на профилактике и раннем выявлении осложнений [32].
Сахарный диабет имеет перечень важных факторов риска, отслеживание которых, повсеместно рекомендуется врачами. В этот перечень входит:
наследственность, ожирение (сахар в крови, повышаясь, имеет свойство повышать нормальную кон-цетрацию инсулина, что влечёт за собой избыточное содержание жировой ткани), малоподвижный образ жизни, прогрессирующий атеросклероз (особенно осложнённый артериальной гипертонией и ишемической болезнью сердца), угнетающие синтез инсулина токсические компоненты алкоголя или табачных изделий, а также бесконтрольный приём гормональных или мочегонных средств может послужить причиной для манифестации СД [33]. Однако стоит уделить внимание социальнопсихологическим факторам, которые так же могут послужить причиной возникновения СД. К социально-психологическим факторам относится: острый и хронический стресс, депрессия, повышенная тревожность или фрустрация. Подобные проблемы значительно могут снизить качество жизни людей, столкнувшихся с СД, в связи с возможным искажением ситуации и перспективы касаемо данного заболевания. Больным СД настоятельно рекомендуется помощь врача-психотерапевта с целью скорректировать нежелательное поведение и эмоциональные реакции. Запущенное состояние СД может привести к определённым последствиям, таким как, например, синдром диабетической стопы. Ведущие факторы риска синдрома диабетической стопы – это повреждение одного или нескольких периферических нервов, периферический атеросклероз сосудов нижних конечностей, деформация стоп, длительное течение установленного сахарного диабета, курение, высокий уровень гликозилированного гемоглобина, несоблюдение мер в подборе правильной обуви, пожилой возраст [34].
Основополагающей стратегией в лечение СДС и возможных гнойно-деструктивных поражений стопы у больных СД является мультидисциплинарный подход. Тактика основывается на объективном состояние пациента, характеристиках осложнений и прогнозе течения заболевания [35]. Лечение может быть хирургическим и консервативным. Консервативная терапия применяется для следующих целей: купирование явлений острого воспаления, улучшение перфузии мягких тканей, разгрузка пораженной конечности и в компенсации сахарного диабета, в коррекции его проявлений и вероятных последствий [36]. Для лечения проявлений ишемического поражения нередко используют вазоактивные препараты (такие как трентал, солкосерил, реопо-лиглюкин), однако по данным исследований, положительного эффекта удалось добиться меньше чем у половины испытуемых пациентов, но данные препараты рекомендуется использовать при хронической артериальной недостаточности [37, 38].
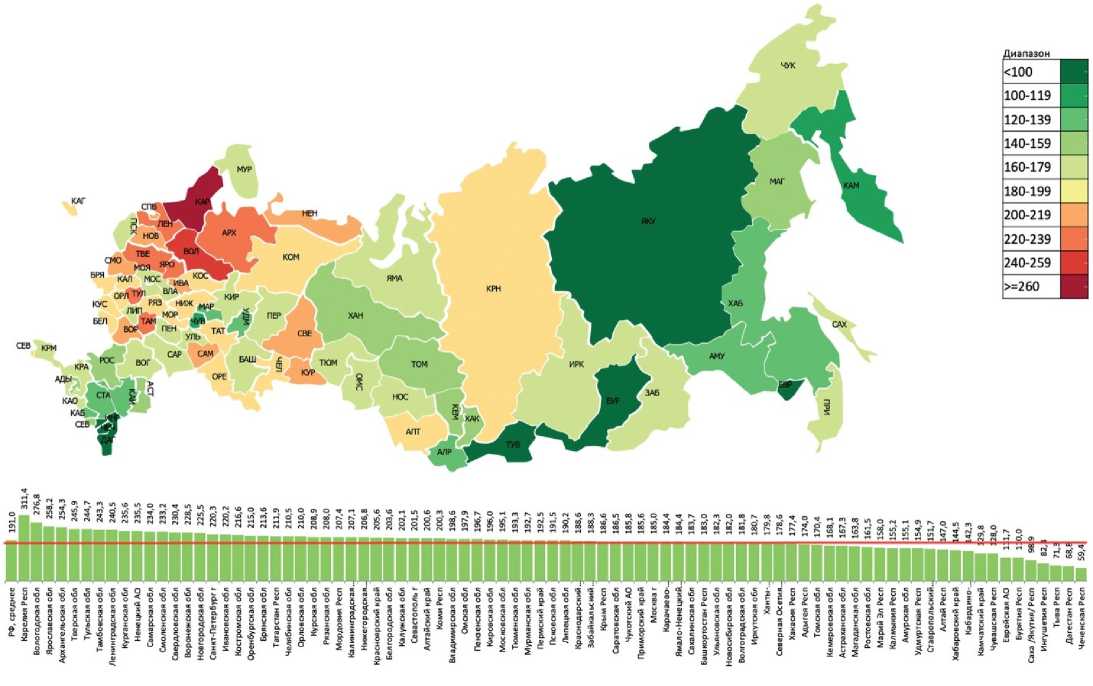
Рисунок 1. Распространённость сахарного диабета 1 типа на 100 тыс. населения, 85 регионов Российской Федерации (на 01.01.2023 г.)
Figure 1. Prevalence of type 1 diabetes per 100 thousand population, 85 regions of the Russian Federation (as of 01.01.2023)
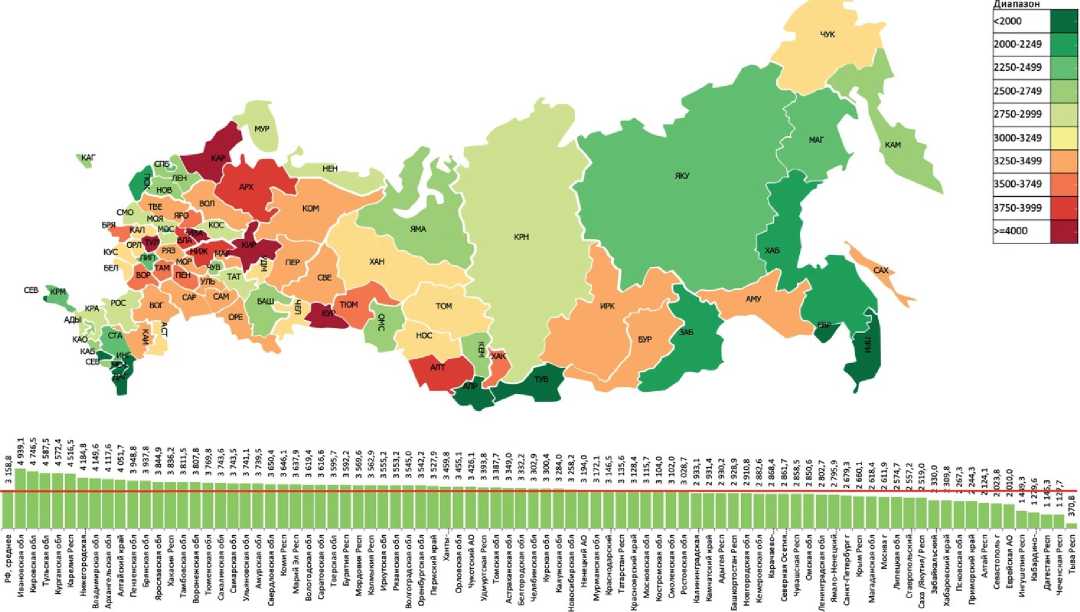
Рисунок 2. Распространённость сахарного диабета 2 типа на 100 тыс. населения, 85 регионов Российской Федерации (на 01.01.2023 г.)
Figure 2. Prevalence of type 2 diabetes per 100 thousand population, 85 regions of the Russian Federation (as of 01.01.2023)
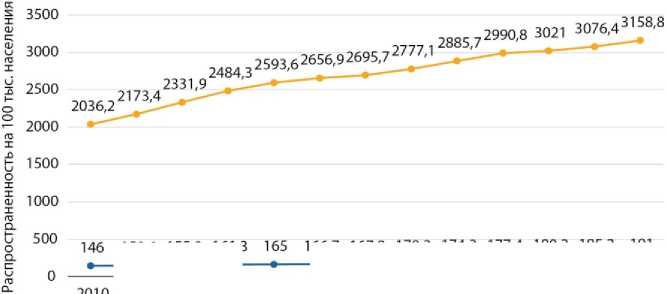
166,7 167,8 170,3 174,3 177,4 180,3 185,2 191
150,6 155,9 161,3
СД1
СД2
2011 2012 2013 2014 2015 2016 2017 2018 2019 2020 2021 2022 Год
Рисунок 3. Динамика распространённости пациентов с сахарным диабетом 1 и 2 типов, значение показателя на 100 тысяч населения, 85 регионов Российской Федерации, 2010–2022 гг.
Figure 3. Dynamics of prevalence of patients with diabetes mellitus types 1 and 2, value of the indicator per 100 thousand population, 85 regions of the Russian Federation, 2010–2022.
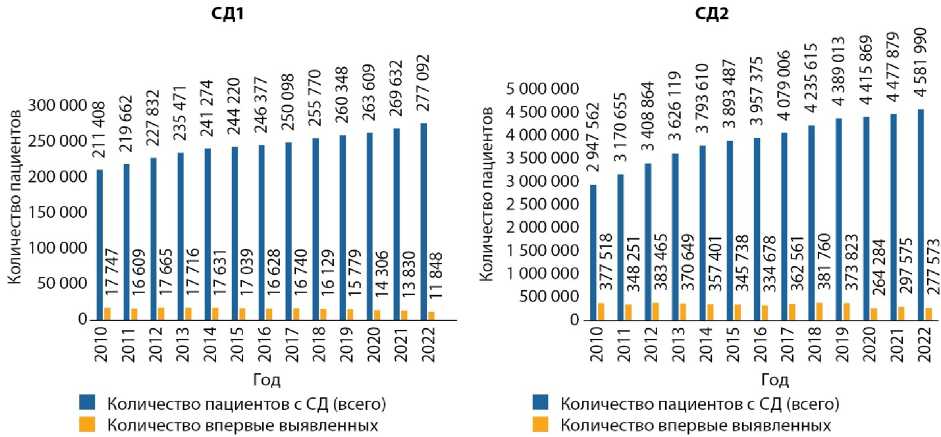
Рисунок 4. Динамика количества пациентов с сахарным диабетом 1 и 2 типа в Российской Федерации, в абсолютных значениях, 2010–2022 гг. Figure 4. Dynamics of the number of patients with diabetes mellitus types 1 and 2 in the Russian Federation, in absolute values, 2010–2022
Кроме местного лечения язвенных дефектов или ран, проводится профилактика и подавление инфекционного поражения, стимулирование репаративных процессов. Но наиболее важным для прогрессирования заживления является непосредственная разгрузка стопы, которая позволяет добиться практически полного заживления раны, а также применение ортезов, иммобилизационных повязок и специальной обуви, что является необходимым компонентов комплексной терапии [39].
Мониторинг частоты развития хронических осложнений сахарного диабета представляет собой объективный инструмент для оценки качества и динамики развития организации медицинской помощи пациентам с данным заболеванием. В 1989 г. была утверждена Сент-Винсентская декларация, получившая поддержку правительств европейских государств и определившая основные векторы организации помощи пациентам с СД. Одной из приоритетных задач, поставленных в рамках данной декларации, являлось снижение частоты развития сосудистых осложнений, в частности, ампутаций нижних конечностей у пациентов с СД, на 50%. Таким образом, Сент-Винсентская декларация заложила фундамент для оптимизации стратегий профилактики и лечения СД, а также его осложнений с целью улучшения качества жизни пациентов и снижения регулярности данного заболевания для системы здравоохранения разных стран. Тем не менее, до настоящего времени достоверная информация, позволяющая оценить прогресс в достижении данной цели, носит ограниченный характер.
СД1
СД2
Острые сердечно-сосудистые
Хрон. сердечно-сосудистая недостаточность
Сахарный диабет
Причина смерти не установлена
Коронавирус/осложнения коронавируса
Нарушение мозгового кровообращения
Заболевания печени, поджелудочной железы, органов ЖКТ
Хроническая почечная недостаточность
Онкология
Заболевания легких, органов дыхательной системы
Инфаркт миокарда
Алкоголь, др. отравления
Инфекции, сепсис
Травмы
Диабетическая кома
Старость и дегенеративные заболевания
Суицид
Гангрена
Гипогликемическая кома
Хрон. сердечно-сосудистая недостаточность
Острые сердечно-сосудистые
Онкология
Нарушение мозгового кровообращения
Коронавирус/осложнения коронавируса
Причина смерти не установлена
Сахарный диа бет
Старость и дегенеративные заболевания
Инфаркт миокарда
Заболевания легких, органов дыхательной системы
Заболевания печени, поджелудочной железы, органов ЖКТ
Хроническая почечная недостаточность
Инфекции, сепсис
Травмы
Гангрена
Алкоголь, др. отравления
Суицид
Диабетическая кома
Гипогликемическая кома
1,0%
0,8%
0,4%
0,3%
0,2%
0,1%
0,0%
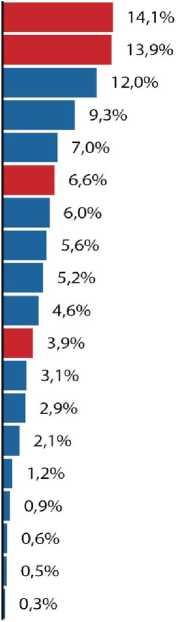
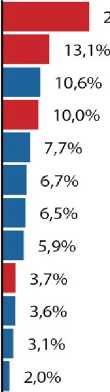
Рисунок 5. Структура смертности пациентов с сахарным диабетом 1 и 2 типа в Российской Федерации (по непосредственной причине смерти) по данным Федерального регистра сахарного диабета, 2022 г. Сердечно-сосудистая патология отмечена красным цветом, другие причины — синим
Figure 5. Mortality structure of patients with diabetes mellitus types 1 and 2 in the Russian Federation (by immediate cause of death) according to the Federal Register of Diabetes Mellitus, 2022. Cardiovascular pathology is marked in red, other causes are in blue
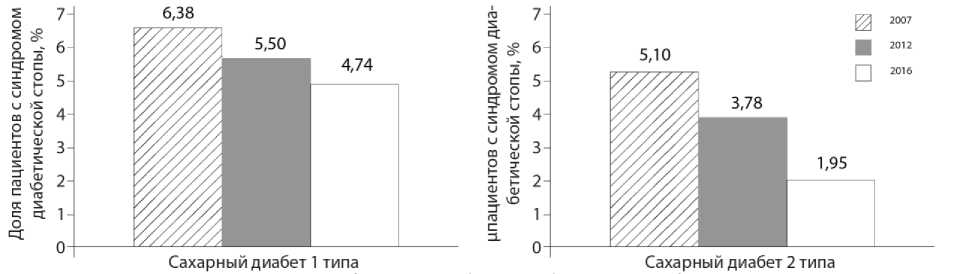
Рисунок 6. Распространённость синдрома диабетической стопы (% пациентов) при сахарном диабете 1 и 2 типа в 2013–2016 гг. по данным Федерального регистра сахарного диабета (81 регион Российской Федерации)
Figure 6. Prevalence of diabetic foot syndrome (% of patients) in type 1 and type 2 diabetes in 2013–2016 according to the Federal Diabetes
Registry (81 regions of the Russian Federation)
В 2016 г. частота регистрации СДС (все стадии) в РФ составила 4,7% при СД1 (473,6/10 тыс. взрослого населения) и 1,9% при СД2 (194,8/10 тыс. взрослого населения). Распространённость СДС в РФ в динамике 2013–2016 гг. имеет тенденцию к некоторому снижению: при СД1 – с 506,3 до 473,6/10 тыс. взрослых больных, при СД2 – с 214,60 до 194,8/10 тыс. взрослых больных (рис. 6).
Углубленный анализ течения заболевания, последующего прогрессирования и результатов лечения пациентов с сахарным диабетом и синдромом диабетической стопы зачастую остаётся вне обозрения большинства исследований, посвящённых данной проблеме, которые преимущественно фокусируются на вопросах профилактики ампутаций нижних конечностей. Тем не менее, немногочис- ленные исследования, затрагивающие ранее изложенные аспекты, указывают на более неблагоприятный прогноз выживаемости пациентов с СДС, особенно перенёсших ампутации нижних конечностей, в сравнении с пациентами, имеющими заболеваниями онкологического характера. Соответственно, обзор научной литературы, посвящённый проблеме СДС, демонстрирует недостаточную осведомленность в вопросе долгосрочной выживаемости и долгосрочных результатов лечения данной категории пациентов, несмотря на имеющиеся данные о крайне неблагоприятном прогнозе [40].
Данный факт подчёркивает необходимость более детального изучения факторов, оказывающих влияние на отдалённый прогноз и выживаемость пациентов с СДС, а также разработки эффективных превентивных мер и терапевтических подходов к осложнениям СД. Это подчеркивает потребность в расширении спектра научных исследований в области СДС с целью углубленного анализа аспектов, определяющих долгосрочные исходы заболевания и выживаемость пациентов. Таким образом, дальнейшее развитие исследований в данном направлении представляется крайне актуальным и необходимым для улучшения прогноза и качества жизни пациентов с СДС [41].
Следует отметить, что прогноз жизни зависит от уровня ампутаций: средний срок выживания в группе пациентов с СД с малыми ампутациями составил 51 месяцац, что оказалось достоверно больше, чем в группе пациентов с высокими ампутациями – 40 месяцев (p = 0,016). С экономической точки зрения, СДС представляет одну из наиболее затратных патологий: по данным Международной федерации диабета (IDF), лечение больных с СДС в 5 раз повышает стоимость расходов на лечение.
Синдром диабетической стопы представляет собой серьёзное осложнение сахарного диабета, ко- торое несёт непосредственную угрозу ампутаций нижних конечностей, приводя к потере трудоспособности, снижению качества и сокращению продолжительности жизни пациентов, а также повышению социально-экономической тяжести, связанной с лечением данного заболевания. В связи с этим, изучение эпидемиологических характеристик СДС приобретает особую актуальность и значимость. В данной работе впервые представлены данные о частоте развития СДС и ампутаций нижних конечностей, стратифицированные по уровню и форме поражения, полученные на основании анализа Федерального регистра больных СД (ФРСД) Российской Федерации. Результаты данного исследования вносят существенный вклад в понимание масштабов проблемы СДС и могут служить основой для разработки эффективных стратегий профилактики и лечения данного осложнения СД, направленных на снижение частоты ампутаций, улучшение качества жизни пациентов и оптимизацию использования ресурсов здравоохранения.
По данным по уровню ампутаций у взрослых пациентов с СД1 и СД2 в динамике 2013–2016 гг. отмечалась положительная динамика уменьшения доли высоких ампутаций при обоих типах СД: при СД1 – с 43,6% в 2013 г. до 37,0% в 2016 г., при СД2 – с 52,2% в 2013 г. до 45,5% в 2016 г. за счёт перераспределения соотношения в пользу малых хирургических вмешательств. Доля минимальных ампутаций в пределах одного пальца при СД1 возросла с 4,0% в 2013 г. до 10,0% в 2016 г., при СД2 – с 2,8% до 9,1% соответственно (рис. 7). При этом соотношение ампутаций в пределах стопы и на уровне голени оставалось стабильным. Эти данные показывают улучшение качества оказания помощи пациентам с СДС с выполнением органосохраняющих операций на ранних стадиях развития поражения нижних конечностей [42].
о
о
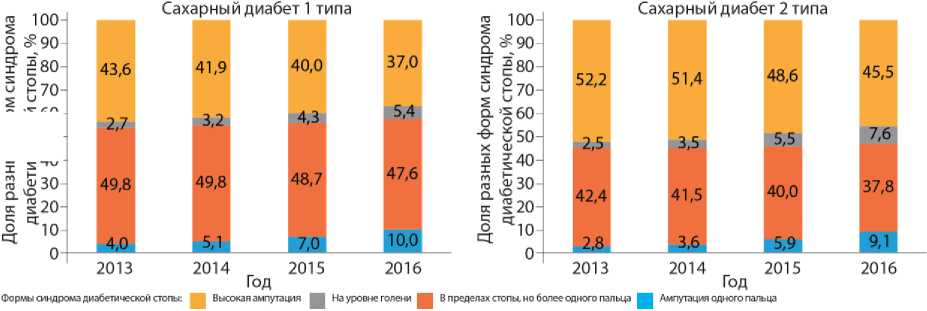
Рисунок 7. Распределение по уровню ампутаций (% пациентов) у взрослых больных с сахарным диабетом 1 и 2 типа в 2013–2016 гг. по данным Федерального регистра сахарного диабета, 81 регион Российской Федерации
Figure 7. Distribution by amputation rate (% of patients) in adult patients with type 1 and type 2 diabetes in 2013–2016 according to the Federal Diabetes Registry, 81 regions of the Russian Federation
5 50
Отметим, что применение ингаляций подогретой кислородно-гелиевой смеси (КГС) показывает обнадеживающие результаты в других областях медицины, что может открыть новые горизонты в лечении пациентов с СДС. Несмотря на то, что традиционно эта методика использовалась в пульмонологии, её возможное влияние на сосудистую систему требует дальнейших исследований.
В целом, подход к лечению синдрома диабетической стопы должен быть комплексным и многогранным, включая как традиционные методы, так и новые технологии, чтобы повысить эффективность терапии и качество жизни пациентов.
На момент написания данной работы в известных Российских и зарубежных литературных источниках найдено скромное количество работ и статей, которые указывали бы на лечение пула пациентов с сахарным диабетом, диабетической стопой, ангиопатиями, дистальными ишемиями, язвенными поражениями нижних конечностей с использованием кислородно-гелиевой смеси. В 99% случаев описание статьи связано с бронхо-лёгочными заболеваниями, ассоциированными с COVID-19, бронхиальной астмой и т.д. [43].
Экспериментальные решения были приняты некоторым отечественными авторами при поражениях артерий нижних конечностей, патологий сердечно-сосудистой системы.
Погорелова Е.А. в ходе исследования использовала ксеноно-кислородно-гелиевую смесь «Ксен ОксиГелиум-20», состоящую из 25% кислорода, 55% гелия и 20% ксенона.
Было установлено, что использование смеси «КсенОксиГелиум-20» способствовало коррекции гипоксии за счёт изменения плотности и растворимости газовой смеси, повышению транспорта кислорода через альвеолярную мембрану, доставке кислорода к тканям. По окончании курса лечения отмечена достоверная положительная динамика нарушенных показателей общей скорости кровотока [44].
Антонов А.А., Буров Н.Е. провели исследования с использованием гелиево-кислородной подогретой газовой смеси и пришли к выводу, что у амбулаторных пациентов с оперированной коронарной недостаточностью сеансы ингаляционного воздействия подогретой КГС, содержащей 77 об.% гелия и 23 об.% кислорода (4 раза по 10 минут с перерывом 10 минут), ведут к достоверному улучшению ПИПСС, КДИ, DO2I и ИБ. Положительные изменения ПИПСС и ИБ достоверно сохраняются до 48 часов после последнего 10-минутного сеанса ингаляционного воздействия КГС. Положительные изменения КДИ и DO2I достоверно сохраняются до 24 часов после последнего 10-минутного сеанса ингаляции КГС, что даёт основы для дальнейшего перспективного применения КГС у больных с сахарным диабетом, осложнённым трофическими нарушениями нижних конечностей.
Обсуждение
Подогретая кислородно-гелиевая смесь обладает множеством преимуществ в лечении различных заболеваний. Механизм её действия базируется на нескольких ключевых аспектах, включая снижение аэродинамического сопротивления, улучшение газообмена и снижение нагрузки на дыхательные мышцы. Высокая диффузионная способность гелия позволяет эффективнее выводить углекислый газ из организма. Применение данной смеси охватывает широкий спектр патологий, таких как обструктивные заболевания, острый респираторный дистресс-синдром, бронхиальная астма, хроническая обструктивная болезнь лёгких, различные пневмонии и заболевания, связанные с COVID-19, атеросклеротическое поражение артерий нижних конечностей. Особый интерес представляет использование смеси в условиях после экстубации, когда необходимо восстановить дыхательную функцию и снизить риск осложнений. Одним из значительных преимуществ этого метода является его безопасность. При соблюдении правильных концентраций компоненты смеси не обладают токсичными или канцерогенными свойствами, благодаря чему метод может быть применим для различных категорий пациентов, включая тех, кто страдает от коморбидных состояний. Кроме того, влияние подогретой кислородно-гелиевой смеси на психоэмоциональный статус и когнитивные функции пациентов подчёркивает её многогранное положительное действие [45]. Это актуально для коморбидных пациентов и особенно важно для пациентов с синдромом диабетической стопы, длительно незаживающими язвенным поражениями нижних конечностей. На данный момент исследование данной методики является перспективным направлением. Хотя количество научных работ по этой теме ограничено, но уже имеющиеся данные основательно поддерживают применение подогретой кислородно-гелиевой смеси как ценного дополнения к классическим методам лечения. Если дальнейшие исследования подтвердят её эффективность, она может занять важное место в современном арсенале комплексного лечения.
Выводы
Подогретая кислородно-гелиевая смесь имеет высокую перспективу для активного применения в лечении дистальной ишемии нижних конечностей. Гелий обладает уникальными физическими свойствами, такими как низкая плотность и высокая теплопроводность, что делает его идеальным компонентом для улучшения газообмена. Подогрев смеси позволяет ещё больше повысить эффективность ле- чения, обеспечивая лучшее проникновение кислорода в ткани и улучшая выведение углекислого газа.
Однако стоит отметить, что для успешного внедрения данного метода в клиническую практику необходимы дополнительные исследования. Важно разработать протоколы применения подогретой кислородно-гелиевой смеси, определить оптималь- ные дозировки и режимы лечения, а также установить критерии оценки эффективности терапии. Это позволит медицинскому сообществу уверенно использовать этот метод в повседневной практике и улучшить результаты лечения пациентов с ишемией нижних конечностей.


