Флуориметрическое определение серебра (I) и цинка (II) в виде комплексов с органическими реагентами
Автор: Беляева Е.Н., Окина Е.В., Ускова Е.Н.
Журнал: Огарёв-online @ogarev-online
Статья в выпуске: 19 т.4, 2016 года.
Бесплатный доступ
В настоящее время широко исследуются производные имидазола и акридина, что связано с высокой избирательностью и эффективностью при количественном определении элементов в результате комплексообразования. Изучена возможность применения новых органических реагентов для флуориметрического определения микроколичеств серебра и цинка в различных объектах.
4-дибром-4, 5-дифенил-2(2-гидроксифенол)имидазол, 9-метилакридин, серебро (i), флуориметрический метод, цинк (ii)
Короткий адрес: https://sciup.org/147249190
IDR: 147249190 | УДК: 543.426:543.544-414.7
Текст научной статьи Флуориметрическое определение серебра (I) и цинка (II) в виде комплексов с органическими реагентами
Для определения микроколичеств металлов актуальна проблема получения и исследования новых комплексообразователей и разработки на их основе новых методик анализа. В настоящее время исследуется возможность применения производных имидазола и акридина, что связано с высокой избирательностью и эффективностью их использования в качестве активных комплексообразующих агентов при количественном спектроскопическом определении ионов металлов. Производные имидазола широко используются как органические аналитические реагенты благодаря своим комплексообразующим свойствам, которые обусловлены существованием свободной электронной пары у гетероциклического атома азота, а наличие гидроксильной группы фенильного радикала облегчает образование комплексов. Производные имидазола, акридина и их комплексы с ионами металлов способны к флуоресценции, что может быть использовано для количественного определения [1; 2].
В качестве комплексообразующих реагентов использовали органические вещества, синтезированные на кафедре органической химии Мордовского государственного университета имени Н. П. Огарёва:
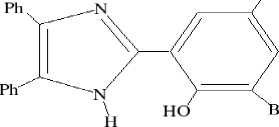
4,5-дифенил-2(2-гидроксифенол)имидазол ( Im )
2,4-дибром-4,5-дифенил-2(2-гидроксифенол)имидазол ( Br-Im )
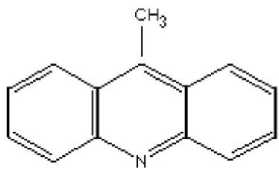
9-метилакридин ( Acr )
Элементный состав и брутто-формула синтезированных реагентов установлены с помощью CHNSCl-анализатора Vario Micro Cube (Elementar). Измерение оптической плотности растворов и сканирование спектров поглощения комплексов металлов с органическими реагентами было проведено на спектрофотометре UV-1800 (SHIMADZU) в диапазоне длин волн от 200 до 600 нм. Величину рН растворов контролировали с помощью универсального иономера «Анион-4154» с индикаторным стеклянным электродом ЭСЛ-003. Измерение сигнала атомной абсорбции проводилось на атомно-абсорбционном спектрофотометре АА-7000 (SHIMADZU) в непламенном режиме атомизации.
Для установления возможности комплексообразования и определения состава комплексов ионов Ag (I), Zn(II) с изученными реагентами было произведено исследование спектров поглощения растворов (С(Ме) = 10-5 моль/л) с варьируемыми соотношениями «металл-реагент». Спектры поглощения комплексов серебра с изученными реагентами представляют собой широкую полосу с одним максимумом светопоглощения при λ = 342 нм (Ag-Im), λ = 340 нм (Ag-Br-Im), λ = 323 нм (Ag-Acr). Сравнение спектров чистых реагентов и спектров их комплексов с ионами изученных металлов показало, что контрастность аналитической реакции составила 10‒25 нм. Зависимость оптической плотности раствора с оптимальным соотношением металл-реагент от рН показывает, что комплекс Ag-Acr образуется в слабощелочной среде при рН 8, а комплексы ионов серебра с замещенными имидазолами в кислой среде при рН 5.
Аналогичным образом была исследована возможность образования комплекса Zn (II) с Im , в результате чего было установлено, что образование активно поглощающего комплекса наблюдается в более кислой среде при рН 3,0 при молярных соотношениях Zn- Im 1:2. При изучении комплексообразования цинка с 2,4-дибром-4,5-дифенил-2(2-гидроксифенол)имидазолом и 9-метилакридином установлено, что ионы цинка с данными реагентами устойчивых комплексных соединений не образуют.
Наличие в исследуемых органических реагентах сопряжения бензольных колец с гидроксо-группами, а также гетероциклического азота позволяет предположить их способность к флуоресценции. В связи с этим изучены спектры поглощения и эмиссии флуоресценции в интервале длин волн 220‒800 нм, а также оптимальные условия образования флуоресцирующих комплексов.
Установлено, что ионы цинка образуют флуоресцирующий комплекс с 4,5-дифенил-2(2-гидроксифенол)имидазолом . Спектр эмиссии флуоресценции представляет собой широкую бесструктурную полосу с максимумом излучения 395 нм (λ возб = 317 нм). При комплексообразовании ионов цинка с Im происходит смещение значения длины волны относительно значения максимальной длины волны флуоресценции чистого реагента в сторону больших длин волн, что свидетельствует об образовании комплекса. Оценочное значение квантового выхода флуоресценции для комплекса Zn – Im составило 0,65.
Спектры флуоресценции комплекса Ag – Im расположены в более длинноволновой области спектра (λ мах = 430 нм); при комплексообразовании также наблюдается батохромное смещение спектров эмиссии флуоресценции по отношению к спектру чистого реагента (квантовый выход флуоресценции 0,83). При исследовании комплексов Ag – Br-Im установлено, что стоксовское смещение составило 188 нм, а оценочное значение квантового выхода 0,66. Максимальным значением квантового выхода обладает комплекс серебра с 9-метилакридином (0,94), λ мах = 691 нм (λ возб = 295 нм).
На примере флуоресценции комплекса Zn – Im в зависимости от рН в растворе (см. рис. 1) можно сделать вывод о том, что положение спектров флуоресценции комплексов существенно зависит от рН раствора.
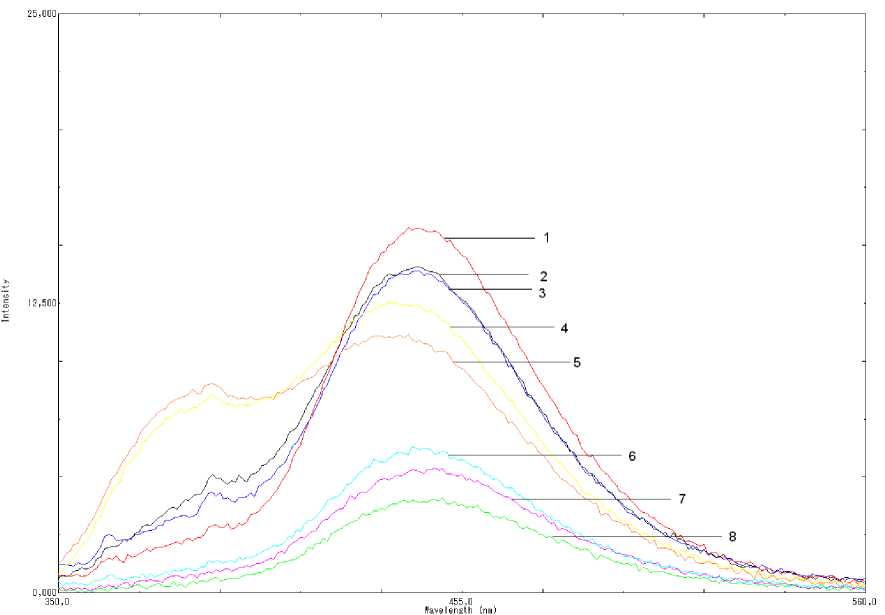
Рис. 1. Зависимость интенсивности флуоресценции комплекса Zn - Im от рН в растворе ( 1 ‒ рН 4; 2 – рН 5; 3 – рН 6; 4 – рН 7; 5 – рН 8; 6 – рН 3; 7 – pH 2; 8 – pH 9, С Zn =10-7 моль/л, C Im =10-7 моль/л, λ возб = 250 нм).
При изучении зависимости величины интенсивности флуоресценции от рН раствора установлено, что рН образования комплекса Zn-Im составляет рН 4; для Ag-Im при рН 6; для Ag-Br-Im рН 2. Образование комплекса Ag - Acr наблюдается в щелочной среде при рН 8.
Для полной характеристики флуоресцирующего комплексного соединения с органическими реагентами были установлены составы комплексов, т.е. стехиометрическое соотношение компонентов в комплексном соединении. По спектрам эмиссии флуоресценции комплексов изученных реагентов с ионами серебра можно сделать вывод о том, что флуоресцирующие комплексы образуются при соотношении 1:1, что является доказательством предполагаемой координации ионов серебра у гетероциклического атома азота за счет его донорных свойств. На основе спектра флуоресценции комплекса цинка с замещенным имидазолом в разных количественных соотношениях при оптимальном pH можно сделать вывод, что комплекс Zn-Im образуется при соотношении 1:2, что отвечает составу Zn-Im 2 .
Изучение 3D-спектров эмиссии флуоресценции комплексов показало, что равновесие в системе «металл-реагент» устанавливается в течение 50 минут для комплекса Zn-Im, что, видимо, связано с более сложной координацией молекул реагента с ионами цинка. Показано, что комплекс Ag- Acr достаточно лабилен, время установления равновесия в системе металл-реагент составляет 10 минут; с увеличением времени контакта интенсивность флуоресценции уменьшается, что, возможно, связано с разрушением комплекса. Установлено, что комплекс Ag-Br-Im обладает максимальной флуоресценцией только в течение 5 минут после смешивания реагента и ионов серебра. При дальнейшем контакте интенсивность флуоресценции линейно уменьшается.
Интенсивность флуоресценции пропорционально возрастает с увеличением содержания концентрации металла в растворе, что может быть использовано для разработки методики флуориметрического определения микроколичеств металлов. Для построения градуировочных зависимостей в ряд пробирок вводили раствор, содержащий ионы металла и реагента в интервале концентраций 10-5 до 10-9 моль/л, устанавливая оптимальное значение рН. С использованием подобранных оптимальных условий образования флуоресцирующих комплексов были определены интервалы концентраций металла в растворе комплекса, в котором наблюдается пропорциональная зависимость интенсивности флуоресценции (I) раствора от концентрации металла. Зависимость интенсивности флуоресценции от концентрации цинка имеет линейный характер в широком интервале концентраций 10-5‒10-8 моль/л для системы Zn-Im (уравнение градуировочного графика I = 105,4∙C – 498,6); для комплекса Ag-Im линейная зависимость наблюдается в узком диапазоне 10-5‒10-6 моль/л (уравнение градуировочного графика I = -332,2∙C + 898); градуировочный график зависимости интенсивности флуоресценции комплекса Ag-Br-Im линеен в более широком диапазоне концентраций 10-4‒10-8 моль/л (уравнение градуировочного графика I=174,8∙C – 265,4); для Ag-Acr интервал концентраций 10-6‒10-8 моль/л (уравнение градуировочного графика I = -94,12∙C + 698,9).
Изучение условий полученных флуоресцирующих комплексов Ag-9-метилакридина позволило подобрать оптимальные параметры флуориметрического определения микроколичеств серебра в природной воде с. Чиндяново Дубенского района. Установлено, что определению серебра при оптимальных условиях образования флуоресцирующего комплекса Ag - Acr не мешают ионы Сd (II), Zn (II), Cu (II), Fe (III) и Pb (II). Правильность результатов разработанной методики подтверждена сравнением с результатами, полученными независимым методом атомно-абсорбционной спектроскопии (см. табл. 1).
Таким образом, проверка методики на природной воде показала удовлетворительную воспроизводимость определения микроколичеств серебра. Разработанная методика характеризуется высокой чувствительностью и селективностью, что позволяет использовать количественный флуориметрический анализ для определения микроколичеств ионов металлов в объектах различной природы.
Таблица 1
Результаты определения содержания серебра в природной воде методом «введено-найдено» и атомно-абсорбционным методом (n = 3; P = 0,95)
|
Введено Ag(I), мкг |
Найдено Ag (I), мкг |
S r |
|
|
Флуориметрическим методом |
Атомноабсорбционным методом |
||
|
- |
0,049 |
0,046 |
0,06 |
|
0, 0214 |
0,0204 |
0,0211 |
0,04 |
|
0,2150 |
0,1990 |
0,201 |
0,05 |
|
0,0027 |
0,0030 |
0,0024 |
0,06 |
Список литературы Флуориметрическое определение серебра (I) и цинка (II) в виде комплексов с органическими реагентами
- Головина А. П., Левшин Л. В. Химический люминесцентный анализ неорганических веществ. - М.: Химия, 1978. - 248 с.
- Беккер Ю. Спектроскопия. - М.: Техносфера, 2009. - 528 с. EDN: RBBCUN


