Формирование биопленок Escherichia coli при модификации редокс-статуса клеток
Автор: Лепехина Е.В., Смирнова Г.В., Октябрьский О.Н.
Журнал: Вестник Пермского университета. Серия: Биология @vestnik-psu-bio
Рубрика: Микробиология
Статья в выпуске: 4, 2016 года.
Бесплатный доступ
Исследована способность к биопленкообразованию у бактерий Escherichia coli, имеющих мутации по компонентам редокс-систем глутатиона и тиоредоксина и по регулятору общего стрессового ответа RpoS при разных ростовых температурах. Выявленная статистически значимая корреляция между удельным биопленкообразованием бактерий и экспрессией антиоксидантного гена katG при 37°С указывает на возможный вклад активации OxyR регулона при формировании биопленок бактериями. Мониторинг экспрессии гена sodA в исследуемых мутантах при 37°С показал 1.15-1.8-кратное ее повышение у gshA, gor, trxA, gshAtrxA и gortrxB мутантов. Установлена прямая зависимость между биопленкообразованием и экспрессией гена sodA в этих же условиях. Наличие мутаций по компонентам тиоловых редокс-систем значительно изменяло профиль зависимости продукции биопленок от температуры, что, вероятно, связано с нарушениями в редокс-регуляции путей передачи внутриклеточных сигналов. Показаны участие RpoS в процессе биопленкообразования при оптимальной ростовой температуре и RpoS-зависимый характер индукции биопленкообразования при 24°С и 44°С.
Биопленкообразование, тиоловые редокс-системы, окислительный стресс, дисульфидный стресс
Короткий адрес: https://sciup.org/147204792
IDR: 147204792 | УДК: 579.22
Biofilm formation of Escherichia coli under the redox-status modification
The ability of biofilm formation in Escherichia coli bearing mutants in the components of glutathione and thioredoxin redox systems, as well as in the regulator of the general stress response RpoS was studied at different growth temperatures. Statistically significant correlation between specific bacteria biofilm formation and expression of the antioxidant gene katG was revealed at 37°C. This indicates a possible contribution of the OxyR regulon activation in the formation of bacteria biofilms. Monitoring of the sodA gene expression in thiol redox system mutants at 37°C showed 1.15-1.8-fold increase in gshA, gor, trxA, gshAtrxA gortrxB mutants. A direct relationship between the biofilm formation and expression of the gene sodA under the same conditions was established. The presence of mutations in components of the thiol redox systems significantly changed the production of biofilms under temperature stresses, which is probably due to the interruptions in the redox regulation of intracellular signaling pathways. It was shown the RpoS participation in biofilm formation at the optimum growth temperature and RpoS-dependent nature of biofilm formation induction in 24°C and 44°C.
Текст научной статьи Формирование биопленок Escherichia coli при модификации редокс-статуса клеток
В отличие от планктонных свободно плавающих одиночных бактерий, биопленки представляют собой микробные консорциумы прикрепленных к субстрату и погруженных в эксграклегочный матрикс клеток Этот жизненный стиль бактерий характеризуется высокой устойчивостью ко всем типам стрессовых воздействий, включая действие антибиотиков и дезин-фвКТанТОВ. ЧТО приводит к существенным медицинским и техническим проблемам и стимулирует исследование факторов, влияющих на биопленкообразова- иис [Mah et al.. 2003; Николаев. Плакунов. 2007]. Изменения условий окружающей среды напрямую влияют на формирование и дисперсию биопленок. В качестве стимулов, влияющих на образование био-пленок. могут выступать доступность питательных компонентов, железа и кислорода в среде, осмотический шок и другие виды стрессов, межклеточная сигнализация и т.д.
Известно, что как в эукариотических, так и в прокариотических клетках многие ключевые регу-
(С Лепехина Е В., Смирнова Г. В., Октябрьский О. Н., 2016
ляторы и ферменты содержат существенные SH-группы* окисление которых сопровождается образованием дисульфидных связей и изменением активности этих молекул* В качестве оксидантов SH-групп могут выступать активные формы кислорода, например Н2О2 в случае OxyR* регулирующего ответ на пероксидный стресс, или хиноны дыхательной цепи* как в случае сенсорной киназы АгсВ, отвечающей на изменение условий аэрации. Восстановление дисульфидных связей в белках может осуществляться с участием глутаредоксинов и тиоредоксинов* окисленные формы которых, в свою очередь, восстанавливаются при помощи глутатиона (GSH) и глутатионредуктазы (GOR) или тиоредоксинредуктазы, соответственно [Potamitou, Holmgren, Vlamis-Gardikas, 2002, Октябрьский, Смирнова, 2007]. Под контролем OxyR и Arc АВ находятся малые РНК OxyS и ArcZ, которые ингибируют подвижность бактерий Е. coh, связываясь с матричной РНК jlhDC, а также влияют на уровень RpoS и, прямо или косвенно, на экспрессию гена cxgD, кодирующего ключевой регулятор, контролирующий биопленкообразование. Кроме того* OxyR участвует в регуляции адгезина AG43. необходимого для образования биопленок на различных поверхностях [Beloin* Roux. Ghigo* 2008]. Таким образом, можно ожидать, что изменение рсдокс-ситуации в клетках должно модулировать их способность к формированию биопЛС-НОК. В данной работе мы изучали влияние мутаций в компонентах редокс-систем глутатиона и тиоре-доксина на биопленкообразование Е. coli при разных ростовых температурах
Материалы и методы исследования
Штаммы бактерий и условия культивирования* Объектом исследования служили бактерии Е. coll BW25113 (A(«raD-croB)567, AlacZ4787(: :rmB-3), Л- rph-L A(rhaD-rhoB)568, hsdR514) и одиночные делеционные мутанты JW2663 (AgshA). JW3467 (Agor), JW0833 (Ag^), JW1051 (Ag^B). JW5856 (A^), JW0871 <^rxB\ JW5536 <^rcB). JW2755 (Arei4), JW0427 (AcfpP) и JW5437 (ДкроВ) из коллекции Keio [Baba ct al* 2006]* Кроме того, использовали сконструированные в нашей лаборатории методом трансформации плазмид и трансакции с фагом PI двойные мутанты NM3655 (A^/lI^I) и NM3761 (EgortrxB\ а также штаммы, содержащие одновременно соответствующие мутации и слияния промоторов генов katG и sodA СО структурным геном iacZ^ кодирующим 0-галактозидазу.
Для проведения экспериментов бактерии Е. coh выращивали при 37°С на минимальной среде М9 (Na2HPOrl2H2O - 15.13 г/л: КН2РО4 - 3 г/л: NH.C1 - 1 г/л; NaCl - 0.5 г/л: MgSO<7 Н2О - 0.246 г/л; СаС12 - 0.011 г/л) [Miller* 1972] с добавлением 0* 15%-ной глюкозы и антибиотиков, к которым был устойчив исследуемый штамм* затем клетки центрифугировали и ресуспендировали в 5 мл среды М9 (0.4% глюкозы) с добавлением 0.2%-ных казаминовых кислот и тиамина (10 мкг/мл) до значения оптической плотности OD6W = 0.1* В лунки полистирольных планшетов вносили по 100 мкл суспензии бактериальных клеток или среды М9 (контроль)* культивировали НО минут при 37°С в термостатируемом шейкере ST-32 ELMI* а затем помещали в термостат при температурах 2 4° С* 37°С или 44 °C.
Способность к биоплеикообразовапшо определяли по модифицированной методике, описанной Naves et al. [2008]. Для этого через 21 ч. измеряли OD^jq, сливали содержимое лунок, дважды отмывали стерильным физраствором по 250 pl и сушили на открытом воздухе 30 мин. Затем вносили в лунки по 150 pl 0.1%-ного раствора генциан-виолета и оставляли на 30 мин., после чего удаляли краситель, промывали 5 раз по 200 pl водой и подсушивали в течение 40 мин. Дтя количественного определения биопленкообразования в лунки вносили по 200 ц1 96%-ного этанола, пипетирова-ли, переносили по 125 pl в новый планшет и измеряли оптическую плотность связанных с красителем клеток и контрольных лунок на микроплан-шетном спектрофотометре xMarkTM Bio-Rad при длине волны 540 нм.
Расчеты проводили, согласно формулам BF = АВ - CW, где BF - валовое биопленкообразование, АВ -OD540 окрашенных бактериальных клеток, CW -OD540 окрашенных контрольных лунок;
sBF = (АВ - CW)/AOD6№ где sBF - удельное биопленкообразование, AOD^ - разность между ODW0 планктонной культуры и OD№) бактерий без среды.
Экспрессию генов оценивали путем измерения 0-галакгозидазной активности в клетках репортерных штаммов Е* coh, несущих генные слияния katG;:lacZ и sodA::lacZ при температурах 24°С 37°С и 44°С по методу’ Миллера [Miller. 1972].
Подвижность бактерий определяли путем измерения диаметра зоны роста на полужидком агаре (0.3%) через сутки интубации при 30 °C по методике* описанной Pittman et al. [2002]*
Статистическую обработку экспериментальных данных осуществляли с помощью пакета программ Microsoft Excel (Microsoft Office 2003) и Sta-tistica 6.0* вычисляя среднее значение* стандартную ошибку7 и доверительный интервал. Каждый результат показан как среднее значение не менее чем из пяти независимых экспериментов ± стандартная ошибка среднего. Достоверность различий между средними величинами оценивали согласно критерию Стьюдента, различия считались значимыми при р < 0.05*
Результаты и их обсуждение
Мутации по компонентам тиоловых редокс-систем слабо влияли на способность к биопленко-образованию при оптимальной температуре 37°С. В отсутствии глутаредоксина В этот параметр снижался в 1.2 раза, а у двойного мутанта gortrxB и мутанта по тиоредоксину I биопленкообразова-ние возрастало в 1.3 и L2 раза, соответственно, по сравнению с клетками дикого типа (рис* 1).
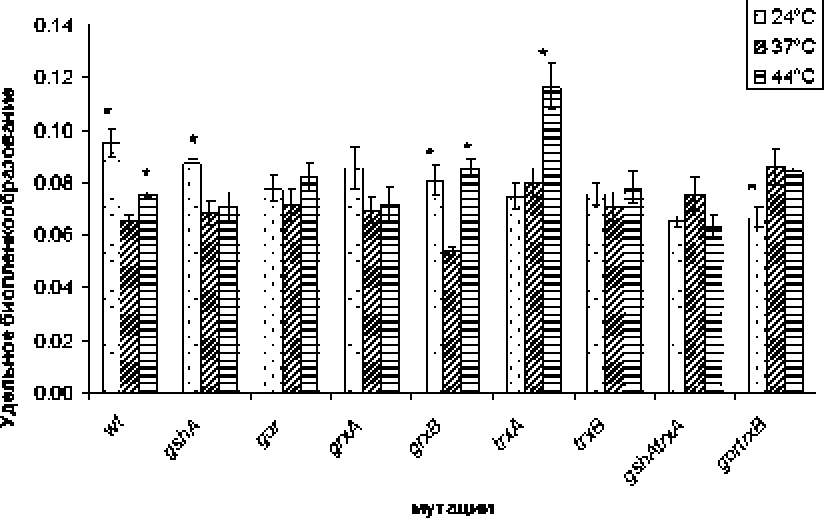
Рис. I* Способность к биопленкообразованию мутантов Е. coh по тиоловым редокс-системам при разных температурах культивирования
В то же время мутации по компонентам тиоловых редокс-систем значительно влияли на подвижность бактерий при температуре 30°С. Максимальное ингибирование подвижности (от 2 до 6 раз) было характерно для штаммов* несущих мутации gor. grxB. trxA „ gshA trxA и gortrxB.
За исключением делеции по глутаредоксину В* во всех \гутантах по компонентам тиоловых редокс-систем* и? особенно, у двойных мутантов в первые два часа инкубации в планшетах наблюдалось возрастание экспрессии гена katG относительно ее значения в родительском штамме (рис. 2)* что является следствием активации регуляторного белка OxyR в условиях дисульфидного стресса* испытываемого этими мутантами. Была выявлена статистически значимая корреляция между удельным биопленкообразованием бактерий и экспрессией гена katG при 37°С (г = 0.69* р < 0.05). В этих условиях возрастает также экспрессия OxyR-контролируемого гена шъ5\ кодирующего малую регуляторную РНК OxyS. Индукция OxyS приводит к ингибированию FlhDC регулона, что может объяснить наблюдаемое нами снижение подвижности у мутантных бактерий.
Вероятно, дисульфидный стресс влияет и на активность сенсорной киназы АгсВ. которая ингибируется при окислении ее редокс-активных цистеиновых остатков, локализованных в цитоплазме. Известно, что редуктанты (дигиотреитол и меркап тоэтанол) повышают* а оксидант хлорамин значительно снижает активность АгсВ [Malpica el al** 2004]. Следует ожидать* что в условиях дисульфидного стресса активность АгсВ будет ингибироваться* что сопровождается дефосфорилированием транскрипционного регулятора АгсА* репрессирующего многие гены* участвующие в дыхательном метаболизме* Под негативным контролем двухкомпонентной системы АгсАВ находится малая регуляторная РНК ArcZ* которая способна ингибировать подвижность бактерий* одновременно стимулируя продукцию биопленок за счет активи-рующего эффекта на центральный регулятор био-пленкообразования CsgD. Таким образом* этот молекулярный механизм может вносить вклад в наблюдаемую нами стимуляцию биопленкообразо-вания у мутантов по генам системы тиоредоксина. Под негативным контролем АгсАВ системы находится ген sodA. кодирующий Mn-су пероксид-дисмутазу. Мониторинг экспрессии этого гена в мутантах по тиоловым редокс-системам в первые два часа инкубации в планшетах показа*! ее повышение у gshA. gor* trxA, gshAtrxA и gortrxB мутантов в 1.15-1.8 раза (рис. 2)* Следует отметить* что через 21 ч. инкубации в планшете наблюдали 1*2-3.6-кратное снижение экспрессии sodA у бактерий* несущих мутации grol* grxB* trxA. IrxB, gortrxB. Двойной мутант gshAtrxA показывал 20-кратное снижение этого параметра. Стоит отметить* что делеция гена агсВ не влияла на способность к об-
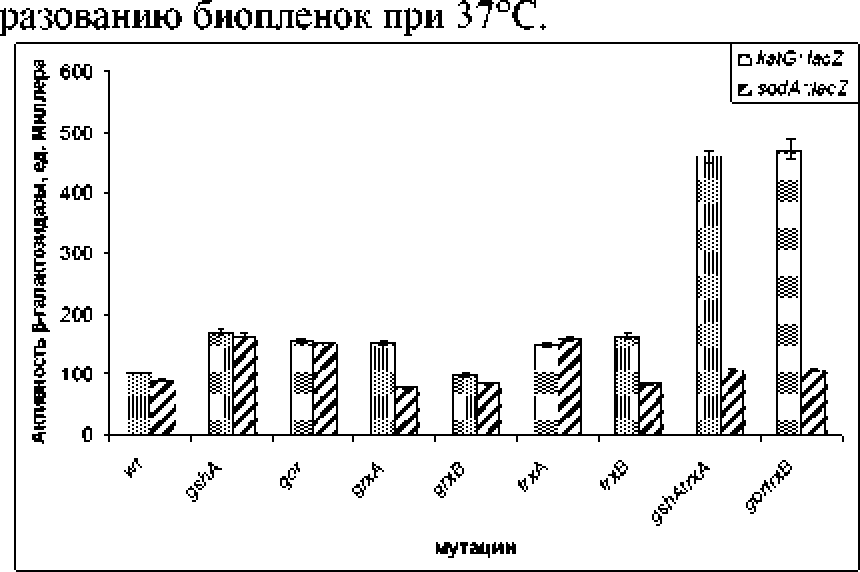
Рис 2, Экспрессия антиоксидантных генов katG и sodA у мутантов Е. coll по тиоловым редокс-сисгемам через 2 ч. экспозиции при 37°С
Ранее было установлено* что наличие RpoS не является обязательным условием для процесса биопленкообразования при оптимальной ростовой температуре [White-Ziegler et al** 2008]. В наших экспериментах при 37°С* штамм, лишенный гена rpoS, продуцировал в 2.1 раза больше биопленок* чем клетки дикого типа* При этом делеции генов relA. кодирующих ppGpp синтетазу* активирующую экспрессию генов rpoS. и с!рР. кодирующих протеазу RpoS* не влияли на степень продукции биопленок (рис. 3). Была выявлена статистически значимая корреляция между валовым биопленко- образованием мутантов по тиоловым редокс-системам и регулятору общего стрессового ответа RpoS и экспрессией гена sodA в первые два часа инкубации в планшете (г = 0.7 L р < 0*05)*
Среди факторов окружающей среды, оказывающих влияние на процесс биопленкообразования, важную роль играет температура культивирования Ранее было показано, что при 37°С в первичном прикреплении Е. colt к субстрату участвуют фимбрии первого типа (пили) и адгезии AG43, а основным компонентом матрикса является PGA [Mika, Hengge* 2013]. При температурах ниже 30°С первичная адгезия осуществляется с участием фимбрий другого типа (curb), при этом матрикс состоит в основном из целлюлозы и колановой кислоты, Показано, что снижение температуры культивирования до 23 °C сопровождается RpoS-зависимой стимуляцией продукции биопленок [White-Ziegler el al„ 2008]. В наших экспериментах для бактерий Е. coli дикого типа было выявлено повышение биопленкообразования при 24 и 44°С. Повышение продукции биопленок при 24°С отсутствовало в ЫрР и rpoS мутантах, но сохранялась в штамме с делецией reLL что подтверждает RpoS-зависимый характер индукции биопленкообразования при этой температуре (рис.З). Аналогичную картину наблюдали и при повышенной температуре 44°С, Стоит отметить, что штамм с мутацией reLA демонстрировал характерные для дикого типа пики биопленкообразования при 24 и 44ЛС
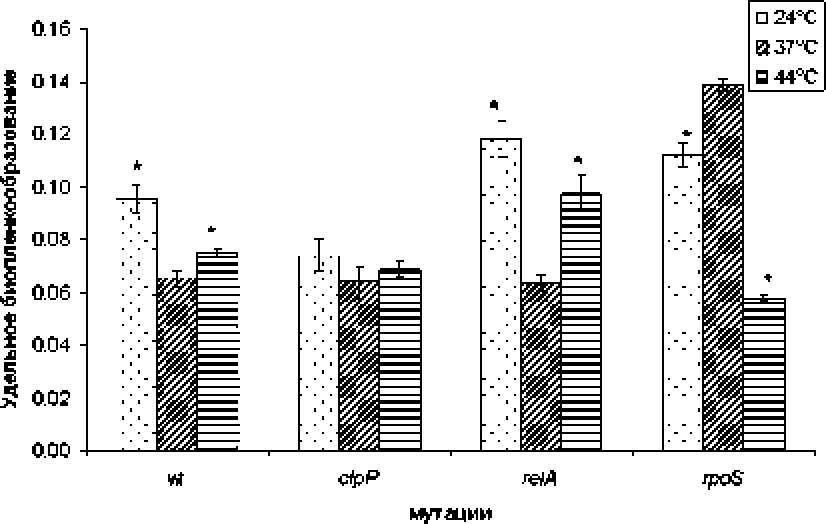
Рис. 3. Способность к биопленкообразованию мутантов Е. со И по генам reiA, clpP и rpoS при разных температурах культивирования
Наличие мутаций по компонентам тиоловых редокс-систем значительно изменяло профиль зависимости продукции биопленок от температуры. Удельное биопленкообразование бактерий не изменялось при сдвиге температур до 24 и 44°С у штаммов, несущих мутации по генам gor, grxA, trxB. gsMtrxA (см. рис. 1). В этих же условиях наблюдали статистически значимую стимуляцию способности к биопленкообразованию у мутанта по глутаредоксину В. Мутант по глутатиону показывал увеличение удельного биопленкообразования при 24°С? а мутант по тиоредоксину I - при 44°С.
Наблюдаемые процессы могут быть связаны с нарушениями в редокс-регуляции путей передачи внутриклеточных сигналов, При 24°С экспрессия антиоксидантного гена katG возрастала у штаммов, мутантных по глутатиону; обоим глутаредок-синам, тиоредоксинредуктазе и у двойного мутанта gortrxB. по сравнению с диким типом, В этих же условиях экспрессия гена sodA повышалась у мутантов по генам системы глутаредоксина и снижалась у двойных мутантов и мутантов по генам системы тиоредоксина, по сравнению с родительским штаммом, Была обнаружена статистически значимая обратная зависимость между уровнем экспрессии гена katG на момент начала холодового стресса и удельным биопленкообразованием при 24 ° С (г = -0.79, р < 0.05). При 44°С экспрессия генов kaiG и sodA значительно снижалась у всех штаммов, по сравнению с 37°С, Статистически значимая корреляция была выявлена при 44°С между валовым биопленкообразованием и экспрессией katG (г = -0.71, р < 0.05),
Известно, что RpoS негативно контролируется Аге АВ двухкомпонентной системой, а малая регуляторная РНК Оху S оказывает ингибирующий эффект на экспрессию гена rpoS. Следовательно, образование S-S связей в регуляторных белках OxyR и АгсВ в тиоловых мутантах, испытывающих дисульфидный стресс, должно ингибировать RpoS-зависимое биопленкообразование при неоптимальных температурах, что и наблюдалось в наших экспериментах.
Заключение
Выявленные нами различия в способности к биопленкообразованию у бактерий Е. cob указывают на модулирующее действие изменений ре-докс-статуса клеток, в основе которого может лежать дисульфидный стресс и активация OxyR ре-гулона. Показан RpoS-зависимый характер индукции биопленкообразования вблизи границ температурного оптимума для роста Е cob. Поскольку многие патогенные микроорганизмы образуют биопленки в инфицированном макроорганизме, а также на поверхности изделий, имеющих медицинское назначение, полученные нами в работе данные открывают возможности для модуляции биопленкообразования путем изменения редокс-статуса среды и клеток.
Работа поддержана грантами РФФИ № 16-04-00762 и № 14-04-96031.
Список литературы Формирование биопленок Escherichia coli при модификации редокс-статуса клеток
- Николаев Ю.А., Плакунов В.К. Биопленка -«Город микробов» или аналог многоклеточного организма?//Микробиология. 2007. Т. 76. С. 149-163.
- Октябрьский О.Н., Смирнова Г.В. Редокс регуляция клеточных функций//Биохимия. 2007. Т. 72. С. 158-174
- Baba T. et al. Construction of Escherichia coli strain K-12 in-frame, single-gene knockout mutants: the Keio Collection//Mol. Syst. Biol. 2006. Vol. 2. P. 1-11
- Beloin C., Roux A., Ghigo J-M. Escherichia coli biofilms//Curr. Top Microbiol. Immunol. 2008. Vol. 322. P. 249-289
- Mah T.F. et al. A genetic basis for Pseudomonas aeruginosa biofilm antibiotic resistance//Nature. 2003. V. 426. P. 306-310
- Malpica R. et al. Identification of a quinone-sensitive redox switch in the ArcB sensor kinase//Proc. Natl. Acad. Sci. 2004. Vol. 101. P. 13318-13323
- Mika F., Hengge R. Small Regulatory RNAs in the control of motility and biofilm Formation in E. coli and Salmonella//Int. J. Mol. Sci. 2013. Vol. 14. P. 4560-4579
- Miller J. N. Experiments in molecular genetics. New York: Cold Spring Harbor Laboratory Press, 1972
- Naves P. et al. Measurement of biofilm formation by clinical isolates of Escherichia coli is methoddependent//J. Appl. Microbiol. 2008. Vol. 105. P. 585-590
- Pittman M.S. et al. Cysteine is exported from the Escherichia coli cytoplasm by CydDC, an ATP-binding cassette-type transporter required for cytochrome assembly//J. Biol. Chem. 2002. Vol. 277. P. 49841-49849
- Potamitou A., Holmgren A., Vlamis-Gardikas A. Protein levels of Escherichia coli thioredoxins and glutaredoxins and their relation to null mutants, growth phase, and function//J. Biol. Chem. 2002. Vol. 277. P. 18561-18567
- Povolotsky T.L., Hengge R. 'Life-style' control networks in Escherichia coli: Signaling by the second messenger c-di-GMP//J Biotechnol. 2012. Vol. 160. P. 10-16
- White-Ziegler C.A. et al. Low temperature (23°C) increases expression of biofilm-, cold-shock-and RpoS-dependent genes in Escherichia coli K-12//Microbiology. 2008. Vol.154. P. 148-166


