Формирование и функционирование микробных матов минерального источника Хойто-Гол (Восточный Саян)
Автор: Кашкак Елена Сергеевна, Гайсин Василь Анварович, Дагурова Ольга Павловна, Брянцева Ирина Андреевна, Данилова Эржена Викторовна
Журнал: Известия Самарского научного центра Российской академии наук @izvestiya-ssc
Рубрика: Общая биология
Статья в выпуске: 2-2 т.18, 2016 года.
Бесплатный доступ
Проведено исследование видового состава бактерий, участвующих в продукции и деструкции органического вещества, в микробных матах источника Хойто-Гол, расположенного в горной системе Восточного Саяна. Химический анализ воды минерального источника показал, что вода относится к гидрокарбонатно-натриевому типу с содержанием сероводорода до 7 мг/л. Сероводород поступает с вулканическими флюидами, а также из донных осадков в результате микробной сульфатредукции. Установлено, что основными формообразующими бактериями микробных матов источника являются цианобактерии Phormidium sp. и бесцветные серобактерии Thiothrix sp. Была обнаружена высокая численность автотрофных и гетеротрофных микроорганизмов (до 108 кл/мл). Отличительной особенностью микробных матов источника Хойто-Гол являлось доминирование и разнообразие бактерий цикла серы. Важная роль бактерий серного цикла в источнике Хойто-Гол подтверждается высокими численностями сульфатредуцирующих и тионовых бактерий, интенсивностями процессов сульфатредукции и аноксигенного фотосинтеза. Выделены чистые культуры пурпурных несерных бактерий ( Rhodopseudomonas palustris, Rhodobacter capsulatus, Rhodomicrobium vannielii ), нитчатых аноксигенных бактерий ( Oscillochloris trichoides ), зеленых серобактерий ( Chlorobium limicola ), тионовых бактерий ( Thiobacillus thioparus ), сульфатредуцирующих бактерий ( Desulfovibrio alcoholivorans ) и показано их участие в цикле серы в микробных матах.
Микробные маты, цианобактерии, аноксигенные фототрофные бактерии, тионовые бактерии, бесцветные серобактерии, сульфатредуцирующие бактерии, хлорофилл, бактериохлорофилл, продукция, деструкция, круговорот серы, сульфидсодержащие источники, восточный саян
Короткий адрес: https://sciup.org/148204495
IDR: 148204495 | УДК: 576.809.51
Formation and functioning of microbial mats in mineral spring Hoito-Gol (Eastern Sayan)
The bacterial species composition involved in the production and destruction of organic matter of microbial mats in the spring Hoito-Gol, located in the Eastern Sayan mountain range, was studied. The mineral spring water relates to hydrocarbonate-sodium type, with the hydrogen sulfide content to 7 mg/l. Hydrogen sulfide stands out from the depths with volcanic fluids and forms in microbial sulfate reduction process in sediments. Microbial mats were formed by cyanobacteria Phormidium sp. and colorless sulfur bacteria Thiothrix sp. High number of autotrophic and heterotrophic microorganisms (up to 108 cells/ml) was detected. A feature of the microbial mats functioning of spring Hojto Gol was dominance and diversity of sulfur cycle bacteria. Important role in the sulfur cycle bacteria in spring Hojto Gol confirmed by high numbers of sulfate-reducing bacteria and sulfur-oxidizing bacteria, and intensive processes of sulfate reduction and anoxic photosynthesis. We obtained pure cultures of purple non-sulfur bacteria ( Rhodopseudomonas palustris, Rhodobacter capsulatus, Rhodomicrobium vannielii ), filamentous anoxigenic bacteria ( Oscillochloris trichoides ), green sulfur bacteria ( Chlorobium limicola ), sulfur-oxidizing bacteria ( Thiobacillus thioparus ), sulfate-reducing bacteria ( Desulfovibrio alcoholivorans ) and showed their activity in sulfur cycle in the microbial mats.
Текст научной статьи Формирование и функционирование микробных матов минерального источника Хойто-Гол (Восточный Саян)
формирования и функционирования матов [7]. Формирование микробных матов определяется многими факторами, такими, как температура, рН, освещение, содержание сероводорода, химический состав воды; расстояние от выхода источника также может влиять на сукцессию микроорганизмов [2, 8].
Сульфидные термальные источники с нейтральными или щелочными значениями рН относительно редко встречаются [2]. Бактерии, которые в них развиваются, часто образуют маты или длинные нити, которые могут быть белого или ярко-желтого цвета из-за осажденной серы. В этих источниках важнейшим абиотическим фактором, влияющим на формирование микробного сообщества, является сероводород. К такому типу источников относится мезотермальный источник Хойто-Гол, расположенный в горной системе Восточного Саяна. Особенности формирования микробных матов и оценка активности физиологических групп микроорганизмов в матах этого источника изучены недостаточно полно. Ранее были исследовано влияние экологических условий на распределение микроорганизмов и роль микроорганизмов в травер-тинобразовании [9-11].
Цель исследования :– изучение особенностей формирования и функционирования микробных матов сульфид-содержащего источника Хойто-Гол.
Материалы и методики исследования. Минеральный источник Хойто-Гол имеет 5 выходов воды, расположенных вниз по течению реки Аршан (приток реки Хойто-Гол) на высоте 1712 м над уровнем моря
(52.37.255 N, 099.00.875 E). Пробы воды и микробных матов отбирали летом 2013 г. Определение физикохимических характеристик воды проводили с помощью портативных приборов и стандартных методов гидрохимии [12]. Скорости микробных процессов определяли радиоизотопным методом [13]. Учет численности зеленых нитчатых бактерий, зеленых и пурпурных серобактерий, пурпурных несерных бактерий, тионовых, целлюлозоразлагающих, амилолитических, протеолитических, сульфатредуцирующих бактерий проводили методом предельных разведений на селективных питательных средах [14]. Морфологию клеток, размеры и подвижность изучали микроскопированием с помощью световых микроскопов Axiostar plus (Carl Zeiss, Германия) и Olympus BX 41 (Olympus, Япония). Исследование поверхности и элементного состава микробных матов и пленок, образовавшихся при культивировании тионовых бактерий, проводили с помощью сканирующего электронного микроскопа SEM TM-1000 (HITACHI, Япония). Определение таксономической принадлежности цианобактерий проводили на основании морфологических признаков по определителям [15, 16]. Пигментный состав фототрофных бактерий определяли по положению максимумов на спектрах поглощения пигментов, полученных на спектрофотометре СФ-56 (ЛОМО, Россия).
ДНК клеток монокультур аноксигенных нитчатых фототрофных бактерий выделяли с помощью ЦТАБ-метода с незначительными изменениями [17].
ДНК клеток всех остальных культур бактерий выделяли с помощью метода, описанного ранее Булыгиной с соавторами [18]. Молекулярно-генетическую идентификацию монокультур аноксигенных фототрофных бактерий и чистых культур сероокисляющих и суль-фатредуцирующих бактерий проводили посредством анализа последовательностей генов 16S рРНК и fmoA (Fenna–Matthews–Olson protein) в Центре «Биоинженерия» РАН (г. Москва). Сравнительный анализ нуклеотидных данных с последовательностями базы данных GenBank проводили с помощью программных пакетов BLAST .
Результаты исследования и их обсуждение.
Характеристика минерального источника Хойто-Гол. В период исследования температура воды в местах отбора проб составляла 32,5-34,0°С, рН воды был нейтральным (табл. 1). Тип воды источников – гидрокарбонатно-натриевый. Содержание гидрокар-бонат-ионов составляло более 400 мг/дм3, содержание СО 2 достигало 57,0 мг/дм3. Содержание ионов Na+ составляло 143-149 мг/дм3. Низкий окислительновосстановительный потенциал (от -23 до -130 мВ) обусловлен, скорее всего, наличием сероводорода, поступающего с вулканическими эксгаляциями, а также из донных осадков в процессе сульфатредукции. Содержание сероводорода колебалось от 0,52 до 7,05 мг/дм3. По литературным данным, содержание сульфида может достигать 20 мг/л [9]. Концентрация ионов SO 4 2-достигала 33 мг/дм3, а Сl- – 24 мг/дм3.
Таблица 1. Физико-химические и микробиологические показатели источника Хойто-Гол
|
Станция |
Описание микробных матов |
T, °C |
рН |
H 2 S, мг/л |
Видовой состав матообразующих форм бактерий |
|
Hg1 верхний выход источника |
тонкая зеленая биопленка толщиной 1 мм |
34,0 |
7,32 |
6,69 |
цианобактерии Phormidium sp., Anaba-ena sp., Microcystis sp. |
|
Hg2 новый выход |
темно-зеленый мат толщиной 5 мм |
33,6 |
7,33 |
7,03 |
цианобактерии Phormidium sp., Ana-baena sp., Microcystis sp. |
|
далее по ручью: Hg2-1 в 3 м от ст. Hg2 |
зеленый мат с белыми и рыжими обрастаниями толщиной до 2 см |
33,4 |
7,45 |
7,05 |
цианобактерии Phormidium sp., Ana-baena sp., Oscillatoria sp., Synechococcus sp., Gloeocapsa magma , бесцветные серобактерии Thiothrix sp. |
|
Hg2-2 в 5 м от ст. Hg2 |
серный мат с зелеными вкраплениями толщиной 1 см |
32,6 |
7,84 |
7,28 |
цианобактерии Phormidium sp., Oscilla-toria sp., Gloeocapsa magma , Synechococ-cus sp., бесцветные серобактерии Thiothrix sp. |
|
Hg2-3 ручей после ванного комплекса №1 |
зеленый мат с белыми обрастаниями толщиной 1 см |
32,5 |
7,65 |
7,17 |
цианобактерии Phormidium sp., Oscilla-toria sp., Gloeocapsa magma , Sy-nechococcus sp., бесцветные серобактерии Thiothrix sp. |
|
Hg2-4 ручей после ванного комплекса №2 |
светло-зеленый мат толщиной 7 мм |
32,7 |
7,35 |
7,03 |
цианобактерии Phormidium sp., Ana-baena sp., Oscillatoria sp., Gloeocapsa magma , Microcystis sp. |
|
Hg3 новый выход «Питьевой источник» |
тонкая зеленая биопленка толщиной 2 мм |
33,5 |
7,32 |
0,52 |
цианобактерии Phormidium sp., Anaba-ena sp., Microcystis sp. |
Описание микробных матов. В зоне выходов и вниз по ручью исследуемого источника развивались микробные маты толщиной до 2 см, которые были представлены зоной оксигенного фотосинтеза с преобладающим развитием зеленых скоплений цианобактерий и зоной развития серных бактерий (табл. 1). На верхнем выходе Hg1 и выходе питьевого источника Hg3 развивались тонкие микробные маты зеленого цвета толщиной 1-2 мм, на выходе Hg2 микробный мат был толще – до 5 мм. Основу матов на выходах источников составляли цианобактерии Phormidium sp., Ana-baena sp., Microcystis sp. Спектры поглощения пигментов из микробных матов подтверждают преобладание цианобактерий, для которых характерно наличие хлорофилла α с максимумом при 675 нм (рис. 1-1).
По изливу минерального ручья на станциях Hg2-1, Hg2-2, Hg2-3 и Hg2-4 наблюдались микробные маты толщиной до 2 см, состоящие в основном из нитчатых цианобактерий и бесцветных серобактерий Thiothrix sp. Видовой состав цианобактерий увеличивается за счет появления Oscillatoria sp., Gloeocapsa magma и Synechococcus sp. Спектры поглощения пигментов из микробных матов показывают наличие цианобактерий с хлорофиллом α (максимум поглощения при 674 нм) и аноксигенных фототрофных бактерий, содержащих ответственные за поглощение света бактериохлорофиллы (рис. 1-2). Максимум инфракрасного поглощения в клетке при 745 нм характерен для бактериохлорофилла с , имеющегося у всех зеленых серобактерий класса Chlorobi и у некоторых нитчатых аноксигенных фототрофов класса Chloroflexia . Пики 805 нм и 875 нм на спектрах поглощения пигментов в клетке указывают на присутствие бактериохлорофилла а , преобладающего у большинства пурпурных фототрофных бактерий, у всех зеленых серобактерий и нитчатых аноксигенных фототрофных бактерий.
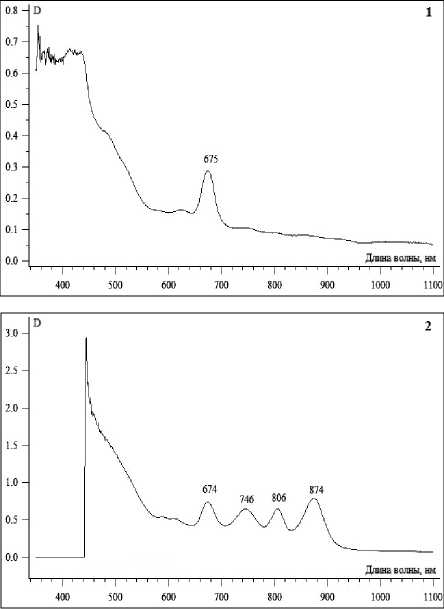
Рис. 1. Спектр поглощения микробного мата: 1 – со станции Hg2; 2 – со станции Hg2-1
Появлению в составе микробного мата бесцветных серобактерий Thiothrix sp. способствовало развитие мата в условиях проточной воды, что необходимо для создания градиента сероводорода и кислорода [19, с. 166-171]. На поверхности микробного мата формируются белые минеральные отложения. Результаты исследования элементного состава показали, что они состоят из элементной серы, содержание которой достигает 99% (рис. 2). Бесцветные серобактерии участвуют в аккумуляции и кристаллизации серы и играют важную роль в поведении системы в целом, так как в ночное время окисление соединений серы оказывается основной статьей расхода кислорода [20].

Рис. 2. Минеральные отложения: 1 – формирующиеся на поверхности микробного мата со станции Hg2-1;
2 – формирующихся на поверхности микробного мата
Интенсивность продукции и деструкции органического вещества в микробных матах. Скорость фотосинтеза в микробных матах была равна 0,17-7,61 мг С/(дм3∙сут) (табл. 2). Значительный вклад в осуществление процесса вносят аноксигенные фототрофы – скорость аноксигенного фотосинтеза составила 0,09-4,8 мгС/(дм3∙сут). Хемосинтез в микробных матах протекал со скоростью 0,05-1,43 мгС/(дм3∙сут), а гетеротрофная ассимиляция СО2 варьировала от 0,05 до 0,78 мгС/(дм3∙сут). Значения продукционных процессов исследуемого источника были ниже, чем в более высокотемпературных гидротермах [21, 22]. Были определены скорости сульфатредукции и метаногенеза, завершающие процесс анаэробной деструкции органического вещества. Скорость сульфатредукции в микробных матах исследуемого источника составила 0,04-0,93 мгS/(дм3∙сут) при расходе углерода на этот процесс 0,04-0,70 мгC/(дм3∙сут). В зеленых матах с преимущественным развитием цианобактерий, расход органического вещества на сульфатредукцию и метаногенез были примерно одинаковым. В мате с белыми обрастаниями, где происходит появление серобактерий, скорость сульфатредукции намного превышала интенсивность метаногенеза. Образование первичными анаэробами низкомолекулярных органических веществ, присутствие сульфатов способствуют активной деятельности сульфатредуцирующих бактерий.
Таблица 2. Скорость процессов продукции и деструкции в микробных матах источника Хойто-Гол
|
Процессы |
Hg1 |
Hg2 |
Hg 2-1 |
Hg2-2 |
Hg2-3 |
|
общий фотосинтез, мгС/(дм3∙сут) |
2,36 |
7,61 |
6,03 |
0,17 |
5,99 |
|
аноксигенный фотосинтез, мгС/(дм3∙сут) |
1,71 |
3,4 |
3,2 |
0,09 |
0,58 |
|
хемосинтез, мгС/(дм3∙сут) |
0,24 |
1,43 |
1,16 |
0,03 |
0,62 |
|
гетеротрофная ассимиляция СО 2 , мгС/(дм3∙сут) |
0,26 |
0,19 |
0,37 |
0,02 |
0,78 |
|
сульфатредукция, мгS/(дм3∙cут) |
0,04 |
0,28 |
0,42 |
0,93 |
0,27 |
|
расход С при сульфатредукции, мгС/(дм3∙cут) |
0,03 |
0,21 |
0,32 |
0,70 |
0,25 |
|
метаногенез, мгС/(дм3∙сут) |
0,02 |
0,06 |
0,001 |
- |
- |
|
расход С при метаногенезе, мгС/(дм3∙cут) |
0,10 |
0,23 |
0,005 |
- |
- |
Количественный учет различных физиологических групп микроорганизмов. Численность аноксигенных фототрофных бактерий, вклад которых в процесс фотосинтеза составляет около 50%, достигала 104-105 кл/см3. Кроме фототрофных бактерий, в продукции органического вещества в микробных матах участвуют также сероокисляющие бактерии, ассимилируя углекислый газ и используя энергию окисления сероводорода. Количество сероокисляющих бактерий варьировало в пределах 104-106 кл/см3. На начальных этапах деструкции главную роль играют бактерии-гидролитики, разлагающие полимерные соединения [23, с. 143-157]. Доминирующими были протеолитические бактерии, их численность достигала 108 кл/см3 в толстом продуктивном мате.
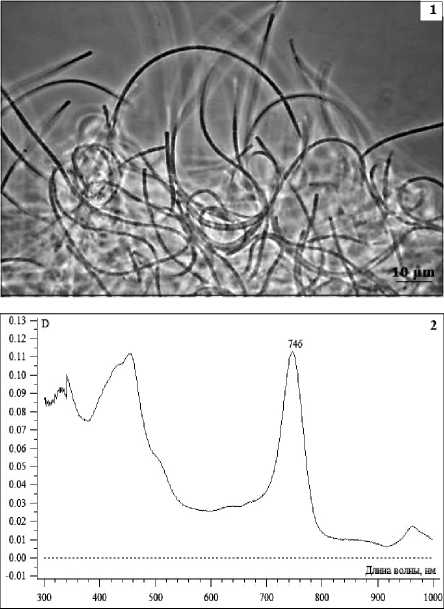
Рис. 3. 1 – морфология нитчатой аноксигенной фото-трофной бактерии Oscillochloris trichoides, изолированной из микробного мата Hg2; 2 – спектр поглощения клеток культуры Oscillochloris trichoides
Количество бактерий, разлагающих крахмал, варьировало от 105 до 107 кл/см3. Максимальная численность целлюлозоразлагающих бактерий достигала 107 кл/см3.Активная роль на конечных этапах деструкции органического вещества в микробных матах принадлежит сульфатредуцирующим бактериям, численность которых составляла 104–106 кл/см3 при использовании лактата натрия в качестве источника углерода и энергии.
Выделение и идентификация культур аноксигенных нитчатых фототрофных бактерий. Из микробных матов Hg2, Hg2-3 были выделены 2 монокультуры аноксигенных нитчатых фототрофных бактерий. На среде, содержащей сульфид, они образовывали колонии светло-зеленого цвета диаметром до 2 мм. Полученные культуры представляли собой тонкие нити с газовыми вакуолями толщиной до 5 мкм (рис. 31). В качестве основного пигмента бактерии содержали бактериохлорофилл с с максимумом поглощения в клетках при 746 нм (рис. 3-2). Филогенетический анализ, основанный на сравнении нуклеотидных последовательностей гена 16S рРНК, показал, что штаммы относятся к виду Oscillochloris trichoides (99% сходства).
Зеленые серобактерии. Были получены 3 культуры зеленых серобактерий, которые участвуют в окислении сульфида при фотосинтезе, с образованием элементной серы вне клеток. При росте на агаре они образовывали колонии темно-зеленого цвета, диаметром 1-2 мм. Морфологически бактерии представляли собой палочковидные клетки, формируя короткие ветвящиеся цепочки, и соответствовали видам рода Chlorobium (рис. 4-1). Основным пигментом у них был бактериохлорофилл с (максимум поглощения 742 нм) (рис. 4-2). При сравнении аминокислотной последовательности ФМО-протеина ( fmo A), полученной при трансляции in silico фрагмента гена fmo A, амплифицированно-го из выделенной нами культуры, с референтными последовательностями, было определено, что она наиболее близка к виду Chlorobium limicola.
Несерные пурпурные бактерии присутствовали в микробных матах во всех исследованных станциях. Было выделено 7 чистых культур несерных пурпурных бактерий, морфологически соответствующих родам Rhodobacter, Rhodopseudomonas и Rhodomicrobium. Несерные пурпурные бактерии рода Rhodobacter sp. морфологически были представлены короткими овальными палочками. В анаэробной среде образовывали колонии темно-коричневого цвета, а в аэробной среде бордового цвета. Бактерии рода Rhodomicrobium sp. представляли собой короткие овальные палочки, размножающиеся почкованием с образованием гифоподобных тонких нитей, что характерно для известного вида Rhodomicrobium vannielii. Данные филогенетического анализа подтвердили, что бактерия относится к виду Rhodomicrobium vannielii (99% сходства). Два остальных морфотипа выделенных несерных пурпурных бактерий филогенетически были близки к видам Rhodopseudomonas palustris и Rhodopseudomonas faecalis. Подвижные палочковидные бактерии, размножаются почкованием. В старых культурах образуют розеткоподобные кластеры.
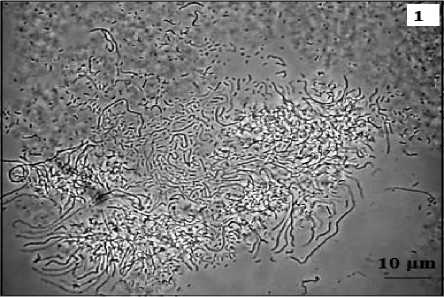
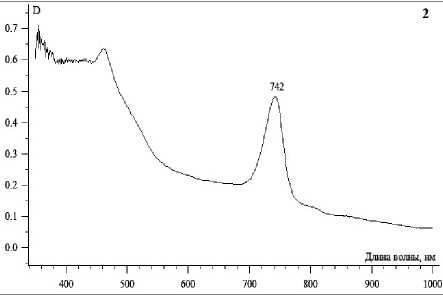
Рис. 4. 1 – морфология зеленой серобактерии Chlorobium limicola, выделенной из микробного мата станции Hg2-3; 2 – спектр поглощения клеток культуры Chlorobium limicola
Тионовые бактерии. Были получены 4 чистые культуры тионовых бактерий, которые были представлены подвижными одиночными и парными палочками длиной до 1,5 мкм. На основании данных нуклеотидных последовательностей гена 16S рРНК культуры соответствовали виду Thiobacillus thioparus, идентичность с которым составила 99%. При культивировании среда мутнела на 3-5 сутки, и на ее поверхности появлялась белая пленка. Результаты исследования элементного состава пленки показали, что она состоит из элементной серы, содержание которой достигает 100%.
Сульфатредуцирующие бактерии. Из микробных матов было выделено 2 чистые культуры суль-фатредуцирующих бактерий, которые представлены грамотрицательными вибрионами, подвижными за счет одного полярно расположенного жгутика. Филогенетический анализ, основанный на сравнении нуклеотидных последовательностей гена 16S рРНК, показал, что штаммы близки между собой и относятся к виду Desulfovibrio alcoholivorans (99% сходства).
Выводы: м инеральный источник Хойто-Гол относится к гидрокарбонатно-натриевому типу с наличием сероводорода. Экологические условия среды обитания микробных сообществ в исследуемом источнике являются благоприятными для развития и функционирования бактерий, участвующих в продукции и деструкции органического вещества. В микробных матах источника основными формообразующими бактериями являются цианобактерии Phormidium sp. и бесцветные серобактерии Thiothrix sp. В продукции органического вещества участвуют фототрофные бактерии, бесцветные серобактерии и тионовые бактерии. Отличительной особенностью микробных матов источника Хойто-Гол являлось доминирование и разнообразие бактерий цикла серы. Важная роль бактерий серного цикла в источнике Хойто-Гол подтверждается высокими численностями сульфатредуцирующих и тионовых бактерий, интенсивностями процессов сульфатредук-ции и аноксигенного фотосинтеза. Выделены чистые культуры пурпурных несерных бактерий ( Rhodopseu-domonas palustris , Rhodobacter capsulatus , Rhodomicrobium vannielii ), нитчатых аноксигенных бактерий ( Oscillochlo-ris trichoides ), зеленых серобактерий ( Chlorobium limicola), тионовых бактерий (Thiobacillus thioparus), сульфатредуцирующих бактерий (Desulfovibrio alcoholivorans) и показано их участие в цикле серы в микробных матах. Выделенные штаммы бактерий могут быть использованы в биотехнологии, в частности в процессах биоремедиации загрязненных территорий.
Работа выполнена в рамках бюджетного проекта VI.55.1.2. «Филогенетическое разнообразие и экологическая роль прокариот в экстремальных природных экосистемах». Отдельные этапы работы выполнены при финансовой поддержке грантов Министерства образования и науки РФ № 1990, РФФИ 15-04-01275-а, 15-44-04335-р_сибирь_a.
Список литературы Формирование и функционирование микробных матов минерального источника Хойто-Гол (Восточный Саян)
- Заварзин, Г.А. Лекции по природоведческой микробиологии. -М.: Изд-во «Наука», 2003. 348 с.
- Skirnisdottir, S. Influence of Sulfide and Temperature on Species Composition and Community Structure of Hot Spring Microbial Mats/S. Skirnisdottir, G.O. Hreggvidsson, S. Hjӧrleifsdottir et al.//Appl. Environ. Microbiol. 2000. V. 66. № 7. P. 2835-2841.
- Намсараев, З.Б. Микробные сообщества щелочных гидротерм/З.Б. Намсараев, В.М. Горленко, Б.Б. Намсараев, Д.Д. Бархутова. -Новосибирск: Изд-во СО РАН, 2006. 111 с.
- Ley, R.E. Unexpected diversity and complexity of the Guerrero Negro hypersaline microbial mat/R.E. Ley, J.K. Harris, J. Wilcox et al.//Appl. Environ. Microbiol. 2006. V. 72. № 5. P. 3685-3695.
- Калашников, А.М. Аноксигенные фототрофные бактерии микробных сообществ термального источника Горячинск (Прибайкалье)/А.М. Калашников, В.А. Гайсин, М.В. Сухачева М.В. и др.//Микробиология. 2014. Т. 83. № 4. С. 484-499.
- Gaisin, V.A. Filamentous anoxygenic phototrophic bacteria from cyanobacterial mats of Alla hot springs (Barguzin Valley, Russia)/V.A. Gaisin, A.M. Kalashnikov, M.V. Sukhacheva et al.//Extremophiles. 2015. V. 19. № 6. P. 1067-1076.
- Miller, S.R. Bar-coded pyrosequencing reveals shared bacterial community properties along the temperature gradients of two alkaline hot springs in Yellowstone National Park/S.R. Miller, A.L. Strong, K.L. Jones, M.C. Ungerer//Appl. Environ. Microbiol. 2009. V. 75. № 13. P. 4565-4572.
- Everroad, R.G. Diversification of Bacterial Community Composition along a Temperature Gradient at a Thermal Spring/R.G. Everroad, H. Otaki, K. Matsuura, S. Haruta//Microbes Environ. 2012. V. 27. № 4. P. 374-381.
- Данилова, Э.В. Влияние экологических условий на распределение функциональных групп микроорганизмов в минеральных источниках Хойто-Гол (Восточные Саяны)/Э.В. Данилова, Д.Д. Бархутова, А.В. Брянская//Сибирский экологический журнал. 2009. № 1. С. 45-53.
- Татаринов, А.В. Бактериальные сообщества термального источника Хойто-Гол (Восточные Саяны) и эколого-геологические условия их формирования/А.В. Татаринов, Э.В. Данилова, Л.И. Яловик и др.//Геохимия. 2010. № 2. С. 164-173.
- Цыренова, Д.Д. Влияние физико-химических условий на распространение цианобактерий в термальном источнике Хойто-Гол (Восточные Саяны)/Д.Д. Цыренова, Э.В. Данилова, В.В. Хахинов//Вестник Бурятского государственного университета. 2010. №3. С. 16-19.
- Намсараев, Б.Б. Полевой практикум по водной микробиологии и гидрохимии: методическое пособие/Б.Б. Намсараев, В.М. Горленко, З.Б. Намсараев, В.В. Хахинов. -М.-Улан-Удэ: Изд-во Бурятского госуниверситета, 2005. 87 с.
- Pimenov, N.V. In situ activities in thermal environments/N.V. Pimenov, E.A. Bonch-Osmolovskaya//In Methods in microbiology. Elsevier, London, United Kingdom. 2006. V. 35. Р. 29-53.
- Кузнецов, С.И. Методы изучения водных микроорганизмов/С.И. Кузнецов, Г.А. Дубинина. -М.: Изд-во «Наука», 1989. 288 с.
- Komàrek, J. Cyanoprokariota 1. Teil: Chroococcales//Süsswasserflora von Mitteleuropa/Eds. Ettl H., Gärtner G., Heynig H., Mollenhauer D./J. Komàrek, K. Anagnostidis. -Jena, Stuttgard, Lübeck, Ulm; G. Fischer, 1999. Bd. 19/1. 548 p.
- Komàrek, J. Cyanoprokariota 2. Teil: Oscillatoriales//Süsswasserflora von Mitteleuropa/J. Komàrek, K. Anagnostidis. -B. Büdel, G. Gärtner, L. Krienitz, M. Schagerl (Hrsg.), 2007. Bd. 19/2. 759 p.
- Wilson, K. Preparation of Geomic DNA from Bacteria//Curr. Protocols Mol. Biol. 2001. 00:2.4.1-2.4.5.
- Булыгина, Е.С. Изучение нуклеотидных последовательностей nifH генов у представителей метанотрофных бактерий/Е.С. Булыгина, Б.Б. Кузнецов, А.И. Марусина и др.//Микробиология. 2002. Т. 71. № 4. С. 500-508.
- Заварзин, Г.А. Литотрофные микроорганизмы. -М.: Изд-во «Наука», 1972. 323 с.
- Лазарева, Е.В. Исследование распределения элементов между цианобактериальным сообществом и карбонатной постройкой термального источника методом РФА СИ/Е.В. Лазарева, С.М. Жмодик, И.В. Петрова и др.//Поверхность. Рентгеновские, синхротронные и нейтронные исследования. 2012. Т. 5. С. 77-85.
- Горленко, В.М. Формирование микробных матов в горячих источниках и активность продукционных и деструкционных процессов/В.М. Горленко, Е.А. Бонч-Осмоловская//В кн. Кальдерные микроорганизмы. -М.: Изд-во «Наука», 1989. С. 53-64.
- Брянская, А.В. Биогеохимические процессы в альгобактериальных матах щелочного термального Уринского источника/А.В. Брянская, З.Б. Намсараев, О.М. Калашникова и др./Микробиология. 2006. Т. 75. № 5. С. 702-712.
- Намсараев, Б.Б. Геохимическая деятельность микроорганизмов гидротерм Байкальской рифтовой зоны/Б.Б. Намсараев, Д.Д. Бархутова, Э.В. Данилова и др. -Новосибирск: Академическое изд-во «Гео», 2011. 302 с.


